温度对模拟白酒体系氢键缔合影响分析*
2011-01-13杨星曾新安
杨星,曾新安
众所周知,水和乙醇在白酒中占主要比例,人们用不同的检测仪器和理论方法对其在各种条件下的变化进行了广泛的探索研究[1-7]。陈淑玲、刘鹏飞等人采用W ilhel my吊片法测量了不同体积分数下醇水溶液在 25~65℃的表面张力值,结果表明,在适当的浓度下当温度超过某确定值时,被测溶液的表面张力随温度升高而增大[8]。Akira和Masashi利用拉曼光谱对日本清酒和相同浓度的乙醇-水溶液在不同温度下羟基变化情况进行研究,发现温度降低可以促进体系内强氢键缔合[9];武千钧,林洪等人研究了啤酒在不同温度和溶解氧含量条件下其老化物质和香气成分的变化,得到减少成品啤酒的溶解氧含量和降低贮存温度可以提高其抗老化能力[10]。温度对酒口感的影响很大,在白酒陈酿工艺中,专家认为必须避免在高温下储酒,因为体系内过快的氧化反应会造成酒口味发生很大变化[11],可以说,温度控制在酿酒行业中有着重大意义。而在现实环境中由于地域性或者季节性的各种原因,造成各大酒厂储存酒的环境温度相差很大,从而使酒的口感发生明显的变化;迄今为止对酒口感变化影响主要是通过感官评定来确定,而对于温度影响白酒口感的深层原因,相关研究涉及较少。本文从分子氢键缔合角度出发并利用氢谱核磁共振仪对白酒模拟体系进行研究,初步探讨了温度与白酒体系口感变化的内在联系。
氢谱核磁共振仪(hydrogen nuclearmagnetic resonance)是研究溶液氢键缔合的常用仪器,1H NMR能测定质子的相对数量及判断缔合的类型,更重要的是可以反映分子间氢键缔合的细节情况[12]。当氢键X—H…Y形成时,由于质子接受体 (Y)存在,形成的静电场将 H拉向 Y,而将 X-H键的电子推向 X,使 H周围电子云密度降低,去屏蔽效应增加,质子化学位移升高,1H NMR谱图向低场移动,因此质子化学位移越大,缔合度也就越大,与此相反,谱图向高场移动说明体系内氢键缔合度减小;同时氢键缔合还受浓度、温度、压力等众多因素的影响[13]。乙醇-水溶液在1H NMR谱图中出现 4个质子峰,而白酒体系只有3个峰,其中乙醇质子峰与水质子峰在谱图中处于重叠状态;为了简化白酒成分以及细致地研究体系中各质子峰在变温情况下的细微谱图变化,本文采用乙醇-水溶液模拟白酒体系作为研究对象,在一定温度范围内对体积分数为 40%和 60%的乙醇-水溶液的氢键缔合变化展开研究并从中探讨温度变化对白酒口感的影响。
1 材料与方法
1.1 材料与试剂
氘代丙酮 (内含体积分数为 0.03%的 T MS,美国 CI L公司);无水乙醇 (天津市富宇精细化工有限公司分析纯);高纯水 (电导率低至 0.04μs/cm)。
1.2 仪器与设备
AV 400 MHz核磁共振波谱仪 (瑞士 Bruker公司,数据经 MestRec 470软件包处理);EPED-E型ED I超纯水系统装置,南京易普易达科技发展有限公司。
1.3 方法
1.3.1 核磁共振波谱仪主要参数
探头:ATB四核反向探头;定标法:内标法;谱宽:6410 Hz;累加次数:8;脉冲延迟:1;增益:0;共振频率:400 MHz;脉冲序列:s2pul;90度脉冲宽度:6.7;进样初始温度:18℃。
1.3.2 样品氢谱核磁共振测定
配制体积分数为 40%和 60%的乙醇-水溶液,静置 4 h,混匀后立即进行检测。在 18~58℃条件下测定乙醇-水溶液的谱图变化情况,以 T MS定标,谱图源数据经MestRec 470软件包处理,相关数据均为3次平均实验所得。
1.3.2 氢键缔合的平均寿命计算[12]。
采用式 (1)进行计算。

式中:△ν1/2为水质子峰的半高宽 (Hz);T2为1H NMR仪的横向迟豫时间;τH2O为体系内氢键缔合结构的平均寿命。
2 结果与分析
2.1 不同温度下乙醇-水溶液谱图变化情况
酒溶液的各分子间发生的氢键缔合变化会导致其内部微观分子结构发生相应转变,而最终会影响到酒的口感变化[9]。体系中分子氢键缔合情况可以在谱图的峰型以及化学位移中表现出来,图1显示的是体积分数为 40%和 60%乙醇-水溶液在各温度下1H NMR谱图变化情况。
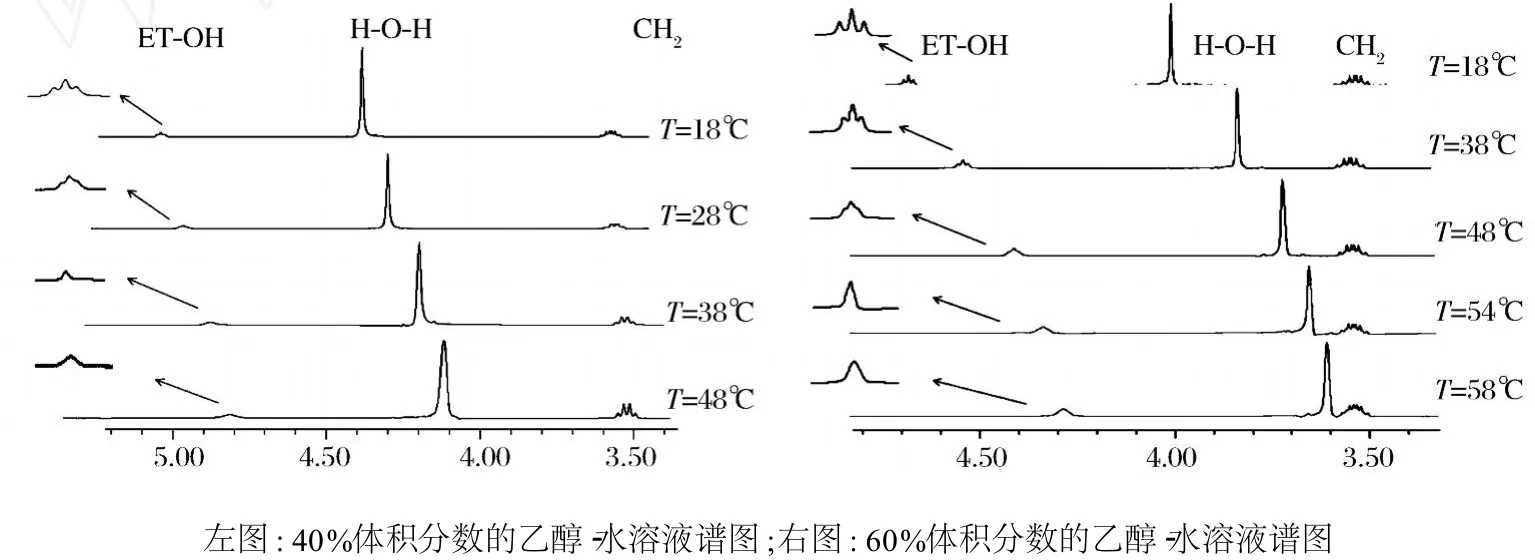
图1 不同温度下乙醇-水溶液1HNMR图谱变化
由于体系中 CH3质子谱图变化趋势和 CH2差不多,所以在图中没标示出来。由图1可知,随着温度的升高,体积分数为 40%和 60%的乙醇羟基质子峰和水的质子峰都向高场移动,氢键缔合减弱;同时乙醇羟基质子峰峰型也发生了巨大的变化,随着温度的逐渐升高,其清晰的峰型越来越不明显,40%和 60%体积分数的乙醇-水溶液分别在 38℃和 54℃下变为单峰,以上论述与 Akira等人利用拉曼光谱得到的结论大致相同[9]。温度升高促使乙醇-水溶液1H NMR谱图变化,其原因可能是体系中温度的升高使得醇-水体系热运动加剧,质子周边电子活动剧烈从而更易逃逸氢键的束缚,导致去屏蔽效应减弱,化学位移向高场变化,最终体系内氢键缔合度下降,反映在微观缔合结构上就是水中氢键扭曲、变型或遭到完全破坏从而降低了体系分子间的缔合[14]。并且,在较低温度下,乙醇分子羟基质子峰由于受到其他质子的影响而发生耦合,裂分为三重峰;随着环境温度的升高,氢键缔合作用减少,质子间的交换速度加快导致质子三重峰型变模糊最终形成单峰,从图1中还得出,随着温度的升高,不同乙醇浓度溶液其乙醇分子羟基质子峰峰型由三重峰转变为单峰时具有不同的温度临界点:40%乙醇溶液大致在 38℃,而 60%乙醇溶液在58℃。
乙醇-水体系氢键缔合结构处于断裂-缔合的动态状态中,为大致得到体系内缔合结构在变温条件下其频率变化情况,所以先求出体系中氢键缔合的平均寿命[13],故引入公式 (1):

其中为水质子峰的半高宽 (Hz),T2是1H NMR仪的横向迟豫时间,为某固定值,缔合结构变化频率与其平均寿命τH2O成反比关系。从公式 (1)可知,缔合结构平均寿命与成反比,也就是说,水质子谱峰的半高宽越大,其寿命越短,缔合结构频率变化也就越快。从图1中可大致得出,随着温度的升高,越来越宽,说明缔合结构的平均寿命越来越短,缔合体结构变化越来越快,而此过程又容易产生不稳定的分子结构,醇水中的分子结构直接影响到其口感变化,从而导致在温度过高情况下的白酒口感生硬及具有强烈的醇烈感,刺激性强,整体感觉不和谐,口味发生巨大变化。
2.2 温度与羟基质子化学位移间的线性关系
温度对氢键缔合有影响,反映在谱图上主要就是质子谱图峰化学位移的变化。图2表示的是 40%和60%体积分数的乙醇-水溶液各羟基质子化学位移和温度的关系图。

图2 40%和 60%体积分数乙醇-水溶液中羟基化学位移与温度的线性关系
由图2可知,温度与乙醇和水分子的羟基质子化学位移的变化具有线性相关性,40%体积分数乙醇-水溶液其各羟基质子化学位移和温度间拟合后的关系公式分别是δOH= -0.009T+5.268和δH-O-H=-0.008T+4.611,线性度为 0.952和 0.992;60%体积分数乙醇-水溶液拟合后公式为δOH= -0.011T+5.011和δH-O-H= -0.010T+4.283,线性度为 1和0.999。Birgit等人认为,体系中若存在强氢键缔合,其温度系数 dδ/dT≤0.3×10-6/℃[15],由以上拟合出来的公式可知在 40%和 60%体积分数的乙醇-水溶液中两羟基质子的温度系数分别为 0.009、0.008和0.011、0.010,都远小于 0.3 ×10-6/℃,从而可以得出乙醇-水体系主要是由强氢键缔合组成的微观分子结构,其受温度的影响很大,而对于真实白酒体系,其所含的各种风味物质总体来讲增强了体系内的氢键缔合结构,受温度的影响也很大[9];同时,按照温度系数Q10=2的原理,即温度为 (t+10)℃时典型反应速率大约为温度为(t)℃时的 2倍[11],得出如果适当升高储藏温度可以加速白酒陈酿速度,但又因为温度与羟基化学位移的线性关系,若储藏温度太高,可能会导致体系中强氢键缔合维系着的微观结构遭到破坏,陈酿效果更不明显,所以找到既可以缩短陈酿时间,又不至于破坏白酒体系整体微观结构的储藏温度是当前必须深入探讨的课题。
3 结 论
白酒体系中微观结构的变化会引起口感及其他方面的综合变化,储藏温度过高会加速酒老熟过程,但又可能使其口感变得粗糙难入口。本文模拟白酒体系进行温度单因素研究,发现 40%和 60%乙醇-水溶液随着温度的升高,其氢键缔合结构减弱甚至遭到破坏,质子间交换速度变快,氢键缔合结构的频率变化增加。在此过程中,发现了 40%和 60%体积分数乙醇-水溶液各羟基质子化学位移与温度间存在一定线性关系,其线性公式分别为δOH= -0.009T+5.268、δH-O-H= -0.008T+4.611 和 δOH= -0.011T+5.011、δH-O-H= -0.010T+4.283。从中可知,白酒体系的口感变化与温度有密切的线性关系,温度越高,白酒体系微观结构变化越突出,口感更粗糙。本实验只是对白酒模拟体系不同温度下储藏初期的氢键缔合情况进行了研究,为白酒体系在变温条件下口感发生变化的现象提供了一定的数据理论支持,至于体系在各温度下的长期储藏中的缔合状态需进一步研究探讨。
[1] Koji Yoshida,Ayuko Kitajo,Toshio Yamaguchi.17O NMR relaxation study of dynamics ofwatermolecules in aqueous mixtures ofmethanol,ethanol,and 1-propanol over a temperature range of 283-403 K[J].Journal of Molecular Liquids,2006,125:158-163.
[2] Stephenso S K,Offeman R D,Robertson G H,et al.Ethanol and water capacities of alcohols:A molecular dynamics study[J].Chemical Engineering Science,2006,61:5 834-5 840.
[3] Solm Mejía,Juan F Espinal,FanorMondragón.Cooperative effects on the structure and stability of(ethanol)3-water,(methanol)3-water heterotetramers and(ethanol)4,(methanol)4tetramers[J].Journal of Molecular Structure:THEOCHEM,2009,901:186-193.
[4] 樊婧,刘慧霞,曹绍俊,等 .不同温度对甘蔗糖料固定化酒精发酵的影响[J].中国酿造,2010,215(2):114-116.
[5] 郑飞云,姜甜,董建军,等 .酒类主要风味物质对乙醇-水体系中氢键的影响[J].食品科学,2010,31(09):106-113.
[6] 李高阳,丁霄霖 .正己烷-乙醇-水三元体系的相平衡研究[J].食品科学,2008,29(08):91-103.
[7] 杨琼,胡 蓉,张书然,等 .温度对测定乙醇含量近红外模型的影响[J].分析试验室,2008,27(S2):38-40.
[8] 陈淑玲,刘鹏飞,朱志强,等 .几种醇类水溶液表面张力的实验研究[J].北京交通大学学报,2008,32(01):112-116.
[9] Akira Nose,Masashi Hojo.REV IEW hydrogen bonding of water-ethanol in alcoholic beverages[J].Journal of Bloscience and Bioengineering,2006,102(4):269-280.
[10] 武千钧,林 洪,李 梅,等 .温度和氧对啤酒老化的影响[J].食品与发酵工业,2006,32(4):1-4.
[11] 赵光鳌 .葡萄酒酿造学——原理及应用 [M].北京:中国轻工业出版社,2001:243.
[12] 王乃兴 .核磁共振谱学—在有机化学中的应用[M].北京:化学工业出版社,2006:56-57.
[13] 张广宏,马文霞,万会军 .氢键的类型和本质[J].化学教育,2007,30(7):72-76.
[14] Jiang Ruo-mu,Edwin L Sibert III.How do hydrogen bonds break in small alcohol oligomers[J].J Phys Chem A,2009,113:7 275-7 285.
[15] Birgit Hakkarainen,Kahee Fujita,Stefan I mmel,et al.1H NMR studies on the hydrogen-bonding network in mono-altrob-cyclodextrin and its complex with adamantane-1-carboxylic acid[J].Carbohydrate Research,2005,340:1 539-1 545.
