肺癌患者PICC相关性静脉血栓的风险预测列线图模型构建与评价
2022-05-13高利琴赵林芳杨方英孙晶晶华荣誉吴红娟王慧勤顾玉炎毕丹凤
高利琴,赵林芳,杨方英,孙晶晶,华荣誉,吴红娟,王慧勤,顾玉炎,周 萍,毕丹凤
1.浙江大学医学院附属邵逸夫医院,浙江杭州 310016;2.中国科学院大学附属肿瘤医院,浙江杭州 310022
经外周静脉置入中心静脉导管(peripherally inserted central catheter,PICC)是目前肺癌患者最为常用的中心静脉导管之一。PICC相关性静脉血栓(PICC-related venous thrombosis,PICC-RVT)是指PICC置管后,由于穿刺或导管直接损伤血管内膜、患者自身状态等因素使PICC所在的血管内壁及导管附壁形成血凝块的过程[1],主要包括症状性血栓与非症状性血栓。症状性PICC-RVT在肺癌患者中的发生率较其他部位恶性肿瘤高,为3.4%~7.8%,严重的深静脉血栓可导致患者死亡[2-4]。近些年,血栓风险预测模型逐渐被研究者关注,通过血栓风险分层进行针对性的药物预防性抗凝是首选的解决方法之一。国内外也创建了PICC-RVT风险预测模型,但并未被广泛应用,可能是因为国外的研究应用于国内存在种族差异,国内研究的样本量偏小,且研究对象以无症状性血栓患者为主,缺乏特异性指标[5]。本研究旨在构建肺癌患者PICC-RVT风险预测模型,以期为临床医护人员选择合适的静脉通路,有针对地进行预防性抗凝提供借鉴与支持。
1 对象与方法
1.1 研究对象
本研究将发生症状性PICC-RVT或拔管作为结局指标,调查中国科学院大学附属肿瘤医院2016年1月至2019年12月置入PICC的肺癌患者共5 091例,其中103例患者发生症状性PICC-RVT,4 988例患者拔管前未发生症状性血栓,血栓发生率为2.02%。纳入标准:病理诊断为肺癌;置管前有近一个月内的胸部增强CT检查;置管前有相关实验室检查。排除标准:心房颤动;伴有慢性阻塞性肺气肿;同时有其他中心静脉导管或起搏器;留置导管期间预防性抗凝。本研究共37个自变量,按照最小样本量应为自变量数的5~10倍,最小随访样本量约为185~370例,考虑到样本流失率再扩大20%。考虑到模型的有效性,样本量增至约1 000例。血栓症状和(或)体征:血管B超诊断为血栓形成,血栓部位包括上肢静脉、颈内静脉、锁骨下静脉、无名静脉。按照发生血栓例数比非血栓例数为1∶9的比例根据随机数字表法从未发生血栓的4 988例患者中抽取927例患者,最终共纳入1 030例研究对象,血栓组103例,非血栓组927例。本研究经中国科学院大学附属肿瘤医院伦理委员会审核并获实施批准,审批号:IRB-2015-232号(科)。
1.2 研究方法
1.2.1研究工具
危险因素调查表采用指标体系构建法,基于文献回顾结合小组讨论产生首轮调查问卷,通过3轮德尔菲专家咨询形成终稿。危险因素调查表包括一级指标:患者因素、导管因素、治疗相关因素;二级指标:患者基本情况、营养状况、原发肿瘤部位、基础疾病、既往治疗史(或留置导管期间的伴随治疗)、实验室检查指标、活动因素、导管材料因素、导管留置时间、导管相关并发症、置管因素、维护因素、静脉输注药物、非静脉输注药物;三级指标:年龄、性别等。
1.2.2数据收集与质量控制
由放射科主治医生通过胸部增强CT结果判断导管行走的锁骨下静脉、无名静脉及上腔静脉受肿瘤压迫的程度。上腔静脉受肿瘤压迫标准:无受压;轻度受压,肿块一侧推压静脉导致静脉压扁变形,受压程度<1/2截面积,受压长度<2 cm;中度受压,肿块一侧推压静脉,静脉变形,或肿块半包围推挤静脉,受压程度1/2~2/3截面积,受压长度2~4 cm;重度受压,受压程度2/3以上截面积,肿瘤全包围静脉引起静脉皱缩样改变或静脉压扁呈月牙形,受压长度>4 cm,直至静脉完全闭塞,侧枝循环形成。无名静脉与锁骨下静脉受压的程度判别:无受压;轻度受压,受压部位静脉直径在5~6 mm左右;中度受压,受压部位静脉直径在3~4 mm左右;重度阻塞,静脉直径<3 mm。其他数据由经过统一培训的调查员收集。采用统一的调查表与判断标准进行数据录入,危险因素调查表中多数数据由PICC置管记录、并发症记录、电子病历系统中导入,再由另一位调查员根据电子病历系统中的护理记录与血管B超等结果进行核实。由于患者的病情与血液指标会随着治疗而变化,因此,血栓组的危险因素指标收集分为置管前与血栓发生时两部分。置管前收集非动态变化的指标以及低密度脂蛋白胆固醇、D-二聚体;动态指标如同时伴有其他导管相关并发症、导管继发性异位、导管所在中心静脉受压、Barthel指数以血栓发生时的指标为准。
1.2.3统计学方法
采用SPSS 24.0软件进行统计学处理,计数资料采用x2检验,以例(%)描述。结合既往研究结果与临床实际情况,将P<0.1的自变量(共13个自变量)纳入二元Logistic回归分析。逐步向前似然比法筛选独立危险因素,最终纳入10个预后参数,使用R软件进一步构建列线图,经过500次自助重复抽样进行内部验证,绘制ROC曲线评价预测模型的区分度,绘制校准曲线评价模型的校准度。
2 结果
2.1 一般资料
本研究共计纳入研究对象1 030例。其中男779例,女251例;右侧PICC置管626例,左侧PICC置管404例;腺癌407例,鳞癌344例,小细胞肺癌194例,其他病理类型85例。103例血栓组患者年龄41~80岁,平均(61.64±8.35)岁;927例非血栓组患者年龄23~85岁,平均(61.11±8.81)岁。血栓组Barthel指数90(88.00±14.45)分,非血栓组Barthel指数95(93.55±8.37)分;血栓组患者血栓发生平均时间为置管后47 d,中位时间22 d;非血栓组患者导管留置平均时间93 d,中位时间87 d。
2.2 单因素分析结果
本研究单因素分析结果显示:性别、年龄、病理类型、体质量指数、血型、置管前一个月内有大手术史、置管前一个月内有刺激性药物输入史、高血压史、酗酒史、置管侧、导管材质、导管/穿刺血管直径比、穿刺次数、导管尖端位置、置管时有异位调整、置管护士资质、经导管输入化疗药、经导管输血、经导管输注静脉高营养、血小板计数、甘油三酯指标、高密度脂蛋白胆固醇指标、血纤维蛋白原指标、中心静脉置管史差异无统计学意义(P>0.05)。单因素分析中差异有统计学意义(P<0.05)的自变量(糖尿病病史、伴有其他导管相关并发症除外)见表1。
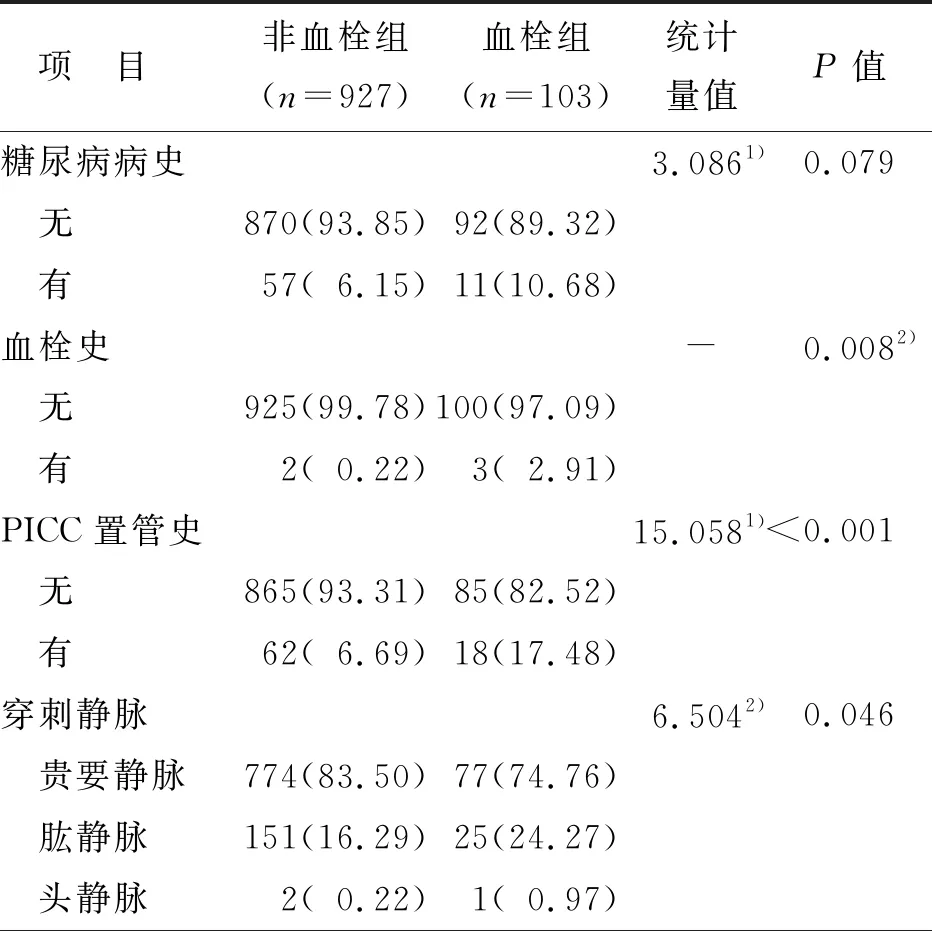
表1 PICC相关性静脉血栓单因素分析
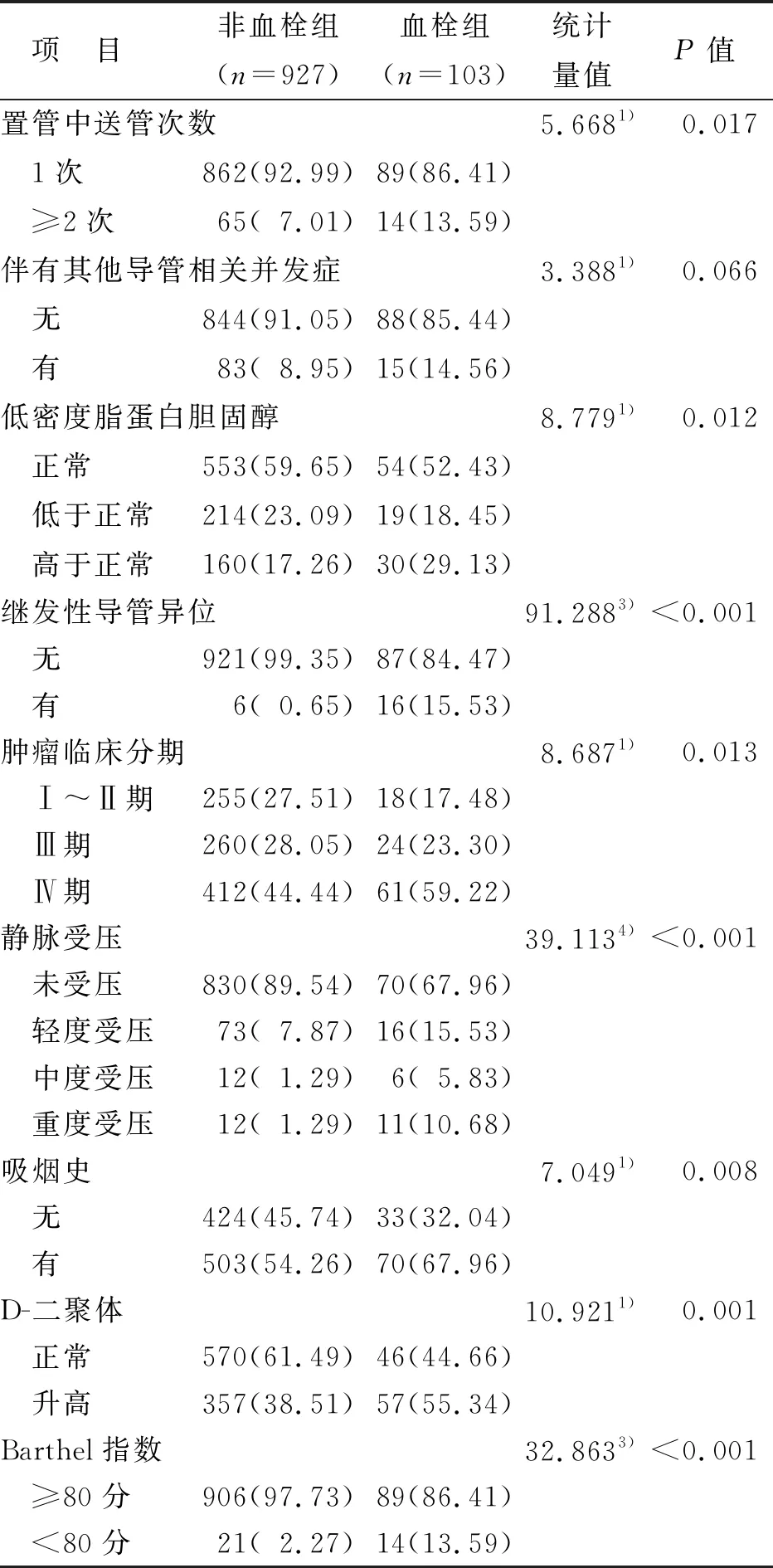
表1(续)
2.3 多因素回归分析结果
将单因素分析中P<0.1的因素作为自变量(自变量赋值见表2),以患者是否发生血栓作为因变量(未发生血栓=0,发生血栓=1),进行二元Logistic回归分析。结果表明:PICC置管史、送管次数≥2次、伴有其他导管相关并发症、低密度脂蛋白胆固醇高、继发性导管异位、肿瘤临床分期Ⅳ期、导管所在静脉受压、吸烟史、D-二聚体指标升高、Barthel指数<80分是肺癌患者发生PICC-RVT的独立危险因素,见表3。

表2 自变量赋值表
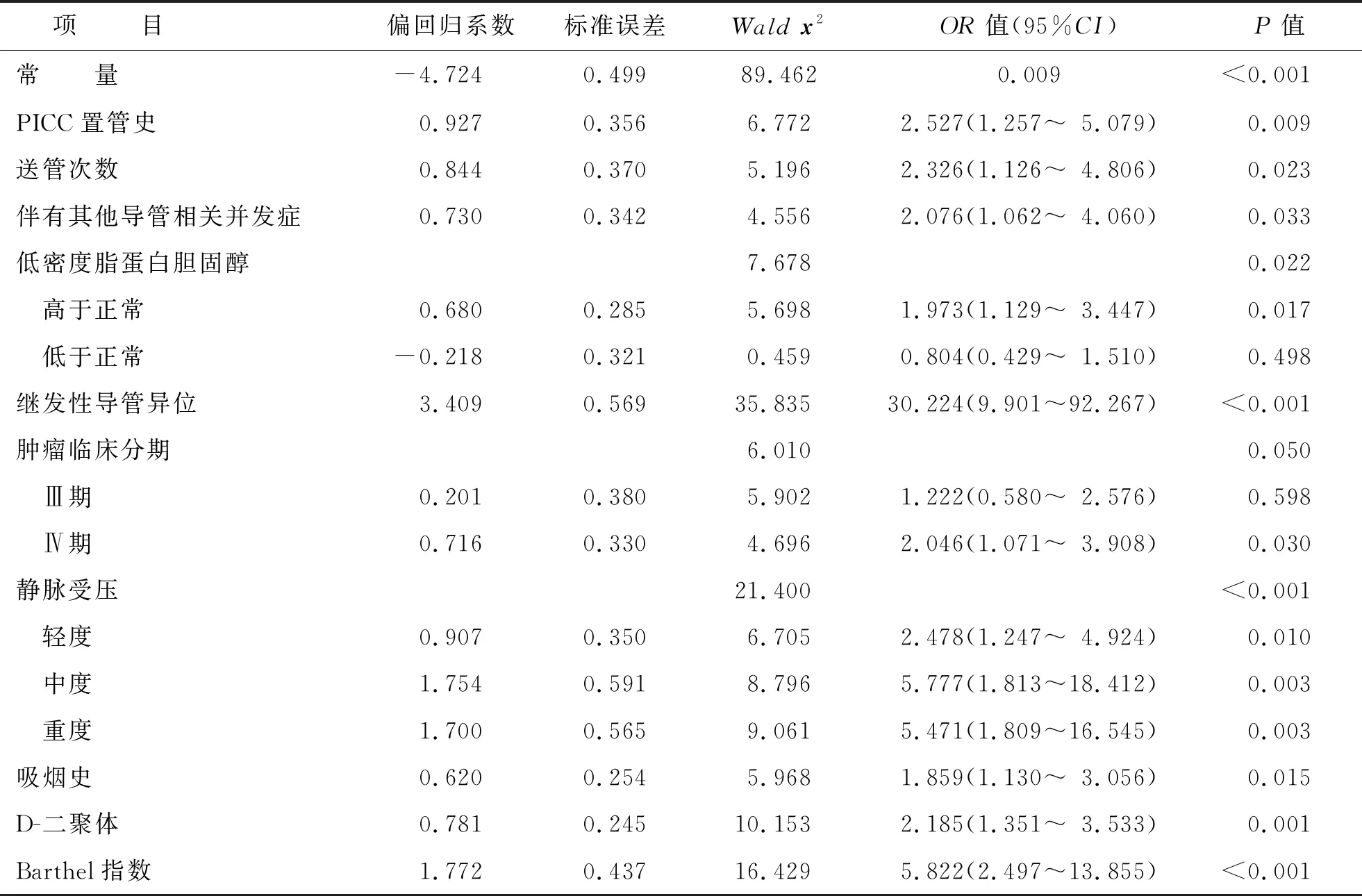
表3 二元Logistic回归分析结果
2.4 列线图模型及内部验证结果
将筛选出的独立危险因素纳入R软件(版本号3.4.3)构建列线图模型,风险预测全模型的ROC曲线下面积(AUC)为0.794(95%CI:0.744~0.845),特异度0.825,敏感度0.643,准确度0.808,阳性似然比3.679,阴性似然比0.433。模型采用Bootstrap经500次自助重抽样,验证集模型AUC 0.795(95%CI:0.745~0.845)。肺癌PICC-RVT风险预测模型ROC曲线见图1(a),肺癌PICC-RVT校准曲线见图1(b)。肺癌PICC-RVT风险预测列线图模型及举例见图2,假设1例肺癌患者临床分期为Ⅳ期,Barthel指数<80分,置管前D-二聚体指标>232 ng/mL,上腔静脉中度受压,风险总分为20+44+23+50=137分,对应的血栓风险概率为58%,在选择中心静脉导管时避免选择PICC,规避PICC-RVT的风险。
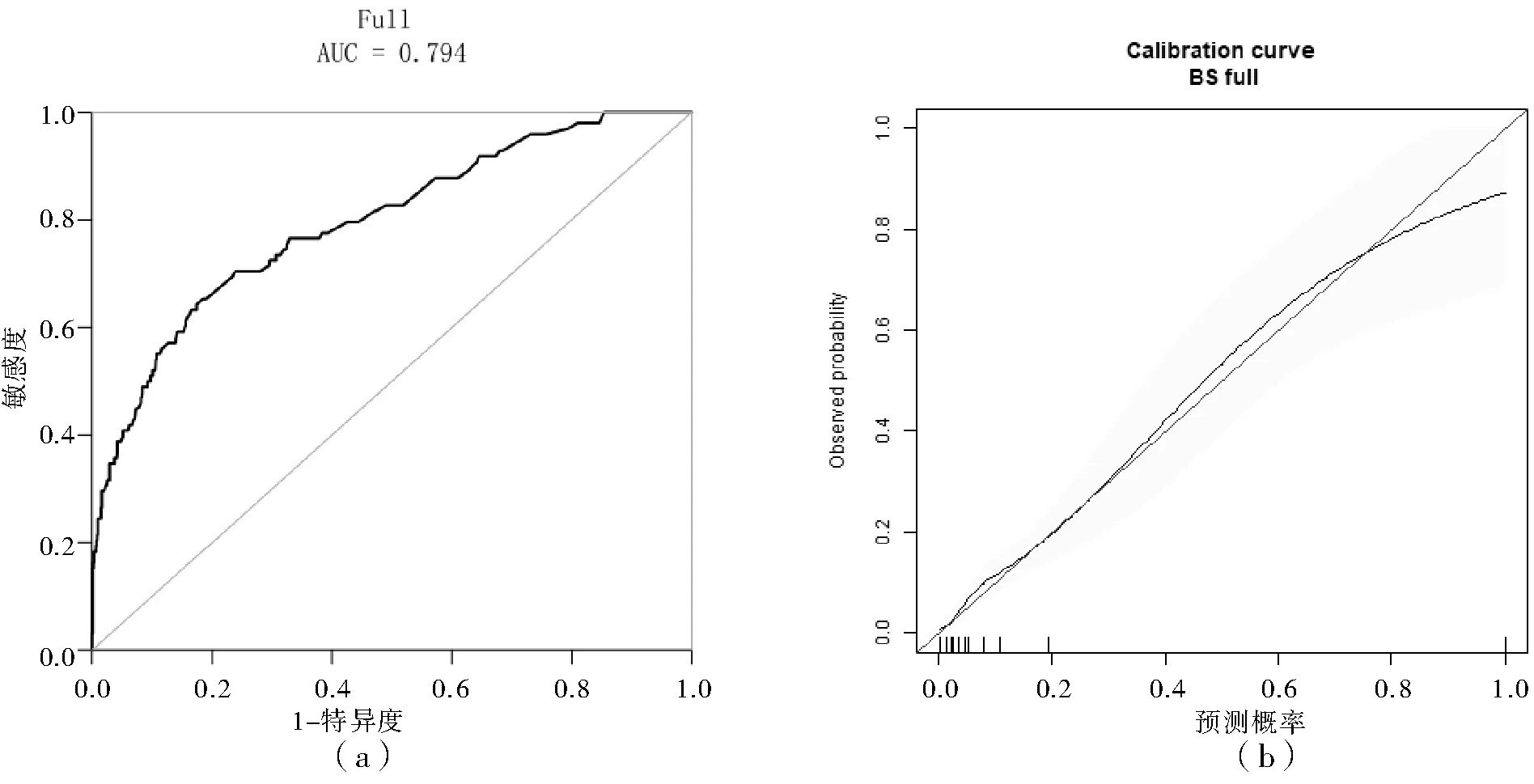
图1 肺癌PICC-RVT风险预测模型ROC曲线及校准曲线
3 讨论
3.1 模型的可读性与内部验证
本模型通过Bootstrap 法重复采样500次进行内部验证,通过AUC来分析模型的区分度,AUC在0.6以下为低区分度,0.6~0.75为中区分度,0.75以上为高区分度,全模型与验证集模型AUC>0.75,表明本预测模型具有高区分度。图2校准曲线显示预测值与实际值之间差别小,说明模型具有较好的拟合度。
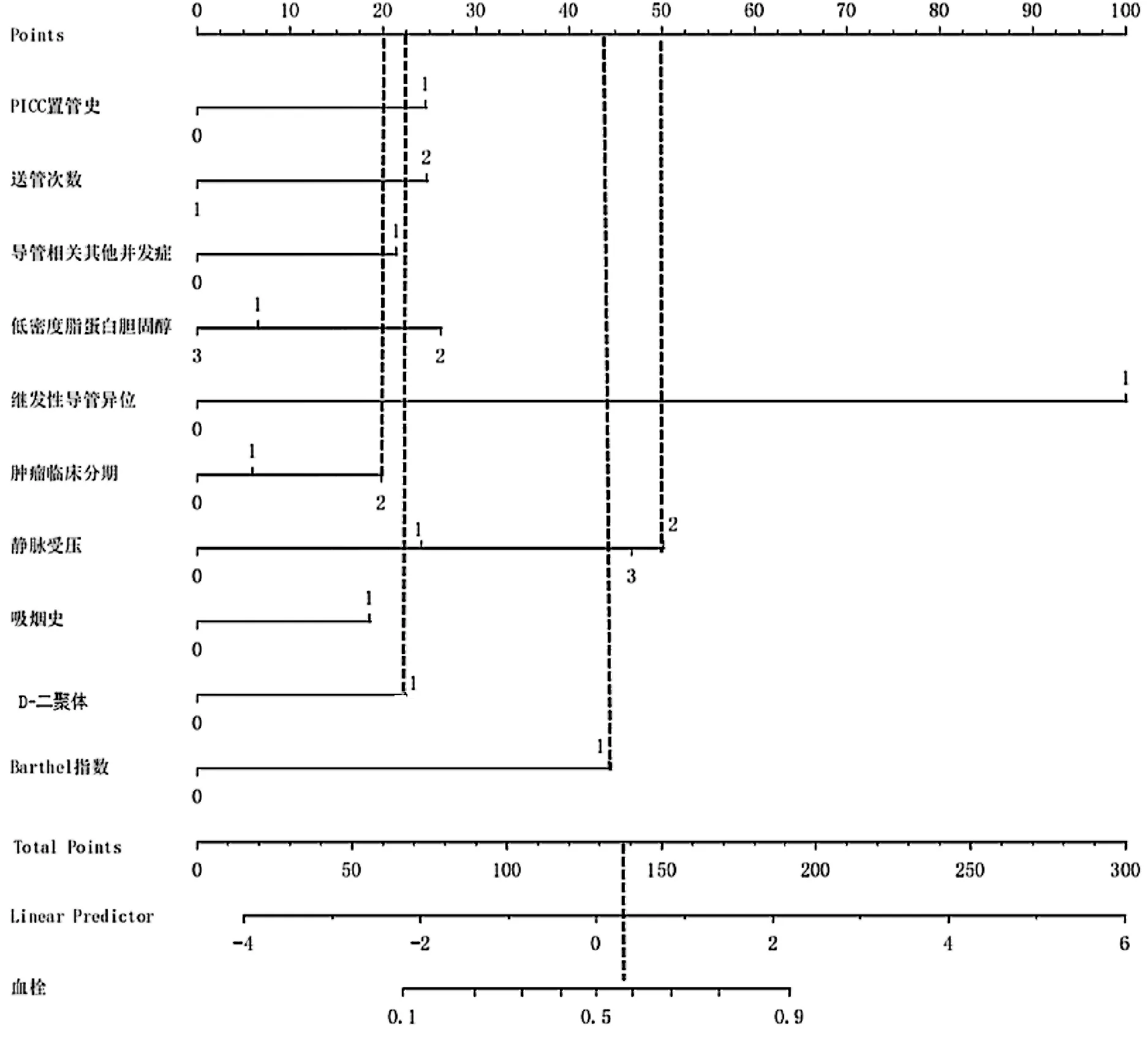
图2 肺癌PICC-RVT风险预测列线图模型及举例
3.2 本研究发现的PICC-RVT危险因素
根据Virchow血栓形成理论,血流瘀滞、血管内膜受损、血液高凝状态是血栓形成三大要素[6]。PICC-RVT作为血栓的一种特殊类型,血栓的形成与导管密切相关,同时与患者自身状况有关,本研究发现的PICC-RVT独立危险因素按照Virchow理论归纳如下。
3.2.1血流瘀滞
本研究发现的主要与血流瘀滞有关的独立危险因素:导管所在中心静脉受压(按照轻、中、重度的程度OR值分别为2.478、5.777、5.471),继发性导管异位(OR=30.224),Barthel指数<80分(OR=5.882)。当PICC所在的上腔静脉、无名静脉、锁骨下静脉受到轻、中、重度压迫时血栓发生率增加,对应的列线图分值为24分、50分、47分。肺癌较其他部位的恶性肿瘤更容易出现上腔静脉压迫综合征(superior vena cava syndrome,SVCS),肿瘤压迫上述静脉会导致血流瘀滞,此时如果存在PICC,更容易导致血栓的发生,肿瘤甚至可以直接侵袭血管,发生自发性血栓,因此SVCS为PICC的禁忌证,但更多肺癌患者虽上腔静脉受压但症状、体征隐匿,置管前仅凭症状、体征观察法较难评估到问题,置管后会导致血栓的发生[7]。此外,当PICC所在中心静脉重度受压时,导管所在静脉血流瘀滞或者血液逆流,带管期间有可能发生继发性导管异位。继发性导管异位或导管漂移是指PICC置管成功后,首次X线摄片检查导管头端在上腔静脉,但留置期间导管头端移行至上腔静脉以外的位置或导管在静脉内打圈、打结、反折等现象。当PICC导管尖端不在上腔静脉内,其所在静脉血流量不如上腔静脉,或由于打圈、反折的导管使血流不畅,可导致血栓的发生[8]。仇晓霞等[9]研究显示,PICC继发性导管异位导致深静脉血栓发生率高达42.86%。相比其他部位的恶性肿瘤,肺癌患者更容易出现因咳嗽等引起胸腔内压力改变的情况,从而增加继发性导管异位的发生率。本研究结果显示,继发性导管异位引起血栓风险增高,对应列线图得分100分,居各类危险因素之首。本研究多因素分析结果中静脉重度受压OR值反而减小,可能与重度受压患者中继发性导管异位比例增高,以及此类患者中送管次数≥2次有关。同时,本研究发现血栓组Barthel指数明显低于非血栓组,Barthel指数<80分为血栓危险因素,Barthel指数<80分的患者血栓风险OR值为5.822,列线图分值44分。Barthel指数低的患者日常生活需要更多的家属帮助,卧床时间增加,降低了血流速度,增加血栓的发生率,与Seeley等[10]的PICC血栓风险模型结果中卧床不起的患者血栓风险高相一致。
3.2.2血液的高凝状态
本研究发现的主要与血液高凝有关的独立危险因素:Ⅳ期肺癌,D-二聚体指标高,低密度脂蛋白胆固醇高。本研究多因素分析结果显示,Ⅳ期肺癌患者的血栓发生率较Ⅰ~Ⅱ期患者高(OR=2.046),对应列线图评分20分,Ⅲ期的肺癌患者与Ⅰ~Ⅱ期肺癌患者相比差异无统计学意义(P=0.598)。在密西根PICC血栓评分中活动性癌症评分高达3分(≥4分为高危)[11],也与COMPASS-CAT模型[12]、王有福等[13]的研究结果相似。Ⅳ期的恶性肿瘤当肿瘤细胞进入血液循环后,与内皮细胞、血小板等相互作用,释放促凝物质、黏蛋白、组织因子等破坏血管内皮细胞,从而引起纤维蛋白原升高和凝血因子的激活,导致了患者的高凝状态[14]。D-二聚体是纤维蛋白在溶解过程中的降解产物,是反映机体凝血后继发纤维蛋白溶解状态的一个敏感而又特异的指标,可作为预测血栓形成的重要指标[15]。本研究结果显示,D-二聚体指标高于正常值的肺癌患者血栓发生率较高(OR=2.185),对应列线图分值23分,与蒿若楠[16]、陈江琼等[17]的研究结果相似。低密度脂蛋白胆固醇是在血浆中由极低密度脂蛋白胆固醇转变而来,其合成部位主要在血管内,高浓度低密度脂蛋白胆固醇是动脉粥样硬化的危险因素,与心肌梗死和血管疾病死亡风险的增加密切相关[18]。在本研究的多因素分析中,低密度脂蛋白胆固醇升高也是PICC-RVT的独立危险因素(OR=1.973),这与王卫等[19]、杨方英等[20]的研究结果相似。
3.2.3血管内膜的破坏
本研究结果中主要与血管内膜破坏相关的独立危险因素:有吸烟史的肺癌患者PICC-RVT风险比没有吸烟史的患者高(OR=1.859),送管次数≥2次比送管一次成功的患者高(OR=2.326);有PICC置管史比首次置管的患者高(OR=2.527);伴有其他导管相关并发症较未发生并发症的患者高(OR=2.076)。吸烟能直接破坏血管内皮,并通过影响血小板体积和膜流动性从而对血栓的形成有显著的促进作用[21]。吸烟可作为预测血栓性疾病的危险因子之一,该结果与王瑞丽[22]的研究结果相似。置管过程中多次送管会导致静脉内膜受损,该结果与华荣誉等[23]的研究结果相似。PICC置管后的无症状性血栓高达35%~79%,再次置管会损伤原有损伤的静脉,导致血栓的形成[24]。本研究除继发性导管异位以外的导管相关并发症包括皮炎、置管口局部感染、导管相关血流感染、堵管。皮炎患者由于皮肤屏障的破坏,容易导致感染,PICC-RVT与感染互为因果,互相促进,尤其在化脓性细菌如金黄色葡萄球菌感染的患者中,血栓风险率更高。本研究发现伴有导管并发症的患者血栓发生率高,与杨方英等[25]研究结果相似。堵管本身与导管尖端位置的改变密切相关,而导管尖端位置不在上腔静脉时,已被证实与血栓发生关系密切[26]。
3.3 本研究未涉及的危险因素及部分阴性结果解读
本研究整体血栓发生率为2.02%,较其他文献报道的低,分析可能因为本研究中置管采用集中PICC穿刺,在静脉、导管、置管方式的选择上已应用了目前最佳证据,极少选择头静脉,采用单腔导管,B超引导改良塞丁格技术下上臂置管已经达到100%,将尖端未进入上腔静脉的导管一律只做中线导管使用。穿刺一次成功与穿刺2次以上的患者血栓风险差异无统计学意义,与细针穿刺的损伤降低有关。蒿若楠[16]、陈江琼等[17]研究结果认为糖尿病可增加肿瘤化疗患者PICC-RVT的形成。本研究将糖尿病病史纳入多因素分析中,差异无统计学意义。糖尿病可以引起血管的病变,还会降低抵抗力,并发穿刺点感染乃至血流感染,本研究中差异无统计学意义可能与纳入的糖尿病患者数据较少有关。
3.4 本研究的创新性与局限性
本研究发现了PICC-RVT风险预测模型的两个新的独立危险因素:导管所在中心静脉受压和继发性导管异位。通过多学科合作,借助于增强CT对导管所在静脉受压程度进行分级,建立了与PICC相关的静脉受压程度分级标准,相比于现有中心静脉狭窄的William Standford分级[27],后者仅适用于评估上腔静脉支架植入的适应证,前者对于肺癌PICC置管前评估具有重要的意义。同时,回顾资料时,静脉受压分级与血栓统计由不同的人员进行,避免了偏倚的发生。本研究的局限性在于未进行模型的外部验证,需要今后进一步的研究予以完善。
