两种检测HBV RNA方法在核苷(酸)类似物经治和初治慢性乙型肝炎患者中的相关性和一致性评价
2020-08-13王雪刚张新枝杨澍甘苏琴刘诗郝坤艳周彬于乐成
王雪刚 张新枝 杨澍 甘苏琴 刘诗 郝坤艳 周彬 于乐成
近年来,随着乙型肝炎病毒(Hepatitis B virus, HBV)抗病毒药物,主要是核苷(酸)类似物(Nucleoside/nucleotide Analogues, NAs)的广泛使用,慢性乙型肝炎(chronic hepatitis B,CHB)患者的病毒复制及肝脏炎症均得到了很好的控制[1-2]。在丙氨酸氨基转移酶(ALT)等肝生化指标持续正常、乙型肝炎表面抗原(HBsAg)下降不明显、HBV DNA和HBeAg检测不出的情况下,如何更精准地监测患者病毒复制情况和选择合理的停药时机,是目前临床实践中常见的问题[3]。随着这些新问题的提出,HBV RNA作为新的可能反映肝细胞内HBV cccDNA水平的血清学指标,近年来迅速成为临床和相关基础研究人员关注的一个热点。
HBV是一种DNA病毒,近年来一直以血清HBV DNA水平作为反映患者病毒复制水平的指标。血清HBV RNA的检测早在1994年就有文献报道,研究者利用PCR和RT-PCR可以同时从HBV相关肝癌和CHB患者血清检测到HBV DNA和HBV RNA[4-5]。由于当时对HBV RNA临床意义的认知不如HBV DNA和HBsAg明确,所以在相当长的时间里未得到临床医生和科研工作者应有的重视。2015年以来,研究者们发现在HBV DNA获得持续抑制的患者中,仍然能检测到血清HBV RNA,其存在的意义和价值立即引起了临床医生和研究者的极大兴趣[6-8]。
随着对血清HBV RNA临床应用的关注,许多检测HBV RNA的方法和试剂盒也应运而生。我们对比了文献报道中常用的“互补DNA末端快速扩增法”(rapid amplication of complimentary DNA-ends,RACE)和一种Sansure国产试剂盒检测CHB患者血清HBV RNA的效能,采样两种方法对治疗和未治疗患者血清中的HBV RNA水平检测值进行了评价,以期探讨不同检测方法在临床应用中的一致性和可替代性。
资料与方法
一、研究对象
收集2018年6—9月在南方医科大学南方医院肝病门诊就诊的CHB患者,排除接受干扰素、合并丙型肝炎病毒或人类免疫缺陷病毒等其他病毒感染的患者。共纳入101例,其中未接受NAs治疗患者39例,曾经或正在接受NAs治疗者62例,均为参加常规随访的患者。所有患者均已签署知情同意书,项目经南方医科大学南方医院伦理委员会批准。
二、HBV DNA及HBsAg等血清学指标的检测
三、血清HBV RNA检测
第二种方法采用圣湘公司HBV RNA定量试剂盒(科研用HBV RNA PCR-荧光探针法定量检测试剂盒,Sansure法试剂盒),在公司技术人员指导下,完全按照试剂盒说明的步骤操作。通过逆转录 HBV 核酸中的 pgRNA(经 DNA 酶消化),利用针对 HBV pgRNA 序列设计的一组特异性引物与荧光探针,配以 PCR 反应液,应用一步法逆转录实时荧光定量 PCR 检测技术,通过荧光信号的变化实现 HBV pgRNA 的定量检测。PCR 检测体系含有阳性内对照(内标)和四个定量参考品,通过检测内标基因来监测提取核酸中是否具有 PCR 抑制物,评价核酸提取的质量,避免 PCR 假阴性。PCR 检测体系含有内参比荧光 ROX,用于校正加样误差和管间差异,便于仪器自动分析报告荧光与内参比荧光ROX的比值。
四、统计学处理
采用Graphpad 8.0软件进行统计分析及统计绘图,组间均值比较采用t检验;HBV DNA与HBV RNA及两种HBV RNA检测结果的相关性采用R值进行计算;两种方法检测的HBV RNA 在未治疗和治疗患者中的一致性用Bland-Altman图表示;两种HBV RNA之间的关系采用线性回归方程表示。
结 果
一、患者一般情况
101例患者的性别、年龄分布、HBeAg阳性的人数,以及ALT、HBsAg、HBV DNA水平的中位数和范围见表1。
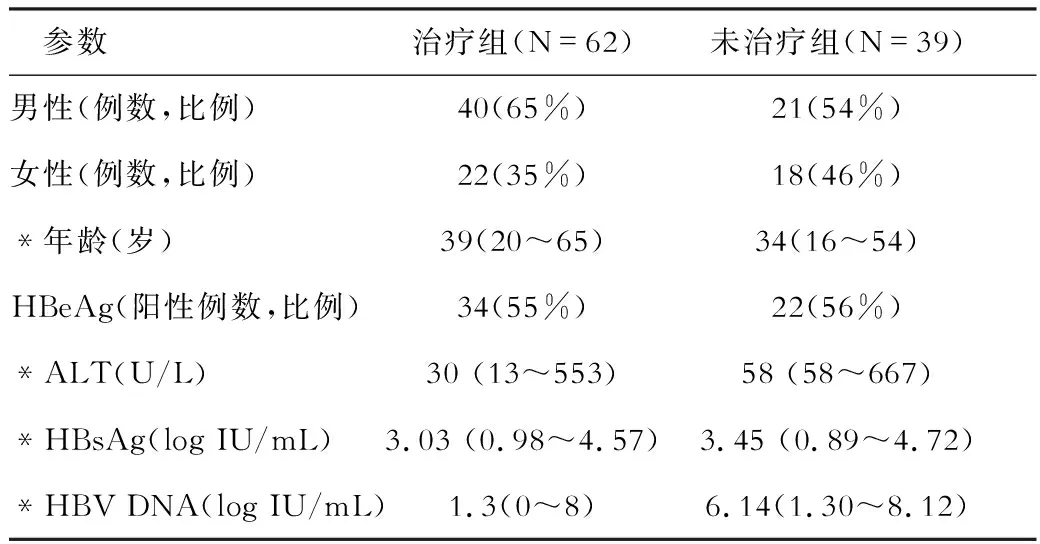
表1 治疗组和未治疗组患者的一般情况
二、治疗组和未治疗组的HBsAg水平和HBV DNA水平
两组患者的HBsAg水平差异有统计学意义(P=0.0023),未治疗组的HBsAg平均值明显高于治疗组(3.382与2.691 lg U/L)。HBV DNA水平在两组间差异有统计学意义(P<0.001),未治疗组的HBV DNA平均值明显高于治疗组(5.842对1.656 lg IU/mL)。见图1。
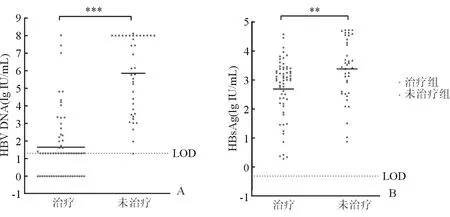
图1 治疗组和未治疗组患者HBsAg和HBV DNA水平比较
三、两种HBV RNA检测方法的检测效能
按照Sansure法的试剂说明,其线性范围为 3×102~1.00×109拷贝/mL,检测下限(Low level of detection, LOD)为100拷贝/mL. 本实验室按照文献建立的RACE法的线性范围为4×103~4×1010拷贝/mL,LOD为3 890 拷贝/mL。虽然数值显示RACE法比Sansure法的LOD更高,但是在本研究中检测相同的临床样本,RACE法比Sansure法的检测值平均高出0.68 lg 拷贝/mL。
四、治疗组和未治疗组的HBV RNA水平
两组患者的血清HBV RNA水平在治疗组和未治疗组间差异有统计学意义,但差异不如HBV DNA水平的组间差异显著(P=0.0134)。两种方法相比,RACE法比Sansure法检测到的阳性患者更多,分别在101例患者中检测出60和56例。RACE法比Sansure法的检出平均检值更高,分别为3.16 lg 拷贝/mL和2.53 lg 拷贝/mL。治疗组中RACE和Sansure的HBV RNA平均值分别为2.259 lg 拷贝/mL和1.650 lg 拷贝/mL(P=0.153 2);未治疗组中RACE和Sansure的HBV RNA平均值分别为4.583 lg 拷贝/mL和3.878 lg 拷贝/mL(P=0.308 6)。两种方法检测值的差异无统计学意义(图2)。
例如:在《数学广角——搭配(二)》一课的课堂教学过程中,我就是以构建生活化教学情境的方式,促进生态化小学数学课堂的构建的。
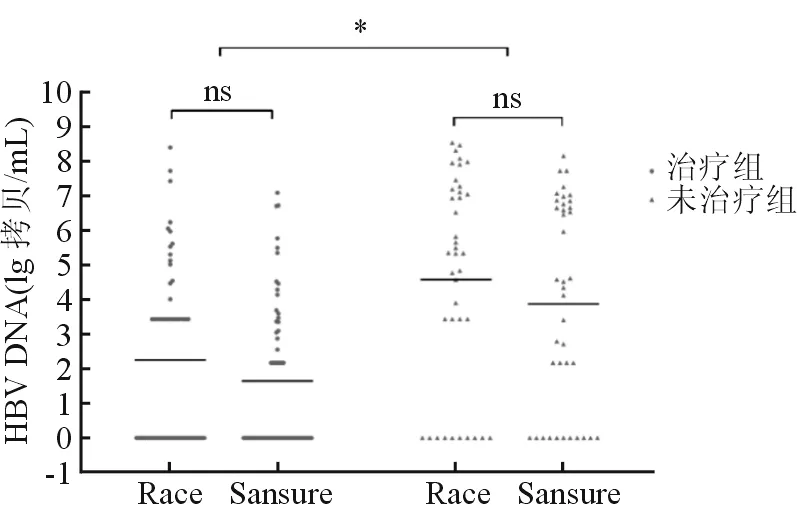
图2 治疗组和未治疗组患者HBV RNA水平比较
五、治疗组和未治疗组患者HBV DNA与HBV RNA水平的相关性
在治疗组中血清HBV DNA水平与HBV RNA水平没有相关性,RACE法R2= 0.440 6,Sansure法R2= 0.508 1(图3A)。
在未治疗组中,两种方法均显示血清HBV DNA水平与HBV RNA水平显著相关,RACE法R2=0.844 8,Sansure法R2= 0.866 7(图3B)。
将治疗组和未治疗组混合分析,相关性不佳,RACE法R2= 0.610 0,Sansure法R2= 0.653 0(图3C)。
RACE法和Sansure法的HBV RNA检测值具有显著的相关性。总体上两种方法检测值经相关性检验为R2=0.8740,具有显著相关性(图3D)。
两种方法在治疗和未治疗患者中的一致性采用Bland-Altman图表示(图4)。以两种测量结果的差值为纵轴,以测量结果的均数为横轴,绘制散点图,用虚线标注出95%一致性界限(95% limits of agreement, 95% LoA)。95% LoA的范围较窄(两个目标之间的差值在治疗组为-1.789到0.22 lg 拷贝/mL,未治疗组为-2.25到0.53 lg 拷贝/mL)。以RACE法为基准,Sansure法的偏差在治疗组为-0.78 lg 拷贝/mL,在未治疗组为-0.86 lg 拷贝/mL。偏差值均小于2,两种检测值的一致性好(图4)。经deming线性回归分析,以Race法结果作为X,以Sansure法结果作为Y,两者的回归方程为Y=0.9189X-0.3754。
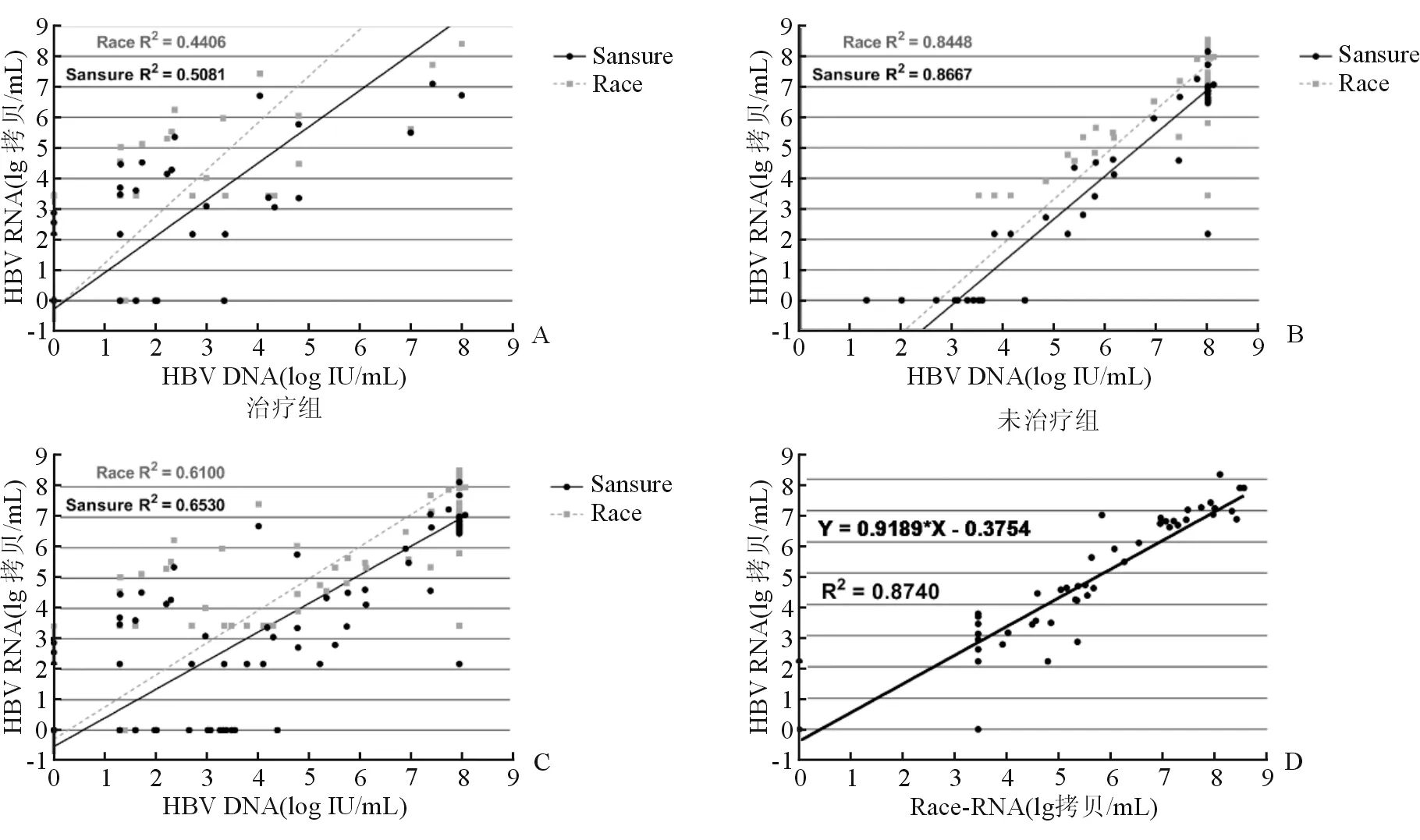
图3 HBV DNA水平与HBV RNA水平的相关性及两种HBV RNA检测值的相关性
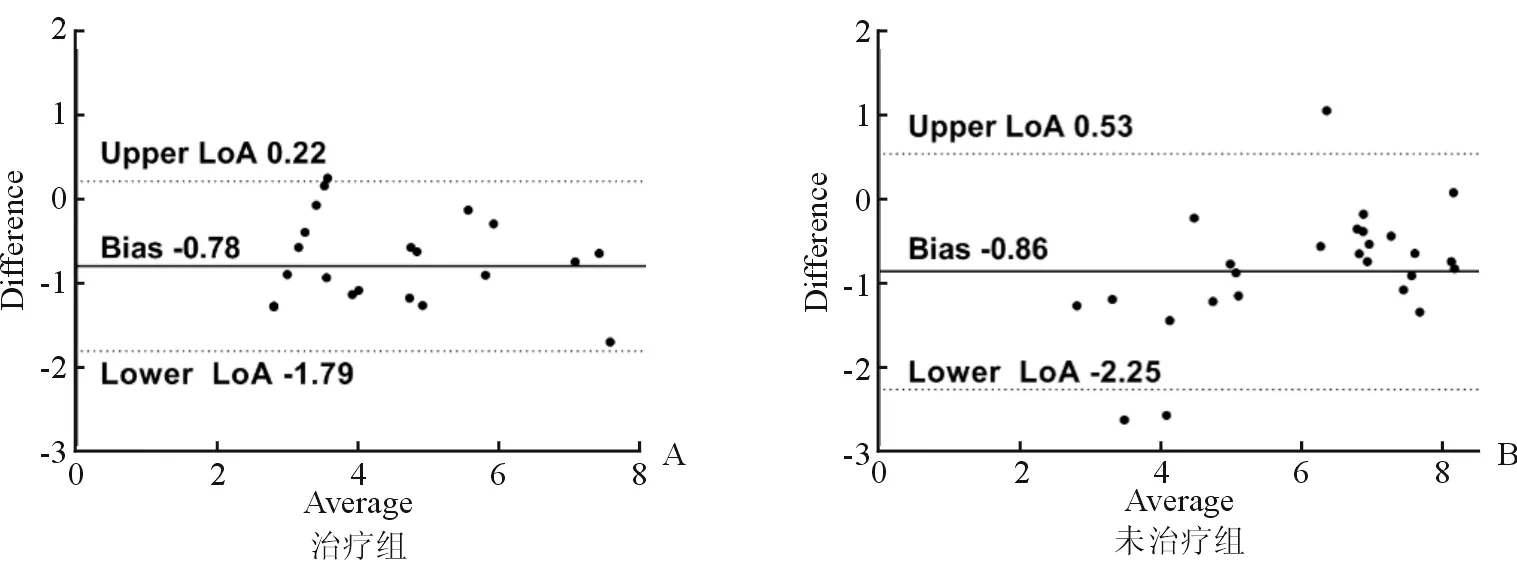
图4 两种检测方法HBV RNA水平在治疗和未治疗患者中的Bland-Altman一致性分析
讨 论
HBV在复制过程中会产生5种HBV mRNA,在早期的研究中,研究者们虽然利用RT-PCR检测到血清中存在HBV RNA,但未进一步探索其具体组成。近年报道血清HBV RNA有3.5 kb pgRNA、截断的RNA、剪切的RNA等多种存在形式[10-12]。2016年Wang 等利用HBV 特异性引物分别扩增并定量检测血清总HBV RNA(包括上述5种mRNA)和HBV 3.5 kb mRNA,发现总HBV RNA的量与3.5 kb mRNA的量无明显差异,因此推断血清中HBV RNA主要为3.5 kb mRNA,而3.5 kb mRNA包括两种mRNA,即pre-C mRNA和pgRNA。Wang等进一步设计HBV特异性引物分别扩增pre-C mRNA与pgRNA的总和,结果未检测到pre-C mRNA扩增产物,因此证实血清HBV RNA主要是3.5 kb pgRNA[7]。2018年,Bai等报道血清中HBV RNA主要是pgRNA或3’端已被降解的pgRNA,长度从3.5 kb到几百bp之间呈现出异质性,这些RNA主要存在于核心颗粒中,大多数以抗原抗体复合物的形式存在于血清中,少数也存在于完整的病毒颗粒中[13]。
本文应用的RACE法即是只能检测带A尾的HBV RNA,由于其第一步逆转录时的引物只能靶向A尾,因此只有带A尾的RNA能被检测出来。而本文应用的Sansure法则是需要DNA酶消化的一步法RT-qPCR法,该方法的好处是可以同时检测带A尾和不带A尾的RNA;缺点是应用DNA酶消化后,一方面需要质控HBV DNA是否已经被完全消化干净(试剂盒设计了相关质控对照),另一方面需考虑DNA酶对HBV RNA也有消耗作用(Sansure试剂盒无相关质控对照),这会导致HBV RNA的水平被低估。从理论上讲,Sansure法能检测的RNA种类更多,其水平应该更高。但是本研究结果显示RACE法在未治疗和治疗患者中的检测值均高于Sansure法。除了考虑到不同方法的敏感性不同,还需考虑DNA酶对HBV RNA的消耗作用可能影响了Sansure法的检测水平。
另外,我们也注意到,治疗组和未治疗组的HBV DNA水平具有显著差异,而HBV RNA的水平差异没有HBV DNA显著,在治疗组患者中这种趋势更加明显。这种情况的出现主要是由于在接受治疗的患者中大多数HBV DNA已经转阴,但是部分患者HBV RNA仍然是阳性。在62例治疗组患者中,HBV DNA阳性患者为21例,Sansure法检测的阳性患者为26例,RACE法检测的阳性患者为31例。这使得各组的平均值也有所不同,提示Sansure法的敏感性仍有改进和提升空间。
两种检测方法在治疗组患者中均比HBV DNA能检测到更多阳性患者,这主要是由于NAs治疗阻断了HBV RNA的逆转录过程,而对从cccDNA到HBV RNA的转录过程并没有影响。由于HBV RNA是cccDNA的直接下游产物,患者从HBV DNA转阴到HBV RNA转阴还需要cccDNA的耗竭作为中间过程,我们最近的一项研究阐明了这中间的时间差[15]。在血清HBV DNA与HBV RNA水平的相关性分析中,只在未治疗组患者中观察到了两者的显著相关性,而在治疗组患者中未观察到相关性。这也与上述NAs治疗阻断HBV RNA逆转录的机制有关。这部分结果也与雅培公司的报道一致[16]。虽然实验效能评价中LOD数值Sansure法比RACE法更低,但是相同样本用两个方法同时检测的检测值则是RACE法更高,这主要是由于两个方法使用的标准品不一致:RACE法采用本实验室自己合成的标准品,Sansure法采用相应试剂盒提供的标准品,其线性范围和LOD值并不具有可比性。如果HBV RNA检测能像HBV DNA的检测系统一样,有世界卫生组织(World health organization, WHO)提供的统一的以IU为单位的标准品进行标定,则不同平台的结果,其线性范围和LOD之间才具有可比性[17]。
虽然从原理上来说,本研究的两种方法检测的是不同种类的HBV RNA,即Sansure法可同时检测带A尾和不带A尾的RNA,而RACE法只能检测到带A尾的RNA。但是我们的结果显示,总体上Sansure法和RACE法的相关性和一致性较好,并可通过线性回归公式由一个检测值推算出另一个检测值。雅培公司建立了一种自动化的、同时靶向X区和C区的HBV RNA检测方法,其结果用HBV DNA的标准品作为参比时,在治疗的患者中HBV RNA的水平比HBV DNA平均高(2.45 ± 1.13)lg[16]。但在我们的结果中,治疗组患者中除了HBV DNA阴性的样本外,Sansure法和RACE法的平均检测值均低于HBV DNA的检测值。说明这两种检测方法的效能仍需进一步提高。
在未接受NAs治疗的患者中,血清HBV DNA水平与HBV RNA水平具有很好的相关性,因此用HBV DNA水平来检测HBV的复制水平是很可靠的办法。但是在接受NAs治疗的很多患者血清HBV DNA已经低于LOD,这时候血清HBV RNA即成为更有效、更可靠的监测病毒复制和预测临床疗效的标志物。我们已经发现RACE法在较多的研究报道中被应用于预测NAs和干扰素治疗应答或者病程进展,具有较好的预测效能。目前尚未见Sansure法应用于临床的报道。另外,两种方法均未见应用于NAs停药复发的预测[6, 8, 18-19]。鉴于目前尚无HBV RNA的标准检测方法,没有统一标准品,也没有批准用于临床检测的商业试剂盒,不同方法的临床应用场景还需进一步探索。因此,较合理的做法是我们在应用HBV RNA水平作为标志物用于病情监测和预测应答之前,首先需要对不同的方法学进行比较和评估,然后再挑选出合适的方法应用于临床相关研究。
