国标法测定鱼肉中组胺的方法改进
2019-04-15,,,,,
,, ,,,
(海南省食品检验检测中心,海南海口 570000)
组织胺(Histamine)是由组氨酸脱羧酶(Histidine decarboxylase,HDC)催化L-组氨酸脱羧生成的一种重要生理活性物质,是一种广泛存在于人体组织中的活性胺化合物。作为身体内的一种化学传导物质,可以影响许多细胞的反应,包括过敏、炎性反应、胃酸分泌等,也可以影响脑部神经传导[1]。鱼体内含有较多的组氨酸,当鱼体不新鲜或者发生腐败时,污染鱼体的细菌如组胺无色杆菌,就会产生脱羧酶,使组氨酸脱羧生成组胺。如果摄入的组胺超过人体的忍受范围,就会引发过敏性中毒;发生组胺中毒时,人体会产生局部或全身毛细管扩张、支气管收缩等现象,主要症状为脸红、头晕、心慌、胸闷和呼吸窘迫等,部分病人还会有眼结膜充血、瞳孔散大、视物模糊、脸发涨、口舌及四肢发麻、恶心、呕吐腹泻、寻麻疹、全身潮红、血压下降等不良反应[2-3]。国内也时有组胺中毒事件发生,2010年4月张家港市某公司15名职员因食用变质青占鱼引起组胺中毒[4],2014年8月浙江省宁海县某公司部分职工因食用鲐鱼而出现组胺中毒现象[5]等。因此,需要对组胺进行科学测定及监控。
水产品中组胺的测定方法有高效液相色谱法、薄层层析法、生物学法、分光光度法等[6]。近年来,酶联免疫吸附测定(ELISA)及毛细管电泳等方法也被用来进行组胺的检测。高效液相色谱法根据衍生方式不同,可分为柱前衍生法和柱后衍生法,检测灵敏度高,分析准确,适合于大批量样品的组胺含量测定,但成本高[7];薄层色谱法设备简单,操作容易,但相比于高效液相色谱法其灵敏度较低[8];生物化学法主要利用氧化酶与组胺反应生成过氧化氢,通过测定生成物含量确定组胺浓度,方法选择性强,灵敏度高,但存在生物固化膜不稳定等缺点[9]。
目前,我国测定鱼类中组胺的方法为国标法GB 5009.208-2016《食品安全国家标准 食品中生物胺的测定》,其中第二法分光光度法具有不需要贵重仪器、成本低等优点,但操作步骤复杂繁琐,提取效率低,重复性较差。本文在国标法第二法的基础上,通过研究改进提取方法及简化萃取步骤等方式,以期获得更为精确有效的组胺提取测定方法,为今后组胺新标准方法的建立提供科学的参考依据。
1 材料与方法
1.1 材料与仪器
新鲜带鱼、海鳗鱼、秋刀鱼、马鲛鱼、黄花鱼、红线鱼、金昌鱼、沙丁鱼 海南地区超市或农贸市场;三氯乙酸、正戊醇 分析纯,国药集团化学试剂有限公司;无水碳酸钠、氢氧化钠、盐酸、亚硝酸钠 分析纯,广州化学试剂厂;对硝基苯胺 分析纯,美国阿拉丁工业公司;二磷酸组胺 纯度>98.0%,上海安谱实验科技股份有限公司。
FW135样品粉碎机 天津市泰斯特仪器有限公司;数显多位涡旋混匀器 德国海道尔夫集团;HH-S数显恒温水浴锅 常州翔天实验仪器厂;MS1602S电子分析天平 梅特勒-托利多(常州)精密仪器有限公司;Mili-Q A10超纯水机 密理博中国有限公司;SK7200B超声波清洗机 上海科导超声仪器有限公司;UV-2600紫外可见分光光度计 岛津公司。
1.2 实验方法
1.2.1 样品处理 将市售新鲜鱼(为保证改进法普遍适用于大多数鱼类,方法改进中样品选择为随机选取海南地区常见可食用鱼,见1.1)宰杀,除去不可食用的鱼头、内脏及鱼刺部分,用自来水清洗并沥干水分,使用样品粉碎机绞碎至匀浆状态,备用。
1.2.2 方法改进 对国标法GB 5009.208-2016《食品安全国家标准 食品中生物胺的测定》中第二法分光光度法进行方法改进。
1.2.2.1 甲液的改进 对硝基苯胺难以在盐酸(1+11)溶液中完全溶解,进行长时间多次振荡、超声、加热,仍有大量对硝基苯胺呈固态无法溶解,导致标准曲线显色过浅且不成系列,上机测试后所得标准曲线线性较差。改变后甲液的配制步骤为:称取0.5 g对硝基苯胺,加5 mL浓盐酸溶解后,混匀超声(60 W,20 ℃)5 min,使对硝基苯胺完全溶解,再加水稀释至200 mL。使用该甲液,其他操作参考国标法第12.2.2条,配制标准曲线,测定其相关性。
1.2.2.2 三氯乙酸浸提条件的改进 随机取市售新鲜沙丁鱼、秋刀鱼、红线鱼、黄花鱼、金昌鱼为样品,准确称取1.2.1中鱼肉糜10.00 g,置于50 mL聚四氟乙烯离心管中,加入20 mL三氯乙酸溶液(100 g/L)后,放入60 ℃水浴锅中保温0.5 h进行浸提[10]。浸提后试样参照国标方法第12.2条操作进行分析测定,将国标法测定组胺含量与改进法进行对比。
1.2.2.3 正戊醇和盐酸提取方式的改进 随机取市售新鲜马鲛鱼、带鱼、红线鱼为样品,对按1.2.2.2中方法浸提得到的滤液进行萃取净化。将离心管振荡2 min混匀,滤纸过滤,准确吸取2.0 mL滤液置于15 mL离心管中,逐滴加入氢氧化钠溶液(250 g/L)调节pH10~12(使用pH试纸控制酸碱度),加入3 mL正戊醇,涡旋振摇提取5 min,静置分层,用洁净吸管提取正戊醇提取液(上层),重复提取并合并提取液,用正戊醇定容至10 mL,摇匀。准确吸取2.0 mL正戊醇提取液置于15 mL聚四氟乙烯离心管中,加入3 mL盐酸(1+11)溶液涡旋振摇提取5 min,静置分层,用洁净吸管吸取盐酸提取液(下层),重复提取并合并提取液,用盐酸(1+11)溶液定容至10 mL,得到测定用样品溶液。将该样品溶液按国标方法第12.2.2条操作进行测定。将国标法测定组胺含量与改进法进行对比。
1.2.2.4 戊醇和盐酸提取次数的选择 在使用1.2.2.1、1.2.2.2、1.2.2.3中方法处理的基础上,为简化国标法的测定,重新探索正戊醇及盐酸的最适提取次数(3次提取进行分析),并参照国标方法第12.2.2条操作进行测定。以市售新鲜马鲛鱼及沙丁鱼为样品,分别测定同一样品在不同提取次数下的组胺浓度,并将最终得出的最适提取次数与国标法进行对比,同时进行显著性分析。
1.2.2.5 酸提取液使用量的选择 参照国标方法第12.2.2条操作选择合适的盐酸提取液使用量,分别测定标准溶液在加入1.0 mL、2.0 mL盐酸(1+11)溶液时的吸光度,以国标法盐酸提取液使用量为参照做对比实验。
1.2.3 胺的测定 吸取1.0 mL试样提取液(经1.2.2改进法处理后盐酸提取液)于10 mL比色管中,加入3 mL碳酸钠溶液(50 g/L),3 mL偶氮试剂(甲液:见1.2.2.1;乙液:5 g/L亚硝酸钠溶液,现用现配。吸取甲液5 mL、乙液40 mL混合)。加水至10 mL,混匀,放置10 min。用分光光度计在480 nm下测量吸光值。
样品中组胺的含量按下式计算:
式中:X:试样中组胺的含量(mg/100 g);m1:试样中组胺的吸光度值对应的组胺质量(μg);V1:加入三氯乙酸溶液的体积(mL);10:第一个是正戊醇提取液的体积(mL),第二个是盐酸提取液的体积(mL);m2:取样量(g);2:第一个是三氯乙酸提取液的体积(mL);第二个是正戊醇提取液的体积(mL);V2:盐酸提取液的体积(mL);100、1000:换算系数。
1.2.4 准确度实验 以新鲜海鳗鱼,红线鱼,带鱼为样品,按1.2.2中改进法处理,在1.2.3测定中,分别加入组胺10、20、40 μg,后定容至10 mL。加标后测定其组胺浓度,同时计算加标回收率。加标回收率计算公式为:
回收率(%)=(测得值-本底值)×100/加标值。
1.2.5 密度实验 取新鲜红线鱼,带鱼,黄花鱼,按1.2.2中改进法处理并进行测定,每个样品平行测定10次,同时计算相对标准偏差。
1.3 数据处理
所有实验重复3次,实验数据采用平均值表示,组间进行显著性分析(p=0.05),数据处理及图表绘制均使用Microsoft Excel 2007软件。
2 结果与分析
2.1 方法改进实验结果分析
2.1.1 甲液的改进效果 由图1可知,组胺在0~20 μg范围内吸光值呈现良好线性关系,y=0.0279x-0.0012,相关系数r=0.9991。改进法中对硝基苯胺可完全溶解,因此使用改进法进行实验,得到的标准曲线显色正常,并且吸光度可呈良好线性关系。

图1 改进甲液所得组胺浓度标准曲线Fig.1 Standard curve of histamine concentration for preparing A solution by modified method
2.1.2 氯乙酸浸提条件的改进效果 由表1可知,改进后浸提效果与国标法大致相同,但现行的国标法在前处理时,需用三氯乙酸溶液浸泡2~3 h,因此对比可见,改进法浸提所需时间短,效率更高。

表1 不同条件下三氯乙酸浸提组胺含量对比(mg/100 g)Table 1 Comparison of histamine concentration of trichloroacetic acid solution under different conditions(mg/100 g)
2.1.3 戊醇和盐酸提取方式的改进效果 由表2可以看出,使用离心管涡旋振荡法提取样品,所得测定结果RSD为1.19%~5.50%;而使用国标法时,RSD为11.39%~16.30%,且对于同一样品,离心管涡旋振荡法所测结果数值高于国标法。以此可知,离心管涡旋振荡法提取效果及精密度均优于国标法。这是由于使用分液漏斗进行提取,过程操作复杂,步骤繁琐,且在分液漏斗多次转移过程中会有部分滤液与器皿粘连,导致样品损失,误差偏大,而改进法简化了转移及提取步骤,有效减少了提取过程中的样品损失。
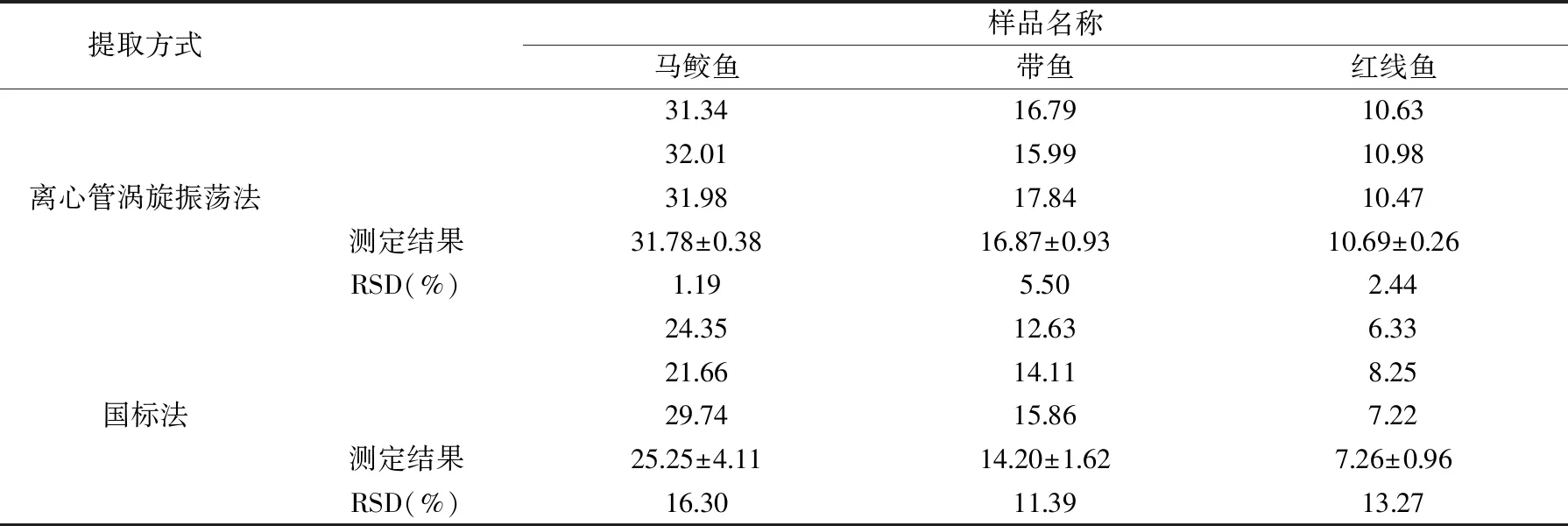
表2 不同提取方式含量测定结果对比Table 2 Comparison of the determination results of different extraction methods
2.1.4 戊醇和盐酸提取次数的选择 由表3可知,涡旋振荡法提取,正戊醇提取3次,盐酸提取2次时,提取效果与国标法大致相同;由图2对比,不同盐酸提取次数对组胺测定结果无显著性差异(t=0.44,p>0.05)。因此,使用改进法进行提取后,只需正戊醇提取3次,盐酸提取2次,既可完成滤液的萃取。

表3 不同提取次数组胺含量结果对比(mg/100 g)Table 3 Comparison of histamine concentration of different extraction times(mg/100 g)

图2 不同盐酸提取次数结果对比图Fig.2 Comparison of the precision of different hydrochloric acid extraction times
2.1.5 盐酸提取液使用量的选择 由表4可以看出,加入2.0 mL盐酸溶液的标液吸光值很小且不稳定,而加入1.0 mL盐酸溶液时,所测吸光值正常且有较好重复性。因此,改进法中盐酸提取液使用量应为1.0 mL。这是由于在国标法中,样品溶液酸度过高,会造成溶液浑浊,从而影响显色,使测定结果偏低。窦红顺[11]、王新惠等[12]的研究也证明了这一点。而改进法通过减少盐酸提取液使用量,从而保证了样品管与标准管酸度的一致。

表4 不同盐酸溶液加入量吸光值对比Table 4 Comparison of absorbance value of different hydrochloric acid addition
2.2 准确度实验
由表5可见,1.2.2中改进法测定回收率分别为92.90%~94.70%、91.50%~94.10%、100.20%~102.20%,由此可知,该改进法具有较高准确度。

表5 样品加标回收率试验Table 5 Test of recovery rate of sample adding
2.3 精密度实验
由表6可见,改进法1.2.2的测定RSD在1.84%~2.32%,精密度较高。

表6 方法精密度试验Table 6 Precision test of the method
3 结论
对国标法(GB 5009.208-2016)第二法组胺的测定进行了改进。将对硝基苯胺溶液的配制溶剂改为浓盐酸;选择水浴60 ℃保温0.5 h的方式代替室温浸泡2~3 h;并改进了萃取步骤,提取过程采用离心管旋涡振荡提取代替分液漏斗振摇提取,提高了提取效率并获得了更优的提取效果;改盐酸提取3次为提取2次,与国标法相比无显著性差异(t=0.44,p>0.05),提取效果不变而效率提高;改取盐酸提取液为1.0 mL,保证了样品与标准系列取样量的一致性。该改进法操作简单,快速,具有较高的精密度和回收率,可以更好地用于鱼类中组胺的测定。
