固相萃取-气相色谱法测定合成气制烯烃产物中的含氧化合物
2014-12-26刘俊彦田文卿李继文顾松园
刘俊彦 , 田文卿, 李继文, 王 川, 顾松园
(上海石油化工研究院表征分析部,上海201208)
合成气制烯烃(syngas-to-olefin,SGTO)是指以合成气(CO +H2)为原料,制得C2~C4烯烃及副产汽、柴油等馏分的反应[1-3]。合成过程中主要副产物为含氧化合物,主要包括醛、酮、醇等,并且随着碳数增加,含氧化合物种类增多。含氧化合物的测定对于催化剂及动力学反应机理的研究有着不可忽视的作用。因此开发SGTO 复杂烯烃产物体系中微量含氧化合物分析方法意义重大[4,5]。
复杂烯烃产物体系的现有分析方法可分为两大类:一类是以单一毛细管柱分离分析组分;另一类是以多维色谱和阀切换的方式进行分离分析[6-8]。大多数分析方法均未对烯烃样品作预处理,因此存在大峰覆盖小峰和拖尾重叠等问题,进而导致微量组分(如含氧化合物杂质等)分析结果不准确。Huff Jr等[6]给出了C1~C30的烷烃、烯烃、异构烷烃和少数环烷烃的分析结果,对含氧化合物仅考虑了醛、直链醇和甲基酮。Snavely 等[7]报道了复杂烯烃产物体系中的伯醇分析结果。Dictor 等[8]给出复杂烯烃产物体系中伯醇、醛和酮的分析结果。使用柱色谱分离技术可以对复杂烯烃产物进行预处理。柱色谱分离技术广泛应用于馏分油、重质油、煤液化油和岩石可溶有机物的分离和分析,主要使用极性不同的淋洗液洗脱产物,实现复杂体系中族组分分离。樊改仙等[9]以两步柱色谱法对Fischer-Tropsch 合成(F-T synthesis)液相产物冷阱油进行预处理,实现烷烃、烯烃及有机含氧化合物的族分离,并采用GC-MS 对各族组分进行了分离鉴定。但柱色谱分离耗时较长,并且需要专业的柱色谱分离毛细管与较熟练的操作技能,同时需要的样品量也较大,因此对于常规样品预处理而言稍显复杂。
固相萃取技术(SPE)自20 世纪70 年代后期问世以来,由于其高效、可靠且简单实用而在许多领域得到了广泛应用[10-15],是近年来发展迅速的样品前处理技术之一。一般针对目标化合物的性质,采用合适的萃取填料与洗脱条件进行样品预处理,以达到富集目标分析物与简化本底的作用。近几年来,SPE 技术也逐渐在石油化工产品的分析中得到广泛应用。徐延勤等[16]采用Ag-SiO2固相萃取技术将含烯烃柴油分离为饱和烃组分和芳烃、烯烃混合组分,并采用气相色谱-质谱和核磁共振等手段考察其分离效果,采用气相色谱/场电离-飞行时间质谱(GC/FI-TOF MS)测定芳烃、烯烃混合组分的烯烃含量和碳数分布。罗凡等[17]采用固相萃取-高效液相色谱法测定了茶油中的酚酸类物质,使用二醇基固相萃取小柱(Diol-SPE)建立了同时分离、检测茶油中23 种酚类物质的方法。
本文使用固相萃取技术对SGTO 复杂烯烃产物进行了样品预处理,弥补了单根气相色谱柱分离的局限性。首先采用C18 SPE 小柱进行预处理,优化了甲醇/水洗脱条件,实现了分离样品中含氧化合物与烃类组分的目的。再使用气相色谱-质谱(GCMS)对微量的高碳数含氧化合物进行定性、定量分析。本方法提高了目标化合物分析的灵敏度并降低了本底杂质对分析结果的干扰。
1 实验部分
1.1 仪器与试剂
Agilent 7890 气相色谱仪-5975 质谱检测器;HP-Innowax 毛细管色谱柱(60 m×0.25 mm×0.25 μm);ProElut C18-U 小柱(200 mg/3 mL,DIMKA公司)。正丙醇、正丁醇、正戊醇、正己醇、正庚醇、正壬醇、2-丁酮、2-戊酮、2-己酮、2-庚酮、2-辛酮、2-壬酮均购自Sigma 公司,纯度均大于99%。丙酮、乙醇、甲醇、正己烷为分析纯,Milli-Q 超纯水。
1.2 标准样品的配制
准确称取正构2-酮、正构醇标准品,用正己烷定容,配制标准储备液。准确移取上述储备液,用正己烷定容,配成1#~4#标准溶液,质量浓度见表1。
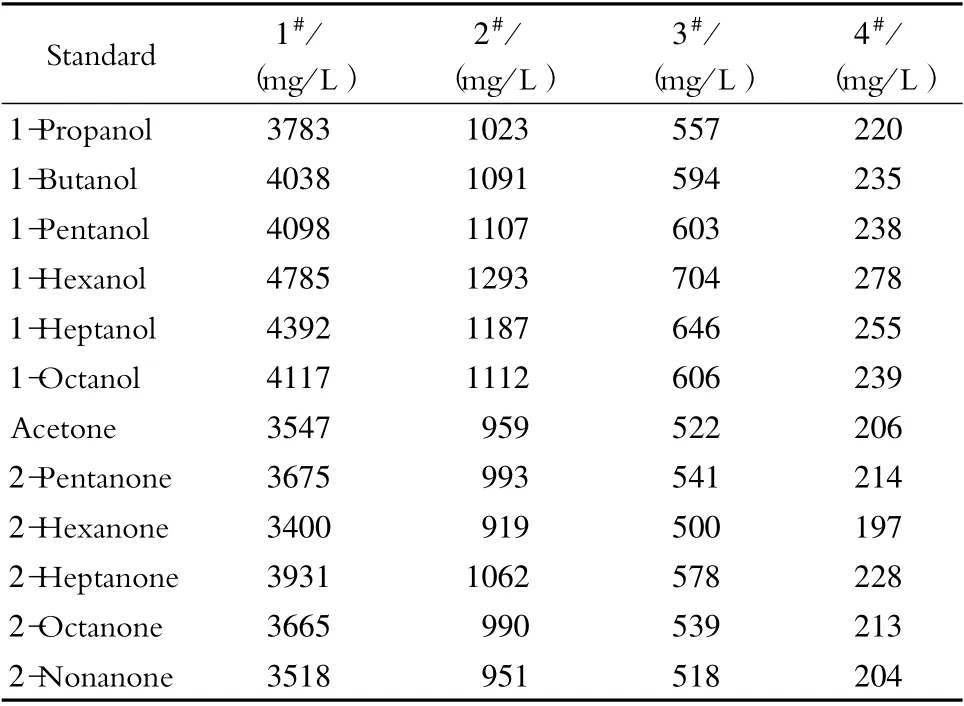
表1 标准溶液的质量浓度Table 1 Mass concentrations of the standard solutions
1.3 样品预处理
依次使10 mL 甲醇、10 mL H2O 流经C18 小柱,活化并平衡小柱,弃去流出液;加入100 μL 标准溶液或SGTO 样品,收集流出液;加入2.5 mL 60%(v/v)的甲醇水溶液,收集馏分,并与上样后的流出液合并,定容至2.6 mL。整个操作流程中保持C18小柱湿润。
1.4 GC-MS 分析条件
载气(He)流量为0.6 mL/min。柱温程序:初始温度50 ℃,保持10 min;以升温速率5 ℃/min升至220 ℃,保持10 min。分流比为10∶1,进样体积为1.0 μL。进样口气化温度为250 ℃,质谱检测器离子源温度为230 ℃,四极杆温度为150 ℃,界面温度为280 ℃,电离能量为70 eV。用全扫描方式采集数据,扫描范围m/z 20 ~550。
1.5 GC-FID 分析条件
载气(N2)流量为1 mL/min。柱温程序:初始温度50 ℃,保持10 min;以升温速率5 ℃/min升至220 ℃,保持10 min。分流比为10∶1,进样体积为1.0 μL。进样口气化温度为250 ℃,FID 检测器温度为250 ℃,H2流量为40 mL/min,空气流量为450 mL/min,尾吹气(N2)流量为20 mL/min。
1.6 实际样品的测定
测定正构醇与正构2-酮相对正己烷的FID 校正因子,取SGTO 反应装置的油相样品中的0 ~200℃馏分进行样品预处理与含氧化合物分析。
2 结果与讨论
2.1 SPE 洗脱条件的优化
C18 小柱填料的基底为硅球,利用硅烷化反应在硅球表面上键合了十八烷烃链,并通过端基封端反应封闭了裸露的硅羟基。由于C18 填料表面疏水性较强,因此对极性化合物保留较弱,可通过调整洗脱液条件区分极性与弱极性化合物。常用C18小柱洗脱液为不同浓度的甲醇水溶液,随着甲醇浓度提高,洗脱能力增强。
同类含氧化合物的极性随着碳数增加而减弱,其在C18 小柱上的保留行为可能与部分弱极性化合物相近。SGTO 产物中弱极性化合物包括大量的烯烃产物与少量的芳烃副产物。因此有必要考察不同浓度甲醇水溶液的洗脱馏分组成,优化洗脱条件,避免弱极性烃类与含氧化合物在C18 小柱上的共流出现象。而同碳数的同类含氧化合物,可以大致分为正构体与非正构体。由于分子间相互作用力的影响,正构含氧化合物的烷烃链与C18 填料表面的烷烃链具有较强的相互作用,非正构含氧化合物与C18 填料的相互作用力则相对较弱。如己醇可以大致分为正己醇与非正己醇两大类,正己醇在C18 小柱上的保留是所有己醇的同分异构体中最强的。因此在研究洗脱馏分组成的实验中,以正构含氧化合物洗脱是否完全作标尺,表征某一碳数下的某一种类含氧化合物是否被完全洗脱。
活化C18 小柱后上样100 μL 1#标准溶液,依次使用含0、10%、20%、30%、40%、50%、60%、70%、80%、90%与100%(v/v,下同)的甲醇水溶液洗脱,洗脱液的体积为1.5 mL,收集馏分并使用气相色谱进行分析。以正构含氧化合物的峰面积为纵坐标,不同甲醇含量为横坐标作图(见图1)。以正己醇为例,甲醇含量在0 ~20%范围内,正己醇的峰面积逐渐增大,并在20% 时达最大值;随着洗脱液中甲醇含量的继续增加,正己醇峰面积逐渐减小,在40%甲醇水溶液中没有检出正己醇的明显信号,因此可以认为在该洗脱条件下,己醇(包括正己醇与其同分异构体)完全从C18 小柱上流出。分析实际样品的结果表明,随着甲醇的含量大于60% 并继续升高,少量芳烃开始从C18 小柱上洗脱下来,70% 时烯烃主产物开始从C18 小柱上洗脱下来,因此确定60%甲醇水溶液为最佳洗脱溶液。
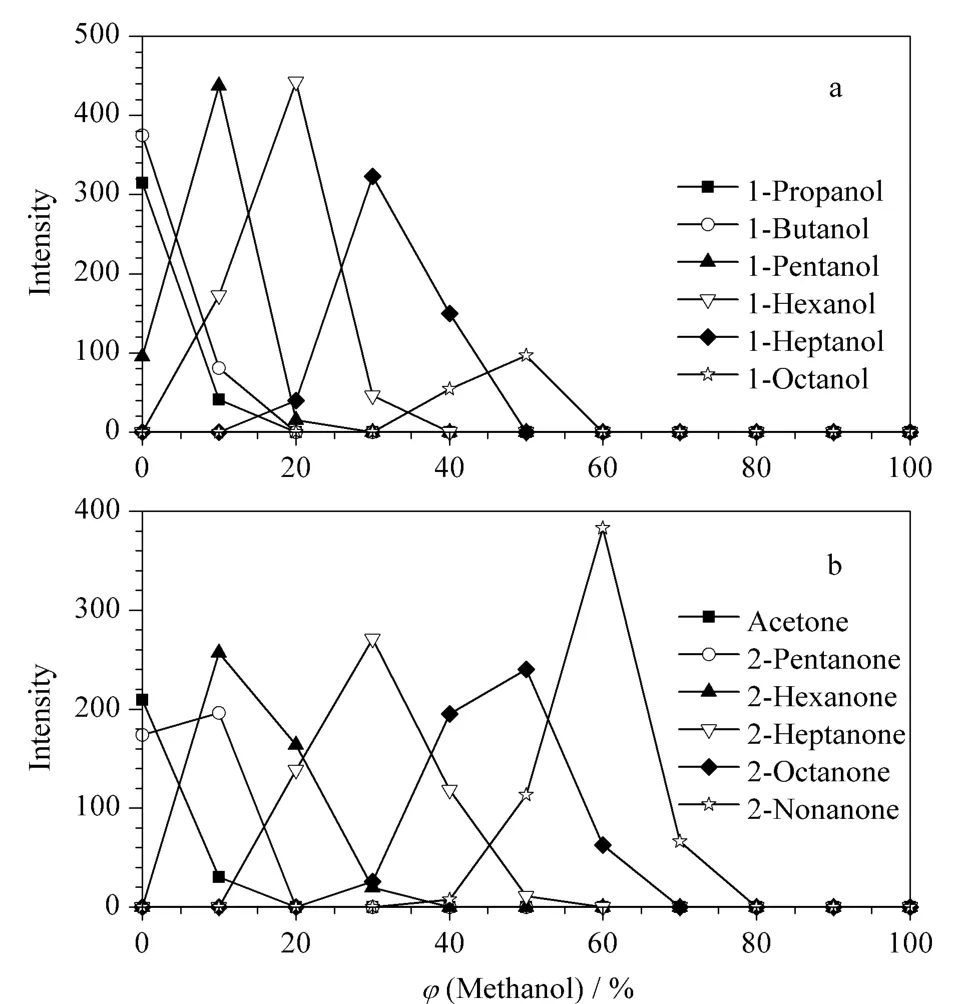
图1 洗脱液中甲醇体积分数对(a)正构醇和(b)正构2-酮标准品信号强度的影响Fig.1 Effect of the volume percentage of methanol in elution solution on the signal intensities of (a)n-alkanol and (b)n-ketone standards
在相同的上样条件下,依次用8 组60% 甲醇水溶液洗脱,每组体积为0.5 mL,依次收集馏分并使用气相色谱进行分析(见图2)。可以看到,2 mL 60%甲醇水溶液将大多数含氧化合物全部洗脱,在第7 组洗脱液的馏分中检出少量2-壬酮,但仅占2-壬酮总量的4.9%。同时,实际样品的分析结果表明,当60%甲醇水溶液的洗脱体积大于2.5 mL 时,少量芳烃副产物开始从C18 小柱上洗脱下来,此类芳烃副产物在色谱上的保留时间与部分目标含氧化合物相近,可能会影响分析结果,因此确定洗脱液为2.5 mL 60%甲醇水溶液。

图2 洗脱液的体积对(a)正构醇和(b)正构2-酮标准品信号强度的影响Fig.2 Effect of the volume of elution solution on the signal intensities of (a)n-alkanol and (b)nketone standards
2.2 回收率与重复性
取两份2#标准样品各100 μL,一份进C18 小柱预处理后收集馏分并使用PE 管定容至2.6 mL,一份使用60% 甲醇水溶液稀释并使用PE 管定容至2.6 mL。在相同仪器条件下进行色谱分析,比较标准样品在预处理前后的色谱峰面积并计算回收率,结果见表2。相对于未进行预处理的样品而言,醇类含氧化合物的方法回收率在88% ~98% 之间,酮类含氧化合物的方法回收率在64% ~87% 之间。酮类含氧化合物的回收率较低,可能由于其羰基与C18 填料具有较强的分子间作用力,并且随着酮类含氧化合物的碳数逐渐增加,非极性增强,分子间作用力增大,导致回收率下降。醇类含氧化合物与C18 填料的不可逆吸附现象不显著,方法的回收率较理想。
在相同操作条件与仪器工作条件下,对2#标准样品平行进行6 次预处理操作,重复性实验结果见表2。该方法对于醇类含氧化合物的相对标准偏差(RSD,n =6)小于3%,对于酮类含氧化合物的RSD (n =6)小于3%。该预处理方法重复性理想。
2.3 线性范围和定量限
对1#~4#标准样品进行预处理,将流出液定容至2.6 mL,分析各标准品的信号强度。在相同预处理条件下,分别以正构醇与正构2-酮标准品的质量浓度(X,mg/L)为横坐标,峰面积(Y)为纵坐标绘制标准曲线,以10 倍信噪比确定定量限(LOQ),结果见表3。标准品在197 ~4 785 mg/L 内有较好的线性,醇类与酮类含氧化合物的线性相关系数均大于0.99。可以认为在该线性范围内,酮类含氧化合物经过预处理后损失的量与其含量呈线性关系。
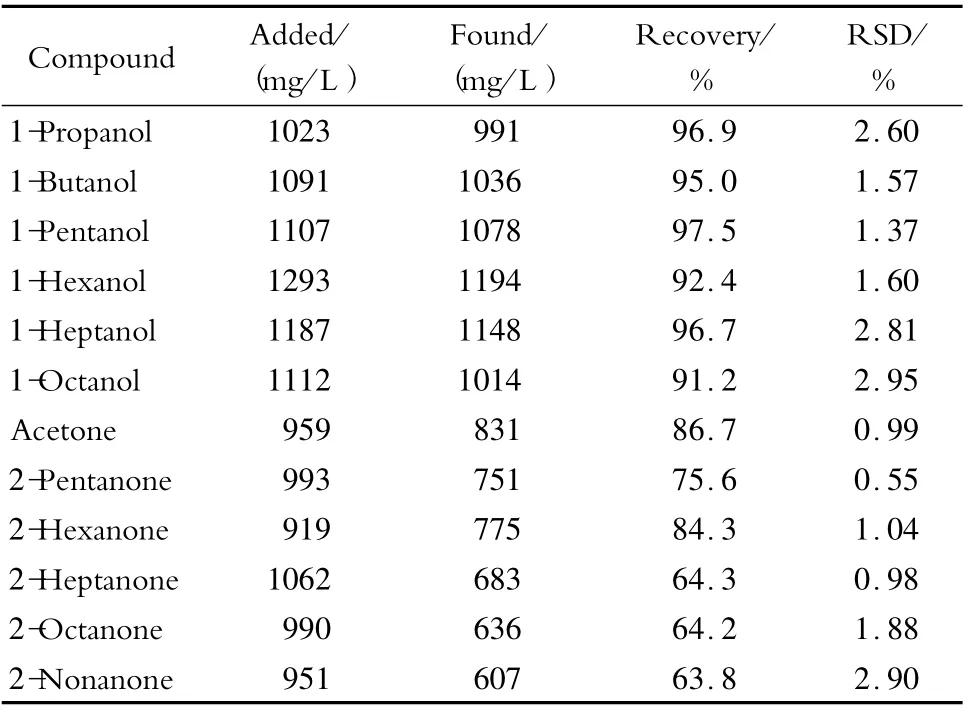
表2 标准样品回收率与重复性(n =6)Table 2 Repeatabilities and recoveries of the standard samples (n =6)
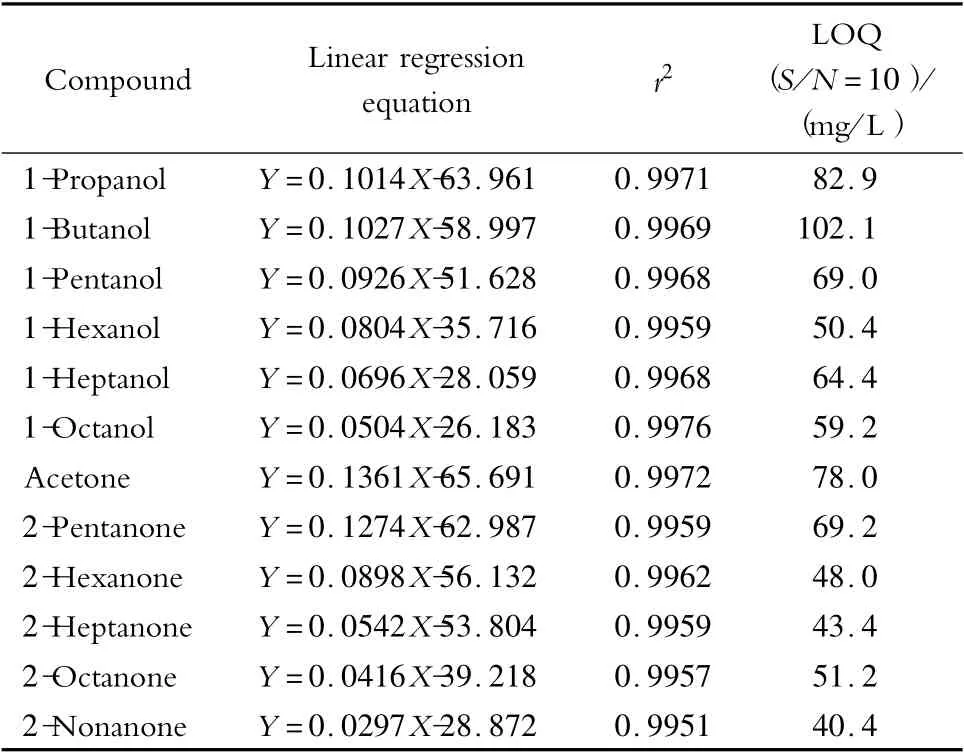
表3 标准样品的线性曲线、回归系数与定量限Table 3 Linear regression equations,regression coefficients (r2 ) and LOQs of the standard samples
2.4 实际样品的分析
SGTO 产物中以弱极性的烷烯烃为主要成分,包括芳烃与含氧化合物。使用C18 小柱处理样品后,烷烯烃在小柱上有一定的保留,极性较强的含氧化合物则易与烷烯烃分离,避免了GC-MS 直接分析样品造成的峰重叠与峰干扰现象。
使用GC-MS 对实际样品进行定性分析,比较SGTO 产物预处理前后的总离子流色谱图(见图3)发现,由于SGTO 产物组成复杂且烯烃含量较高,无法通过GC-MS 直接分析鉴定微量含氧化合物。样品经过C18 小柱处理后,不存在烯烃等主要产物对含氧化合物的出峰干扰。共鉴定出67 种含氧化合物,其中主要以正构的醇、酮为主。
GC-MS 也可以通过特征离子定量,但由于实际样品中含氧化合物种类繁多,因此使用GC-MS 定量稍显繁琐。对于相同碳数的同类型含氧化合物而言,其在FID 上具有相似的响应因子,因此使用其正构2-酮、正构醇的响应因子作为同碳数酮、醇的FID 响应因子,对67 种含氧化合物进行定量。使用相同的预处理步骤分别处理100 μL 标准品与100 μL 实际样品,分别将最终收集的流出液定容至2.6 mL,在相同的GC-FID 条件下对实际样品中的含氧化合物进行定量分析,结果见表4。
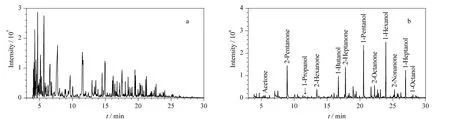
图3 (a)未经和(b)经过C18 柱预处理的SGTO 产物的GC-MS 总离子流色谱图Fig.3 Total ion current chromatograms for the SGTO products (a)before and (b)after C18 column pretreatment

表4 SGTO 产物中的含氧化合物分析结果Table 4 Analysis results of the oxygenates in SGTO products
3 结论
采用C18 小柱将SGTO 复杂产物分离为含氧化合物与烃类,从而降低了待测样品的复杂性,提高了含氧化合物分析的灵敏度。验证了复杂烯烃体系中微量含氧化合物杂质准确分析方法的可能性。
该预处理方法具有良好的线性,成功定量SGTO产物中67 种含氧化合物。该预处理方法操作简单、快速、样品需求量小,使用常规耗材并在10 min 内能够完成样品的预处理工作。分析结果对SGTO 工艺催化剂、动力学深入研究提供了必要的基础数据。
由于反应原料与传统石油化工存在较大差异,因此传统化工分析方法不适用于新型煤化工的反应产物。本研究工作探索了固相萃取技术应用于煤化工反应产物分析的可能性,可以进一步拓展至特异性功能材料用于杂元素副产物的分析,为煤化工产品分析提供了一种新的技术手段与思路。
[1] Yang H J. Shandong Industrial Technology (杨海军. 山东工业技术),2013(15):122
[2] Hu X T,Li Z Y,Huang G X. Petrochemical Technology(胡徐腾,李振宇,黄格省. 石油化工),2012,41(8):869
[3] Jiao Z K,Zhu L X,Sun J C,et al. Industrial Catalysis(焦祖凯,朱连勋,孙锦昌,等. 工业催化),2013,21(7):10
[4] Zhang L P,Xin Z. Applied Chemical Industry (张丽平,辛忠.应用化工),2009,38(5):731
[5] Dong L,Yang X P. Petrochemical Technology (董丽,杨学萍.石油化工),2012,41(10):1201
[6] Huff Jr G A,Satterfleld C N,Wolf M H. Ind Eng Chem Fundam,1983,22(2):258
[7] Snavely K,Subramaniam B. Ind Eng Chem Res,1997,36:4413
[8] Dictor R A,Bell A T. Ind Eng Chem Fundam,1984,23:252
[9] Fan G X,Xu Y Y,Li Y,et al. Chinese Journal of Chromatography (樊改仙,徐元源,李莹,等. 色谱),2007,25(6):893
[10] Ma N,Chen L,Xiong F. Shanghai Environmental Sciences(马娜,陈玲,熊飞. 上海环境科学),2002,21(3):181
[11] Wu M,Liu Z L,Tian S B,et al. Petroleum Processing and Petrochemicals (吴梅,刘泽龙,田松柏,等. 石油炼制与化工),2006,37(7):58
[12] Ye C P,Feng J,Li W Y,et al. Journal of Taiyuan University of Technology (叶翠平,冯杰,李文英,等. 太原理工大学学报),2010,41(5):661
[13] Zhou R,Sha X,Zhao G H,et al. Analytical Instrumentation(周蓉,沙雪,赵国辉,等. 分析仪器),2012(3):95
[14] Zhao H X,Liu H P,Yan Z Y. Chinese Journal of Chromatography (赵海香,刘海萍,闫早婴. 色谱),2014,32(3):294
[15] Jia Y Y,Tan J H,Xu C,et al. Chinese Journal of Chromatography (贾妍艳,谭建华,徐晨,等. 色谱),2014,32(3):263
[16] Xu Y Q,Zhu X Y,Liu Z L,et al. Acta Petrolei Sinica:Petroleum Processing Section (徐延勤,祝馨怡,刘泽龙,等.石油学报:石油加工),2010,26(3):431
[17] Luo F,Fei X Q,Fang X Z,et al. Journal of Instrumental Analysis (罗凡,费学谦,方学智,等. 分析测试学报),2011,30(6):696
