白术清炒过程中颜色变化与5-羟甲基糠醛的相关性分析及拐点研究
2024-03-07王宏贤史可王春燕李元红康冰亚陈天朝
王宏贤,史可,王春燕,李元红,康冰亚,陈天朝,✉
(1. 河南中医药大学第一附属医院,河南 郑州 450000; 2. 河南中医药大学,河南 郑州 450008)
白术为菊科植物白术(AtractylodesmacrocephalaKoidz.)的干燥根茎,南北朝前无白术、苍术之分,统称为“术”,《神农本草经》收载了“术”,列为上品,宋代本草开始区分白术、苍术,自此二者明确分用[1-2]。白术主要含有挥发油类、内酯类、多糖等化学成分,具有健脾益气、燥湿利水、止汗、安胎的功效,可发挥调节胃肠运动、保肝、抗炎、抗肿瘤等药理作用[3-4]。历代文献对白术炒法记载最多,可见炒法为白术最主要的炮制方法,主要分为清炒和加辅料炒两类[5],炒制后燥性减弱,健脾作用增强[6]。炮制品外观颜色是判断其炮制程度及品质最直观的指标,与其内在化学成分变化密切相关,可以有效反映其质量优劣。本实验分析清炒过程中白术颜色、氧化值、5-羟甲基糠醛(5-HMF)含量的动态变化及相关性,并通过其炮制过程中各指标的动态变化情况分析炮制拐点,以期为白术清炒过程中颜色变化及炮制程度的判断及中药炮制品质量控制的数据化提供参考。
1 仪器与材料
1.1 仪器
炒药机(型号:CY-25,温州顶历医疗器械有限公司);电子天平(型号:DT-300,上海医用激光仪器厂常熟分厂);高速万能粉碎机(型号:FW-600,科伟永兴仪器有限公司);高效液相色谱仪(型号:1260,美国Agilent 公司);薄层成像仪(型号:TLC VISUALIZER2型,瑞士卡玛公司)。
1.2 饮片与试剂
白术(安徽人民中药饮片有限公司,批号:201202)经河南中医药大学第一附属医院陈天朝主任药师鉴定符合2020 版《中华人民共和国药典》一部饮片项下规定的质量标准。
5-羟甲基糠醛(5-HMF,上海源叶生物技术有限公司,批号:B21832,纯度 ≥ 98%);甲醇(Sigma 试剂有限公司,色谱纯);甲醇(天津市永大化学有限公司,分析纯);95%乙醇(天津市永大化学有限公司,分析纯);硫代硫酸钠(郑州派尼化学试剂厂,分析纯);碘化钾(汕头市西陇化工厂有限公司,分析纯);高锰酸钾(深圳市南山区锦久辰化工品商行,分析纯);浓硫酸(天津市永大化学有限公司,分析纯);纯化水(河南中医药大学第一附属医院制剂车间)。
2 方法
2.1 实验因素及因素水平的确定
本研究基于白术单味药材的清炒,由“火候”出发确定炮制过程中起决定因素的主要是炒制时的温度和时间,因此选择炮制时间与炮制温度两个影响因素作为研究目标。炮制过程使用滚筒式炒药机进行药材的炒制,CY-25 炒药机温控变化刻度为5 ℃/次,且经过前期预实验测得白术药材在180 ℃下炒制20 min 已呈现炭化状态,故而选取终点温度为180 ℃,每2 min为一变化梯度,设置11个变化水平,炮制时间共22 min。
2.2 样品的制备
将生白术饮片按大小均匀分类,分成11 份,每份(50 ± 5)g,另取1份生品饮片备用,共12份样品。打开滚筒式炒药机,功率7 kW,滚筒转速20 r/min,固定炮制温度为180 ℃,待炒药机稳定在180 ℃后放入药材,并开始计时,炮制时间范围为0~22 min,具体见表1,待到达炒制时间后,关闭炒药机,取出药材,放置至常温,制得清炒白术的不同炮制样品。

表1 白术不同样品的制备参数
2.3 颜色值测定
2.3.1 图像采集
将炒制后的白术饮片按编号依次排列,分别置于干净透明的培养皿上,然后放入薄层扫描仪中,选择反射光照射,采集图像,图像信息见图1。

图1 白术不同样品薄层扫描图
2.3.2 RGB数据采集及HSI数值转换
使用MATLAB R2016软件将采集好的图像依次通过程序代码分析,生成各自的RGB(红绿蓝)图像,从每个样品RGB 图像中均匀选取30 个点,取平均值,然后将平均值进行HSI 转换,得到(色调H,饱和度S,亮度I)数据。HSI与RGB转换公式如下。
2.4 氧化值测定
精密称取白术不同样品饮片细粉2.0 g,置于500 mL 圆底烧瓶中,加水200 mL,混匀后接蒸馏装置,精确收集前50 mL 蒸馏液,备用。精密称取KMnO40.158 g,纯水溶解并定容于500 mL 容量瓶内,配制成浓度为0.002 mol/L 的KMnO4溶液,转移至棕色试剂瓶内保存备用。精密称取Na2S2O33.16 g,纯水溶解并定容于1 000 mL 容量瓶中,配制成浓度为0.02 mol/L 的Na2S2O3溶液,转移至棕色试剂瓶内,缓缓煮沸10 min,冷却,放置两周后滤过备用。根据文献[7-8]分别用移液管准确量取5 mL 上述蒸馏液于滴定瓶内,加入5 mL H2SO4水溶液(硫酸∶水 = 1∶4)和10 mL 0.002 mol/L KMnO4溶液,振荡均匀,室温下静置30 min,然后加入5 mL 0.15g/mL KI溶液,用Na2S2O3溶液进行滴定,当溶液由深黄色变成浅黄色时,加入淀粉指示剂1 mL,继续滴定,当颜色变为无色时,记录消耗的Na2S2O3溶液体积为A(mL)。另外进行空白试验,用等量的水重复以上操作,记录消耗Na2S2O3溶液体积为B(mL)。平行测定3次,取平均值。
OX= (B-A) ×C× 200/(5 × 0.002 ×V×M)
其中:OX为氧化值,即蒸馏液所消耗的KMnO4的毫升数(mL/g);B为空白实验消耗的Na2S2O3溶液的体积(mL);A为样品消耗的Na2S2O3溶液的体积(mL);C为Na2S2O3溶液的浓度(mol/L);V为馏分的取样量(mL);5 为硫代硫酸钠与高锰酸钾的反应摩尔当量比;0.002 为KMnO4溶液的浓度(mol/L);200 为样品体积(mL);M为称取样品的质量。
2.5 5-HMF含量测定
2.5.1 对照品溶液的制备
精密称取5-HMF 对照品20 mg 于100 mL 容量瓶内,加50%甲醇溶解并定容至刻度线,摇匀,即得对照品溶液。
2.5.2 供试品溶液的制备
精密称取白术不同样品细粉0.5 g,分别置于具塞锥形瓶中,加入80%甲醇20 mL,称重,超声处理50 min,冷却至室温,称重,用甲醇补足失去的重量,过滤,收集滤液于50 mL 容量瓶,并定容于刻度,取上清液2 mL,离心5 min(12 000 r/min),用0.45 μm 微孔滤膜过滤,即得供试品溶液。
2.5.3 色谱条件
色谱柱:Agilent 反向色谱柱HC-C18(5 μm,4.6 mm × 250 mm);流动相:甲醇-水(5∶95);检测波长:284 nm;体积流量:1.0 mL/min;柱温:30 ℃;进样量:10 μL。色谱图见图2。

图2 对照品和供试品HPLC色谱图
2.5.4 线性关系考察
分别精密吸取1、2、4、6、8、10 mL 对照品溶液于25 mL容量瓶中,加甲醇定容至刻度,制成不同浓度的对照品溶液,按“2.5.3”项下色谱条件分别进样测定,以峰面积为纵坐标,对照品浓度为横坐标,绘制标准曲线,得方程Y= 2 296.9X+ 0.299 1,R2= 0.999 1。表明5-HMF在0.008~0.080 μg/μL范围内线性关系良好。
2.5.5 精密度考察
精密吸取5-HMF 对照品溶液,按“2.5.3”项下色谱条件测定,连续测定6次,记录峰面积,计算RSD 值,经计算RSD值为0.003 9%,说明此仪器精密度良好。
2.5.6 重复性考察
精密称取白术-5号样品细粉6份,按“2.4.2”项下方法制备供试品溶液,按“2.5.3”项下色谱条件进样,记录峰面积,计算RSD 值,经计算RSD 值为0.077 6%,说明该测定方法重复性良好。
2.5.7 稳定性考察
精密吸取白术-5 号供试品溶液,分别于0、10、20、30、40、50、60 min不同时间点,按“2.5.3”项下色谱条件进样测定,记录峰面积,计算RSD值,经计算RSD值为0.085 5%,说明该供试品溶液在60 min内稳定性良好。
2.5.8 加样回收率考察
精密称取白术-5 号样品细粉6 份,每份1.0 g,精密加入1 mL 对照品溶液,按“2.5.2”项下方法制备供试品溶液,按“2.5.3”项下色谱条件进样,记录峰面积,计算回收率及RSD 值,经计算5-HMF 的RSD 值为0.99%,平均加样回收率为98.86%,加样回收率均在95%~105%范围内,说明此方法具有可行性。
2.5.9 含量测定
按照“2.5.2”项下制备供试品溶液,再按照“2.5.3”项下色谱条件进样测定,记录峰面积,计算5-HMF含量。
3 结果
3.1 白术不同样品颜色值、氧化值、5-HMF 含量测定结果
对12批白术样品进行测定,测定结果见表2。
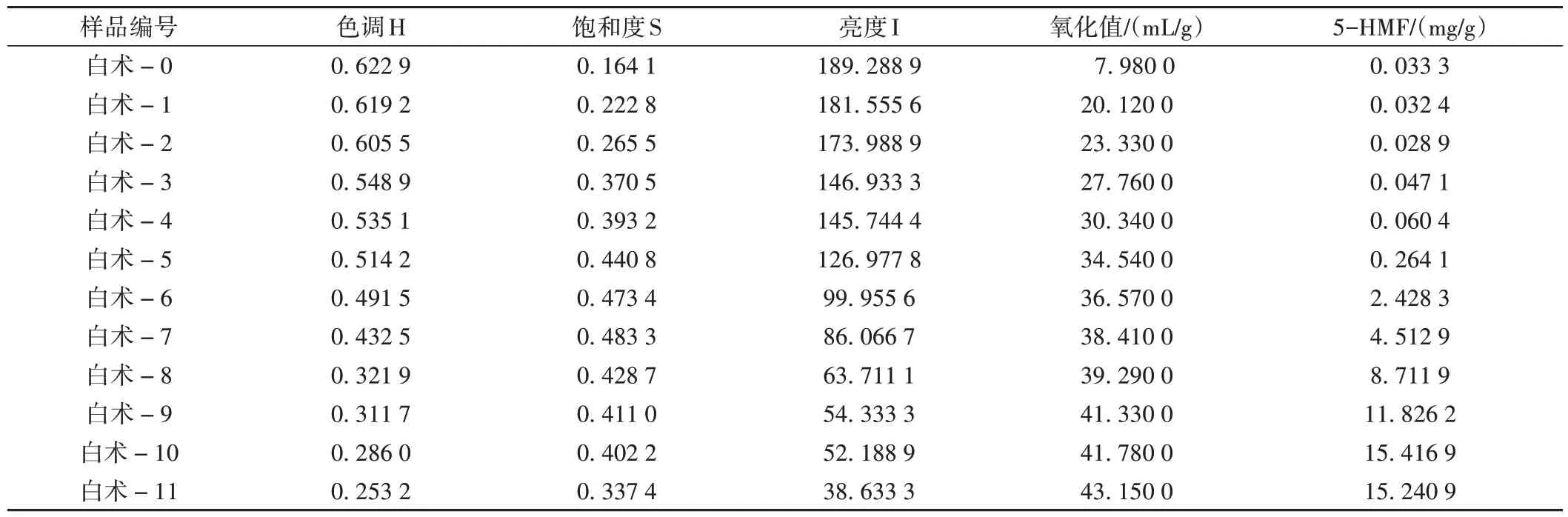
表2 白术不同样品颜色值、氧化值、5-HMF含量测定结果
3.2 白术清炒过程中颜色值、氧化值、5-HMF 含量的动态变化
白术不同样品在180 ℃炮制温度下,其色调H、亮度I均会随着炮制时间的增加而降低,而饱和度S则随炮制时间先增大再减小,在第14 min时达到最大值,而后逐渐降低,而14 min正是白术由炒黄进入炒焦的一个时间点,因此可用饱和度S来指征白术清炒的炒黄阶段。白术炮制品随着炮制时间的增加,其氧化程度不断加深,且随着变化程度的不断加深,氧化值的增加速率不断减小。其中0~2 min时氧化程度变化最为迅速,2~10 min为白术的炒黄阶段;10~18 min 为白术的炒焦阶段;18~22 min 为白术的炒炭阶段。随着炮制时间的增加,5-HMF 含量整体呈增加趋势,在0~10 min白术的炒黄阶段,5-HMF含量差别不大,从10 min开始,白术进入炒焦阶段,此时5-HMF含量骤然增加,20 min后进入炒炭阶段,5-HMF含量基本保持稳定。变化趋势见图3~6。

图3 色调H和饱和度S随炮制时间动态变化图
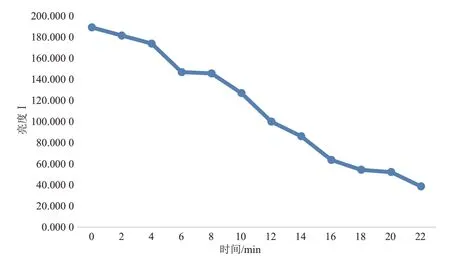
图4 亮度I随炮制时间动态变化图

图5 氧化值随炮制时间动态变化图

图6 5-HMF含量随炮制时间动态变化图
3.3 相关性分析
采用SPSS21.0 软件对白术不同样品的颜色值、氧化值、5-HMF 含量进行Pearson 相关性分析,结果见表3。结果显示色调H 与亮度I 呈极显著正相关,色调H 与氧化值、5-HMF 含量均呈极显著负相关;饱和度S 与亮度I 呈显著负相关,饱和度S 与氧化值呈极显著正相关;亮度I 与氧化值、5-HMF 含量均呈极显著负相关;氧化值与5-HMF含量呈极显著正相关。
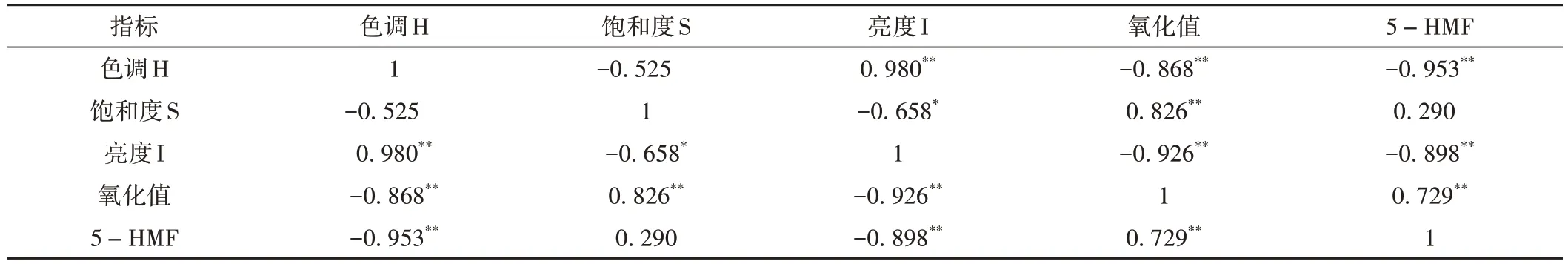
表3 相关性分析表
3.4 颜色值与5-HMF含量的回归分析
以5-HMF含量为因变量,以色调H、亮度I为自变量,进行线性回归分析时,VIF > 5,存在共线性,因此选择逐步stepwise法,进行逐步回归分析,经过模型自动识别,最终余下色调H一项显著自变量在模型中,得出回归模型为Y(5-HMF)= 24.928-43.398X(H),R2= 0.908,而且模型通过F检验(F= 98.826,P= 0.000 < 0.05),说明模型有效。
3.5 颜色值与氧化值的回归分析
以氧化值为因变量,以色调H、饱和度S、亮度I 为自变量,选择逐步stepwise 法,进行逐步回归分析,经过模型自动识别,最终余下饱和度S、亮度I 两项显著自变量在模型中,得出回归模型为Y(氧化值)= 32.219 +40.323X(S)-0.132X(I),R2= 0.941,而且模型通过F检验(F= 71.563,P= 0.000 < 0.05),说明模型有效。
3.6 炮制拐点分析
以饱和度S 为因变量,以炮制时间为自变量,进行回归分析,得出回归模型为Y(S)= 0.143 + 0.046X(时间)-0.002,R2= 0.966,而且模型通过F检验(F=126.531,P= 0.000 < 0.05),说明模型有效。由动态变化分析可知,当炮制时间 ≥ 14 min时,白术由炒黄进入炒焦阶段,代入模型,即满足饱和度S ≥ 0.395时,可认为白术进入炒焦阶段,即白术-5 号样品开始,才达到炒焦状态。以氧化值为因变量,以炮制时间为自变量,进行回归分析,得出回归模型为Y(氧化值)= 16.825 +1.384X(时间),R2= 0.882,而且模型通过F检验(F=74.660,P= 0.000 < 0.05),说明模型有效。由动态变化分析可知,当炮制时间 ≥ 10 min时,白术由炒黄进入炒焦阶段,代入模型,即满足氧化值 ≥ 30.665时,可认为白术进入炒焦阶段;当炮制时间 ≥ 18 min 时,白术由炒焦进入炒炭阶段,代入模型,即满足氧化值 ≥ 41.737时,可认为白术进入炒炭阶段;即白术-5号样品~白术-9号样品才达到炒焦状态,白术-10号样品~白术-11号样品才达到炒炭状态。以5-HMF含量为因变量,以炮制时间为自变量,进行回归分析,得出回归模型为Y(5-HMF)= -3.716 + 0.782X(时间),R2= 0.821,而且模型通过F检验(F= 45.826,P= 0.000 < 0.05),说明模型有效。由动态变化分析可知,当炮制时间≥10 min时,白术由炒黄进入炒焦阶段,代入模型,即满足5-HMF 含量 ≥4.104 时,可认为白术进入炒焦阶段;当炮制时间 ≥20 min时,白术由炒焦进入炒炭阶段,代入模型,即满足5-HMF含量 ≥ 11.924时,可认为白术进入炒炭阶段;即白术-7 号样品~白术-9 号样品才达到炒焦状态,白术-10号样品~白术-11号样品才达到炒炭状态。
4 讨论
4.1 中药的加热炮制
中药炮制是一项我国独有的、具有传统特色的制药技术,也是中医临床用药最显著的特色之一[9]。中药经过加工炮制后发生了多种复杂的化学反应,如水解反应、分解反应、氧化反应等,随着这些化学反应的发生而变化的物质基础,正是中药炮制前后外观、性味归经、功效主治发生改变的重要原因[10]。将中药饮片置于室温环境中,饮片将在室温条件下发生缓慢的氧化过程,该氧化过程主要表现为饮片外部的物性指标发生缓慢改变,而内部的化学成分变化甚微,基本维持原有的状态。将中药饮片置于加热的炮制环境中,饮片将会发生快速的氧化过程,该氧化过程可以让饮片内部和外部的性质都发生改变,外部表现为饮片外观的“形、色、气、味、质”改变,内部表现为原有化学成分增加或减少或产生新的成分等。其实加热炮制的过程就是中药饮片不断吸收外部能量的过程,当所吸收的能量达到其内部各分子发生反应所需要的活化能时,饮片便会发生内部与外部的一系列变化,形成不同的中药炮制品。
4.2 白术炮制方法的选择
炒制为白术的主流炮制方法,生白术因含大量挥发油而燥性显著,炒制品可缓和其燥性,常见有焦白术、白术炭、麸炒白术、土炒白术等,其中仅麸炒白术被收录在《中华人民共和国药典》(2020 年版)中,是临床常用且疗效明确的白术炮制品,而清炒白术只在华南地区使用较多[11-13]。白术炒焦后醒脾作用增强,可用于脾湿有寒,炒炭后收敛止血作用增加,可用于慢性腹泻、久痢出血等[14]。现代文献也多集中于麸炒白术,对清炒炮制过程中的炒黄、炒焦、炒炭品研究较少,本研究测定白术清炒过程中颜色值、氧化值、5-HMF 含量的动态变化,可为白术清炒炮制品的研究提供参考。
4.3 颜色与5-HMF的相关性分析
颜色是中药质量评价的重要指标,也是最直观的外在特征,与中药内在成分密切相关[15-16]。本实验选用HSI 颜色模型,此模型用色调H、饱和度S、亮度I 三参数描述颜色特征。由动态变化可知,随着炮制程度的加深,色调H 与亮度I 均呈现出下降的趋势,表明白术饮片在炮制过程中颜色逐渐变得暗淡与偏暖色调,饱和度S 呈现出先升高再降低的变化趋势,并且当白术开始进入炒炭阶段时饱和度S 开始降低,即当白术炮制品在进入炒炭的临界点时饱和度最大。5-羟甲基糠醛(5-HMF)是多数中药及其炮制品中存在的一个共有成分,具有抗炎、抗氧化、免疫调节等多种现代药理作用[17],在中药应用过程中作为质量控制指标物具有重要意义[18]。5-HMF 主要来源于两个方面,一是由糖类成分在一定的温度、湿度、pH 值等条件下发生脱水反应形成,二是由氨基化合物(蛋白质和氨基酸)和羰基化合物(还原糖类)发生Maillard 反应生成[19]。含多糖的中药在加热炮制过程中,可能发生Maillard 反应生成类黑精大分子、还原酮、还原醛等化合物[20],其中包括5-HMF,但炮制须达到一定程度才能产生5-HMF,而且饮片的炮制程度越深,所测得的5-HMF含量越高。潘欢欢等[21-22]研究发现,白术炒制过程中挥发性成分发生明显改变,炮制过程中增加的成分有14 种,相对含量大于6.0%的成分有反式-2,4-庚二烯醛、5-HMF、石竹素等。因此探究颜色与5-HMF 的相关性极具意义,分析发现5-HMF 含量与色调H、亮度I 均呈极显著负相关,进行逐步回归得到模型Y(5-HMF)= 24.928-43.398X(H),R2= 0.908,意味着H 可以解释5-HMF 含量的90.8%变化原因,即随着炮制程度的加深,白术饮片的外观颜色越偏向暖红或暖棕色调,越暗,而5-HMF 含量越来越多,这与白术炮制品传统外观色泽判别标准和含量测定结果相符,但动态变化分析显示炮制达到一定程度,5-HMF 含量也会出现略下降的趋势。
本实验立足于白术清炒法,研究其炮制过程中其颜色值、氧化值、5-HMF 含量的动态变化,分析白术炮制过程中颜色、氧化值、5-HMF 含量的相关性及拐点,可为白术清炒过程中颜色变化及炮制程度的判断提供参考依据。
