利用深度学习实现CT图像上腰骶椎各结构分割及椎间盘自动定位的可行性研究
2024-03-01田靖一王可欣吴鹏升李家轮张晓东王霄英
田靖一,王可欣,吴鹏升,李家轮,张晓东,王霄英
CT图像因具有良好的空间与密度分辨率,有利于观察椎小关节骨质增生、韧带增厚骨化对椎管造成的压迫程度。对于椎体细微骨折、有无游离骨片等具有较好的检出效能。腰椎CT检查常作为腰椎退行性骨关节病、脊柱骨折的重要检查手段[1,2]。椎体的自动分割及精准定位作为影像诊断一部分,能够为病灶定位、术中所需各影像学参数测量以及术后随访评估奠定基础,减少诊断医师阅片时间、避免医师手工测量引起的误差。
本研究中利用深度学习完成腰骶椎各椎体、椎间盘、硬膜囊的分割,并通过连通域算法完成腰椎诸椎间盘定位,以便后续研究中获得相应水平硬膜囊径线的测量值。
材料与方法
本研究经北京大学第一医院伦理审查委员会的批准[批件号:2019(169)],按照本单位人工智能(artificial intelligence,AI)项目研发规范执行研究方案。
1.用例定义
根据本单位AI训练项目管理方法,首先定义研发腰椎CT图像上主要解剖结构AI分割模型的用户样例(Use Case)。包括模型的ID、临床问题、场景描述、模型在实际工作中的调用流程、模型输入和输出数据的结构等。AI模型返回结果定义为腰椎椎体、椎间盘、硬膜囊的坐标。
2.研究队列的建立
回顾性搜收集2020年12月1日-2021年3月29日于本院行腰椎平扫CT的连续病例资料,纳入标准:腰椎CT检查包含清晰腰骶椎结构的病例。排除标准:①腰椎术后存在较重金属伪影;②存在明显脊柱畸形;③椎体存在明显溶骨性骨质破坏。最终搜收集135例患者154人次的CT检查图像,将该组图像数据用于腰骶椎各主要结构分割模型的训练。
3.CT扫描方案及图像处理
本院腰椎CT图像数据来源于本科5台CT设备:Philips iCT256、GE Discovery CT750 HD、GE LightSpeed VCT、Simens Somatom Definition Flash、Simens Somatom Force,扫描层厚5 mm,重建层厚1~1.25 mm、层间距1~1.25 mm。
4.图像标注
将腰椎CT扫描的原始DICOM图像转换为NIFTI格式,由一名具有5年影像诊断经验的住院医师使用ITK-SNAP软件(Version 3.6.0,http://www.itksnap.org/)对扫描范围内胸腰骶椎椎体及其附件结构、椎间盘及硬膜囊逐层标注,再由一名具有26年以上影像诊断经验的主任医师对标签进行审核、修改后确认。
椎体及其附件结构包括骨质增生及骨赘部分;椎间盘包括髓核压迹、游离髓核部分;硬膜囊以硬脊膜囊为界,不包含神经根出口部分。
5.模型训练
对本院154例图像数据进行腰骶椎各主要结构进行模型训练,显存使用GPU NVIDIA®Tesla P100 16G,软件使用包括Python3.6、Pytorch0.4.1、OpenCV、NumPy、Simple ITK,以Adam作训练优化器。对图像数据进行预处理,设置窗宽为300 HU、窗位为1000 HU,图像像素数设为256×160×128,图像扩增技术包括旋转、随机噪声、透视变换、倾斜、平移。将图像按8:1:1比例随机分为训练集(n=125)、调优集(n=14)、测试集(n=15),同一患者多次扫描的图像均分到相同的数据集中。训练3D U-Net分割模型的参数如下:nfilter=16,每次读取图像数=2,训练次数=400,学习率=0.0001。
6.椎间盘及椎体自动定位
在基于模型分割完成的骶椎及腰椎各椎间盘标签的基础上,应用连通域分析算法,以骶椎为基准线,自下而上依次标记为L5-S1椎间盘、L5椎体、L4-5椎间盘、…、T12-L1椎间盘、…。对于体积<5000像素的连通域认为小连通域,计算该连通域与邻近椎间盘最短距离归为同一椎间盘。
7.模型评价
客观评价:用测试集数据的Dice相似系数(dDice similarity coefficient,DSC)、体积相似度(volume similarity,VS)及Hausdorff距离(Hausdorff distance,HD)作为评价模型分割效能的指标。DSC及VS取值范围为0~1,值越接近1代表模型预测结果与手工标注结果一致性越高,HD距离越小,代表模型模型分割精度越高。
主观评价:由一名高年资医师完成。包括对分割效果的评价和椎间盘及椎体定位的评价。对测试集数据的分割的目标区域进行满意度评估时,正确分割目标区域认为满意,可应用于后续评价椎体病变及完成椎体各结构径线的测量;未正确分割目标区域认为不满意,无法用于后续评价椎体病变及完成椎体各结构径线的测量。医师对椎间盘和椎体做出定位,并与模型自动定位的结果对比。
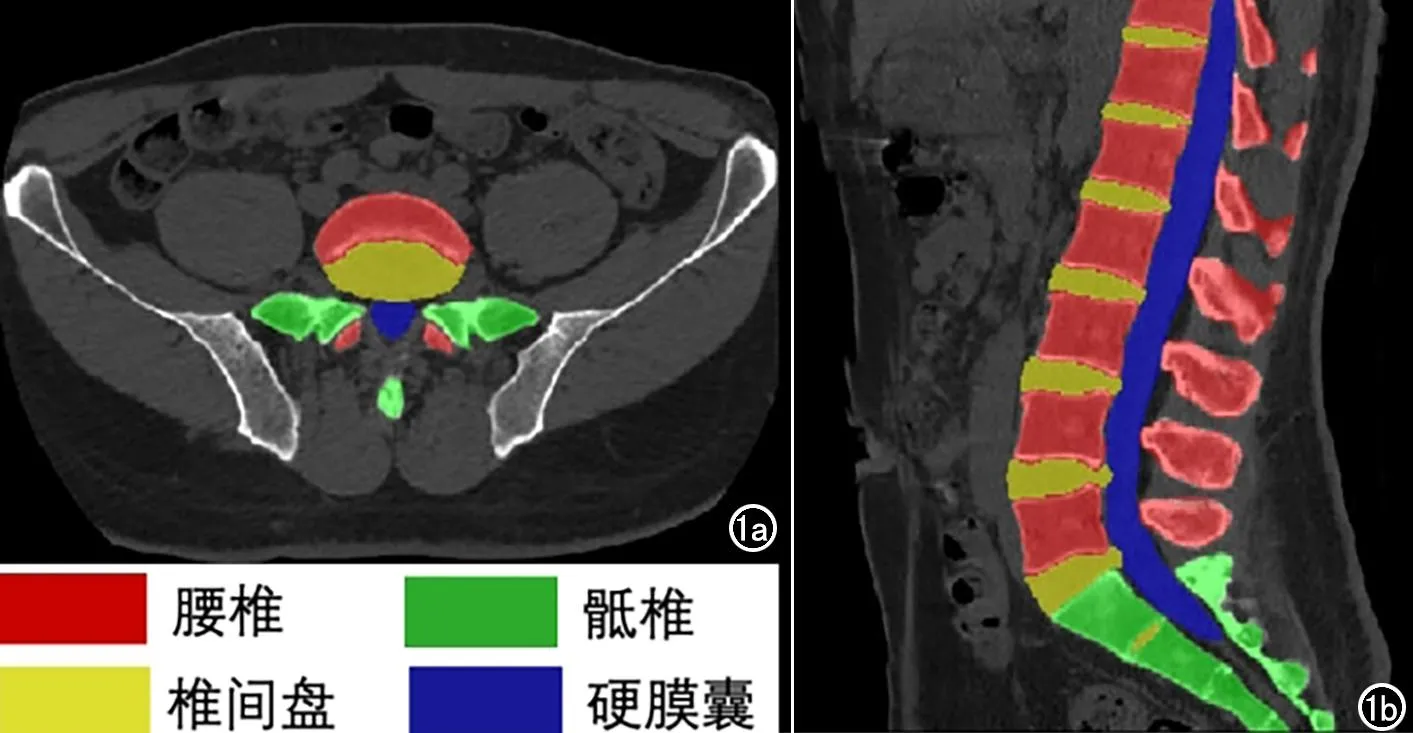
图1 医师手工标注腰骶椎各主要结构标签示例。a)轴面图示腰骶椎、椎间盘层面医师手工标注标签,红色为腰椎椎体、黄色为椎间盘、绿色为骶椎椎体、蓝色为硬膜囊;b)腰椎正中矢状面示医师手工标注各结构标签。
8.统计学分析
结 果
1.患者临床信息
154个全部入组数据的临床信息见表1。患者年龄中位数为58.5 [40.0,70.0]岁,男性50%。诊断包括:腰椎骨质退变、椎管狭窄、椎间盘突出(膨出)、椎体滑脱、峡部裂、移行椎、轻度腰椎侧弯、骨折、椎管内占位、骨岛等。患者各项临床信息在训练集、调优集、测试集之间的差异均无统计学意义(全部P>0.05)。
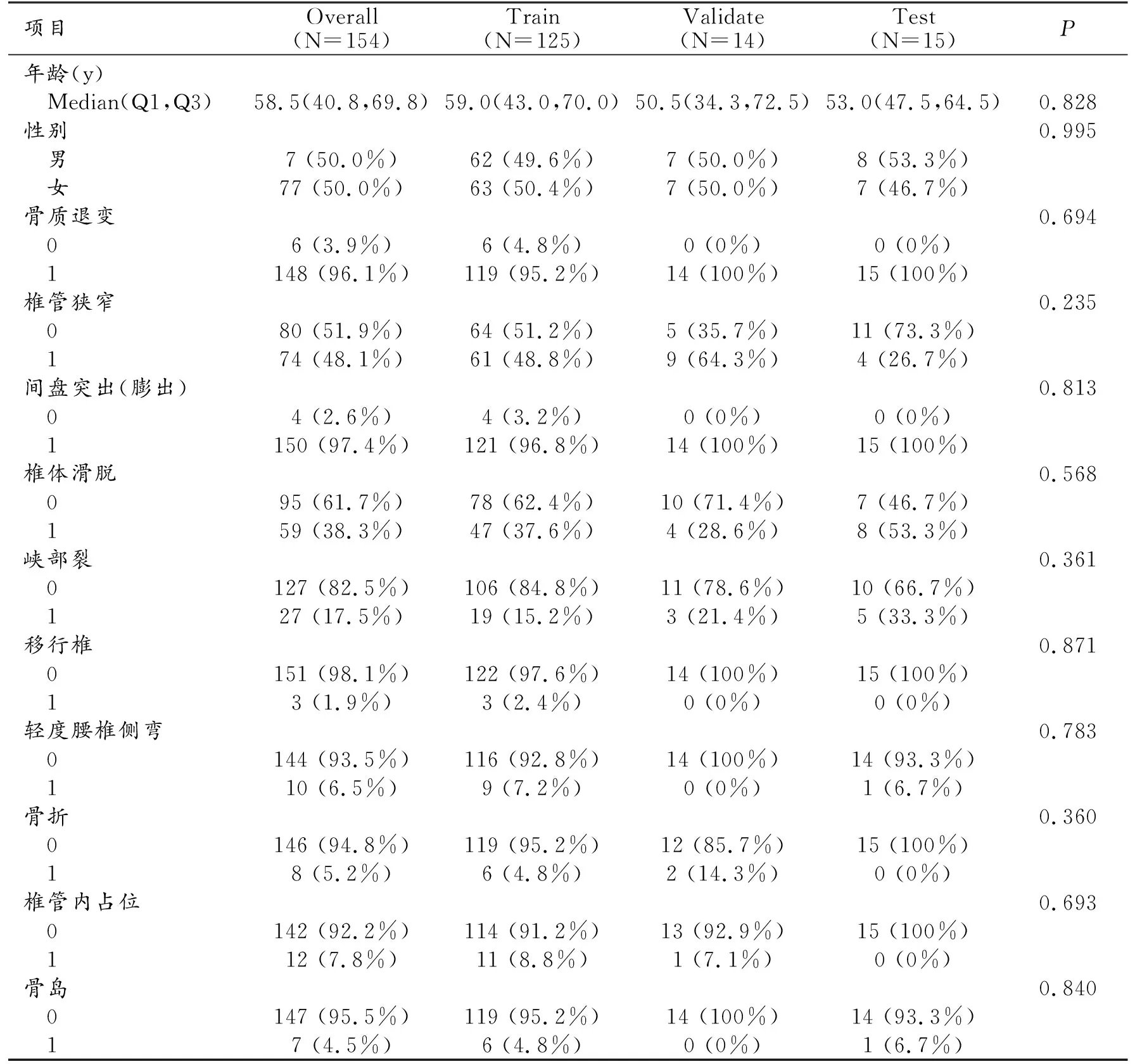
表1 患者临床信息
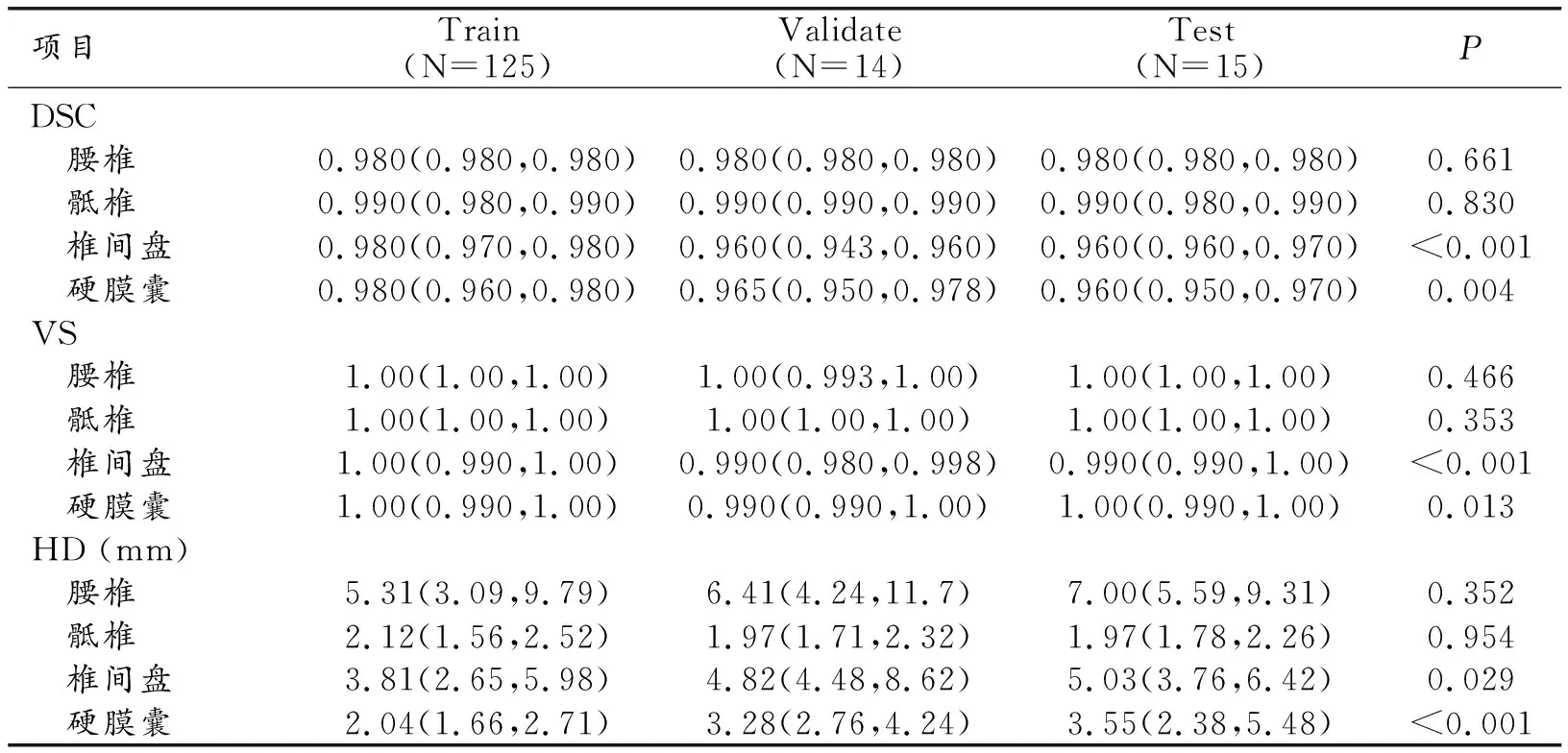
表2 3U-Net模型对腰骶椎各结构的分割效能指标[median(Q1, Q3)]
2.3D U-Net模型的分割效能
主观评价:3D U-Net模型对椎间盘分割结果均为满意,可满足后续椎间盘自动定位的需求,模型对腰骶椎椎体及其附件结构、硬膜囊分割满意度均为98.7%,两结构分割模型各有两例未能完全正确分割目标区域(图2),其中:①2例模型预测结果存在腰骶椎标签的穿插、错位;②1例模型误将腹主动脉管腔预测为硬膜囊结构;③1例模型误将椎管内软组织密度占位预测为正常硬膜囊结构。
客观评价:以医师手工标注的腰椎、骶椎、椎间盘和硬膜囊各结构标签为参考标准,3D U-Net模型对测试集中各结构的分割结果与手工标注结果覆盖率较高,其分割的腰椎、骶椎、椎间盘、硬膜囊的DSC值及VS值均>0.96,HD距离中位数分别为7.00 mm、1.97 mm、5.03 mm和3.55 mm。训练集、调优集和测试集,腰椎、骶椎的DICS、VS和HD的差异均无统计学意义(P>0.05),达到了后续对椎体及附件结构进行各径线测量的要求;椎间盘和硬膜囊的DICS、VS和HD的差异均有统计学意义(P<0.05),椎间盘与相邻椎体终板交界区域、硬膜囊与黄韧带交界区域及脊髓终丝处模型分割结果稍差(图3、4)。
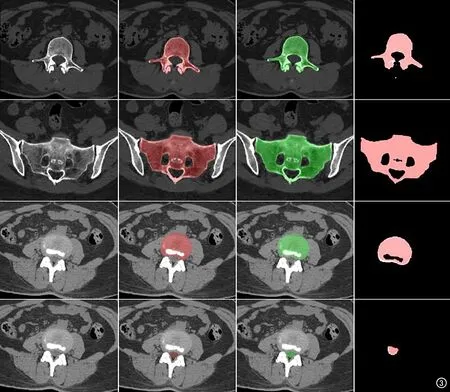
图3 测试集中腰骶椎椎体、椎间盘及硬膜囊分割模型标注及预测结果图(轴位面)。从左至右依次为原始CT图像、医师手工标注各结构图像(红色标签)、模型预测各结构图像(绿色标签)、医师标注和模型预测对照图(白色为模型预测超出部分)。从上至下依次为腰椎、骶椎、椎间盘及硬膜囊结构。

图4 测试集中腰骶椎椎体、椎间盘及硬膜囊分割模型标注及预测结果图(腰椎正中矢状位面)。从左至右依次为原始CT图像、医师手工标注各结构图像(红色标签)、模型预测各结构图像(绿色标签)、医师标注和模型预测对照图(白色为模型预测超出部分)。从上至下依次为腰椎、骶椎、椎间盘及硬膜囊结构。
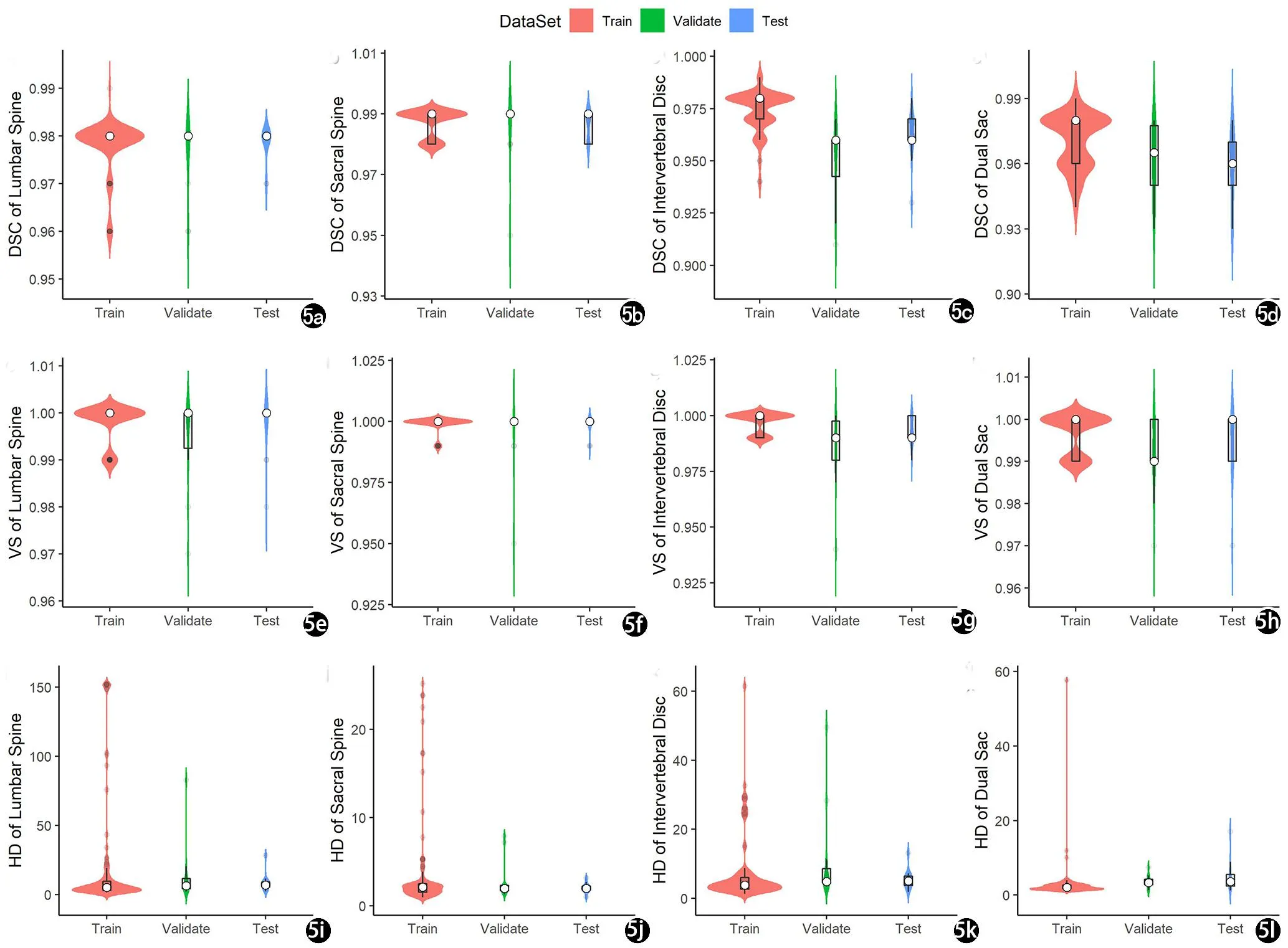
图5 3U-Net模型对腰骶椎各结构的在训练集、调优集和测试集的分割效能指标。a)腰椎标签各数据集DSC值; b) 骶椎标签各数据集DSC值; c) 椎间盘标签各数据集DSC值; d) 硬膜囊各数据集DSC值; e) 腰椎标签各数据集VS值; f) 骶椎标签各数据集VS值; g) 椎间盘标签各数据集VS值; h) 硬膜囊各数据集VS值; i) 腰椎标签各数据集HD值; j) 骶椎标签各数据集HD值; k) 椎间盘标签各数据集HD值; l) 硬膜囊各数据集HD值。
3.椎体自动定位的一致性分析
以脊柱为单位统计,模型预测与医师判定结果的符合率为98.7%(152/154)。154例中有2例出现定位错误,其中1例为腰5双侧横突肥大,与骶骨脊形成假关节;模型预测将腰5椎体识别为骶1椎体,实际腰5-骶1椎间盘未识别。另1例为移行椎,腰5骶化(图6)。

图6 测试集中模型自动定位与医师判定结果对照。a)腰椎冠状面图示腰5双侧横突肥大、伴假关节面形成(红框); b) 模型预测各椎间盘标签并定位; c) 医师标注各椎间盘位置; d) 腰椎冠状面图示移行椎,腰5骶化,腰5双侧横突与骶骨侧块融合(红框); e) 模型预测各椎间盘标签并定位;f)医师标注各椎间盘位置。
讨 论
在临床诊疗过程中,以脊柱疾病引起的腰痛是最常见的就诊原因之一,CT和MRI是临床诊断及治疗过程中不可缺少的常规检查方法,其中MRI为诊断脊柱疾病的首选检查方法,例如椎间盘突出、椎管狭窄等。同时,也需要CT图像观察骨质结构及密度的改变,如腰椎骨折、骨质破坏等;并应用CT重建技术对椎弓根、椎体上进行各影像参数测量[3,4]。所有这些临床的应用,都以精准的定位和准确的识别椎体各结构为先决条件。
近年来,随着U-Net卷积神经网络在医学图像分割中的广泛应用,已有多位学者在CT、MR图像上应用不同学习网络完成腰椎各结构的分割及定位,且结果较为准确[5-9]。本研究中所建立的CT图像上腰椎各主要结构的3D U-Net分割模型具有较好的分割效能,与医师手工标注标签相比,各分割模型预测标签在测试集中亦具有良好的准确性。既往Cheng等的研究中,采用两阶段的Destiny-U-Net进行椎体自动定位和分割,对椎体分割的Dice系数为0.953±0.014,Hausdorff距离为(4.013±2.128)mm;Yu等[10]基于多图谱分割算法对21张腰椎CT图像进行各椎体分割,Dice系数为0.939±1.0,Hausdorff距离为(0.41±0.08)mm。本研究与既往研究相比,采用了更大的数据量构建分割模型,腰、骶椎分割模型预测结果的Dice值和Hausdorff距离优于同类研究,达到了后续进一步对椎体及附件结构各径线测量的要求。同时本研究完成了椎间盘及硬膜囊结构的分割,测试集中,椎间盘及硬膜囊的Dice系数均>0.96,达到了基于椎间盘标签进行自动定位及各椎间盘水平硬膜囊径线测量的需求。
椎体自动定位方面,既往研究在椎体定位中多基于椎体形态,采用随机森林、决策树、YOLOv5等算法实现[7,11-13]。但基于椎体的自动定位仍面临一些挑战,例如创伤或病理性骨折引起的椎体形态改变导致椎体定位偏移。也有部分学者在MR图像中以椎间盘为标志定位,应用Dijkstra’s最短距离算法完成椎间盘的自动检出及定位[14],定位精度达96.25%。在本研究中,我们训练了3D U-Net模型用于分割腰骶椎各主要结构,并基于模型预测的椎间盘标签,应用连通域算法可以简单、快速完成椎间盘的自动定位,定位准确率达98.7%。
本研究还存在一定的局限性,此次入组的数据为临床工作中的实际病例,病种以腰椎退行性骨关节病为主,后续研究我们将针对多种脊柱疾病收集大样本数据来提升模型的泛化能力,也为进一步术前影像参数测量做准备。椎间盘定位方面,本研究中因先天发育变异所致的腰5横突肥大,考虑后续研究中增加一批同类样本数据进行学习,从而实现椎间盘自动定位的精准度。对于存在移行椎的病例,我们考虑在实际临床工作中,医师仍需结合颈胸椎影像图像判定是否存在移行椎,此类模型预测出现的偏移尚可接受。
本研究旨在为腰椎CT图像自动化评估流程打下基础。本研究提出的深度学习模型可完成腰、骶椎椎体、椎间盘及硬膜囊的自动分割和定位,有望用于腰椎CT图像上病变的定位和测量,如腰椎骨折患者术前椎弓根径线测量、腰椎管狭窄患者各椎间盘水平硬膜囊的径线测量等,并将测量结果自动生成在结构化报告里,在日常的工作中,可减轻影像医师繁琐的测量任务,提高工作效率、增加报告的可读性及临床应用性。
