乳清蛋白治疗腹膜透析患者低蛋白血症效果的前瞻性研究
2024-02-02邵耀中梁嫦娜耿瀛洲靳引红常露元吕晶
邵耀中,梁嫦娜,耿瀛洲,靳引红,常露元,吕晶
(西安交通大学第一附属医院肾脏内科,西安 710061)
腹膜透析 (peritoneal dialysis,PD) 是临床常见的肾脏替代治疗手段,具有居家操作方便、残余肾功能保护效果好、交叉感染风险较低等优点,已成为很多尿毒症患者的首选。目前,我国PD患者已超4万例,约20%透析患者为持续性非卧床PD[1]。临床上,PD相关的研究重点多关注腹膜炎、透析充分性、钙磷代谢、贫血等问题,而忽视了营养不良。国内外多项研究[2-4]显示,PD患者营养不良发生率为30%~50%。营养不良是导致患者残余肾功能丢失、死亡率增高的重要原因。有研究[5]显示,低蛋白血症在营养不良的PD患者中普遍存在,这与PD液丢失蛋白、腹膜感染、机体高分解代谢及蛋白质摄入不足等原因相关[6]。因此,治疗低蛋白血症是改善PD患者预后的关键。乳清蛋白是一种从牛奶蛋白中提取的成分,富含必需氨基酸[7],同时也提供丰富的生物活性肽,对癌症、乙型肝炎、骨质疏松及心血管疾病具有潜在益处[8-9],作为营养制剂广泛应用于多个领域。研究[10-11]显示,乳清蛋白除补充营养外还具有增加细胞抗氧化能力、调节肠道菌群、改善能量平衡和代谢的作用。已有研究[12]表明乳清蛋白可以显著改善维持性血液透析患者蛋白质能量消耗状态。本研究探讨乳清蛋白治疗PD患者低蛋白血症的效果,旨在为临床上PD患者低蛋白血症的治疗提供参考。
1 材料与方法
1.1 研究对象及分组
选取2019年8月至2020年8月西安交通大学第一附属医院PD中心进行规律随访的PD患者。纳入标准:(1) 年龄18~70岁;(2) 规律PD门诊随诊患者,且规律PD时间≥1个月;(3) 神志清楚,有能力并且愿意接受评定者;(4) 血清白蛋白<35 g/L[13]和 (或)标准化蛋白分解率 (normalized protein catabolic rate,nPCR) <0.8 g/ (kg·d)。排除标准:(1) 近1个月内发生严重感染 (腹膜炎等);(2) 存在严重肝脏疾病、心功能失代偿、肠道吸收功能障碍、肿瘤、AIDS等感染性疾病;(3) 对蛋白制剂过敏;(4) 拒绝签署知情同意书;(5) 神志不清。退出标准:(1) 发生腹膜炎;(2) 其他严重感染;(3) 发生严重心脑血管等并发症无法继续完成研究。本研究获得医院伦理委员会批准 (NO.XJTU1AF2021LSK-247),患者知情同意并签署了知情同意书。
共纳入100例,随机分为研究组和对照组,每组50例。研究组给予正常蛋白饮食[0.8~1.0 g/ (kg·d) ],同时摄入乳清蛋白粉[0.6 g/ (kg·d) ],45~90 g/d,1~2次/d,饭前30 min或与正餐同时食用,连续32周。对照组给予高蛋白饮食,每日蛋白摄入量为1.2 g/ (kg·d),高蛋白饮食以鸡蛋清、鸡肉、鱼肉、虾肉、豆腐、牛奶或酸奶为主。根据患者蛋白需求 (每日按1.2 g计算,体质量50 kg患者需要60 g蛋白) 折合成相应蛋白量(包括主食中蛋白含量) 来推荐食谱,保证优质蛋白占50%,连续32周。
1.2 检测指标
在治疗前 (治疗0周)及治疗8、16、32周时检测患者各项指标,包括一般指标[年龄、性别、体质量指数 (body mass index,BMI)、是否合并糖尿病]、生物化学指标[血红蛋白 (hemoglobin,Hb)、血清白蛋白 (albumin,ALB)、前白蛋白 (prealbumin,PA)、甘油三酯 (triglyceride,TG)、总胆固醇 (total cholesterol,TC)、血磷 (phosphorus,P)、低密度脂蛋白 (low density lipoprotein,LDL)、高密度脂蛋白 (high density lipoprotein,HDL)、血肌酐 (serum creatinine,Scr)、尿素氮(blood urea nitrogen,BUN)、估算肾小球滤过率 (estimated glomerular filtration rate,eGFR)、总尿素清除指数 (total spKt/Vurea,TKt/V)、总肌酐清除率 (total creatinine clearance rate,TCcr) ]、人体生物学指标[握力(hand grip strength,HG)、肱三头肌皮褶厚度 (triceps skinfold,TSF)、上臂围 (arm circumference,AMC)、上臂肌围 (mid-arm muscle circumference,MAMC) ]。
1.3 检测方法
1.3.1 生物化学指标:患者入组时,治疗0、8、16、32周时空腹采集静脉血3 mL,采用全自动生化分析仪检测各项指标。
1.3.2 人体测量:采用标准方法测量并计算患者透析后BMI、AMC、TSF。BMI=体质量/身高2,AMC=上臂中点处的围长-3.14×TSF。TSF测量方法:选取部位为肩峰与尺骨鹰嘴连线中点,用左手拇指和食、中指将被测部位皮肤下皮组织夹提起来,在该皮褶提起点的下方用皮褶计测量厚度,把右拇指松开皮褶计卡钳钳柄,使钳尖部充分夹住皮褶,在皮褶计指针快速回落后立即读数。连续测量3次,取平均值。
1.4 统计学分析
采用SPSS 26.0软件进行统计分析。正态分布的计量资料采用±s表示,2组比较采用独立样本t检验,组内比较采用重复测量方差分析。非正态分布的计量资料采用M(P25~P75) 表示,2组间比较采用Mann-WhitneyU秩和检验。计数资料采用率 (%) 表示,2组间比较采用χ2检验。P< 0.05为差异有统计学意义。
2 结果
研究期间共有5例 (1例最新确诊合并肿瘤,1例死亡,3例发生腹膜感染) 退出,其中研究组3例,对照组2例。
2.1 2组一般情况比较
结果显示,2组患者年龄、性别、BMI、是否合并糖尿病比较无统计学差异 (均P> 0.05)。2组HB、ALB、PA、HG、AMC、MAMC、TSF等指标比较均无统计学差异 (均P> 0.05),具有可比性。见表1。
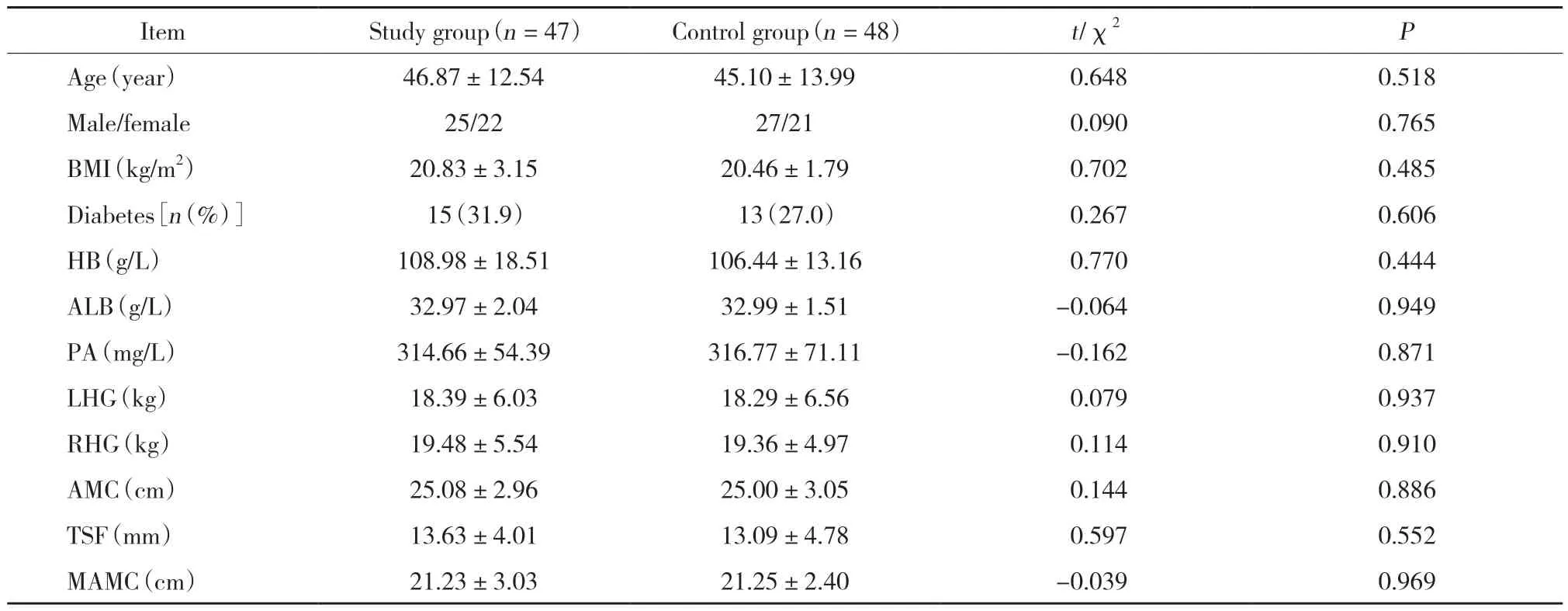
表1 患者基线资料比较Tab.1 Comparison of baseline data between study and control groups
2.2 2组饮食干预后各项生物化学指标比较
结果显示,与0周比较,研究组16、32周时ALB、PA升高显著 (均P< 0.05),而HB、P却无统计学差异(均P> 0.05);研究组8周时HB、ALB、PA、P也无统计学差异 (均P> 0.05)。与0周比较,对照组各时间点HB、ALB、PA、P均无统计学差异 (均P> 0.05)。见表2。
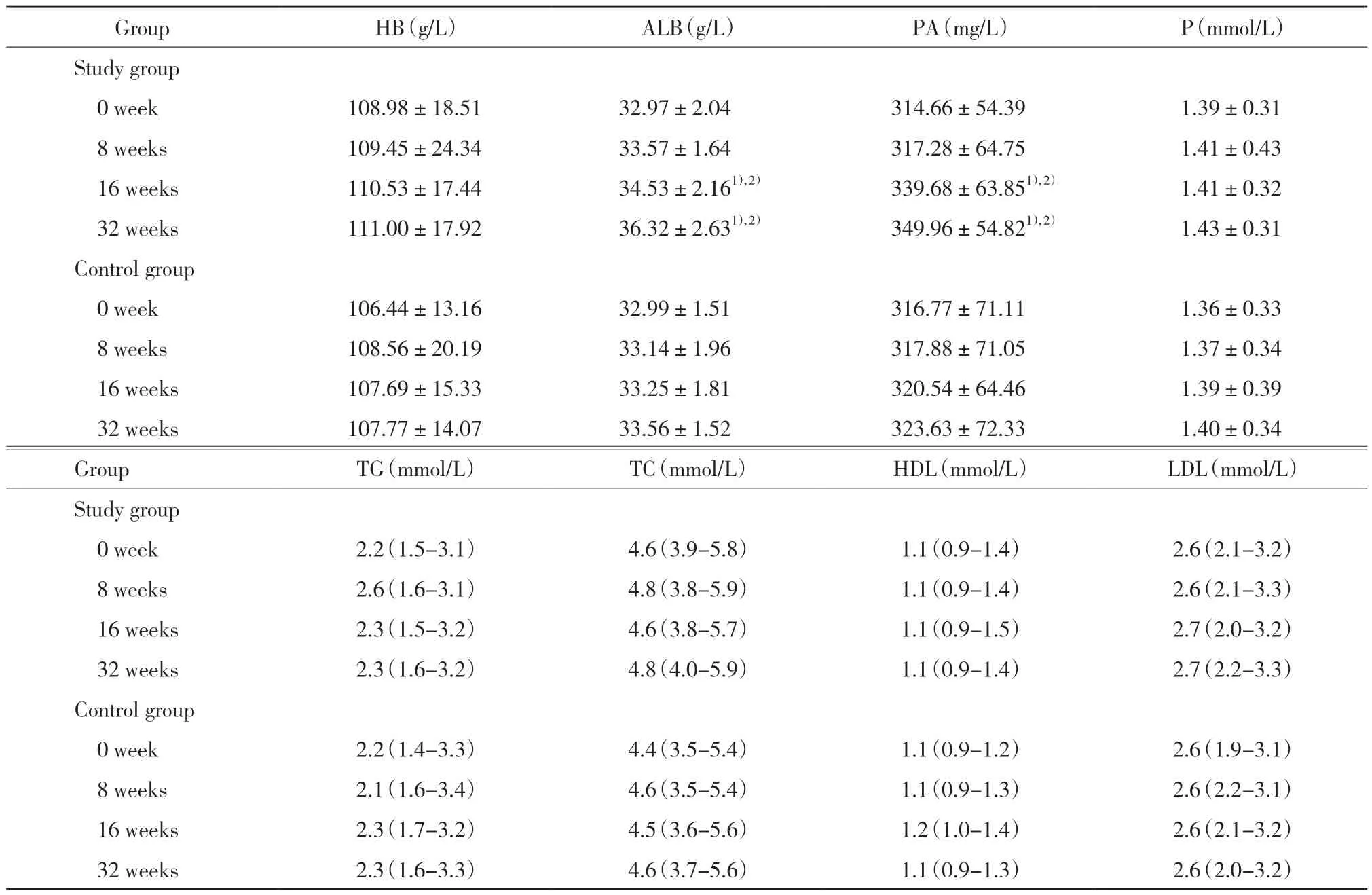
表2 2组饮食干预后的各项血清学指标比较Tab.2 Comparison of serological measures between study and control groups
2组各时间点TG、TC、HDL、LDL、Scr、BUN、eGFR、尿量、TKt/V和TCcr比较无统计学差异 (均P> 0.05)。与对照组比较,研究组16、32周时ALB、PA明显升高,差异均有统计学意义 (P< 0.05)。见表2、表3。

表3 2组各时间点透析充分性指标比较Tab.3 Comparison of dialysis adequacy measures between study and control groups
2.3 2组饮食干预后人体测量生物学指标比较
结果显示,与0周比较,研究组患者8、16、32周时LHG升高,差异有统计学意义 (均P< 0.05);研究组患者16、32周时RHG升高,差异有统计学意义 (均P< 0.05);。而其他各时间点各指标比较均无统计学差异 (均P> 0.05)。对照组患者各时间点LHG、RHG比较差异均无统计学意义 (均P> 0.05)。2组BMI组内及组间比较均无统计学差异 (均P> 0.05)。见表4。

表4 2组饮食干预后人营养指标比较Tab.4 Comparison of nutritional measures between study and control groups
2组患者各时间点AMC、TSF、MAMC比较差异均无统计学意义 (均P> 0.05)。与对照组比较,研究组8、16、32周时LHG明显升高;16、32周时RHG明显升高,差异均有统计学意义 (均P< 0.05)。见表4。
3 讨论
PD是治疗终末期肾病的有效替代方式。随着PD技术的不断推广与应用,其多种并发症也逐渐凸显。营养不良是PD患者严重的并发症之一,患者常伴有消瘦、体质量下降、食欲不振、全身乏力、免疫力下降、容易感染等表现,严重影响患者的生活质量,加重家庭负担[14]。同时,营养不良也是PD患者高住院率、高死亡率的危险因素,是预测合并症的最显著指标之一[15]。研究[16]显示,PD患者营养不良的发生率随着透析时间延长而升高。有效的营养支持有助于降低死亡率,提高生活质量,缩短住院时间[17]。因此,密切监测PD患者的营养状况,正确评价营养不良、尽早发现及预防营养不良对减少并发症、改善预后有重要意义。我国2005年制定的《维持性PD共识》[18]中关于营养不良的评价推荐综合评估,包括ALB、PA,标准蛋白分解率、饮食评估每日蛋白摄入、改良主观综合性营养评估法、人体测量 (包括体质量、皮褶厚度、上臂周径、双能量X线吸收法以及生物电阻抗分析等)。另外,最新的1项研究[19]也提示标化氮表现率蛋白当量、饮食蛋白摄入量、nPCR、AMC与持续性非卧床PD患者营养不良密切相关。
ALB作为评估营养状况的重要指标得到广泛应用。同时,低蛋白血症也是提示透析患者营养不良的重要指征[20]。目前,PD共识[21-22]建议患者每日蛋白摄入达到1.2 g/ (kg·d),而对于透析稳定的患者来说达到0.9~1.0 g/ (kg·d) 即可满足需要。
本研究纳入了年龄18~70岁的PD患者,排除感染、肿瘤、高分解代谢状态等所导致的低蛋白血症,因此认为入组患者低蛋白血症的发生可能与蛋白能量摄入不足有关,可以通过增加蛋白摄入来提高ALB水平,改善患者的营养状况。目前,临床上常指导透析患者服用α-酮酸增加氨基酸及蛋白质合成[23],但是α-酮酸存在口感一般、吸收率有限 (尤其老年PD患者)、价格昂贵等缺点。另外,在膳食蛋白摄入足量的情况下复方α-酮酸的改善效果可能更好。因此,合理的蛋白摄入非常重要。指南[24]建议患者多摄入氨基酸成分组成合理、磷/蛋白质比例低、吸收利用率高的优质蛋白。乳清蛋白是继酪蛋白之后,因氨基酸组成最合理、吸收率高等诸多优势被推为“蛋白之王”。本研究结果显示,2组治疗期间残肾功能和PD指标比较无统计学差异 (均P>0.05),无论是研究组还是对照组,治疗8周时ALB、PA、HB等指标均无明显改善。研究组治疗8周时左手HG改善,治疗16、32周时ALB、PA以及双手HG均显著升高 (均P< 0.05),而TG、TC、LDL以及P均无明显改变 (均P> 0.05),提示乳清蛋白粉摄入可能改善了患者的营养状况,特别是在改善ALB、PA和HG上效果明显。HG代表上肢肌力,是机体肌肉丧失程度的可靠指标[25];而且对血脂以及血P无明显影响。研究组AMC、MAMC尚无明显改善,残肾功能和PD指标无明显变化,考虑可能是乳清蛋白粉的使用时间较短所致。而对照组的营养状况指标ALB、PA、HB、HG、AMC、TSF、MAMC均无明显改善,可能与个人饮食习惯较为固定,饮食指导的调整幅度较小,以及患者的依从性等均有关系。因此,临床上需要重视PD患者饮食,加强饮食指导,从而更好地改善患者的营养状况。
综上所述,对于单纯因摄入不足或丢失过多导致低蛋白血症的PD患者,增加乳清蛋白摄入可以明显改善营养状况,治疗效果优于高蛋白饮食。但本研究未针对合并糖尿病的PD患者纳入空腹血糖、糖化血红蛋白的基线数据及实验数据的采集,后续实验设计可针对合并糖尿病的PD患者进行更深入研究。
