Co(acac)2催化氧化乙苯制备苯乙酮的研究
2023-12-06代炜朱剑波宋玉强张相新尹洪珊闵建中
代炜,朱剑波,,宋玉强,*,张相新,尹洪珊,闵建中
(1.山东键兴新材料科技有限公司,山东 济宁 370800;2.山东键邦新材料股份有限公司,山东 济宁 370800)
目前,选择性氧化芳香烃侧链仍是精细化工领域有机合成研究的难点及重点,同样是石油化工领域工业生产中的技术重心。芳香烃侧链氧化的关键在于催化剂催化效率。芳香烃侧链氧化根据不同的氧化方式,可分为催化氧化法、电解氧化法及化学氧化法[1]。化学氧化法操作简单、反应条件友好,有较高选择性用来制备芳香类醇、醛、酮、酸、酚等[2-3]。近年来,催化氧化技术通常在催化剂的诱导下,以廉价易得的氧气/空气或过氧化氢等来催化氧化有机物制备目的产物。催化氧化分为气相法和液相法。催化氧化因其清洁环保、低廉成本及较高的收率而备受关注。而催化氧化中,液相法是催化氧化发展的主要方向。
乙苯作为取代芳香烃的代表物质,同样是芳香烃氧化研究的首选。作为乙苯氧化的重要产物,苯乙酮既可以用作化工原料,还可作为中间体应用于精细化工,香料,农药,医药,染料等领域。因其有沸点高、稳定性高、令人愉快的芳香气味等诸多优点,也可作为溶剂使用。苯乙酮溶解能力类似环己酮,能溶解多种纤维素和树脂等,日常使用时多作为混合溶剂使用。在香料领域使用时,可以用来调配含羞草、紫丁香、山楂、香烟香精和皂用香精等。苯乙酮在医药领域有机合成领域通常用作合成布洛芬、苦杏仁酸等[4]。
苯乙酮的工业化制备方法主要是傅-克酰基化反应,乙苯直接氧化法,乙苯催化氧化法。傅-克酰基化反应是苯在AlCl3等路易斯酸存在下与酰卤/酸酐等作用酰基化反应合成苯乙酮,因其副产物卤化氢/醋酸高温下对设备腐蚀性强,污染严重,产率低,所以该法已经淘汰。乙苯直接氧化法在常压条件下,直接氧化乙苯制苯乙酮,该法对环境不友好且乙苯转化效率差,同时后处理阶段还存在分离和提纯困难,生产成本高等缺点,不适于工业生产。乙苯催化氧化法以空气/氧气或双氧水为氧化剂,在催化剂作用下选择性氧化乙苯合成苯乙酮,反应过程中时常伴有1-苯乙醇和苯甲酸等生成。该法反应条件温和、安全性高、环境友好、工艺操作简便等优点,是一种绿色生产工艺,是工业生产苯乙酮的重要工艺[5]。但是,乙苯氧化为自由基链式反应,苯乙酮仅仅是乙苯氧化过程的其中一种主要产物,开发高活性、高选择性及环境友好的催化剂仍然是乙苯催化氧化合成苯乙酮的关键。
Co(acac)2用于乙苯氧化催化具有较大优势,本文深入探究催化氧化乙苯制苯乙酮的反应过程,通过对反应过程中反应时间、反应温度、空气流速和催化剂用量等工艺参数对催化氧化合成苯乙酮效果的分析,确定最优的合成方案。
1 实验部分
1.1 实验试剂与仪器
乙苯:工业级;Co(acac)2:分析纯,上海麦克林生化科技有限公司;乙酸钴(Ⅱ):分析纯,上海麦克林生化科技有限公司;环烷酸钴:工业级;1-苯乙醇:分析纯,上海麦克林生化科技有限公司;苯乙酮:色谱纯,天津市大茂化学试剂厂。
DF-101S集热式恒温加热磁力搅拌器:巩义市予华仪器有限责任公司;DA7002型静音无油空气压缩机:江苏岱洛医疗科技有限公司;GC9800气相色谱仪:上海科创色谱仪器有限公司。
1.2 实验操作步骤
在500 mL三口烧瓶中,先后加入乙苯200 g和当量的催化剂,打开磁力搅拌器加热开关设定温度升温,待温度升至所需反应温度,维持10 min,通入空气(可通过气体流量计前调节阀调节控制空气流速),持续反应。实验开始后按预定时间间隔取样,直至实验结束。产物过滤后通过GC检测定量分析。
本文以Co(acac)2为催化剂,研究了反应过程中的反应时间、反应温度、空气流速和催化剂用量等工艺参数对催化氧化合成苯乙酮的影响并确定最优的合成方案。
1.3 产物分析及参数计算方法
本实验所得产物的定量分析采用GC高效气相色谱仪进行,进样量为0.2 μL。色谱操作条件:兰州中科凯迪化工新技术有限公司SE-30毛细管色谱柱(30 m×0.25 mm×0.33 μm);柱箱温度80 ℃;汽化温度180 ℃;FID温度200 ℃;空气柱前压力0.05 MPa,H2柱前压力0.1 MPa,高纯N2柱前压力0.05 MPa;程序升温:柱初温80 ℃(停留10 min),升温14 min,升温至220 ℃(停留10 min)[6]。

(1)

(2)
根据GC测得的反应物含量,计算乙苯转化率和苯乙酮收率,计算公式分别为式(1)、式(2)。
2 结果和讨论
2.1 反应时间对反应的影响
为探究反应时间对Co(acac)2催化氧化乙苯反应的影响,做如下实验。在500 mL三口烧瓶中,先后加入乙苯(200 g),Co(acac)2(0.2 g),加热到反应温度100 ℃,维持10 min,通入空气,空气流速100 mL/min。反应开始后,每4 h取样一次,样品过滤后进入气相色谱检测定量分析,考察乙苯氧化反应的主要产物含量随反应时间的变化,结果如图1所示。

图1 乙苯氧化主要产物含量随时长变化
由图1可见,乙苯催化氧化反应的主要氧化产物有苯乙酮、1-苯乙醇。1-苯乙醇含量在反应初期8 h内迅速上升,随着时间推移逐渐增加到峰值后略有下降并维持平稳状态;1-苯乙醇含量在反应中后期相对稳定,该规律同样适用于醋酸钴、环烷酸钴等钴系催化剂的乙苯催化氧化。反应前中期苯乙酮含量增加迅猛,但反应后期苯乙酮含量增加缓慢。这是因为乙苯催化氧化是自由基反应过程,在100 ℃和催化剂作用下氧化反应很快被引发,首先生成初级产物乙基苯过氧化氢,乙基苯过氧化氢进一步被分解生成苯乙酮、1-苯乙醇,同时过度氧化还会产生相应的醛或酸,如图2所示。
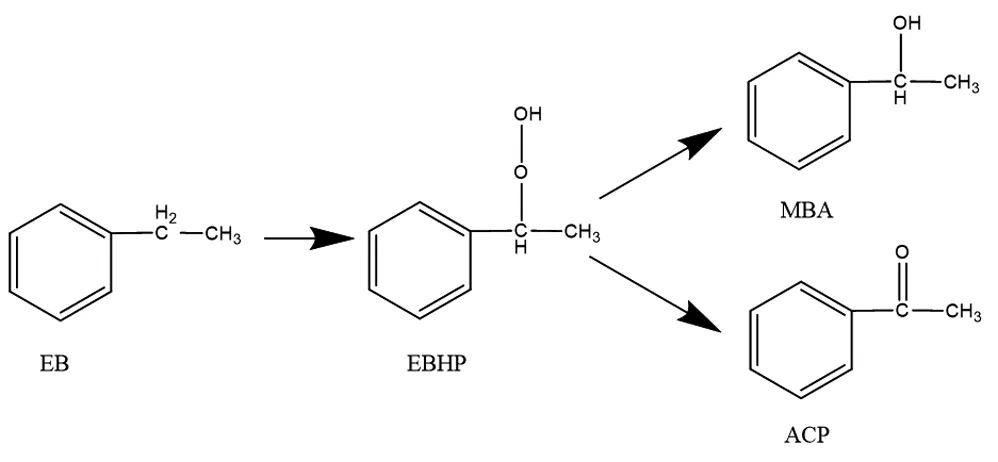
图2 乙苯氧化反应过程
从图3中可以看出,反应前期,乙苯转化率低,随着反应的进行,乙苯转化率显著提升,反应进行到20 h时,转化率增幅趋于平缓,而苯乙酮收率在乙苯氧化开始后即呈现缓慢上升趋势,随着反应的进行,苯乙酮收率逐渐趋于平稳并保持在较高水平。从图1和图3可见,反应液中苯乙酮含量远大于其他产物含量,苯乙酮是乙苯催化氧化的主要产物。
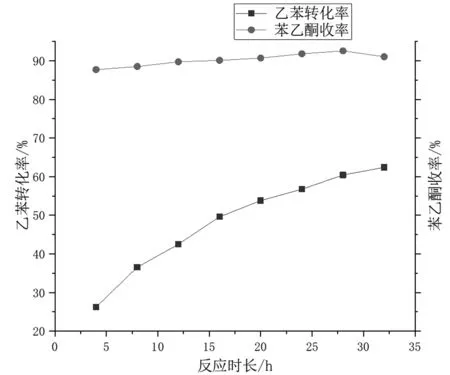
图3 乙苯转化率和苯乙酮收率与反应时长的关系
2.2 反应温度对反应的影响
为探究反应温度对Co(acac)2催化氧化乙苯反应的影响,做如下实验。在500 mL三口烧瓶中,先后加入乙苯(200 g),Co(acac)2(0.2 g),加热到设定反应温度,维持10 min,通入空气(空气流速100 mL/min)。维持反应时间为28 h,反应结束后取样,样品过滤后进入气相色谱检测定量分析,将所得气相数据通过简单计算后得出乙苯转化率和苯乙酮收率,数据如图4所示。
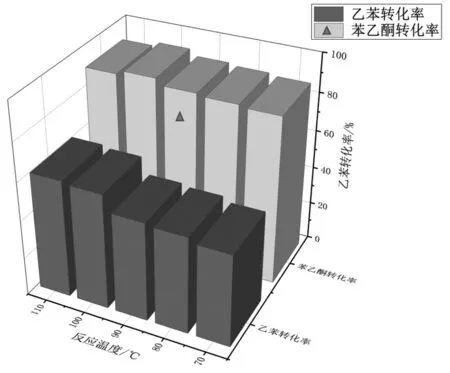
图4 乙苯转化率和苯乙酮收率与反应温度的关系
由图4可得结论,当反应温度较低时,乙苯转化率不足50%,乙苯转化率随着反应温度提高而显著提升,实验数据说明提高乙苯催化氧化反应效率依赖于反应温度的提高,在此过程中苯乙酮收率提升幅度较小,反应温度稳定在100 ℃时,苯乙酮收率达到顶峰,继续提高反应温度,对乙苯转化率提升增幅无较大益处,但苯乙酮收率下降趋势明显。说明在Co(acac)2作用下,反应温度相同时,乙基苯过氧化氢分解生成苯乙酮和1-苯乙醇的速率大致相当,但在高温作用下过氧化生成大量副产物醛或酸,从而导致苯乙酮收率在温度较低时基本不随反应温度变化而变化,温度过高时略有下降。醋酸钴和环烷酸钴等钴催化剂催化氧化乙苯时同样存在该现象。该组实验中,苯乙酮收率一直保持较高水平,温度超过100 ℃后,略有下降,可能的原因是高温导致副反应生成大量副产物醛或酸等。
2.3 空气流速的影响
为探究空气流速对Co(acac)2催化氧化乙苯反应的影响,做如下实验。在500 mL三口烧瓶中,先后加入乙苯(200 g),Co(acac)2(0.2 g),加热到反应温度100 ℃,维持10 min,通入空气,设定空气流速。维持反应时间为28 h,反应结束后取样,样品过滤后进入气相色谱检测定量分析,将所得气相数据通过简单计算后得出乙苯转化率和苯乙酮收率,数据如图5所示。
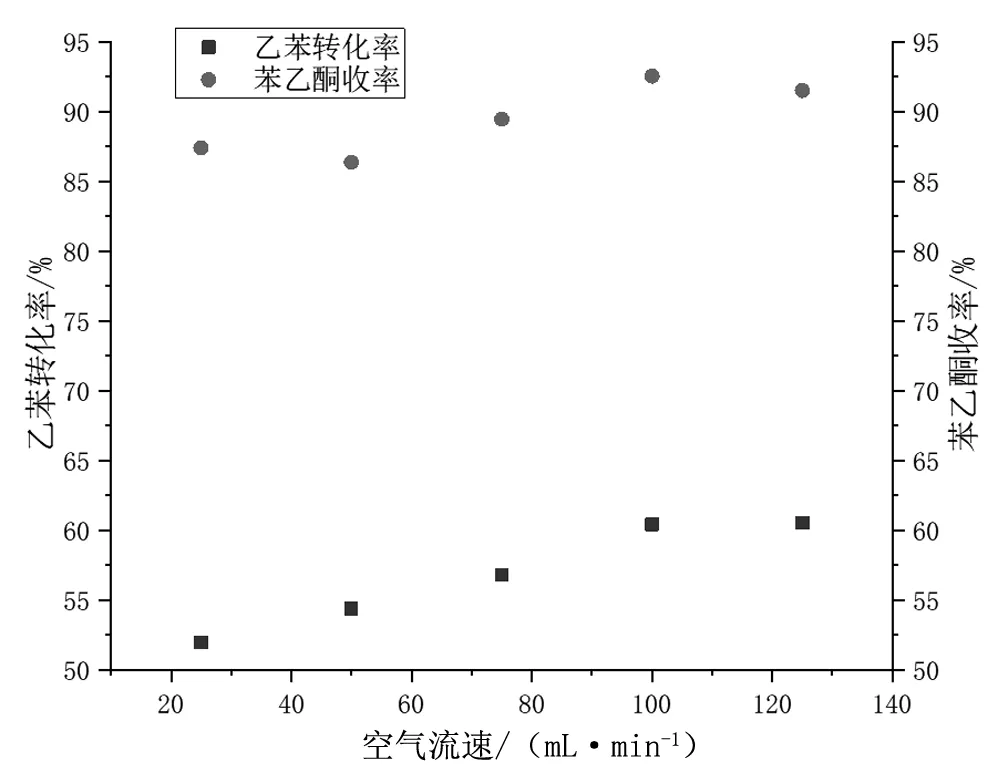
图5 乙苯转化率和苯乙酮收率与空气流速的关系
观察图5可知,当氧化反应开始,通入空气流速较少时,乙苯转化率较低,其原因可能是当空气流速较小时,参与氧化反应的氧化剂明显不够,仅有少量乙苯参与反应,故导致乙苯转化率较低。乙苯转化率随着空气流速的增加而呈现线性增加,而苯乙酮收率增幅较窄。100 mL/min为最佳空气流速,乙苯转化率最优,乙苯转化率为60.43%,苯乙酮收率最高,苯乙酮收率为92.55%。此时溶液中的氧气溶解度达到饱和,参与氧化反应的氧化剂明显增多,乙苯大量氧化。空气流速继续升高至125 mL/min时,乙苯转化率和苯乙酮收率不再继续提升,可能原因为过量氧气不再参与氧化反应,直接通过排空阀排出,此时苯乙酮收率趋于稳定[7]。
2.4 催化剂用量的影响
为探究催化剂用量对Co(acac)2催化氧化乙苯反应的影响,做如下实验。在500 mL三口烧瓶中,先后加入乙苯(200 g),Co(acac)2(0.2 g),加热到反应温度100 ℃,维持10 min,通入空气(空气流速100 mL/min)。反应开始后,每4 h取样一次,维持反应时间为28 h,样品进入气相色谱检测定量分析,将所得气相数据通过简单计算后得出乙苯转化率和苯乙酮收率,数据如图6和图7所示。

图6 催化剂用量对乙苯转化率的影响

图7 催化剂用量对苯乙酮收率的影响
由图6和图7可见,当无催化氧化时,乙苯转化率随反应时间延长而缓慢增大,并趋于平缓,而苯乙酮收率随反应时间延长而下降。说明苯乙酮是乙苯氧化反应过程的主要产物,反应液中1-苯乙醇的含量小于苯乙酮含量,另外在28 h反应时间内乙苯氧化转化率维持在较低水平,可知乙苯无催化氧化过程始终处于自由基反应的诱导期,实验结果表明在无催化氧化时,自由基生成速度较慢,无法产生足够多的自由基,引发链式反应,因此苯乙酮的收率相对较差。当添加一定质量分数催化剂(≥0.5‰)后,乙苯氧化速率显著提升,乙苯转化率在反应初期快速上升,而苯乙酮收率则随着反应时间缓慢上升。逐渐增加催化剂用量,特别是达到Co(acac)2最佳质量分数1% 时,苯乙酮收率达到最高。催化剂质量分数继续增加至2%时,苯乙酮收率反而呈现缓慢下降趋势。由此可以看出,采用Co(acac)2催化氧化制备苯乙酮,催化剂用量较少。比较Co(acac)2和醋酸钴(Ⅱ)及环烷酸钴催化剂,可知乙酰丙酮钴催化剂用量最少且能获得较高的苯乙酮收率的同时反应时间增加不大。采用醋酸钴(Ⅱ)或环烷酸钴为催化剂虽然可以快速提升乙苯氧化反应进程度,但反应所获苯乙酮收率则较低,不利于反应产物的分离提纯。因此,从综合效用的角度出发,Co(acac)2生成酮的能力优于醋酸钴和环烷酸钴催化剂[8]。
3 结论
以Co(acac)2为催化剂,研究了反应过程中的反应时间、反应温度、空气流速和催化剂用量等工艺参数对催化氧化合成苯乙酮的影响并确定最优的合成方案。得出以下结论:
(1)Co(acac)2催化乙苯氧化反应是自由基链式反应,氧化反应机理多有争议,现有机理仍处于模拟推测阶段,还需进一步优化完善。
(2)乙苯催化氧化制备苯乙酮的最优合成方案:28 h为最佳反应时间,100 ℃为最佳反应温度,空气作为气源,100 mL/min为最佳流速,Co(acac)2最佳用量为乙苯质量分数1‰,在此合成方案下,乙苯转化率最优,为60.43%,苯乙酮收率最高,为92.55%。
(3)Co(acac)2在催化氧化合成苯乙酮的反应中具有显著优势,它的用量较小、对设备腐蚀较小、成本低廉,能够有效提升氧化效率,降低生产成本,因此具有广阔的工业应用前景。
