光度滴定法测定丁香酸和对香豆酸的解离常数
2023-12-06桂玉娟付洁任佳刘娜夏雁青石铁生
桂玉娟,付洁,任佳,刘娜,夏雁青,石铁生
(枣庄学院 化学化工与材料科学学院,山东 枣庄 277160)
丁香酸(Syringic acid,SA)的化学名称是3,5-二甲氧基-4-羟基苯甲酸,主要存在于枸杞[1]、核桃[2]等水果和谷物中,在植物中通过莽草酸途径合成[3],它具有抗氧化、抗菌、抗炎等生物活性[3-5],对癌症、心血管疾病和糖尿病等疾病的预防具有一定作用[6]。对香豆酸(p-coumaric acid,p-CA) 又叫对羟基肉桂酸,和丁香酸一样,也是酚酸类化合物,它是很多中药如白花蛇草的主要有效成分,而白花蛇草已被研究证明可以诱发MM细胞凋亡[7];另有研究表明对香豆酸可抑制癌细胞增殖,具有抗氧化和抗肿瘤作用[8-10]。丁香酸和对香豆酸在水溶液中分别存在如图1和2所示的解离平衡,它们的不同质子化形态在发生氧化还原反应时其活性可能存在很大差异[11]。迄今为止在25.0 ℃和1.0 mol/L离子强度下,它们在水溶液中的解离平衡常数尚未有报道,我们较为系统地研究了丁香酸和对香豆酸的UV-Vis光谱随溶液pH值的变化,通过光度滴定法获得了二者的解离常数pKa1和pKa2。

图1 丁香酸在水溶液中的解离平衡

图2 对香豆酸在水溶液中的解离平衡
1 实验部分
1.1 仪器与试剂
TU-1950 紫外-可见分光光度计(普析,北京通用,配有1.00 cm厚石英比色皿),水浴恒温槽(Lauda Alpha RA8,德国),Accumet Basic AB150 Plus pH计(Fisher Scientific,美国)。
丁香酸,对香豆酸,高氯酸钠,磷酸,磷酸二氢钠,磷酸氢二钠,磷酸钠,醋酸,醋酸钠,碳酸钠,碳酸氢钠,氯化钠,购于Sigma 或Alfa Aesar 试剂公司,所有试剂均为分析纯。用于校准电极的标准缓冲液pH 值4.00,7.00 和10.00 也购于Alfa Aesar 试剂公司。 溶液均使用二次蒸馏水配制。
1.2 缓冲溶液配制
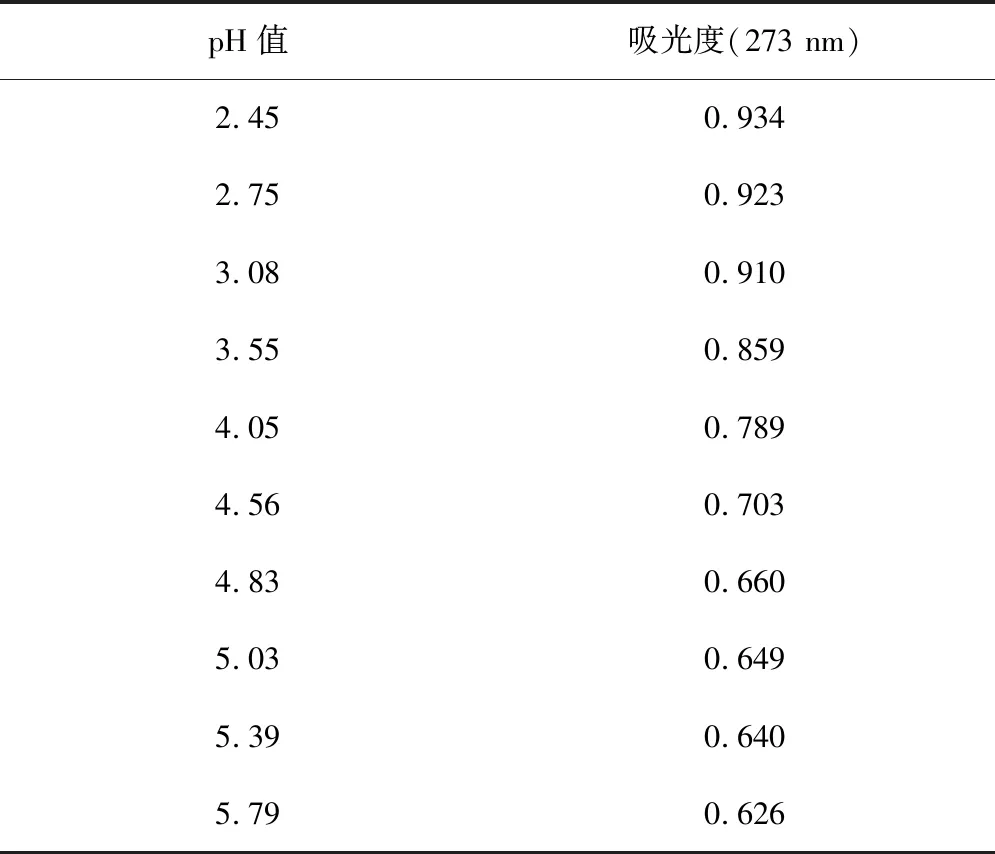
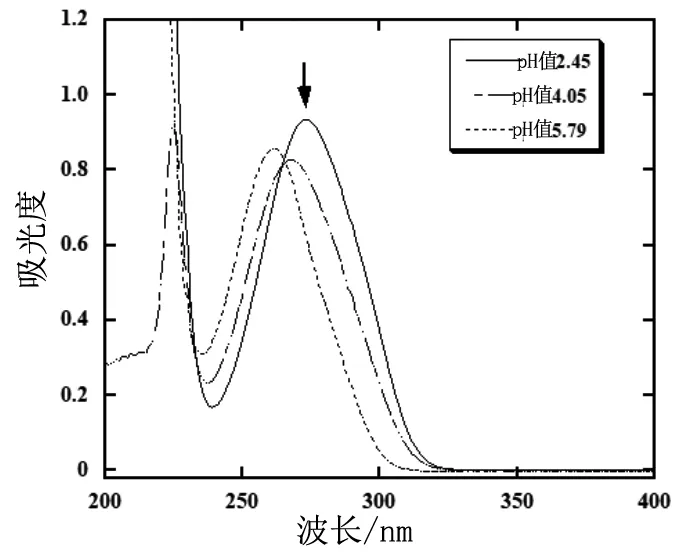
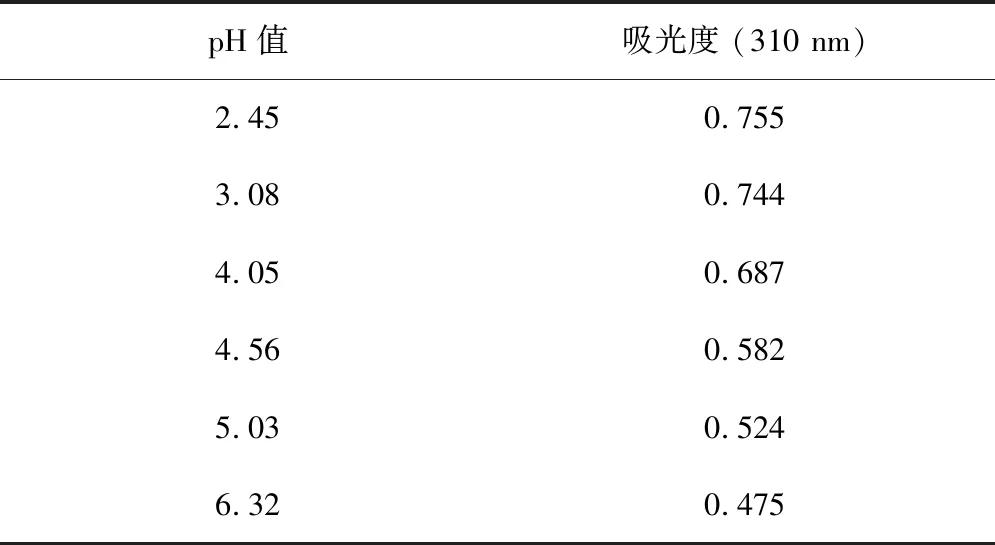
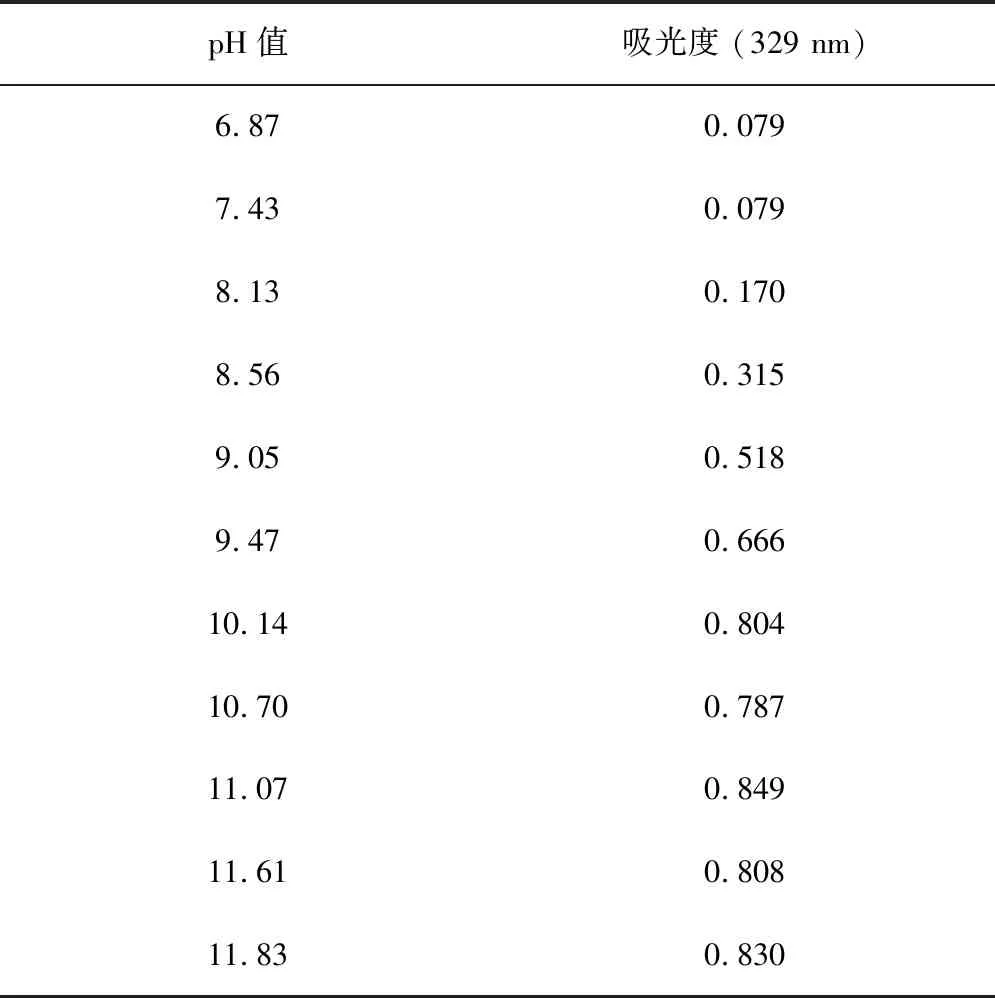
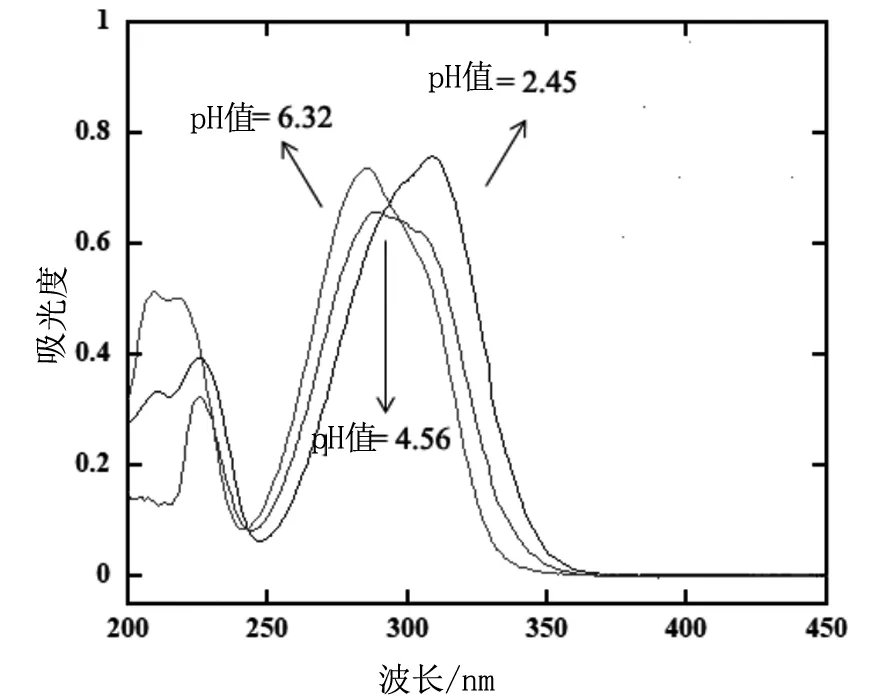
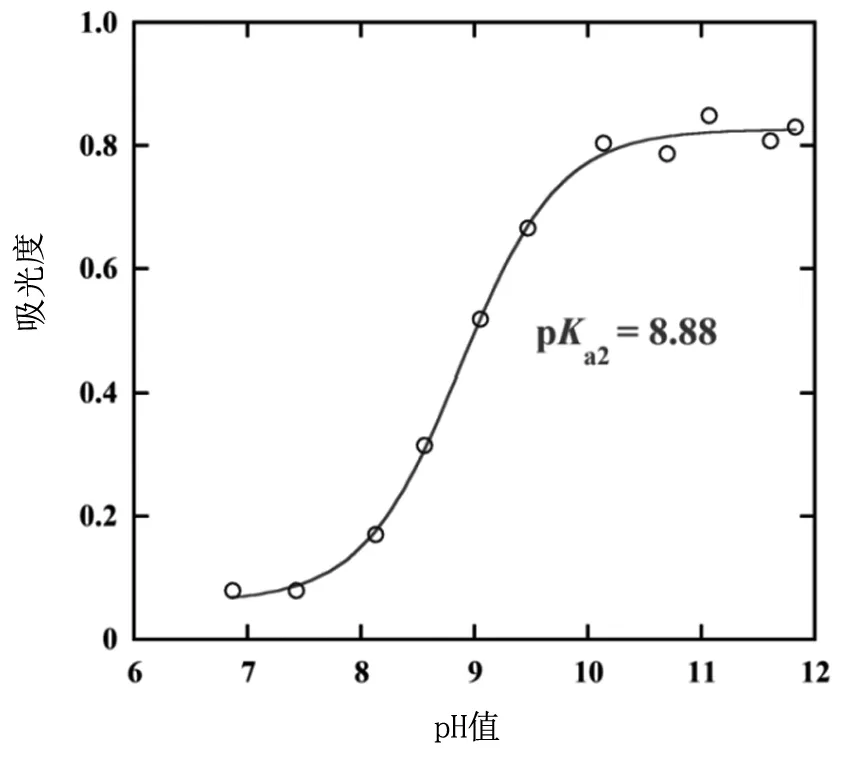
不同的pH值范围各按如下方法配制:1)2.40≤pH值≤3.00由H3PO4和NaH2PO4按一定比例配制;2)3.00 分别称取一定量的丁香酸和对香豆酸固体溶解在1.0 mol/L NaClO4溶液中作为储备液,然后用不同缓冲溶液分别稀释得到0.10 mmol/L丁香酸溶液和0.040 mmol/L对香豆酸溶液(使用时间不超过1 h)。 (1)开启分光光度计电源预热15 min,调节恒温槽温度(控制在(25.0 ± 0.1)℃);(2)打开电脑和软件,设定扫描波长范围:200~400 nm或200~450 nm(采用慢速扫描);(3)放入参比溶液对基线进行校准;(4)装上待测溶液,开始测定。(注意:测量前所有溶液都要恒温10 min。) 在25.0 ℃和1.0 mol/L的离子强度下,我们获得了丁香酸在不同pH值下的光谱图(图3)。可以看出,在273 nm处随着pH值从2.45增加到5.79,吸光度逐渐下降,表1给出了吸光度数值随pH值的变化趋势。 表1 25.0 ℃和1.0 mol/L 离子强度下0.10 mmol/L丁香酸在不同pH值的缓冲溶液中273 nm处的吸光度数据 图3 0.10 mmol/L丁香酸在pH值为2.45,4.05和5.79缓冲溶液中的吸收光谱图 图4 0.10 mmol/L丁香酸在pH值为6.87至11.83的缓冲溶液中的吸收光谱图 当pH值从6.87逐渐增加到11.83时,在260 nm和302 nm处丁香酸的光谱变化非常明显,并且我们观察到在243 nm 和273.4 nm处各存在一个等吸收点,说明其形态II和III两者之间在互相变换。表2给出了在260 nm和302 nm处吸光度数值随pH值的变化。 表2 25.0 ℃和1.0 mol/L离子强度下0.10 mmol/L丁香酸在不同pH值的缓冲溶液中260 nm和302 nm处的吸光度数据 同样地,我们也得到了在25.0 ℃和1.0 mol/L的离子强度下对香豆酸在不同pH值下的光谱(图5和6),表3~4分别给出了在310 nm和329 nm处对香豆酸的吸光度数值随pH值的变化。 表3 25.0 ℃和1.0 mol/L 离子强度下0.040 mmol/L对香豆酸在不同pH值的缓冲溶液中310 nm处的吸光度数据 表4 25 ℃和1.0 mol/L 离子强度下0.040 mmol/L对香豆酸在不同pH值的缓冲溶液中329 nm处的吸光度数据 图5 0.040 mmol/L对香豆酸在pH值为2.45,4.56和6.32缓冲溶液中的吸收光谱图 图6 0.040 mmol/L对香豆酸在pH值为7.43,8.56和11.83缓冲溶液中的吸收光谱图 对于上述光谱随pH值的变化,可以用方程(1)和方程(2)来进行定量的分析[12],式中[SA]tot=1.0×10-4M,ε1、ε2和ε3分别为丁香酸三种质子化形态的摩尔吸光系数。 使用方程(1)对表1中的数据进行非线性最小二乘方拟合,拟合的结果如图7所示。拟合结果非常理想,得到了pKa1=4.08。再次使用方程(2)对表2中的数据进行非线性最小二乘方拟合,拟合的结果如图8所示,得到的结果为:260 nm 下pKa2=8.78,302 nm下pKa2=8.80。因此在两个不同波长得到的结果非常一致,取平均值pKa2=8.79。 图7 使用方程(1)对表1数据拟合得到的关系图 图8 使用方程(2)对表2数据拟合得到的关系图 然后运用方程(3)~(4)分别对表3~4中的数据进行非线性最小二乘方拟合[12],式中[p-CA]tot=4.0×10-5mol/L,ε1、ε2和ε3分别为对香豆酸三种质子化形态的摩尔吸光系数。 拟合结果分别如图9、10所示,从而得到了对香豆酸的pKa1=4.43、pKa2=8.88。 图9 使用方程(3)对表3数据拟合得到的关系图 图10 使用方程(4)对表4数据拟合得到的关系图 在25.0 ℃和1.0 mol/L离子强度下,我们通过研究丁香酸和对香豆酸UV-Vis光谱随pH值的变化,利用光度滴定法分别得到了二者的解离常数pKa1和pKa2,在获得这些解离常数后就可以很容易地分析丁香酸和对香豆酸的3种质子化形态随pH的分布情况,这将对研究它们的抗氧化反应机理具有重要的意义。1.3 待测溶液配制
1.4 光谱测量
2 结果与讨论
2.1 光谱随pH值的变化



2.2 丁香酸和对香豆酸解离常数pKa1和pKa2的导出
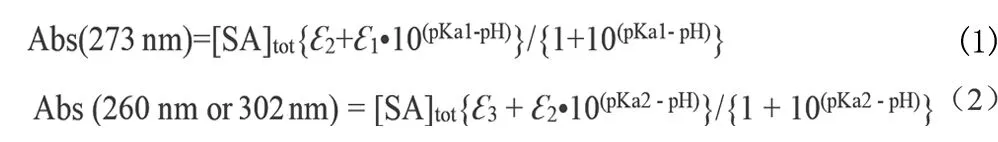




3 结论
