口服抗妇炎胶囊大鼠血浆中移行成分的鉴定*
2023-11-18黄家宇王铭菊刘星村胡滨吴军汤磊李莉
黄家宇,王铭菊,刘星村,胡滨,吴军,汤磊**,李莉**
(1.贵州医科大学 药学院,贵州 贵阳 550025;2.贵州远程制药有限责任公司 质量部,贵州 贵阳 550018)
抗妇炎胶囊是一种源于苗族验方的贵州名优苗族药制剂,全方由杠板归、苦参、连翘、黄柏、当归、益母草、乌药、赤小豆及艾叶组成,用于治疗湿热下注型盆腔炎、慢性宫颈炎、阴道炎、阴痒、出血、赤白带下及痛经等妇科炎症类疾病,疗效显著[1-3]。抗妇炎胶囊已纳入《国家基本用药目录》,为独家专利苗药制剂。目前,有关抗妇炎胶囊的质量[4-6]和药效作用研究较多[7-10],尚未见其体内作用成分与代谢过程的研究报道,且药效物质基础尚不明确。中药口服后药物成分经消化道吸收入血,或经消化酶等作用分解成次生代谢产物被吸收入血;或经肝微粒体酶代谢成有活性的代谢产物,这些成分在血中转运到达作用部位后发挥药效,中药的血清“移行成分”与药物在体内直接作用的物质密切相关。以药物化学研究方法为基础的中药血清药物化学是运用现代分离技术及多维联用技术,该方法通过分析口服中药后血中移行成分,阐明其与药效相关性,探索中药药效物质基础,研究其体内过程[11-12]。本研究拟采用超高效液相色谱(ultra high performance liquid chromatography,UPLC)与离子阱-飞行时间质谱(ion trap time of flight mass spectrometry,IT-TOF-MS)技术联用的方法分析口服抗妇炎胶囊后大鼠血浆中的移行成分,鉴定含药血浆中吸收原型成分和代谢产物,以便为抗妇炎胶囊的药效物质基础的确定奠定基础。
1 材料与方法
1.1 实验材料
1.1.1实验动物 6~7周龄无特异病原体(specific pathogen free,SPF)雌性Sprague-Dawley(SD)大鼠12只,体质量200±20 g,购自学校实验动物中心[SCXK(湘)2019-0014],置于室温23±2 ℃,湿度(55±10)%,12 h昼夜交替环境中,自由饮食,饮水,适应性喂养1周。
1.1.2主要药品及试剂 槐定碱对照品(批号wkq21030106)、盐酸小檗碱对照品(批号wkq21022004)及苦参碱对照品(批号wkq21060212)均购于四川省维克奇生物科技有限公司,抗妇炎胶囊(批号20220106,贵州远程制药公司),甲醇、乙腈(德国Merck公司),甲酸(美国Fisher公司)均为色谱纯,水为纯净水。
1.1.3主要仪器 LCMS-IT-TOF液相色谱-离子阱-飞行时间质谱联用仪(日本岛津公司),微量移液枪(德国Eppendorf公司),MS105DU电子分析天平(瑞士Mettler-Toledo公司),H1-16KR冷冻离心机(湖南可成仪器设备公司),KQ250DA型超声波清洗器(昆山超声仪器公司),QQMD200-1氮吹仪(上海启前电子科技公司)。
1.2 研究方法
1.2.1色谱和质谱条件 (1)色谱条件:色谱柱为Shim-pack XR-ODSⅢ(50 mm×2.0 mm,1.6 μm);柱温30 ℃、进样量2 μL、流速0.3 mL/min;流动相为乙腈(B)-0.1%甲酸溶液(A),洗脱程序为0.01~20 min、5%~100% B,20~30 min、100% B。(2)质谱条件:电喷雾离子源(electrospray ionization,ESI),检测器电压为0.15 kV;雾化气体积流量1.5 L/min;正负离子模式下同时采集,扫描范围80~1 200 m/z;曲型脱溶剂装置(curved solvent removal device,CDL)温度30 ℃,加热块温度30 ℃;质谱设为自动多级MS1、MS2全扫描模式,诱导碰撞解离能量50%,离子累积时间20 ms,LCMS solution工作站进行数据采集与分析。
1.2.2对照品溶液的制备 精密称取苦参碱、槐定碱、盐酸小檗碱对照品适量,置于容量瓶中,加甲醇制成各成分质量浓度分别为5.70、6.39、6.00 mg/L混合对照品溶液。
1.2.3抗妇炎胶囊给药样品溶液的制备 取抗妇炎胶囊内容物4.4 g,溶于0.5%羧甲基纤维素钠溶液40 mL,配制成质量浓度为110 g/L的抗妇炎胶囊灌胃药液,储存至4 ℃冰箱中备用。
1.2.4抗妇炎胶囊体外样品溶液的配制 取抗妇炎胶囊内容物0.5 g,置具塞锥形瓶中,加70%甲醇10 mL,称定质量;超声30 min,放冷,70%甲醇补足减失的质量,0.22 μm滤膜滤过,取续滤液,即得抗妇炎胶囊体外样品溶液。
1.2.5血浆样品的制备 实验前12 h内雌鼠禁食不禁水,给药后2 h恢复自由进食,随机均分为给药组和空白组,给药组雌鼠按照0.02 mL/g灌胃抗妇炎胶囊药液、2次/d、连续3 d,空白组雌鼠灌服同等体积的生理盐水;末次给药1 h后10%水合氯醛(3 μL/g)麻醉各组雌鼠,肝门静脉采血,置于含肝素钠采血管中,4 ℃条件下5 000 r/min离心10 min;取上清液,-20 ℃保存,即得含药血浆样品和空白血浆样品。
1.2.6血浆样品的前处理 取“1.2.5”项下各组雌鼠血浆样品,按1∶3的比例加乙腈,涡旋混匀3 min,5 000 r/min离心10 min;沉淀蛋白,取上清液;氮气吹干后加 50%甲醇200 μL,超声10 min,12 000 r/min离心10 min,取上清液,供UPLC-IT-TOF-MS监测分析。
1.2.7样品测定 采用“1.2.1”项下分析条件,对抗妇炎胶囊体外样品、空白血浆及给药血浆样品进行检测分析。
1.3 统计学分析
采用LCMS solution工作站进行数据处理,分析色谱图和色谱峰的质谱信息,对抗妇炎胶囊体外样品、空白血浆及给药血浆样品进行原型成分和代谢物的检测分析。
2 结果
2.1 UPLC-IT-TOF-MS色谱图的采集
采用经优化色谱质谱条件分析样本,对样品进样正负离子模式下同时扫描,所得的空白组、给药组、混合对照品溶液以及抗妇炎胶囊体外提取液的色谱图见图1和图2所示,提示抗妇炎胶囊体外样品化学成分在此条件下分离良好。

注:A为空白血浆,B为含药血浆,C为对照品溶液,D为体外样品溶液;1为苦参碱,2为槐定碱,3为莱曼碱,4为5,6-去氢羽扇豆碱,5为7,11-去氢苦参碱,6为12α-/5a-/9a-羟基槐果碱或氧化槐果碱或黄叶槐碱,7为去氢12α-羟基槐果碱,8为9α-羟基槐胺碱还原化,9为小檗碱。
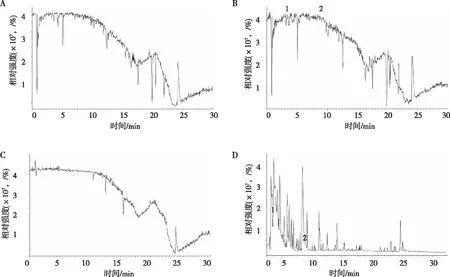
注:A为空白血浆,B为含药血浆,C为对照品溶液,D为体外样品溶液;1为番石榴酸,2为高丽槐素葡萄糖醛酸化产物。
2.2 移行成分
本研究参照对照品二级质谱,鉴定了大鼠口服抗妇炎胶囊后血浆中的11个移行成分,其中原型成分8个、代谢产物3个,抗妇炎胶囊吸收原型成分和代谢产物的液相色谱-质谱数据见表1;鉴定出的8个原型成分为来源于苦参的苦参碱、槐定碱、莱曼碱、12α-/5a-/9a-羟基槐果碱或氧化槐果碱或黄叶槐碱、5,6-去氢羽扇豆碱、7,11-去氢苦参碱、番石榴酸和来源于黄柏的小檗碱,3个代谢产物分别是12α-羟基槐果碱、9α-羟基槐胺碱及高丽槐素的体内代谢物,其裂解、代谢途径见图3~7。

表1 抗妇炎胶囊吸收原型成分和相关代谢产物的液相色谱-质谱数据
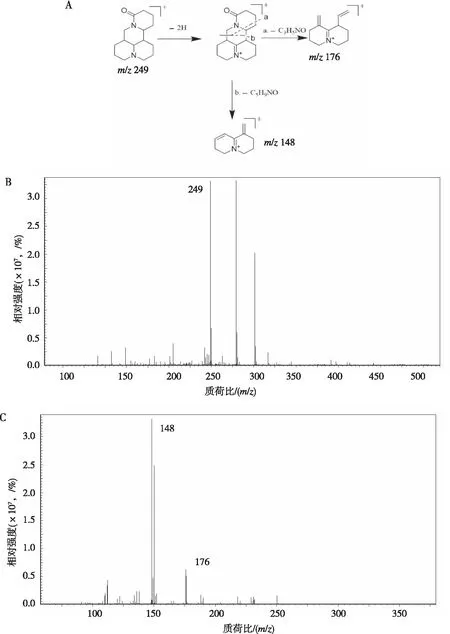
注:A为苦参碱裂解途径,B为苦参碱一级质谱图,C为苦参碱二级质谱图。
2.3 主要色谱峰的质谱分析
2.3.1化合物1正离子模式下,化合物1在含药血浆总离子图与抗妇炎胶囊总离子图中保留时间基本一致,二级质谱碎片一致,准分子离子峰m/z249[M+H]+相对丰度较强,拥有共同二级碎片m/z176、148等,参考对照苦参碱对照品的二级质谱图,推测其结构为苦参碱,可能的裂解途径见图3。
2.3.2化合物7化合物7经计算得到精确分子式为C15H20N2O2,正离子模式下一级质谱准分子离子峰为m/z261[M+H]+,分子量比12α-羟基槐果碱少2 Da(-2H),二级质谱中存在m/z243[M+H-H2O]+等特征碎片离子,结合文献,推测结构为去氢12α-羟基槐果碱,体内可能的代谢途径见图4。

图4 12α-羟基槐果碱的代谢途径
2.3.3化合物8化合物8经计算得到精确分子式为C15H22N2O2,正离子模式下一级质谱准分子离子峰为m/z263[M+H]+,分子量比9α-羟基槐胺碱多2 Da(+2H),二级质谱中存在m/z245[M+H-H2O]+等特征碎片离子,结合文献,推测结构为9α-羟基槐胺碱还原化产物,体内可能的代谢途径见图5。

图5 9α-羟基槐胺碱还原化
2.3.4化合物9正离子模式下,化合物9与抗妇炎胶囊总离子图中小檗碱的保留时间基本一致,二级质谱碎片一致,准分子离子峰m/z336[M+H]+相对丰度最强,拥有共同二级碎片m/z321、292等,参考其它研究,对照小檗碱对照品的一、二级质谱图,推测其结构为小檗碱,可能的裂解途径见图6。
2.3.5化合物11化合物11保留时间8.393 min,经计算得到精确分子式C22H20O11,负离子模式下一级质谱准分子离子峰为m/z 459[M-H]-,分子量比高丽槐素多176 Da(+C6H8O6),二级质谱中存在m/z283[M-H-C6H8O6]-碎片离子,结合文献,推测结构为高丽槐素的葡萄糖醛酸化产物,体内可能的代谢途径见图7。

图7 高丽槐素葡萄糖醛酸化产物
3 讨论
课题组前期已对抗妇炎胶囊体外样品溶液正负离子模式下进样检测分析。经过分析比较精确质荷比及其质谱裂解规律、文献数据等信息,从抗妇炎胶囊70%甲醇提取液中共推断了80个化合物,包括生物碱类37个,黄酮及其苷类27个,有机酸类7个,苯丙素及其苷类3个,苯乙醇苷类3个,其他类化合物3个。本研究分别对单次给药和连续多次给药两种给药方案所得血中移行成分结果进行对比分析,结果表明两种方法下均测得了原型移行成分8个,单次给药仅测得代谢产物1个(去氢 12α-羟基槐果碱);连续多次给药方法下测得代谢产物3个(去氢12α-羟基槐果碱、9α-羟基槐胺碱还原化及高丽槐素葡萄糖醛酸化产物),分析代谢产物有差异的原因可能是多次给药,有利于药物转化吸收,代谢产物易达到较高的浓度而被测出[20]。在样品处理方法上,考察了乙腈、乙酸乙酯和甲醇的去蛋白效果,确定使用乙腈作为处理溶剂。
大鼠口服抗妇炎胶囊后的含药血浆中共鉴定出入血成分11个,其中来自苦参的多为生物碱类成分,苦参中的苦参碱等生物碱类成分,具有广泛的生物活性,其中苦参碱具有抗肿瘤、免疫调节、抗菌、抗病毒、抗寄生虫及抗炎等药理作用[21-22]。在妇科疾病的治疗领域中,苦参碱还具有抗妇科肿瘤作用,具有保护乳腺、子宫内膜及阴道上皮细胞的功能,还能对抗各种致病因子引起的上皮细胞炎性病变[23]。据文献报道,槐定碱和槐胺碱具有抗菌、抗病毒、抗炎、抗肿瘤及抗心律失常等药理活性[24];来自黄柏的小檗碱,具有抗炎、抗菌、抗病毒、降脂、降压、抗氧化的作用[25],对乳腺癌、卵巢癌、宫颈癌、子宫内膜癌等妇科肿瘤具有抑制作用。本研究检出的移行成分与抗妇炎胶囊临床上主要用于治疗盆腔炎、阴道炎、慢性宫颈炎等疾病的功效相符。按照药物代谢途径分析,代谢产物去氢12α-羟基槐果碱和9α-羟基槐胺碱还原产物为抗妇炎胶囊的Ⅰ相代谢产物,高丽槐素葡萄糖醛酸化产物为该制剂的Ⅱ相代谢产物。这些原型成分和代谢产物,可能是抗妇炎胶囊潜在的活性成分。目前临床上已将抗妇炎胶囊用于治疗各类宫颈炎、阴道炎,也被试用于治疗乳腺癌、卵巢癌、宫颈癌和子宫内膜癌等疾病[26]。
本研究通过UPLC与高分辨IT-TOF-MS技术联用检测含药血浆中的代谢产物及原型成分,在正负离子检测模式下鉴定的药源性成分,多为制剂处方中苦参或黄柏的成分或代谢产物,其他药味可能是给药后被快速代谢或入血含量低无法检测而未被检出。本研究初步探究了抗妇炎胶囊在血中的移行成分,为该制剂的药效物质基础研究奠定了基础。
