基于TLR4/MyD88信号通路探究miR-326对抑郁模型脑组织的保护作用
2023-11-06刘威
刘 威
(河北省衡水市人民医院精神心理科,河北 衡水 053000)
抑郁症是最常见的精神疾病之一,症状包括情绪低落、兴趣下降,严重者有自杀倾向[1]。抑郁症的发病率逐年上升。然而,目前的传统抗抑郁药物可能需要数周至数月才能产生有效的反应,约三分之一患者对现有的治疗策略没有反应[2]。抑郁症最有可能是由遗传倾向和环境因素(如早期生活经历、生活事件和慢性压力)之间的复杂相互作用引起的[3]。在抑郁个体的大脑和抑郁的动物模型中已经一致地描述了神经可塑性变化[4-5]。表观遗传机制可能提供了环境压力因素和基因表达之间的联系[6],微小RNA(miRNAs)是由22~25个核苷酸序列组成的非编码RNA,已被确定为生物过程的调节物。miRNAs可以特异性地与其靶mRNA的3'非翻译区(untranslated regions,UTR)结合,以促进mRNA的降解或抑制其翻译[7]。MiRNAs在脑组织中大量存在,并在调节脑功能中发挥许多关键作用,特别是在神经再生、神经可塑性和神经元功能方面[8]。TLR4信号通路参与先天免疫反应和适应性免疫反应的调节,并与抑郁症的免疫炎症过程密切相关[9],是慢性不可预测轻度应激抑郁小鼠海马炎症的主要参与者[10]。TLR4通过胞内白细胞介素 1β(interlenkin 1β,1L-1β)同源结构域激活,利用下游信号分子MyD88,介导效应分子核因子κB(nuclear factor kappa-B,NF-κB)的活化,NF-κB转位入核磷酸化,调节免疫炎症因子的表达[11]。本研究旨在探究抑郁模型中参与脑组织保护的相关机制,建立CUMS大鼠模型,基于下游TLR4/MyD88筛选出上游靶向miR-326,通过干预miR-326来探究miR-326/TLR4/MyD88是否参与了抑郁模型脑组织的保护作用。
1 材料与方法
1.1实验动物 雄性Sprague-Dawley大鼠(200~220 g,8周)由湖北贝恩特生物科技有限公司提供,许可证号SYXK(鄂)2021-0119。实验动物被饲养在干净的动物房中,并给予免费的食物和水,12 h的昼夜交替光照,温度(23±1)℃,湿度(55±2)%。适应性喂养1周后进行实验。
本研究按照《实验动物护理和使用指南》进行,并经医院实验动物中心批准。
1.2慢性不可预测温和应激(chronic unpredictable mild stress,CUMS)诱导抑郁模型 CUMS模型诱导大鼠抑郁[12]。应激方法有束缚、冰水游泳、禁食、禁水、昼夜颠倒、噪音刺激、夹尾等。大鼠每天至少接受一次应激刺激,避免连续4周使用相同的刺激。对照组大鼠(n=6)不接受任何刺激。观察并记录大鼠体重的变化,制备4周CUMS模型后,随机选择18只大鼠,采用蔗糖偏好测试(sucrose preference test,SPT)、旷场测试(open field test,OFT)、强迫游泳测试(forced swim test,FST)、高架十字迷宫(elevated plus maze,EPM)检测大鼠的抑郁样行为。
为了研究miR-326对抑郁大鼠的作用,将CUMS大鼠随机分为CUMS组、CUMS+agomiR NC组和CUMS+agomiR 326组,每组6只。最后1次CUMS暴露后,进行侧脑室注射[13]。具体步骤如下,首先使用戊巴比妥钠(40 mg/kg)麻醉大鼠,将大鼠置于立体定位仪上。在颅骨上的皮肤上做一个切口,用微钻在目标位置(双侧海马)上方的颅骨上打2个小洞。使用微量注射器将20 μL miR-326 agomiR溶液(含有10 nmol miR-326 agomiR)或agomiR NC(含有10 nmol agomiR NC)(广州市锐博生物科技有限公司,广州,中国)双向注射到海马内[14]。注射时间超过5 min,允许缓慢扩散。对照组大鼠以同样的方式注射相同数量的盐水。在注射后1周进行行为测试,之后将大鼠安乐死,收集解剖其大脑并分离下丘脑、海马组织用于生化分析。
1.3SPT SPT是一种广泛接受的类似抑郁行为的测量方法[15]。在测试之前,大鼠保持禁食水,并且用2瓶1%蔗糖溶液使大鼠适应环境。在接下来的24 h内,用自来水替换其中一瓶1%蔗糖溶液。测试当天,给大鼠200 mL自来水和200 mL 1%蔗糖溶液。12 h后,将瓶子交换1次。24 h后,收集瓶子。蔗糖消耗/总水消耗表示为蔗糖偏好。
1.4OFT OFT被用来评估动物的运动。该装置是一个120 cm×90 cm×35 cm的不透明开口盒,周围是黑色的。盒子的底部被白线分成25个正方形。外围的16个方块被认为是外围站点,中间的9个方块被认为是中心区域。在安静的环境中,将大鼠单独放置在装置的角落中,并允许其自由探索5 min。测试前30 min,动物被放入实验室以适应环境。每次测试后,用70%的乙醇彻底清洗该装置。通过VideoTrack动物行为分析系统(VideoTrack 3.0,Viewpoint,French)收集和分析大鼠活动数据。
1.5EPM 使用EPM检测大鼠的焦虑样行为[16]。大鼠被放置在EPM装置的中间,用摄像机记录其行为5 min。大鼠在张开的双臂中度过的时间百分比用作评价焦虑样行为的指标。每次测试后,将迷宫清理干净。
1.6FST FST是评估动物绝望行为的经典方法,可以显示啮齿类动物的抑郁程度[15]。将大鼠置于水温为(25±1)℃、深度为30 cm的垂直有机玻璃圆筒(45 cm×20 cm)中。在5 min内记录大鼠的静止时间。
1.7酶联免疫吸附测定(enzyme-linked immunosorbent assay,ELISA) 定量ELISA试剂盒(ZK-R3347,ZK-R3052和ZK-r 3397;深圳子科生物科技有限公司,深圳,中国)用于测定下丘脑中去甲肾上腺素(norepinephrine,NE)、多巴胺(dopamine,DA)、5-羟色胺(5-hydroxytryptamine,5-HT)的含量。所有操作均严格按照试剂盒说明书进行。
1.8实时荧光定量聚合酶链反应(real-time quantitative polymerase chain reaction,qRT-PCR) 将大鼠海马组织磨碎并加入细胞裂解物中。使用RrimeScript从细胞中提取总RNARTreagen试剂盒(TaKaRa,大连,中国)。用紫外分光光度计检测总RNA纯度,以A260/A280≥1.80为合格标准。根据DBI-2220 Bestar的说明,将来自每个样品的1 μg RNA逆转录成cDNA铥qPCR RT试剂盒(TaKaRa)。使用SYBR进行实时PCR Premix Ex Taq试剂盒(TaKaRa)和iQ5实时PCR检测系统(Bio-Rad Laboratories,California,USA)。PCR反应条件为:95 ℃ 3 min,95 ℃ 30 s,52 ℃ 30 s,73 ℃ 30 s,连续循环38次。引物序列见表1,U6用作内参。采用2-δδCt方法。

表1 qRT-PCR引物序列
1.9双荧光素酶实验 为了阐明miR-326的靶向作用,进行了体外荧光素酶实验,测试miR-326与TLR4 3'UTR之间的相互作用。Targetscan生物信息学网站(https://www.targetscan.org/vert_72/)显示,TLR4是miR-326的潜在目标。锐博生物科技有限公司构建并合成了4种不同的重组载体:pmirGLO-TLR4-WT、pmirGLO-TLR4-MUT。使用Lipofectamine 2000(Invitrogen)将报告载体与miR-326 mimic(或miR-NC)共同转染到HEK293T细胞(中国科学院细胞库,上海,中国)。
1.10Western Blot 总蛋白提取试剂盒(Beyotime,北京,中国)用于从海马组织中提取总蛋白。使用增强型BCA蛋白检测试剂盒(Beyotime)测量蛋白浓度。装载总共50 μg蛋白质,并通过SDS-PAGE分离。然后,将蛋白质转移到聚偏二氟乙烯膜(Immobilon,Millipore,MA)上。室温下用含5%脱脂牛奶的TBST封闭膜2 h。然后,将膜与第一抗体在4 ℃孵育过夜。一抗具体信息如下:TLR4(1∶1 000,ab217274,135 000)、MyD88(1∶1 000,ab219413,33 000)、β-actin(1∶1 000,ab8227,42 000)。用TBST洗涤后,将膜与HRP缀合的山羊抗兔第二抗体在室温孵育2 h。然后,使用增强化学发光试剂显影该膜。所有抗体购自abcam(Cambridge,MA,USA)用NIH Image J 7.0分析每个条带的灰度值。
1.11统计学方法 应用SPSS 21.0统计学软件处理数据。计量资料比较采用独立样本t检验、单因素方差分析和SNK-q检验。P<0.05为差异有统计学意义。
2 结 果
2.1CUMS导致大鼠抑郁样行为 慢性低强度应激是抑郁症的主要原因之一,CUMS通过每天给予模型动物不同的刺激来诱导抑郁。CUMS组大鼠体重、蔗糖消耗量、OFT中心区域停留时间及张开手臂时间低于对照组,FST静止时间明显高于对照组,差异有统计学意义(P<0.05)。见表2。表明,CUMS导致大鼠抑郁样行为。
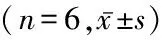
表2 慢性不可预测的轻度应激导致大鼠抑郁样行为
2.2过表达miR-326抑制大鼠抑郁样行为 qRT-PCR显示,暴露于CUMS后,CUMS组大鼠海马组织中miR-326表达显著低于对照组,差异有统计学意义(P<0.05),为了研究miR-326对CUMS大鼠的作用,将miR-326 agomir注射到大鼠海马中,CUMS+agomiR 326组大鼠海马组织中miR-326表达高于CUMS+agomiR NC组,差异有统计学意义(P<0.05)。见表3。体重及行为测试显示,CUMS+agomiR 326组大鼠体重、蔗糖消耗量、OFT中心区域停留时间及开放臂停留时间显著高于CUMS+agomiR NC组,FST静止时间明显低于CUMS+agomiR NC组,差异有统计学意义(P<0.05)。见表4。
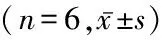
表3 qRT-PCR检测大鼠海马组织miR-326表达水平
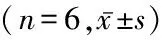
表4 过表达miR-326抑制大鼠抑郁样行为
2.3过表达miR-326保护抑郁大鼠脑组织 根据神经激素假说,抑郁症与DA和/或5-HT代谢调节活动有关。检测下丘脑中的神经递质含量,结果显示,CUMS组NE、DA和5-HT水平显著低于对照组,而上调miR-326的表达后,CUMS+agomiR 326组NE、DA和5-HT水平显著高于CUMS+agomiR NC组,差异有统计学意义(P<0.01)。见表5。表明,海马组织中过表达miR-326保护抑郁大鼠脑组织。
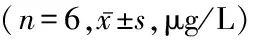
表5 过表达miR-326保护抑郁大鼠脑组织
2.4miR-326靶向调控TLR4/MyD88信号通路发挥对抑郁大鼠的保护作用 为了进一步研究miR-326对抑郁大鼠的潜在作用机制,通过TargetScan(http://www.targetscan.org/vert_72/)预测了miR-326的下游靶基因,并在其中关注到了TLR4。Toll样受体(Toll-like receptors,TLRs)是先天免疫的识别蛋白,发现于脑室周围器官和脉络丛。因此推测miR-326通过TLR4对抑郁大鼠发挥保护作用。TargetScan网站预测miR-326与TLR4的结合位点(图1),然后在HEK293T中进行了双荧光素酶报告实验来验证其靶向结合关系,见表6。Western blot检测各组大鼠海马组织TLR4结果显示,经过CUMS诱导后,CUMS组大鼠TLR4蛋白和MyD88蛋白水平显著高于对照组,而在过表达miR-326后,CUMS+agomiR 326组大鼠TLR4蛋白和MyD88蛋白水平显著降低,差异有统计学意义(P<0.05),见表7。表明,miR-326靶向miR-326靶向调控TLR4/MyD88信号通路发挥对抑郁大鼠的保护作用。

图1 TargetScan网站预测miR-326与TLR4靶向结合位点
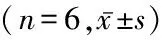
表6 双荧光素酶实验检测miR-326与TLR4靶向结合
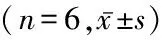
表7 Western blot检测各组海马组织TLR4/MyD88蛋白的表达
3 讨 论
抑郁症是一种常见的精神疾病,其具有一系列对身体、认知、情感和社会活动过程产生影响的症状。它的特点主要是情绪低落,易悲伤,易失眠,且对学习、工作、生活缺乏兴趣等等。作为造成全球社会负担的主要原因之一,抑郁症的主要治疗方法依赖于药物和心理干预[17-18]。虽然这些疗法具有一定的良性效果,但仍有三分之一接受这些抗抑郁药物干预的患者并未产生正反馈,而其他即使产生药物良性反馈的患者由于药物本身的许多不良反应而症状没有得到完全缓解或时常复发[19-20]。因此,探究抑郁症的相关具体调控分子机制,显得尤为重要。临床证据已经表明了神经炎症在抑郁症等脑部疾病中起到的重要作用[21],临床研究和基于啮齿类动物的研究表明,反复暴露于社会和环境的刺激中会引起体内免疫相关的剧烈变化,例如:血液和大脑中促炎细胞因子的大量积累和抗炎细胞因子的减少[22-24],而作为大脑中先天免疫系统中第一道防线的主要细胞成分,小胶质细胞在神经炎症的发生发展中发挥了至关重要的作用[25]。活化的小胶质细胞可以释放促炎细胞因子,如白细胞介素(interleukin,IL)-1、IL-6、肿瘤坏死因子α 和一氧化氮,以及抗炎细胞因子,如IL-4和IL-10。已经有研究明确表明,人类在急性心理应激的刺激下会持续增加循环的炎症因子[26]。CUMS是一种为了模拟社会和环境应激源下心理变化的实验方法[27],已被证实可以引起海马小胶质细胞激活[28-29]。本研究通过CUMS诱导建立抑郁样大鼠模型,并通过各种行为学实验来证实模型的成功建立。
MicroRNA作为一种非编码RNA已经被证明富含于脑组织中,并与多种脑部疾病相关联。miR-139-5p是大脑中富含的神经元miRNA,对抑郁大鼠的神经元起保护作用[30];Li等[31]的研究表明,miR-26a-3p在抑郁大鼠的海马组织中显著下调,其可增强自噬/溶酶体活性,促进突触的可塑性最终抑制神经元凋亡。还有一项研究表明,miR-326低表达可能与抑郁有潜在的联系[32],本研究通过检测CUMS诱导的抑郁大鼠模型海马组织中miR-326发现其呈低表达,进一步,通过miR-326 agomiR上调其在海马中的表达发现其可能对抑郁样行为起抑制作用。
TLR4/MyD88参与了抑郁症的发展[33],本研究通过TargetScan数据库筛选出TLR4上游靶向调控miR-324,并进一步检测到当调控miR-324时,下游TLR4/MyD88通路随之发生变化,这预示着TLR4/MyD88通路可能参与miR-326调控的大鼠抑郁样行为。
总之,在CUMS诱导的抑郁大鼠中,调控miR-326可能通过TLR4/MyD 88对抑郁样行为及大鼠海马区产生影响。虽然仅探究了单一一条分子机制,但未来随着分子机制的一一解析,现在的成果终将成为攻克该病的基石。
