氧化锌烟尘浸出液中锗的分离富集
2023-10-13王梓澎邓志敢陈春林戴兴征魏昶李兴彬李旻廷樊刚
王梓澎,邓志敢,2,陈春林,,戴兴征,魏昶,2,李兴彬,2,李旻廷,2,樊刚,2
(1. 昆明理工大学 冶金与能源工程学院,云南 昆明,650093;2. 昆明理工大学 省部共建复杂有色金属资源清洁利用国家重点实验室,云南 昆明,650093;3. 云南驰宏锌锗股份有限公司,云南 曲靖,655000)
锗是一种重要的稀散元素,因其独特的物理化学性质,广泛应用于光导纤维、红外光学、电子工业等领域[1-2]。锗在地壳中分布较散,在自然界中几乎没有可独立开采的锗矿床[3],主要通过金属冶炼过程中锗的富集物、煤的燃烧产物和锗加工过程中各种废料回收提取。锗具有亲硫性,常伴生于硫化铅锌矿中,我国云南会泽、广东韶关地区铅锌矿中的锗是我国主要的锗资源[1]。
在湿法炼锌过程中,单宁沉锗工艺具有较高的锗回收效率,其工艺流程是通过硫酸浸出富锗烟尘,得到富含锗的浸出液,再通过单宁沉锗得到单宁锗渣[4],最后经洗涤、脱水、干燥后灼烧得到锗精矿。据研究,单宁与锗形成络合物,每个锗原子可接受6 对孤电子,生成一种六配位螯合物,同时利用单宁沉锗,单宁酸消耗量为锗的25~30倍[5-7]。周兆安[8]提出中和沉淀-铁粉还原工艺回收湿法炼锌沉矾上清液中锗,获得锗沉淀率在99%以上,铁沉淀率接近100%,中和渣中锗含量为0.217%,中和渣经弱酸浸出后,锗含量为0.335%。吴慧[9]提出从氧化锌粉中回收锗,经浸出-单宁沉锗流程后,锗直收率在78%~83%。利用单宁沉锗存在单宁消耗量大、单宁酸不能循环使用[1]等问题,并且近年来单宁价格大幅上涨,导致工业成本增加,经济效益大幅降低,同时,大量单宁的加入使得湿法炼锌体系中有机物含量升高,且单宁酸在锌的电解液中能稳定存在8~13 d,降低锌的电解效率[10],增加能耗。
为了解决上述问题,本文作者以氧化锌烟尘浸出液为原料,工业氧化锌烟尘为中和剂,通过中和沉淀-浸出富集锗,基于时间、pH、温度等实验条件及中和剂利用、锗的沉淀展开两段逆流中和沉淀流程,沉淀溶液中含有锗、铁、砷、硅,经除杂后的沉锗后液可直接返回锌冶炼系统;为了验证中和渣中锗浸出效果,在氧压-常压条件下利用硫酸浸出,溶液中铁、砷、硅进入固相,得到富锗浸出液,该过程不引入有机物,在富集锗的同时起到分离、除杂的目的。经除杂后的浸出液可后续用于直接制备GeCl4。
1 实验部分
1.1 实验原料
由于工业氧化锌烟尘来源方便易于获得、经济效益高且后续处理较为简单,因此,选用云南某企业产出的工业氧化锌烟尘作为中和剂。氧化锌烟尘浸出液和工业氧化锌烟尘的化学成分见表1和表2,借助XRD 和SEM-EDS 对工业氧化锌烟尘进行品相组成和微观形貌分析,其XRD 图谱和SEM-EDS图谱如图1和图2所示。

图1 工业氧化锌烟尘XRD图谱Fig. 1 XRD pattern of industrial zinc oxide dust

图2 工业氧化锌烟尘SEM-EDS图谱Fig. 2 SEM-EDS images of industrial zinc oxide dust

表1 氧化锌浸出液主要化学成分(质量浓度)Table 1 Main chemical constituents of zinc oxide leaching solutionmg/L

表2 工业氧化锌烟尘主要化学成分(质量分数)Table 2 Main chemical constituents of industrial zinc oxide dust%
氧化锌烟尘浸出液pH=1.3~1.5,其中,锗和硅大部分以锗酸和硅酸的形式存在。由表1 可知,浸出液中锗质量浓度为209 mg/L,铁含量较高且以Fe2+为主,需避免在中和沉淀过程中大量的Fe2+被氧化成Fe3+,水解致使铁沉淀率过高导致渣率过大的问题;浸出液中含有砷和硅,中和沉淀时会和铁一起沉淀。
由表2可知,氧化锌烟尘中主要有价金属锌含量(质量分数)为56.66%,锗含量较高,具有很高的回收价值,其中硫化物的含量较高包括ZnS、PbS等,可见该工业氧化锌烟尘中杂质较多且含量较高。
由图1 可知:工业氧化锌烟尘主要成分为ZnO、ZnS、PbS,其中,ZnO 起到了中和作用。由图2可看出:氧化锌烟尘颗粒较小,大部分为絮状聚集,同时也有球状形态,分布不均。其中EDS图谱4个点出现了较强的锌、铅、硫、硅等衍射峰,且分布较为集中,可以推测为氧化锌、硫化锌与硫化铅的混合物,也含有锌或者铅的硅酸盐成分。有球形集团的形貌,可以推测是以氧化锌包裹的硫化铅为主的颗粒团[11]。同时,锌、铅、硫等元素分布集中,可推测主体为ZnO、ZnS 和PbS,铁、硅、砷等元素分布较散,附着在ZnO、ZnS和PbS等主体物质上。由于锗亲硅属性,锗大部分赋存于硅酸盐中,部分赋存于金属形成的固体中,同时还有少量以锗的氧化态和硫化态赋存[11],工业氧化锌烟尘中的锗可与浸出液中的锗一起回收富集。该工业氧化锌烟尘中有易浸出的氧化锌、也有难浸出的物相,同时也含有大量的硅,在浸出过程中硅由于游离在溶液中不能聚合长大,会增加固液分离的难度,使得矿浆较难抽滤。
1.2 实验原理
中和沉淀实验是通过溶液中各离子水解后形成相应的水解产物,利用其性质使溶液中锗、铁、砷、硅沉淀下来。实验过程通氧,促使溶液中Fe2+和As3+氧化成Fe3+和As5+,但实验过程需控制通氧量,否则会生成大量Fe3+,导致产渣量过大。
研究表明,Ge4+生成氢氧化物沉淀pH=2.72~3.36,Fe3+生成氢氧化物沉淀pH=1.6,Fe2+生成氢氧化物沉淀pH=6.7,Zn2+生成氢氧化物沉淀pH=5.9[1],因此,通过中和剂调节体系pH=3.5~5.2 的范围内,使溶液中Ge4+和Fe3+生成相应的氢氧化物沉淀下来,同时可防止Fe2+和Zn2+水解。
锗在硫酸溶液中有很多形态,当溶液pH=2.5~7 时,以阴离子状态为主[12]。氧化锌烟尘浸出液pH=1.3~1.5,溶液中锗主要以Ge4+存在,同时含有锗酸[13]。当溶液pH 升高时,锗则以锗酸氢根和重锗酸根存在且带负电荷,由于Fe(OH)3胶体带正电荷,会吸附溶液中带负电荷的锗酸氢根和重锗酸根并一起沉淀下来,该过程可用Langmuir 等吸附等温式描述[1,13]。同时,pH升高,溶液中H+减少,会促进锗酸分解,促使溶液中锗的酸根离子增加,使得产生的Ge-Fe共沉淀增加。
在氧化锌烟尘浸出液中,砷主要以高价的配位阴离子存在,实验过程中通氧,因此,溶液中砷主要以As5+的状态存在。在中和沉淀过程中,当pH<3时,砷则以砷酸铁的稳定形式沉淀,当pH>3时,则与会水解产生的Fe(OH)3胶体形成共沉淀。同时,As5+也会形成砷酸盐沉淀[14]。
在氧化锌烟尘浸出液中,硅主要以硅酸和游离的SiO2方式状态存在,由于SiO2表面带负电荷,会被带正电荷的Fe(OH)3吸附。当加入中和剂后,溶液pH 升高,酸度降低导致硅酸凝聚,随Fe(OH)3一起沉淀。同时,工业氧化锌烟尘中含有部分可溶硅,在中和过程中会进入沉锗后液。
1.3 实验方法
两段逆流中和沉淀-浸出富集锗流程如图3所示。

图3 两段逆流中和沉淀-浸出实验流程Fig. 3 Two-stage countercurrent neutralization precipitation-leaching experiment procedure
将一定量的氧化锌烟尘浸出液放置于三口烧瓶中,放置于恒温水浴锅内进行加热,当温度到达预设值后,称取一定量的工业氧化锌烟尘加入三口烧瓶中。固定搅拌速度为400 r/min,按通氧量60 L/h通入氧气并开始计时,每隔0.5 h通过pH计和pH 试纸测量中和液pH,保证中和液pH 稳定在预设区间内,若pH小于预设值,通过加入适量的工业氧化锌烟尘调节pH。当试验达到预设时间后,通过真空泵抽滤沉锗浆,得到滤液和中和渣。用量筒量取滤液的体积,用pH计测量滤液pH;将湿渣放入真空干燥箱中,在恒温75 ℃条件下进行12 h的烘干,待干燥后称取中和渣干质量,计算渣率等,并将滤液和干渣取样后送样分析。将中和渣用硫酸浸出,考察浸出效果。其中,工业氧化锌烟尘、中和沉淀渣和浸出渣的XRD和SEM-EDS表征采用台式X射线衍射仪(Miniflex600)和场发射扫描电子显微镜(ZEISS Gemini 300)检测;渣中各元素含量通过ICP-OES(Prodigy, Leeman USA)检测。氧化锌浸出液、沉锗后液和浸出液中Zn 通过EDTA 滴定法检测,Fe 通过重铬酸钾滴定法检测,Ge、As 和Si 通过ICP-OES(Prodigy, Leeman USA)检测。
中和沉淀率和浸出率公式分别为:
式中:η为金属沉淀率;V1和V2分别为反应前后溶液体积,mL;c1和c2分别为反应前后溶液中离子质量浓度,mg/L;λ为金属浸出率;ω1和ω2分别为中和渣和浸出渣中元素含量(质量分数),%;m1和m2分别为中和渣和浸出渣质量,g。
2 结果与分析
2.1 中和沉淀过程
2.1.1 时间对中和沉淀效果的影响
在工业氧化锌烟尘用量为30 g,溶液pH=4.5~5.0,原料为1 000 mL 氧化锌烟尘浸出液,温度为45 ℃,通氧量为60 L/h,搅拌转速400 r/min 条件下进行实验,设置时间为2、3、4、5和6 h,考察时间对中和沉淀影响,结果如表3和图4所示。

图4 时间对锗、铁、砷和硅沉淀效果的影响Fig. 4 Effect of time on sedimentation of Ge, Fe, As and Si

表3 不同反应时间下渣与液中锗、铁、砷和硅的含量Table 3 Content of Ge, Fe, As and Si in neutralizing sediment and solution at different times
由表3和图4可见,随着时间的延长,锗、铁沉淀率增加,沉锗后液中锗、铁含量降低,说明延长反应时间会促使溶液中更多Fe2+被氧化和更多Ge4+、Fe3+水解,对锗、铁沉淀有促进作用。但当反应时间太长时,铁会沉淀过多,导致产渣量大,渣中锗含量低;反应时间太短,锗沉淀不完全,也会导致Fe(OH)3胶体不能很好吸附和团聚长大,固液分离困难。将铁沉淀率控制在30%以下时,得到的中和渣渣率稳定,渣中锗含量高。此外,随着反应时间延长,砷的沉淀率增高,后液中的砷质量浓度降低,因为时间增加会产生更多Fe3+,与砷形成共沉淀,同时也会促使As5+形成砷酸盐沉淀下来。随着反应时间延长,硅的沉淀率降低、硅质量浓度上升,这是因为工业氧化锌烟尘中存在可溶性硅,延长反应时间会导致硅溶解进入沉锗后液,但中和渣中砷、硅的含量几乎没有影响。
综上可知,中和时间为5 h 对锗沉淀最有利,得到的中和渣中锗含量高,沉锗后液中锗、铁和砷质量浓度较低。
2.1.2 溶液pH对中和沉淀效果的影响
在时间为5 h,原料为1 000 mL氧化锌烟尘浸出液,温度为45 ℃,通氧量为60 L/h,搅拌转速为400 r/min 条件下进行实验,分别加入22、26、30和49 g工业氧化锌烟尘调节溶液pH,使溶液pH在3.5~4.0、4.0~4.5、4.5~5.0、5.0~5.5,考察不同pH对沉淀影响,结果如表4和图5所示。

图5 pH对锗、铁、砷和硅沉淀效果的影响Fig. 5 Effect of pH on sedimentation of Ge, Fe, As and Si
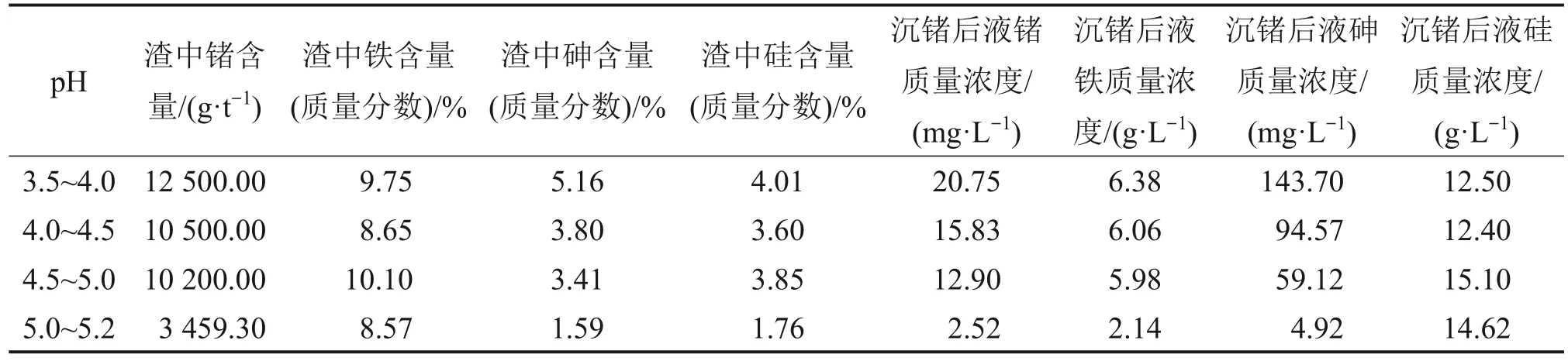
表4 不同pH时渣与液中锗、铁、砷和硅含量Table 4 Content of Ge, Fe, As and Si in neutralizing sediment and solution at different pH
由表4 和图5 可见,随着中和剂添加量增加,锗、铁沉淀率上升,沉锗后液中锗、铁含量降低,说明pH 升高对锗、铁的沉淀率有明显促进作用。因为溶液pH>3.5时,Fe3+、Ge4+已经开始水解,且Fe3+先开始水解,一部分锗与Fe3+形成共沉淀,另一部分Ge4+水解为Ge(OH)4而沉淀下来。当pH=5.0~5.2时,铁沉淀率大幅上升,渣中锗含量下降,虽然pH升高促进锗铁共沉淀,使得后液中锗质量浓度降低,但也会使得更多的铁沉淀下来,导致产渣量过大,渣中锗含量低。若pH过低,会出现锗沉淀不完全和固液分离困难问题。此外,随着溶液pH升高,后液中砷质量浓度降低、硅质量浓度升高,渣中砷和硅含量降低。pH 升高促进As5+形成砷酸盐,促进Fe3+水解而产生更多的共沉淀,但会出现产渣量大的问题,使得渣中砷、硅含量降低。在工业氧化锌烟尘中含有一定量可溶性硅,需加入更多的工业氧化锌烟尘使得pH上升,导致大量可溶性硅进入沉锗后液。
综上可知:当溶液pH=4.0~4.5 时,中和渣中锗含量高,当pH=5.0~5.2 时,后液中锗、铁和砷的质量浓度低,综合可得一段中和沉锗pH=4.0~4.5最好。
2.1.3 温度对中和沉淀效果的影响
在时间为5 h,工业氧化锌烟尘添加量为30 g,pH=4.5~5.0,原料为1 000 mL 氧化锌浸出液,通氧量为60 L/h,搅拌转速为400 r/min条件下进行实验,设置反应温度分别为20、30、45、60、75 和90 ℃,考察温度对中和沉淀影响,结果如表5 和图6所示。

图6 温度对锗、铁、砷和硅沉淀效果的影响Fig. 6 Effect of temperature on sedimentation of Ge, Fe, As and Si
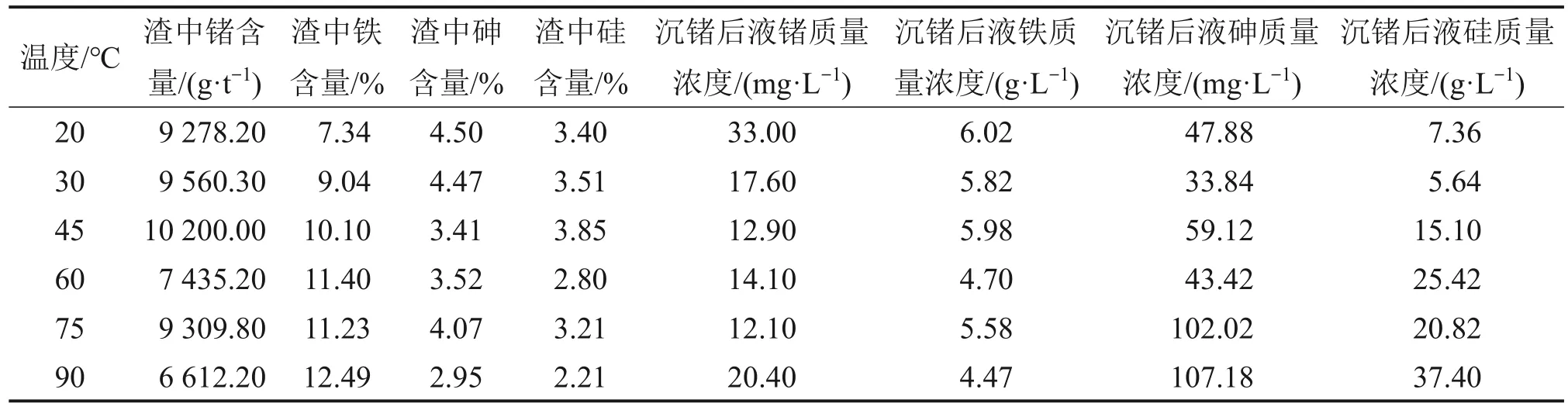
表5 不同温度下渣与液中锗、铁、砷和硅含量Table 5 Content of Ge, Fe, As and Si in neutralizing sediment and solution at different temperatures
由表5和图6可见,随着温度升高,锗、铁的沉淀率上升,后液中锗含量先下降后上升,温度上升至90 ℃时,锗沉淀率降低,后液中锗浓度随着温度升高先下降后上升,同时渣中锗含量随着温度升高而下降。说明温度的升高会促进铁的沉淀从而促进产生锗铁共沉淀,导致铁沉淀过多,出现产渣量大、渣中锗含量低的问题。温度升高到90 ℃时会抑制锗的沉淀,这是因为温度升高后锗酸分解,体系内物质膨胀,胶粒热运动加剧,胶核对离子吸附减弱,使得物质稳定性和形成趋势减弱,同时温度的升高使得大体积的高聚Fe(OH)3解聚为小体积的低聚Fe(OH)3,造成Fe(OH)3胶体逐步转变为低活性的小颗粒针铁矿,从而导致对锗的吸附能力降低。若温度过低则中和剂反应不完全,会导致锗、铁沉淀率低和固液分离困难问题。同理,温度的升高对砷、硅沉淀率也有抑制作用,后液中砷、硅含量升高,渣中砷、硅含量降低。
综上可知,当中和温度为45 ℃时,中和渣中锗含量高,沉锗后液中锗浓度低,同时可节约能耗。
2.1.4 铁对锗沉淀的影响
中和沉淀通过Fe2+氧化成Fe3+后在溶液中水解成Fe(OH)3,与溶液中锗、砷、硅等元素形成共沉淀,铁沉淀量决定了中和渣产渣量、渣中锗含量及锗沉淀率。铁沉淀量与产渣量、渣中锗含量和锗沉淀率的关系如图7所示。

图7 铁沉淀量与产渣量、渣中锗含量和锗沉淀率的关系Fig.7 Relationship between Fe precipitation quality and neutralizing sediment quality, Ge content in sediment and germanium precipitation rate
从图7 可知:随着铁沉淀量增加,锗沉淀率和产渣量增加、渣中锗含量降低。由此说明铁会促进锗的沉淀,这虽然可以提高锗沉淀率,但是Fe(OH)3属于胶体,会吸附溶液中其他离子并形成共沉淀,并且铁的大量沉淀会使得产渣量大、渣中锗含量低。在中和实验时通氧量和pH对铁沉淀量有较大影响,即通氧量增加可以促进Fe2+氧化,pH 升高可以促进Fe3+水解,为了得到锗含量高的中和渣,需控制铁沉淀率在30%以下。
2.2 两段逆流中和沉淀
一段中和沉淀不能同时满足沉锗后液含锗低与渣中含锗高的目的,为提高中和剂利用率、沉锗效率和渣中锗含量,降低渣量和后液锗浓度,提出两段逆流中和沉淀流程。其中,一段温度为45 ℃、pH=4.0~4.5、时间为3 h、所得到一段中和渣作为富锗渣,一段后液中锗质量浓度保持在50~60 mg/L,再进行二段中和沉淀,二段温度为45 ℃、pH=5.0~5.2、时间为1.5 h、通氧量为60 L/h,二段需加入过量工业氧化锌烟尘,保证pH到达预设值,同时,渣中还剩部分未反应的工业氧化锌烟尘,二段中和渣可返回一段继续充当中和剂。主要元素沉淀率如表6所示,后液中主要元素含量如图8所示。

图8 中和液中主要元素含量Fig. 8 Content of main elements in neutralizing solution
从表6可知,经过两段中和沉淀后,锗沉淀率提升至99.08%,铁、砷和硅沉淀率分别为26.72%、99.21%和95.36%。
从图8可知,一段控制pH=4.0~4.5时,沉锗后液中锗质量浓度为53.69 mg/L,渣中锗含量为11 300 g/t,渣中锌含量(质量分数)为29.41%,二段控制pH=5.0~5.5 时,沉锗后液中锗质量浓度为1.98 mg/L,渣中锗含量为2 565.95 g/t。一段渣中锗含量高可用来浸出,一段液继续中和沉淀,二段渣含有未反应的工业氧化锌烟尘,返回一段充当中和剂,二段液可直接返回锌冶炼系统。
2.3 中和渣分析
针对两段逆流中和沉淀得到一段中和渣进行检测,锗含量为11 300 g/t,铁含量为10.01%。借助XRD和SEM-EDS对中和渣进行物象组成和微观形貌分析如图9和图10所示。

图9 中和渣XRD图谱Fig. 9 XRD pattern of neutralizing sediment

图10 中和渣SEM-EDS图谱Fig. 10 SEM-EDS images of neutralizing sediment
从图9可看出:中和渣主要成分为ZnO、ZnS、PbSO4和SiO2。ZnO是中和过程中未完全参与反应留下的;ZnS是氧化锌烟尘中并没有完全反应而进入溶液最后残留到渣中;PbSO4是氧化锌烟尘中的PbS经氧化后转变来的;SiO2来自于工业氧化锌烟尘中未反应而沉淀下来的。
从图10 可以看出:中和渣形貌为不规则的颗粒形状,含有铅、锌、铁、硅、砷等元素,可推测为ZnS、PbS 和部分没有参与中和反应的ZnO;同时含有铅,可推测为PbSO4;铁、砷、硅可推测是与铁一起沉淀的产物,砷有一部分是与Fe3+反应生成的FeAsO4和砷铁共沉淀,同时也有As5+在中和过程中产生的砷酸盐,硅则是SiO2。此外,锗、铁、砷、硅等元素分布均匀,且铁分布密集的地方,锗、砷、硅分布也较密集,铁分布分散的地方,锗、砷、硅也分布较分散,可证明锗、砷、硅元素沉淀行为与铁相关。
2.4 中和渣浸出特征
为考察中和渣是否易于后续回收锗,开展浸出特征研究,通过高温高压浸出的方式可以高效回收渣中锌、锗、铟、铜等元素[15-20]。在时间为4 h、酸度为130 g/L、液固比为5 mL/g、氧分压为0.7 MPa 的条件下,设置温度分别为90 ℃和130 ℃,考察温度对浸出的影响,结果如表7 所示,元素浸出率如图11所示。

图11 不同温度下主要元素浸出率Fig. 11 Leaching rate of main elements at different temperatures

表7 浸出渣和浸出液中Ge、Fe、As和Si元素含量Table 7 Content of Ge、Fe、As and Si in leaching residue and solution
根据表7 和图11 可知:随着温度升高,锗的浸出率升高、浸出渣中锗含量低、浸出液中锗浓度高;在高温条件下,铁、砷、硅等杂质元素进入固相,铁会生成针铁矿、赤铁矿和碱式硫酸铁进入到渣中,Fe3+和As5+会成臭葱石进入到渣中,硅酸会分解形成SiO2进入到渣中。在反应温度为130 ℃时,浸出液中锗质量浓度为1.72 g/L,较前液富集8.23倍,同时,锗铁比由0.027提升至1.387、锗砷比由0.243 提升至0.644、锗硅比由1.332 提升至6.734。一段浸出渣中锗含量为3 148.9 g/t,锗浸出率仅为85.56%,针对锗浸出率不高的问题开展二次浸出实验,设置反应温度为90 ℃、反应时间为2 h、酸度为130 g/L、液固比为5 mL/g、通氧的条件下进行实验,得到浸出渣中锗含量为1 884.9 g/t,浸出液中锗质量浓度为331.1 mg/L,锗浸出率为95.96%,浸出渣中锌含量为2.04%,锌浸出率为98.55%,二段浸出液可返回至一段,在富集锗的同时达到分离除杂目的。
3 结论
1) 以氧化锌烟尘浸出液为原料,工业氧化锌烟尘为中和剂,采用两段逆流中和沉淀达到提高锗沉淀率、中和渣锗含量和中和剂的利用率目的。在一段温度为45 ℃、中和时间为2 h、pH=4.0~4.5,二段温度为45 ℃、中和时间为1.5 h、通氧量为60 L/h、pH=5.0~5.2的条件下,达到一段中和渣含锗11300 g/t,渣中锌含量29.14%,二段沉锗后液中锗质量浓度1.98 mg/L,锗、铁、砷和硅沉淀率分别为99.08%、26.72%、99.21%和95.36%。
2) 在中和沉淀过程中,一部分锗水解形成氢氧化锗沉淀,另一部分与氢氧化铁产生共沉淀;在氧化锌烟尘浸出液中,铁大部分以Fe2+存在,被氧化形成Fe3+后水解沉淀,铁的沉淀率与产渣量成正比,需控制通氧量和pH防止产出大量的渣;砷在溶液以As3+和As5+存在,通氧后中会有大量的As5+,砷与铁形成砷铁共沉淀,同时As5+也会以砷酸盐的方式沉淀;溶液中的硅以硅酸方式存在,在中和沉淀过程中与铁生成硅铁共沉淀,与锗生成锗硅共沉淀,工业氧化锌烟尘中含有可溶性硅,在实验过程中会溶出。
3) 在浸出实验中,氧压浸出可提高锗浸出率和浸出液中锗浓度、降低浸出渣中锗含量;在浸出锗的同时,铁、砷、硅等杂质元素进入固相,铁在氧压下会生成针铁矿、赤铁矿和碱式硫酸铁进入到渣中,铁和砷会形成臭葱石进入到渣中,硅酸会分解形成SiO2进入到渣中。在一段温度为130 ℃、时间为4 h、酸度为130 g/L、液固比为5 mL/g、氧分压为0.7 MPa,得到浸出渣中含锗3148.9 g/t,浸出液中含锗1.72 g/L,锗、铁、砷、硅浸出率分别为85.86%、26.72%、68.33% 和11.39%,锗较原液锗富集8.23 倍,同时,锗铁比由0.027 提升至1.387、锗砷比由0.243 提升至0.644、锗硅比由1.332 提升至6.734。在二段温度为90 ℃、浸出时间为2 h、酸度为130 g/L、液固比为5 mL/g、通氧的条件下,浸出渣中锗含量为1 884.9 g/t,锌含量为2.04%,浸出液中锗质量浓度331.1 mg/L,锗浸出率提升至95.96%,锌浸出率为98.55%,在富集锗的同时达到分离除杂目的。
