不同类型重性精神障碍病人睡眠结构比较及预测模型的建立
2023-10-13栗恺雯郎小娥
栗恺雯,郎小娥,刘 彩,郝 萌
1.山西医科大学第一临床医学院,山西 030001;2.山西医科大学第一医院
重性精神障碍如重度抑郁发作、双相情感障碍和精神分裂症等精神疾病给病人及病人的家庭造成了严重的影响。重性精神疾病与自杀密切相关,患有重性精神疾病的病人自杀风险最高,自杀率为43%~79%[1]。重性精神障碍病人常出现睡眠紊乱,而失眠是抑郁症的常见症状,是抑郁发作发展的一个危险因素[2],失眠和嗜睡是抑郁发作的标准,而睡眠需求减少是躁狂发作的高度特异性症状[3]。精神分裂症病人经常受到睡眠紊乱的困扰,睡眠紊乱会加剧疾病,包括加重精神病和认知障碍[4]。多导睡眠监测(polysomnography,PSG)是在临床和非临床环境中客观评估睡眠特征的金标准方法[5]。Kupfer 等[6-7]提出快速眼动睡眠变化,即快速眼动睡眠潜伏期缩短、总快速眼动睡眠持续时间增加和快速眼动密度增加,是原发性与继发性抑郁症病人的典型睡眠特征;并最早提出快速动眼期(REM)潜伏期缩短为原发性抑郁症的生物学标志。目前,对于精神分裂症、双相情感障碍与重度抑郁发作之间睡眠结构的差异性研究较少,且上述疾病的诊断主要以症状学为依据,迫切需要生物学标志物以鉴别诊断。本研究基于多导睡眠监测探索精神分裂症、双相情感障碍和重度抑郁发作之间的差异,试图找到鉴别3 种疾病的生物学标志物,建立预测模型并进行验证,为临床提供参考。
1 对象与方法
1.1 对象
选取 2021 年3 月—2023 年2 月在山西医科大学第一医院就诊的精神分裂症病人、双相情感障碍病人和重度抑郁发作病人423 例。纳入标准:1)符合《国际疾病与相关健康问题统计分类》(ICD-10)中精神分裂症、双相情感障碍及重度抑郁发作的诊断标准;2)年龄≤45岁。排除标准:1)有躯体疾病史;2)合并其他精神疾病;3)有物质依赖或滥用的病史;4)哺乳期、妊娠期妇女。本研究经山西医科大学第一医院伦理委员会审核批准。
1.2 资料收集方法及内容
收集一般人口学资料以及3 种疾病病人多导睡眠监测参数并进行比较。3 种疾病病人均进行多导睡眠监测,适应其温度、湿度及周边噪声等。采用澳大利亚COMPUMEDICS(康迪)Somte E 多导睡眠监测仪。本研究相关多导睡眠监测参数包括总睡眠时间、卧床时间、清醒时间、睡眠效率、睡眠潜伏期、REM 期潜伏期、N1 期、N2 期、N3 期 及REM 期 持 续 时 间 占 总 睡 眠时间比例。
1.3 统计学方法
采用R4.1.1 进行数据分析。符合正态分布的定量资料用均数±标准差(±s)表示,采用单因素方差分析进行组间比较,两两比较采用SNK 法;不服从正态分布资料用中位数(四分位数)[M(P25,P75)]表示,组间比较采用Kruskal-WallisH检验。定性资料采用频数、百分比(%)表示,组间比较采用χ2检验。对单因素分析有统计学意义的变量绘制相关性热图,探索自变量之间的相关性,利用LASSO 特征选择算法对单因素分析有统计学意义的结果进行二次特征选择,剔除存在共线性或者冗余的自变量,最后进行多分类Logistic 回归分析,以输出识别精神分裂症、双相情感障碍和重度抑郁发作的影响因素,并采用列线图进一步对影响因素进行可视化。采用受试者工作特征曲线(ROC)、校正曲线和决策曲线对构建的回归模型整体效果进行评价。
2 结果
2.1 精神障碍病人一般人口学资料
本研究共纳入423 例病人,年龄16~45 岁;男166例,女257 例;精神分裂症病人100 例,双相情感障碍病人100 例,重度抑郁发作病人223 例。3 种疾病病人年龄、性别、受教育年限比较差异无统计学意义(P>0.05),体质指数(BMI)、病程比较差异有统计学意义(P<0.05)。见表1。

表1 3 种疾病病人一般资料比较
2.2 3种精神障碍病人多导睡眠监测结果比较(见表2)
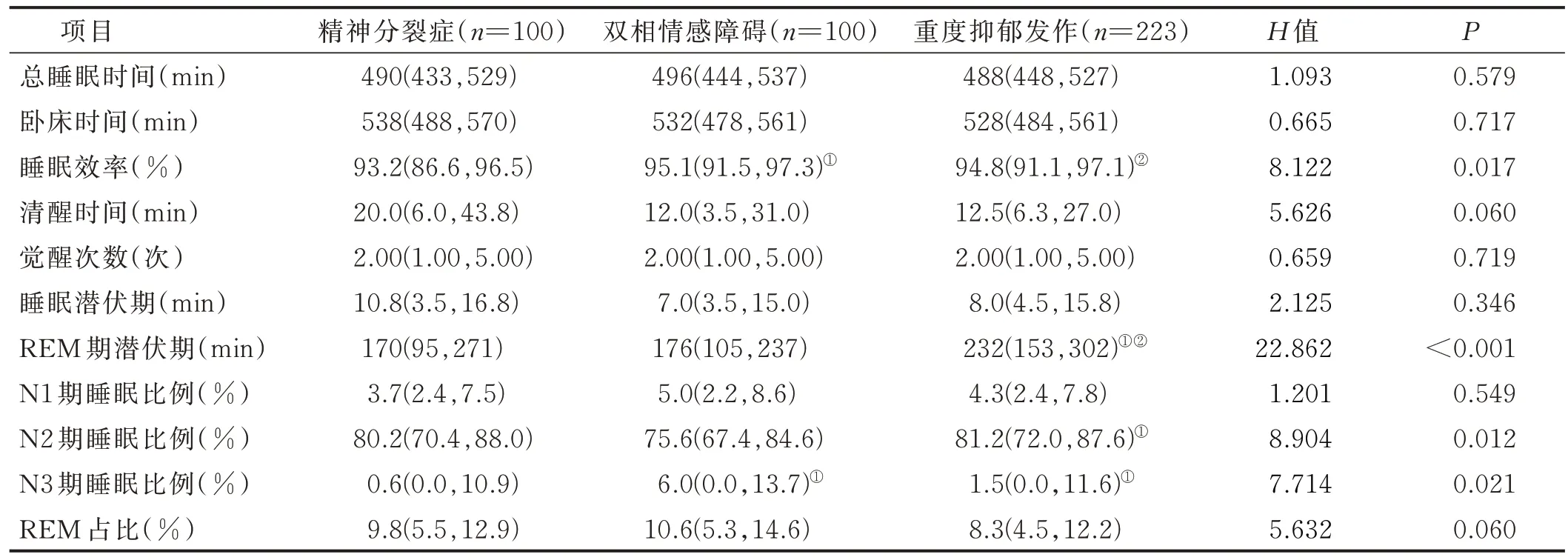
表2 3 种精神障碍病人多导睡眠监测结果比较[M(P25,P75)]
2.3 变量之间的相关性
对单因素有统计学意义的自变量进行相关性分析并绘制相关性热图,结果显示:N3 期睡眠比例和REM期潜伏期、N2 期睡眠比例存在相关性(r=-0.16,P<0.05;r=-0.72,P<0.05);REM 期潜伏期和N2 期睡眠比例之间存在相关性(r=0.26,P<0.05);睡眠效率和N2 期睡眠比例之间存在相关性(r=0.23,P<0.05);BMI 和 病 程 之 间 存 在 相 关 性(r=0.21,P<0.05)。见图1。

图1 自变量相关性热图
2.4 自变量二次选择
利用LASSO 算法实现自变量的二次选择,以剔除存在共线性或者冗余的变量,见图2 和表3,可以看出,当保留5 个特征时,模型的均方误差达到最小,且N3 期睡眠比例系数为0,即N3 期睡眠比例被剔除,保留其他变量。

图2 LASSO 回归模型图

表3 LASSO 回归自变量保留系数
2.5 3 种精神障碍病人睡眠特征影响因素的多重Logistic 回归分析
将LASSO 算法特征选择保留的自变量进行Logistic 回归分析,结果显示:影响精神分裂症和重度抑郁发作的因素包括睡眠效率和REM 期潜伏期,且都是精神分裂症的保护因素(重度抑郁发作的危险因素),即随着睡眠效率和REM 期潜伏期的值增大,病人被诊断为精神分裂症的风险越小(被诊断为重度抑郁发作的风险越大),而值越小,越容易被诊断为精神分裂症(越不容易被诊断为重度抑郁发作)。BMI、病程、REM 期潜伏期、N2 期睡眠比例是双相情感障碍和重度抑郁发作的影响因素,且BMI 和病程是双相情感障碍的危险因素,而REM 期潜伏期和N2 期睡眠比例是双相情感障碍的保护因素,即随着BMI 和病程的值增大,病人被诊断为双相情感障碍的风险增加,而随着REM 期潜伏期和N2 期睡眠比例的增大,病人被诊断为双相情感障碍的风险降低。见表4。

表4 3 种精神障碍病人睡眠特征影响因素的多重Logistic 回归分析结果
2.6 构建回归模型
通过绘制列线图进一步可视化Logistic 回归模型,见图3、图4。可以看出,当睡眠效率=20%,REM期潜伏期=400 min 时,对应个体的总分为90 分,而对应的被诊断为精神分裂症的概率为0.85 左右,而被诊断为重度抑郁发作的概率为0.17 左右。当BMI=18 kg/m2,病程=5 年,REM 期潜伏期=250 min,N2 期睡眠比例为40%时,对应个体的总分为144 分,而对应的被诊断为双相情感障碍的概率为0.48 左右,被诊断为重度抑郁发作的概率则为0.52 左右。

图3 预测精神分裂症和重度抑郁发作的列线图模型

图4 预测双相情感障碍和重度抑郁发作的列线图模型
2.7 回归模型的效果评价
对构建的回归模型的整体效果进行评价,评价指标包括识别重度抑郁发作和精神分裂症的回归模型的ROC 曲线下面积(AUC)及其置信区间、校正曲线以及决策曲线。模型识别重度抑郁发作和精神分裂症AUC 为0.658,识别重度抑郁发作和双相情感障碍AUC 为0.699,模型对3 种疾病的区分度尚可,见图5。模型区分重度抑郁发作和精神分裂症的预测概率和个体的真实概率效果不如模型区分重度抑郁发作和双相情感障碍的效果理想,但总体情况良好,见图6。模型识别重度抑郁发作和精神分裂症的阈值概率为20%~60%时,可以获得较高净获益值,而模型识别重度抑郁发作和双相情感障碍的阈值概率为20%~70%时,可以获得较高净获益值,说明模型具有较好的临床预测效用,见图7。

图5 模型识别重度抑郁发作和精神分裂症、双相情感障碍的ROC 曲线

图6 模型识别重度抑郁发作和精神分裂症、双相情感障碍的校正曲线

图7 模型识别重度抑郁发作和精神分裂症、双相情感障碍的决策曲线
3 讨论
睡眠是中枢神经系统的一种基本运行状态,占据了人类寿命的三分之一,因此,它可能是大脑功能和心理健康最重要的心理生理过程之一[8-9]。研究表明,夜间的睡眠类型与精神分裂症[10]、双相情感障碍[11]以及重度抑郁发作[12]的风险增加有关。
本研究发现,精神分裂症、双相情感障碍与重度抑郁发作病人之间的睡眠结构存在差异,与相关研究结果[13]一致。有研究显示,双相轻躁狂与重度抑郁发作病人之间REM 期潜伏期、睡眠效率、N3 期睡眠比例存在差异,且双相轻躁狂病人的睡眠效率和慢波睡眠的多导睡眠监测参数值更高[14],双相情感障碍Ⅰ型病人与抑郁症病人的各项睡眠指标比较差异无统计学意义[15]。有研究发现,在重度抑郁发作与双相情感障碍中,自杀意念与N4 期睡眠减少以及夜间觉醒高有关,而与抑郁的严重程度无关[16]。2007 年,美国睡眠医学会(American Academy of Sleep Medicine,AASM)已将非快速动眼期(NREM)睡眠中的N3 与N4 期合并为N3 期睡眠。睡眠是一个日常的循环过程,分为REM 和NREM 睡 眠 阶 段[17],NREM 睡 眠 分 为3 个 阶段,表示为N1、N2、N3,这3 个阶段进展到越来越深的睡眠,其特征是明显的睡眠纺锤波和慢波。慢波睡眠(SWS)也被称为N3 阶段睡眠,是NREM 睡眠的最深阶段。抑郁症、双相情感障碍和精神分裂症的个体会受到多种睡眠障碍的影响,包括SWS 异常[18]。SWS刺激与认知能力的提高相关,一项系统性综述发现,每种刺激方法都可以增强受试者慢波功率和/或SWS 持续时间;闭环、同相听觉刺激可以使言语陈述性记忆得到改善;通过慢震荡经颅直流电刺激(so-tDCS)在改善言语陈述性记忆与图片识别记忆表现出混合的功效,在促进位置记忆方面功效有限;SWS 的药理学方法在改善言语陈述性记忆、持续注意力或执行功能方面表现出有限的功效[19]。Duncan 等[20]研究显示,使用氯胺酮可迅速减轻重度抑郁发作和双相情感障碍的抑郁症状并且增加SWS,进一步解释了睡眠慢波是神经元可塑性标志,暗示睡眠和昼夜节律在情绪反应中具有重要作用。REM 期潜伏期和SWS 减少也被证明可以预测精神分裂症的不良预后。多项研究将SWS 与生长激素分泌联系起来,生长激素分泌有助于组织修复和功能恢复。在动物模型中,SWS 的持续时间与大脑蛋白质合成呈正相关。人类研究表明,SWS 不足的精神分裂症病人可能在抽象、刻板思维方面有困难,或者思维的流动性或灵活性下降,认知紊乱,缺乏判断力[21]。
基于人工智能(AI)的临床数据分析,对于精神疾病的早期识别、个体化诊治与转归预测将是今后一段时期内精神医学临床研究以及转化应用的主要选择和关键突破点之一[22]。将机器学习的结果可视化,即转化为易于转化应用的程式,是未来精神医学结合AI 的趋势[23]。本研究通过LASSO 算法,对一般人口学特征与睡眠结构参数进行选择处理,以多元Logistic 回归建立了预测重度抑郁发作与精神分裂症、重度抑郁发作与双相情感障碍的预测模型,相对于重度抑郁发作,精神分裂症的睡眠效率和REM 潜伏期数值较小;双相情感障碍的BMI 值较重度抑郁发作偏大,病程更长,REM 潜伏期和N2 期睡眠比例的数值较重度抑郁发作的数值小;重度抑郁发作与精神分裂症、双相情感障碍分别进行比较,AUC 分别为0.658 与0.699,具有一定的诊断价值,校准曲线和临床决策曲线证实该模型具有较好的临床有效性。
本研究尚存在局限性,首先,本研究未招募健康对照组;其次,由于本研究为回顾性研究,有部分病人曾于施行睡眠监测前预先服用药物,而一些药物(抗抑郁药物、抗精神病药物、镇静催眠药物等)可能会影响睡眠测量,现在人们普遍认为,需要至少7~14 d 的药物清除期才能获得有效的睡眠数据,但为了研究而停药被认为是不道德的;最后,本研究采用的数据为住院病人首次进行监测的多导睡眠图结果,并未排除“首夜效应”,病人首次使用多导睡眠监测的不适应可能会对监测结果造成影响。
4 小结
综上所述,精神分裂症、双相情感障碍和重度抑郁发作病人的睡眠结构存在差异,并且本研究所构建的列线图对精神分裂症与重度抑郁发作、双相情感障碍和重度抑郁发作之间具有较好的临床预测性,为临床鉴别精神障碍提供参考,有利于医护人员的诊疗及护理,有一定的应用价值。
