斑蝥酸钠对卡培他滨在大鼠体内药动学行为的影响 Δ
2023-10-09胡克荣班玉娟贵州医科大学药学院贵阳550004贵州省化学合成药物研发利用工程技术研究中心贵阳550004
胡克荣 ,陈 瑞 ,班玉娟 ,黄 静 (.贵州医科大学药学院,贵阳 550004;.贵州省化学合成药物研发利用工程技术研究中心,贵阳 550004)
斑蝥酸钠是斑蝥素的一种小分子半合成衍生物,作为一种能调节免疫并升高白细胞的广谱抗肿瘤药,在临床上具有重要的应用价值,常与其他化疗药物联合用于中晚期肿瘤治疗[1]。卡培他滨是一种高效的口服氟尿嘧啶氨甲酸酯类化疗药物,在体内可通过逐级酶联反应最终转变为5-氟尿嘧啶,而发挥抗肿瘤作用,已广泛用于胰腺癌、乳腺癌、胃癌等实体瘤的治疗[2—4]。
临床上斑蝥酸钠常联合卡培他滨用于恶性肿瘤的治疗,如斑蝥酸钠维生素B6注射液联合卡培他滨治疗结直肠癌,可有效控制患者疾病进展,疗效显著[5]。斑蝥酸钠维生素B6注射液与卡培他滨联合治疗胃肠道肿瘤,可有效提高单药化疗的有效率,同时减轻化疗所致的骨髓抑制、胃肠道反应等毒性反应[6]。由此可见,二者联合使用可以改善患者的免疫功能,提高化疗效果,改善患者的生存质量。但有研究指出,卡培他滨在联合其他抗肿瘤药物时,会产生许多不良反应,包括厌食、腹泻、呕吐、口腔炎、腹痛、手足综合征和困倦等[7]。出现不良反应后,患者的血液和淋巴系统、肝胆管系统、泌尿系统以及神经系统可能受到损伤,临床主要表现为血糖升高、肝功能异常、肾功能不全以及小脑功能障碍等[8],因此,研究二者联用后的药动学参数变化具有重要意义。基于此,本文拟建立测定大鼠血浆中卡培他滨血药浓度的超高效液相色谱-串联质谱(UPLC-MS/MS)法,通过测定联用斑蝥酸钠和未联用斑蝥酸钠大鼠体内卡培他滨的血药浓度,来计算并比较两者主要的药动学参数,以明确斑蝥酸钠对卡培他滨在大鼠体内药动学行为的影响,旨在为二者联用的安全性和有效性提供理论依据。
1 材料
1.1 主要仪器
本研究所用主要仪器包括1290 LC/TQ型超高效液相色谱仪、TSQ 6470型三重四极杆串联质谱仪及数据处理系统(美国Agilent 公司),GENESPEED1730R 型冷冻高速离心机(香港科技有限公司),JN300-2 型氮气吹扫仪(苏州吉米诺仪器有限公司),FA805N 型十万分之一电子天平(上海菁海仪器有限公司)等。
1.2 主要药品与试剂
卡培他滨对照品(批号420018-201802,纯度≥99%)购自中国食品药品检定研究院;甲苯磺丁脲对照品(内标,批号BD154332,纯度≥98%)购自上海毕得医药科技有限公司;斑蝥酸钠注射液(批号180303,规格2 mL∶0.1 mg)购自贵州金桥药业有限公司;卡培他滨片(批号SH2902,规格0.5 g)购自上海罗氏制药有限公司;肝素钠(批号605K0213,纯度≥99%)购自北京索莱宝科技有限公司;质谱级甲醇、乙腈、甲酸均购自德国Merck公司;水为超纯水。
1.3 动物
SPF 级健康雄性SD 大鼠,体重(230±10)g,由贵州医科大学实验动物中心提供,生产许可证号为SCXK(黔)2018-0001,大鼠在(22±2) ℃的环境下饲养7 d,光照和黑暗各12 h循环,给药前禁食12 h并自由饮水。
2 分析方法的建立
2.1 对照品溶液和内标溶液的制备
分别精密称取卡培他滨对照品或内标适量,加入甲醇溶解,制成质量浓度均为1 mg/mL 的贮备液,用滤膜滤过后,取续滤液,置于4 ℃冰箱保存,临用时用甲醇稀释至所需浓度,即得对照品溶液或内标溶液。
2.2 色谱与质谱条件
本研究的色谱条件为:以Agilent XBridge Aq C18(2.1 mm×50 mm,1.7 μm)为色谱柱,0.1%甲酸溶液(A)- 0.1%甲酸乙腈溶液(B)为流动相进行梯度洗脱(0~1 min,5%B;1~2.5 min,60%B;2.5~3.5 min,80%B;3.5~5.0 min,5%B);流速为0.4 mL/min;柱温为35 ℃;进样量为2 μL。
本研究的质谱条件为:采用电喷雾离子源以正离子模式扫描,扫描方式为选择反应监测;离子源温度为350 ℃;离子化电压为3 500 V;气帘气压为35 psi;雾化气压力为55 psi;辅助气压力为50 psi;卡培他滨、内标定量分析的离子对(m/z)分别为360.16→174.00、271.11→91.00,碰撞能量分别为24、40 eV。
2.3 样品的预处理
精密量取待测血浆样品100 μL,置于1.5 mL离心管中,先加入20 μL内标溶液(质量浓度为200 ng/mL),再加入800 μL乙酸乙酯,涡混10 min后,于4 ℃、13 000 r/min离心10 min。将上层乙酸乙酯层转移至2.0 mL的EP管中,为使药物萃取完全,剩余下层沉淀再加入800 μL乙酸乙酯以同样的方式萃取第2次;合并2次上层萃取液,以37 ℃氮气流吹干。吹干后的残渣储存于-80 ℃冰箱中,临用前加入100 μL 甲醇复溶,涡混10 min 后,以13 000 r/min离心10 min,取上清液进样分析。
2.4 方法学考察
2.4.1 专属性考察
精密量取“2.1”项下对照品贮备液和内标贮备液,用甲醇稀释,制成卡培他滨与内标的混合对照品溶液。取大鼠空白血浆,按“2.3”项下方法预处理,不加内标,制成空白血浆样品。另取大鼠给药2 h 后的血浆样品,按“2.3”项下方法预处理,制成卡培他滨血浆样品。将上述处理后的样品分别按“2.2”项下条件进样分析。如图1所示,卡培他滨、内标的保留时间分别为2.49、2.75 min,卡培他滨的色谱峰与内标峰分离良好,互不干扰,两峰在空白血浆色谱图中相同位置处没有内源性杂质峰干扰,表明该方法专属性良好。
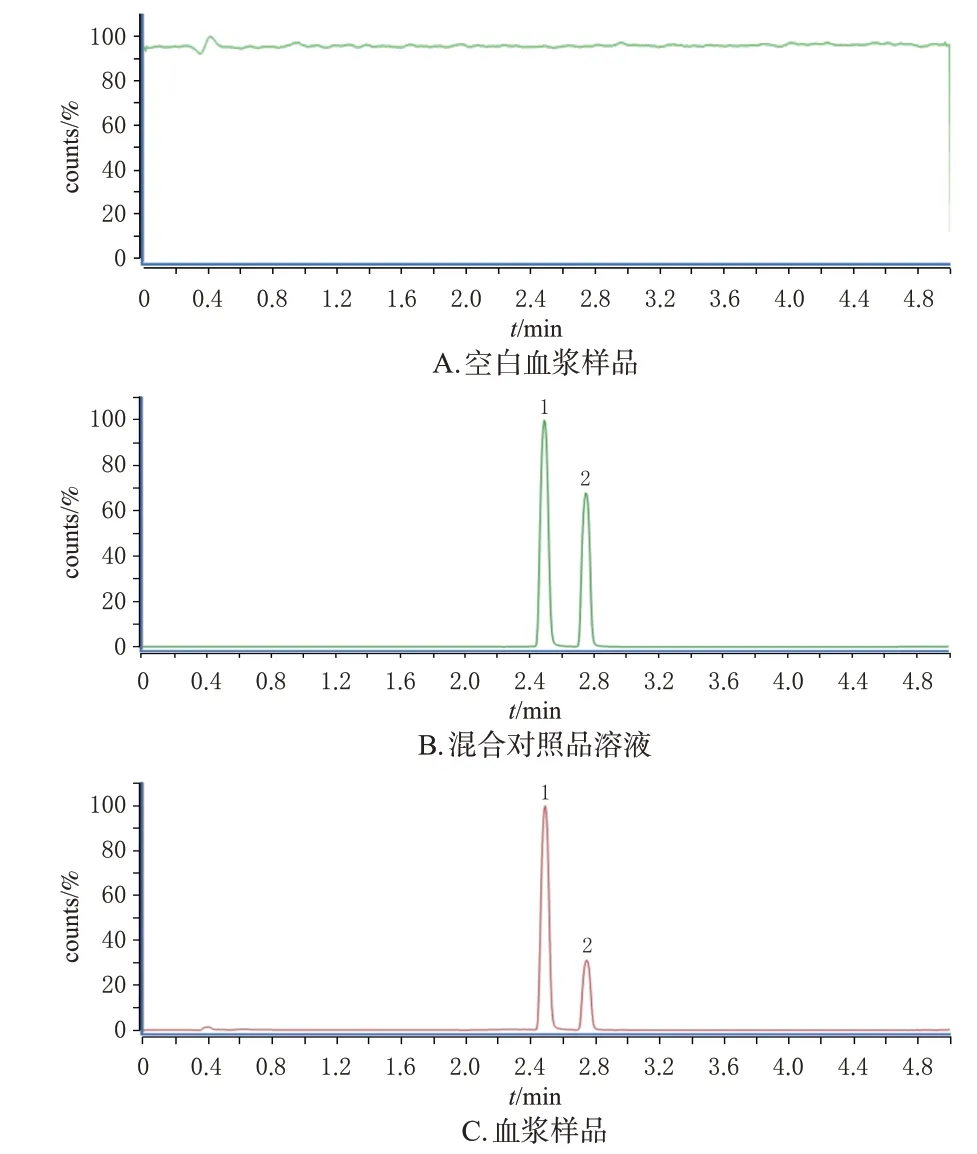
图1 空白血浆样品、混合对照品溶液、血浆样品的色谱图
2.4.2 标准曲线绘制和定量下限考察
取大鼠空白血浆,加入“2.1”项下对照品溶液,制成卡培他滨质量浓度分别为6.25、12.5、25、50、100、200、400、800 ng/mL的标准血浆溶液。按“2.3”项下方法预处理后,再按“2.2”项下条件进样分析,记录峰面积。以对照品质量浓度为横坐标(x)、卡培他滨与内标的峰面积比值为纵坐标(y),用加权最小二乘法计算回归方程。结果显示,卡培他滨的回归方程为y=0.055 2x+0.491 9(R2=0.999 4),线性范围为6.25~800 ng/mL,定量下限为6.25 ng/mL,符合2020 年版《中国药典》(四部)“生物样品定量分析方法验证指导原则”的要求。
2.4.3 精密度和准确度考察
取大鼠空白血浆100 μL,加入“2.1”项下对照品贮备液,制成卡培他滨质量浓度分别为6.25、10、100、600 ng/mL(定量下限和低、中、高质量浓度)的质控血浆样品。按“2.3”项下方法预处理后,再按“2.2”项下条件进样分析,记录峰面积。各浓度连续进样6次考察日内精密度,连续进样5 d 考察日间精密度。将峰面积代入同批随行回归方程计算卡培他滨的质量浓度,并与理论质量浓度相比,计算准确度。如表1显示,日内和日间精密度的RSD 均不高于3.49%(n=6 或n=5),准确度为99.08%~104.79%,符合2020 年版《中国药典》(四部)“生物样品定量分析方法验证指导原则”的要求。

表1 大鼠血浆中卡培他滨的精密度与准确度考察结果
2.4.4 提取回收率和基质效应考察
按“2.4.3”项下方法制备低、中、高质量浓度的质控血浆样品,按“2.3”项下方法处理后,再按“2.2”项下条件进样分析,计算卡培他滨与内标峰面积比(A)。取空白血浆100 μL,按“2.3”项下方法预处理后,再加入相应质量浓度的卡培他滨对照品溶液和内标溶液,使质量浓度与前者一致,按“2.2”项下条件进样分析,计算卡培他滨与内标峰面积比(B)。另制备卡培他滨对照品溶液和内标溶液质量浓度与前者一致的纯溶液(不含血浆),按“2.2”项下条件进样分析,计算卡培他滨与内标峰面积比(C)。按如下公式计算提取回收率和基质效应:提取回收率=A/C×100%,基质效应=B/C×100%。每个质量浓度样品平行制备3 份。如表2 所示,提取回收率为85.31%~91.67%,RSD 均不高于3.02%(n=3);基质效应为85.84%~95.31%,RSD 均不高于3.65%(n=3),符合2020年版《中国药典》(四部)“生物样品定量分析方法验证指导原则”的要求。
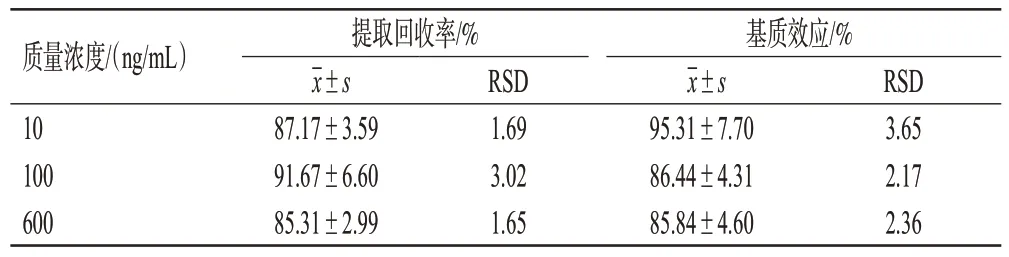
表2 大鼠血浆中卡培他滨的提取回收率和基质效应考察结果(n=3)
2.4.5 稀释可靠性考察
按“2.4.3”项下方法制备质量浓度相当于低、中、高质量浓度质控血浆样品5、20、40倍的卡培他滨质控血浆样品,再用空白血浆进行稀释,使3个质量浓度质控血浆样品的终质量浓度分别为10、100、600 ng/mL,按“2.3”项下方法预处理后,再按“2.2”项下条件进样分析,记录峰面积。每个稀释倍数下各质量浓度样品平行制备3份,根据同批随行回归方程计算卡培他滨的质量浓度。如表3所示,在不同稀释倍数下,所有质量浓度质控血浆样品的RSD均不高于9.84%(n=3),符合2020年版《中国药典》(四部)“生物样品定量分析方法验证指导原则”的要求。

表3 不同稀释倍数下卡培他滨质控血浆样品的稀释可靠性结果(n=3,%)
2.4.6 稳定性考察
按“2.4.3”项下方法制备低、中、高质量浓度的质控血浆样品,每个质量浓度样品平行制备3份,分别于室温(20 ℃)下存放24 h、4 ℃下存放48 h、-80 ℃下存放48 h、-80 ℃和室温下反复冻融3次后,按“2.3”项下方法预处理,再按“2.2”项下条件进样分析,所有样品均按同批随行回归方程计算卡培他滨的质量浓度。结果显示,各样品在上述不同条件下稳定性良好,RSD 均不高于7.24%(n=3),符合2020 年版《中国药典》(四部)“生物样品定量分析方法验证指导原则”的要求。
3 药动学研究
将24 只健康雄性SD 大鼠随机分为4 组:对照1 组、对照2组、实验1组、实验2组,每组6只。对照组大鼠腹腔注射生理盐水0.5 mL/kg,实验组大鼠腹腔注射斑蝥酸钠注射液0.5 mL/kg(相当于25 μg/kg),考虑到临床给药的长期性,故连续给药7 d。第8 天给药后,对照1 组和实验1组大鼠灌胃卡培他滨片5 mg/kg,对照2组和实验2组大鼠静脉注射卡培他滨5 mg/kg[将卡培他滨片研磨成细粉至无颗粒状后,称取一定量的卡培他滨细粉,采用助溶剂(N,N-二甲基乙酰胺-聚乙二醇400-水的体积比为2∶4∶1)溶解后,使卡培他滨的终质量浓度为2.5 mg/mL,配制时先加入N,N-二甲基乙酰胺并超声2 min,再加入聚乙二醇400,涡旋混匀,最后加入水,超声至澄清透明,用于静脉给药]。分别于灌胃卡培他滨后0.25、0.5、0.75、1、1.5、2、4、6、8、12、16、24、30 h 和静脉注射卡培他滨后0.033、0.15、0.5、1、1.5、2、4、6、8、12、16、24、30 h 从大鼠眼眶静脉丛采集全血0.2 mL,置于用肝素钠处理后的1.5 mL 离心管中,以4 ℃、3 500 r/min 离心10 min,分离血浆(血浆的采集和分离过程均在冰浴中进行),将得到的血浆置于-80 ℃冰箱中冻存,待测。取冻存的血浆样品放置至室温,按“2.3”项下方法预处理后,再按“2.2”项下条件进样分析,记录峰面积,并按随行回归方程计算各组大鼠给药后不同时间点血浆中卡培他滨的质量浓度,采用GraphPad Prism 8.0.1 软件绘制药-时曲线。采用DAS 2.0软件和非房室模型统计矩方法计算卡培他滨的药动学参数,计量资料以±s表示,用GraphPad Prism 8.0.1 软件对药动学参数进行配对t检验,检验水准α=0.05。结果见图2和表4。如表4所示,与对照1 组比较,实验1 组的无穷大时间内的平均滞留时间(mean residencetime within infinite time,MRT0-∞)、峰浓度(maximum concentration,cmax)、30 h 内的药-时曲线下面积(area under the concentration-time curve within 30 h,AUC0-30h)、AUC0-∞和生物利用度(bioavailability,F)均显著升高,表观清除率(apparent clearance,CLz/F)均显著降低(P<0.01);与对照2 组比较,实验2 组的半衰期(half-life time,t1/2)、MRT0-30h、MRT0-∞、AUC0-30h、AUC0-∞均显著升高(P<0.01)。
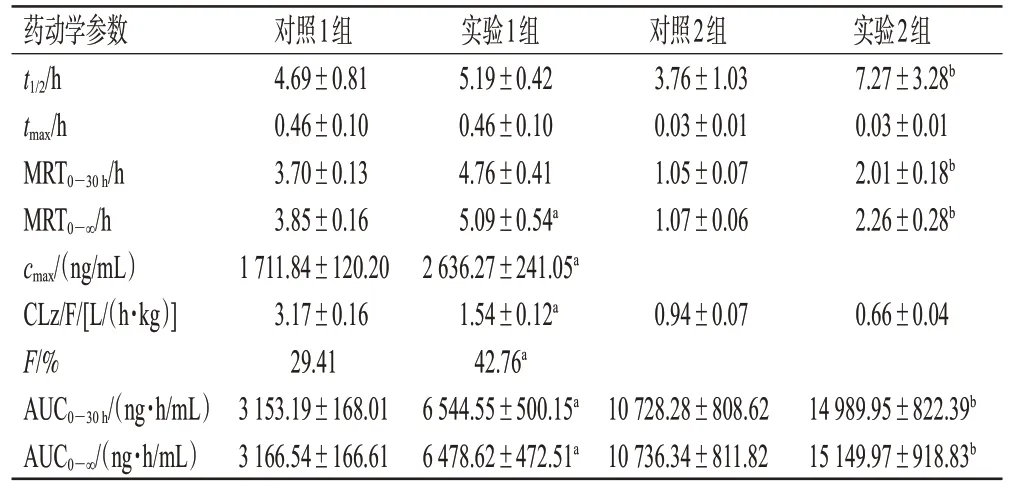
表4 卡培他滨的主要药动学参数
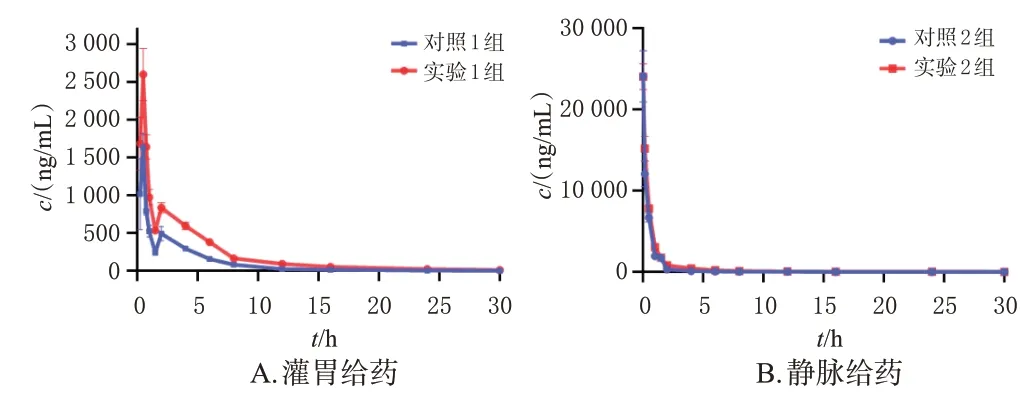
图2 卡培他滨灌胃和静脉给药的药-时曲线
4 讨论
本研究在血浆样品前处理中,分别使用甲醇、乙腈沉淀法以及乙酸乙酯萃取法对样品进行处理,结果发现,样品经甲醇、乙腈沉淀后,使得待测成分稀释而导致灵敏度降低;经氮气吹干后,管内富集了血浆中的内源性杂质,这些杂质进入仪器分析会造成较严重的基质效应。而乙酸乙酯萃取法可以有效地将目标化合物从水相萃取到有机相中,并将大部分基质组分(如磷脂、蛋白质、无机盐等)留在水相中,这样提取出来的样品更加干净,进入仪器分析后峰形良好、基质效应低、提取回收率高。因此,本研究最终选用乙酸乙酯萃取法对样品进行前处理。
合适的给药剂量、给药时间和给药方式是确保实验结果准确可靠的前提。斑蝥酸钠注射液采用连续给药是考虑到临床给药的长期性,给药时间过短可能会导致药效发挥不够完全,给药时间过长则可能导致药物在体内产生蓄积,因此,综合考虑采用连续给药7 d 较为合适。斑蝥酸钠注射液的给药剂量按照人与大鼠标准体重等效剂量系数为6.10 进行换算[9],得到大鼠给药最小剂量为10.13 μg/kg,最大剂量为50.81 μg/kg,选取中等剂量进行给药,最终确定斑蝥酸钠注射液给药剂量为25 μg/kg,即0.5 mL/kg。通过前期预实验发现,卡培他滨灌胃和静脉给药剂量均为5 mg/kg时,进样分析后,两种给药方式下不同时间点的血药浓度均能被准确测定,且不受内源性杂质干扰,准确度高,偏差小。因此,最终确定给药方案为腹腔注射斑蝥酸钠注射液0.5 mL/kg,连续给药7 d;第8 天给药后,灌胃或静脉给予卡培他滨5 mg/kg。
本研究探讨了卡培他滨联用斑蝥酸钠后,卡培他滨在大鼠体内的药动学参数变化,结果发现,斑蝥酸钠能增加卡培他滨在大鼠体内的血浆暴露量,提高口服生物利用度,一定程度上提高了药物的吸收;同时二者联用后,能延长卡培他滨在大鼠体内的平均滞留时间,降低清除率。由此笔者推测,临床上二者联用后可能会影响卡培他滨的疗效及有效作用时间。
