药物关联预测研究技术进展
2023-07-13朱晓敏张云霄
朱晓敏,刘 爽,徐 漫,张云霄
(大连民族大学 计算机科学与工程学院,辽宁 大连 116650)
1 问题提出
随着并发症出现概率越来越高,联合用药成为患者治疗疾病的普遍方法,但药物使用后出现了许多严重的不良反应威胁着患者的生命健康。药物关联(Drug-drug interactions,DDIs)预测是链接预测在生物医学领域方面一个很重要的应用。DDIs指同时或先后应用两种或两种以上药物时,在机体因素参与下药物彼此之间的交互作用发生药动学或药效学变化[1],临床表现为药效增强和毒副作用加重或药效减弱和毒副作用减轻。目前DDIs是药物治疗中一个非常重要的风险因子,它可能给患者带来严重的副作用,甚至是死亡;在药物开发阶段,虽然可以通过大量体内和体外实验筛查出一些可能发生DDIs的药物组合,但需要一定的试验周期和高昂的成本。当药物投入市场后,由于人类生命的复杂性,仍有可能会出现大量新的DDIs。
因此,确定药物间的相互作用对整个医疗行业,甚至整个人类社会都具有重要的研究意义。本文主要从以下几个方面进行总结分析:基于分子表示的方法、机器学习的方法、知识图谱的方法、分类的方法及其它方法进行DDIs预测,并对各个代表性方法的研究背景、优缺点及作用影响进行描述。本文最后介绍了DDIs预测方法中使用的数据源,并分析了该方向面临的挑战,对未来研究趋势进行展望。
1.1 药物关联预测面临的挑战与意义
首先,DDIs预测研究有助于药物研发。一个药物的成功研发往往需要经历三个阶段:候选药物确定、临床前研究和临床研究[2]。在药物研发过程中,能真正达到临床研究级别的药物占比一般不超过千分之一,会产生巨大的成本浪费,而DDIs预测研究将极大地减少药物研发成本。
其次,随着中国人口老龄化的到来,如何减少联合用药时产生的药物副作用成为临床治疗的重点研究内容[3]。DDIs预测可帮助医生避免在联合用药时产生潜在的DDIs风险,对药物的临床治疗有着非比寻常的意义。DDIs预测研究意义总结如下:
(1)DDIs预测可提高发现新药物不良相互作用的机率。通过提前预测新DDIs,药物开发部门或药物安全部门专业人员可从预测出的药物对中进行实验筛选,从而提高药物开发的效率。
(2)DDIs预测可提高新药物的开发效率和安全性。在药物关联预测过程中会发现许多发生DDIs的药物有着共同的化学结构信息。因此,在药物开发过程中有意地避免此类结构,从而减少DDIs发生几率。
(3)DDIs预测增强了个性化药物治疗方案的安全性。根据患者医疗记录为患者推荐个性化治疗方案,可避免对患者造成严重的健康威胁。
2 基于相似性的DDIs预测方法
2.1 基于分子结构相似性进行DDIs预测
2.1.1 方法介绍
Zeng等人[4]提出了基于分子结构相似性的方法进行DDIs预测,用于解决临床试验方法中存在的耗资大、费人力等缺陷。主要步骤为:(1)收集和处理药物结构,在数据库中获取化合物结构信息及线性文本表示,再使用Wash模块对分子结构进行预处理,为最终建模过程做准备;(2)学习结构表示,将分子表示为编码向量结构特征,为每个特征都分配一个特定位置[5];(3)计算相似性度量和数据表示,使用不同度量比较两分子指纹间的相似性,并根据指纹存在的特征数[6]构建相似矩阵,从而获取药物对间的相似性度量
2.1.2 作用与影响
此方法在描述分子结构方面仅需要较少的计算,避免了药物3D结构计算和叠加等问题。未来可以将结构相似性测量和药理学数据库中的知识整合到包含有关靶标和代谢信息的药理学数据库中,实现更可靠、更复杂的DDIs预测系统。
2.1.3 优点
此方法简单、高效,可将结构相似性信息应用于指定药物中,用于分析由代谢酶、转运蛋白、代谢酶抑制引起的药物相互作用[7]原理。
2.2 基于轮廓指纹相似性进行DDIs预测
2.2.1 方法介绍
基于轮廓指纹相似性方法[8]主要通过使用Tanimoto系数比较不同药物间的交互指纹[9],其结果使用Drugs.com等数据库作为参考标准进行验证。模型交互作用图相似性矩阵分两步进行计算:(1)将特定药物表示为载体,通过编纂特定位置代码来预测药物间相互作用的存在;(2)基于药物间的TC相互作用谱相似性进行矩阵计算,模型如图1。
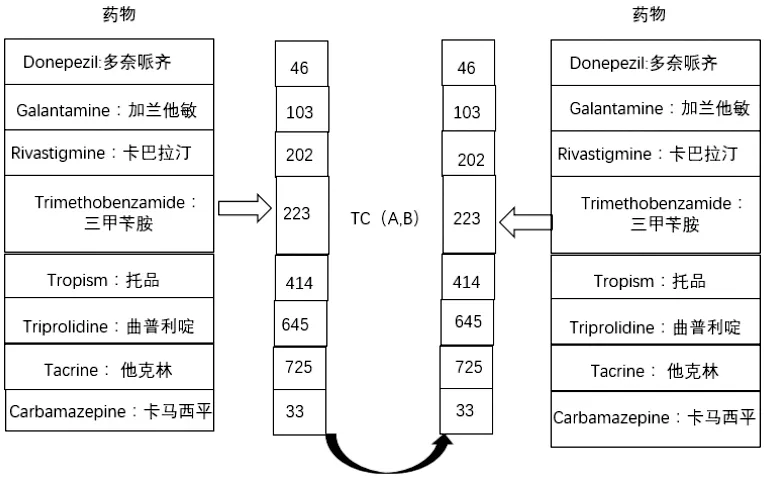
图1 基于轮廓指纹相似性DDIs预测模型图
2.2.2 优点及存在的问题
通过整合化学数据库提供的信息,并引入其它模型集成到系统中,可促进 DDIs预测的完成。但此方法包含的信息有限。
2.3 基于大规模分子结构进行DDIs预测
2.3.1 方法介绍
基于大规模分子结构相似性方法[10]可追溯到药物相互作用候选者信息。研究过程中将药物3D结构作为模板,通过药效团形状筛选识别出具有相似形状和静电特性的其它药物,在协议中使用比对算法计算药物间的相似性[11]。再通过与其它大规模分析方法相结合来完成最终预测,使用交叉验证方法来测试模型[12]的性能,在完善 DDIs预测参考标准数据库的基础上,整合了药物相似性信息。
2.3.2 优点及存在的问题
2D和3D分子结构方法可提供捕捉同一药理学类别药物间分子相似性的机会,使研究人员能够检测属于不同药理学类别药物对之间的高度相似性[13],但缺点是此过程包含的药物目标或不良事件概况信息是有限的,从而限制模型的性能。
3 基于机器学习的DDIs预测方法
3.1 基于图卷积网络方法进行DDIs预测
3.1.1 方法介绍
基于图卷积网络方法[14]通过构建药物副作用的多模式图来解决副作用具有不同类型的边缘性问题。首先基于探索节点网络邻域的随机游走方法来学习节点神经特征对,然后通过学习药物特征表示用作逻辑回归分类器的输入[15],模型如图2。
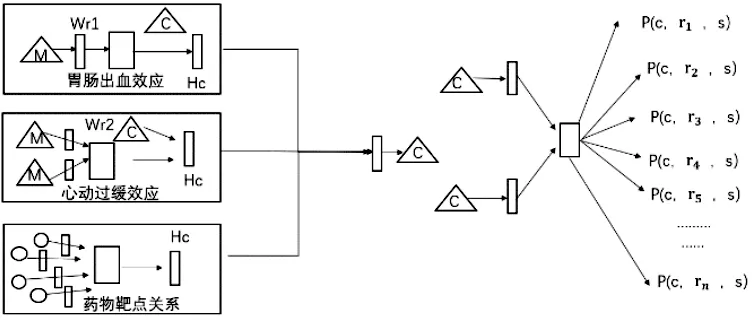
图2 基于图卷积网络进行DDIs预测模型图
3.1.2 作用与影响
此方法进行DDIs预测是将不同种类药物关联信息融合到一个图中,可对不同类型的DDIs事件采用不同模块进行学习,取得了较好的效果。
3.1.3 优点
此方法无需手动完成特征工程操作,可为具有大量边缘类型的多模态图提供有效权重共享形式。
3.2 基于注意力机制方法进行DDIs预测
3.2.1 方法介绍
基于注意力机制的方法[16]可准确预测出拥有潜在关系的药物集,此方法将药物关联预测视为二分类任务,输入是药物SMILES序列。首先将药物分为一维特征编码器和二维特征编码器编码。再将药物的二维原子图特征向量和一维序列特征向量送入多维度特征解码器,通过特征混合生成高维向量。最后在向量上进行解码得到是否发生DDIs作用的标识,模型如图3。
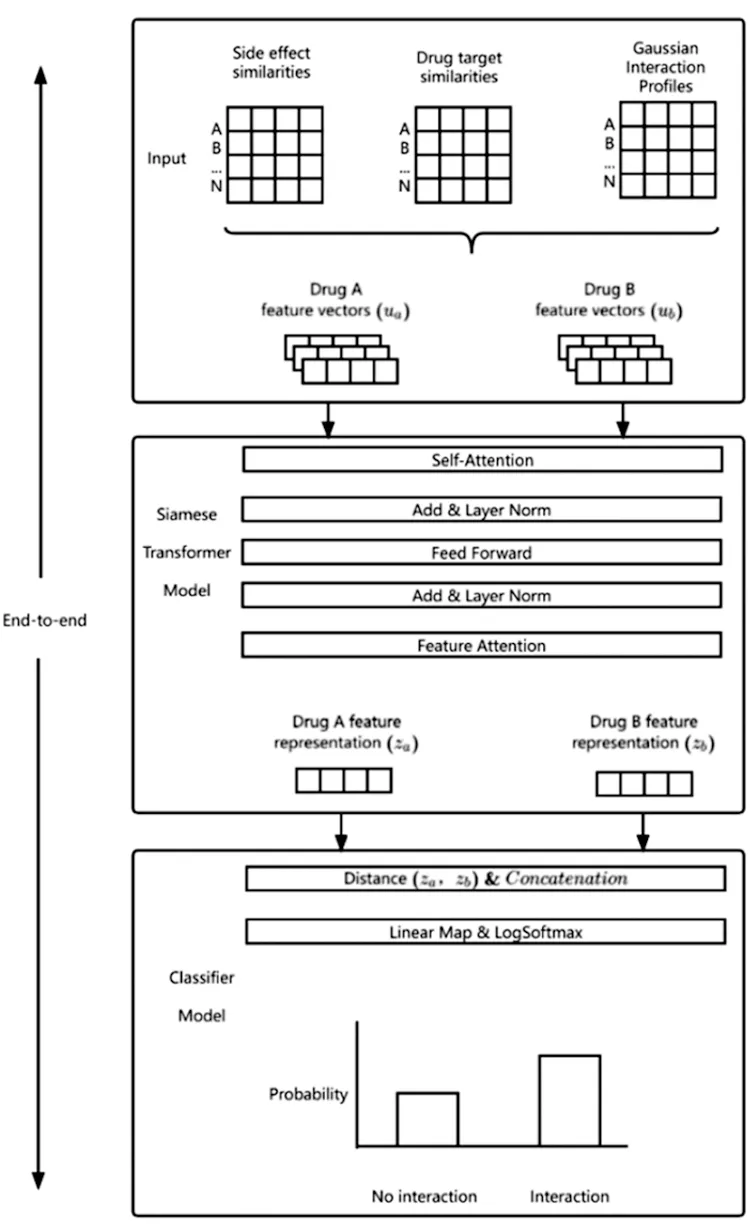
图3 基于注意力机制的DDIs预测模型
3.2.2 优点
此方法证明了多维度特征在DDIs预测中的巨大潜力,此模型可以推广到药物靶点、癌症风险预测等领域。
3.3 基于多重网络嵌入进行DDIs预测
3.3.1 方法介绍
基于多重网络嵌入方法[17]可用于整合多种方法不同方面的有用信息,可用来确定每个网络的定量重要性。首先通过构建包括基于类别的相似网络的多重药物-药物相似网络。然后对每种药物的化学式进行分析,得到药物化学指纹图谱构建为基础的网络。最后,对复用网络信息进行采样和节点特征向量学习,通过Skip-Gram模型对目标函数进行优化,模型如图4。
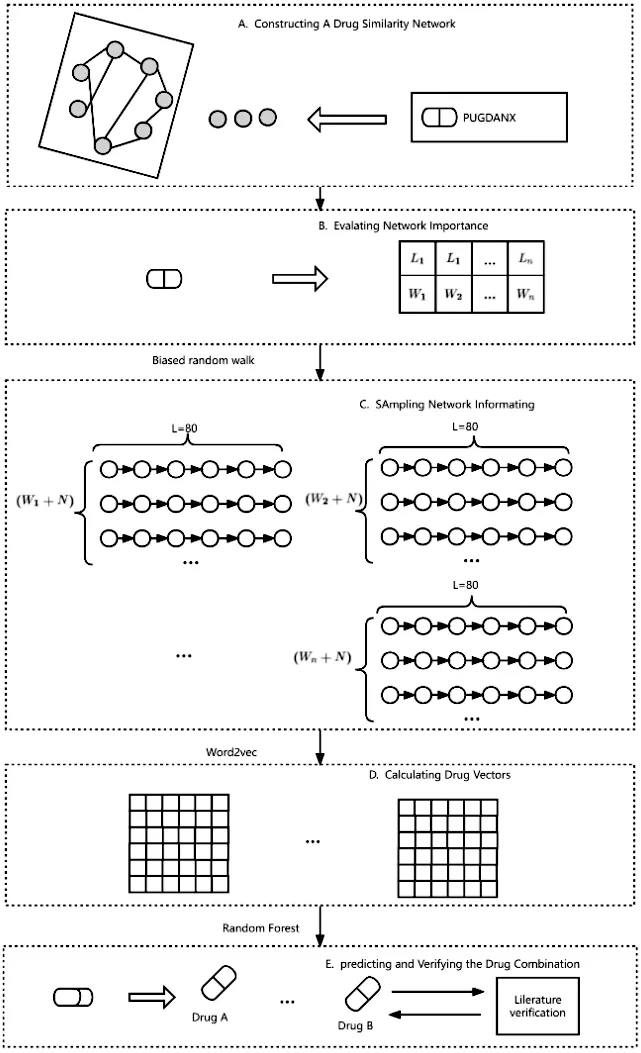
图4 基于多重关系网络的DDIs预测模型
3.3.2 优点及存在的问题
此模型优点是能准确地评估出不同网络的重要性,并利用随机游走等方法提取不同网络拓扑信息,最后确定每个网络定量的重要性。其缺点是模型的性能和伸缩性方面较差。
3.4 基于多源药物特征融合进行DDIs预测
3.4.1 方法介绍
多源药物特征融合方法[18]首先利用自编码器的隐向量作为药物对的新特征进行不同方式的组合,再将组合后的药物特征输入到不同药物融合网络中,得到最终的潜在特征向量,模型如图5。
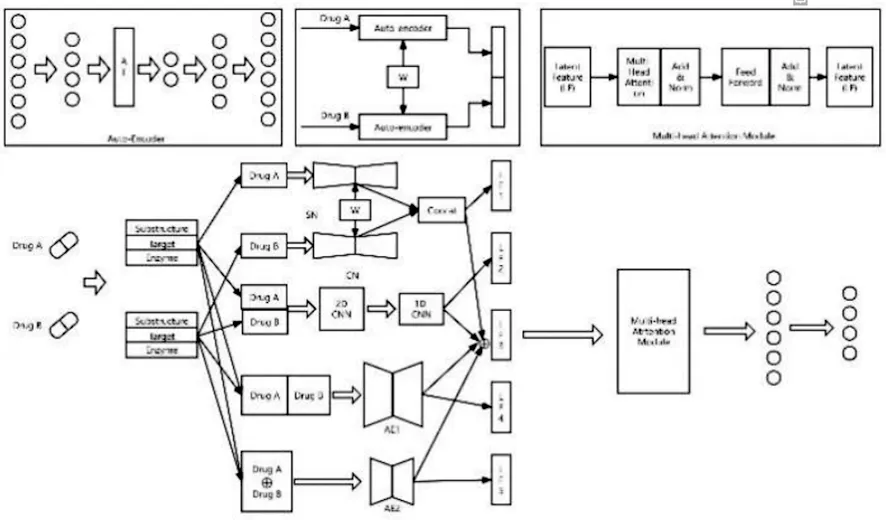
图5 基于多源药物、特征融合的DDIs预测模型
3.4.2 优点
此方法具有混合数据增强策略的有效性,也具有较强的鲁棒性性能。
3.5 基于图增强卷积网络进行DDIs预测
3.5.1 方法介绍
基于图增强卷积网络[19]将图卷积神经网络与注意力网络相结合用于提取药物对间的结构关系,进而实现DDIs预测。首先采用简化分子来分别提取每个DDIs对中的药物图,再通过应用权重共享图卷积神经网络来生成图表示,最后使用sigmoid函数决定最终分类[20]。
3.6 基于深度学习方法进行DDIs预测
3.6.1 方法介绍
基于深度学习的方法[21]首先将输入药物对中的药物结构信息生成特征向量,再将该特征与报告的DDIs类型进行关联,最后将深度学习方法与另一种异质基因网络结合一同进行DDIs预测研究,使用化学结构、药物靶标分类系统作为输入生成描述相关DDIs[22]。
3.6.2 优点
此方法通过给定药物对的输出神经元活性值来优先考虑被替代的药物成员,可更好地了解DDIs。未来可将此方法扩展到DFI等多种化合物的研究。
4 基于知识图谱的DDIs预测方法
4.1 基于知识图谱嵌入方法进行DDIs预测
4.1.1 方法介绍
知识图谱嵌入方法[23]通过捕获局部和全局重要的药物特征进行DDIs预测。数据以知识图的形式出现,将提取到的信息作为交互预测器特征,使用嵌入方法将图中节点投影到密集向量。然后在数据集中收集DDIs信息创建集成图谱,再应用不同知识图谱嵌入技术进行实验,模型如图6。
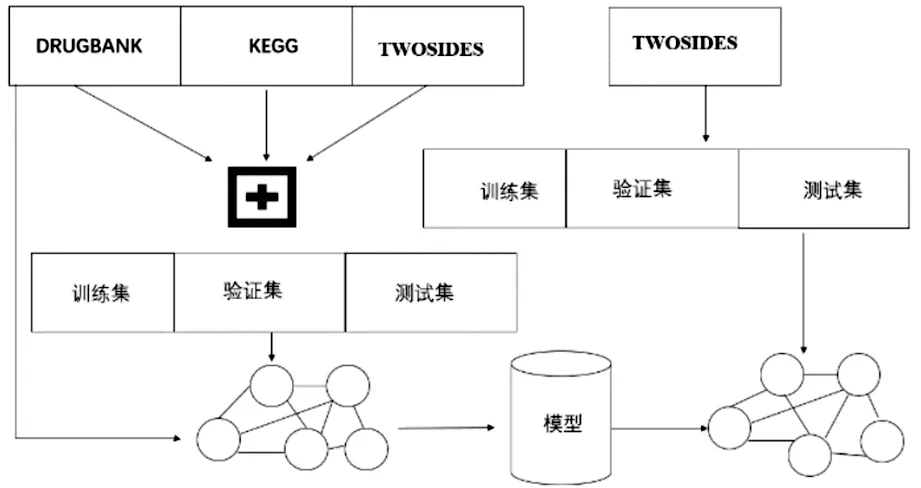
图6 基于知识图谱与LSTM技术进行DDIs流程图
4.1.2 优点及存在的问题
通过组合CNN和LSTM构建网络,其优点是CNN使用卷积滤子捕获药物特征中的局部关系,LSTM从CNN提取特征中提取整体关系,能够捕捉到重要的药物特征,但局限是无法为DDIs预测提供解释,可能会产生数据不平衡问题。
4.2 基于知识图谱与图神经网络进行DDIs预测
4.2.1 方法介绍
基于知识图谱与图神经网络方法[24]通过挖掘KG中每个实体的拓扑结构信息,从各自局部感知域中聚合所有邻域拓扑信息提升DDIs预测性能。从数据集中收集提取包含药物对的DDIs数据源并构建相应的KG;通过在DDIs矩阵和构建的知识图谱中提取药物特征及相关实体邻域结构信息,输出药物潜在表示及当前药物对间的邻域拓扑信息,计算得分并输出预测值。
4.2.2 优点
通过有选择地多次聚合邻域信息,将基于空间的图神经网络方法扩展到知识图谱中,能够学习到拓扑结构信息和知识图谱中的语义关系,进而提升DDIs预测效果。
4.3 基于高效知识图谱进行DDIs预测
4.3.1 方法介绍
基于高效知识图谱的方法[25]是在多类型关系网络上进行评价的,其中子图结构包含图学习任务的丰富信息,通过在子图上设计一个图摘要模块来获得易处理路径,再集成一种新的多通道神经编码机制,从而提高预测性能。
4.3.2 作用与影响
此方法可有效地锚定KG的相关子图,利用大量外部生物医学知识显著改善多类型DDIs预测性能,为DDIs的潜在机制提供合理的线索。
4.3.3 优点
此模型在预测过程中具有可伸缩性;每次传播中采用不同子图形成归纳偏差,可提升模型的泛化能力。
4.4 基于知识图谱胶囊网络方法进行DDIs预测
4.4.1 方法介绍
基于知识图谱胶囊网络方法[26]证明了模型的有效性及可解释性。框架由三个主要部分组成。(1)负样本构造:构建训练过程中所涉及的高质量负样本,对其提出更高的要求;(2)图嵌入层:迭代地从实体接受域中聚合邻居信息并学习实体的表示;为每条边生成注意力权重,然后确定该实体的接受域;(3)胶囊网络层:通过处理给定关系空间下的实体表示来预测两实体在关系空间下是否发生DDIs。
4.4.2 优点
此方法通过结合胶囊网络可捕捉实体在语义空间下的非线性信息并丰富实体的表达,提升模型的预测能力。
5 基于分类的DDIs预测方法
5.1 基于联合用药模式和图匹配进行DDIs预测
5.1.1 方法介绍
联合用药模式和图匹配的方法[27]使用支持向量机进行DDIs预测,其任意顺序的药物组合新内核均在 SVM 框架内进行开发,通过对新内核与其它卷积内核进行比较,找到两个图之间的最佳顶点对应关系。图匹配大致分为两类:第一类是精确图匹配,即找到图和子图的同构并使两图之间的顶点映射是双射的和保边的;第二类是不精确的图匹配,允许在匹配过程中出现错误,最大限度地减少寻找最佳图匹配的总错误。
5.2 基于多任务二元分类进行DDIs预测
5.2.1 方法介绍
基于多任务二元分类方法[28]将DDIs预测表述为二元回归问题,可预测数据实体对之间的二元关系,进而捕获不同数据视图之间所有高阶交互关系。
5.2.2 优点及存在的问题
此模型灵活,允许学习共享和非共享的低秩因子,可对多实体交互进行建模,但各种数据域的交互顺序必须手动确定且依赖应用程序,无法涵盖所有DDIs案例。
5.3 基于多任务半监督学习进行DDIs预测
多任务半监督学习方法[29]解决DDIs标签稀疏性问题有三个技术亮点:(1)利用无重力数据有利于DDIs预测的信息;(2)降低表示特征复杂性并降低过度拟合的风险;(3)利用DDIs信息,可协调集成多种药物特征和多任务学习。
6 基于其它的DDIs预测方法
6.1 基于分子结构信息增强文本进行DDIs预测
6.1.1 方法介绍
分子结构信息增强文本方法[30]通过获得分子图结构中药物对表示,将其与卷积神经网络获得的文本表示连接起来,然后共享任务文本数据集中的标记来训练整个模型。通过对药物进行随机配对并去除阳性对中的药物,以便生成相同数量的伪阴性对,再用分子结构从文本中提取 DDIs关系。
6.1.2 优点及存在的问题
此方法可从分子结构信息中高精度地实现DDIs预测,可减轻标签的差异,进而提升模型的预测能力。
6.2 基于标签传播的方法进行DDIs预测
6.2.1 方法介绍
基于标签传播方法[31]通过高阶相似性来预测 DDIs。首先使用临床 SEs作为预测 DDIs关键特征;然后通过考虑高阶相似性,使用标签传播方法进行DDIs预测。
6.2.2 优点及存在的问题
此方法通过信息最大化来更新药物嵌入,使其具有鲁棒性,能够独立地传播每种特定类型的标签。
7 性能评估
目前主要通过DrugBank数据集[32]进行DDIs预测。数据集包含药物相互作用、靶点、酶等综合信息,支持全面而复杂的搜索。通过结合可视化软件可非常容易地检索到新药物靶标、药物结构等信息,数据集介绍见表1。

表1 数据集介绍
采用AUPR、AUC和F1评分等评价指标对DDIs代表性模型性能在以下实验环境结果进行对比:(1)开发框架TensorFlow/PyTorch;(2)GPU:Geforce GTX 1660Ti;(3)Hard disk:200G;(4) Memory:32G;(5)开发语言:python。
在DrugBank数据集上进行实验得到各结果指标对比如下,模型结果见表2,各个模型的AUPR、F1、Predictor、Mcc、AP@50、AUPRC指标模型图如图7。
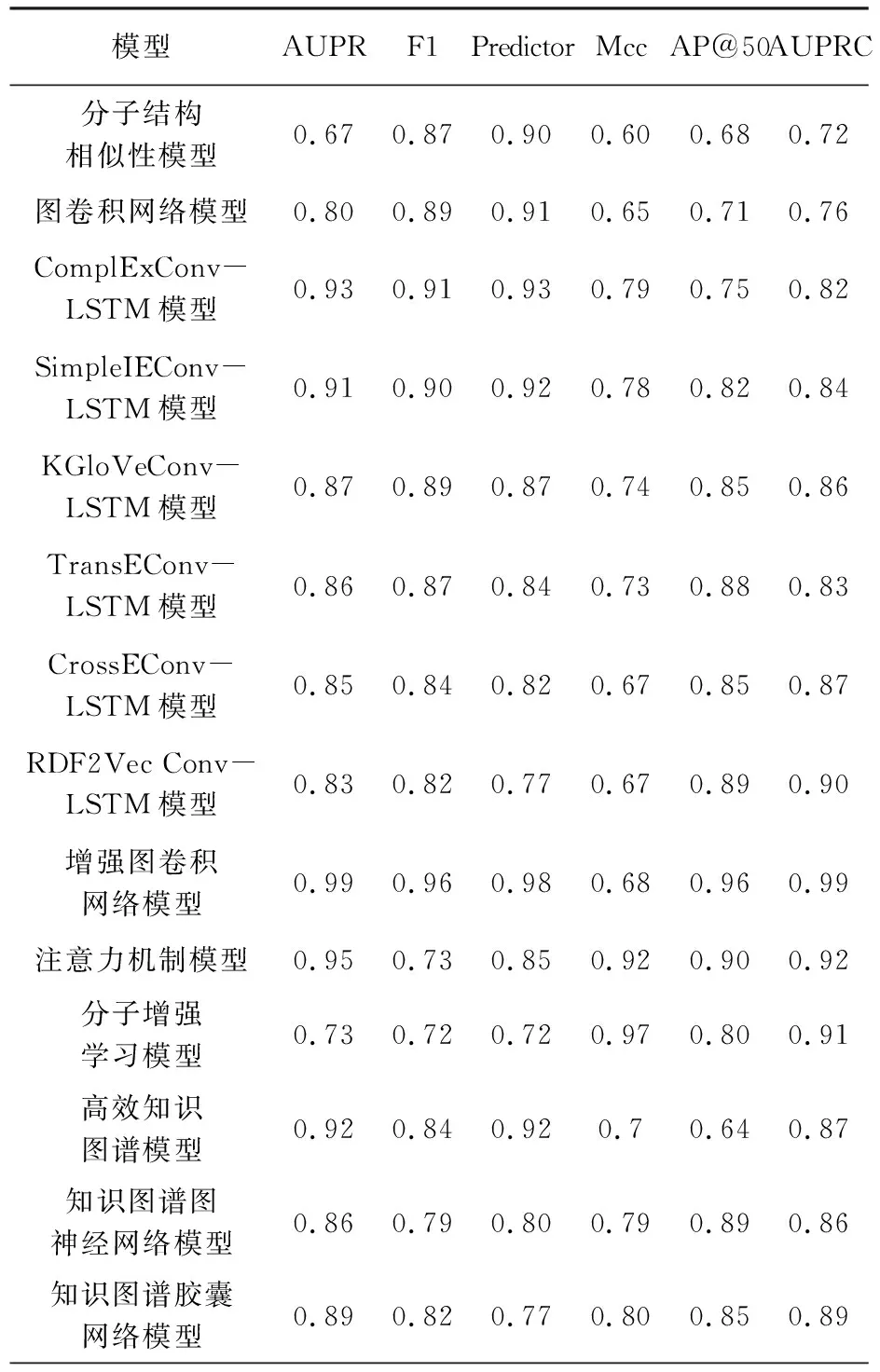
表2 各模型实验结果
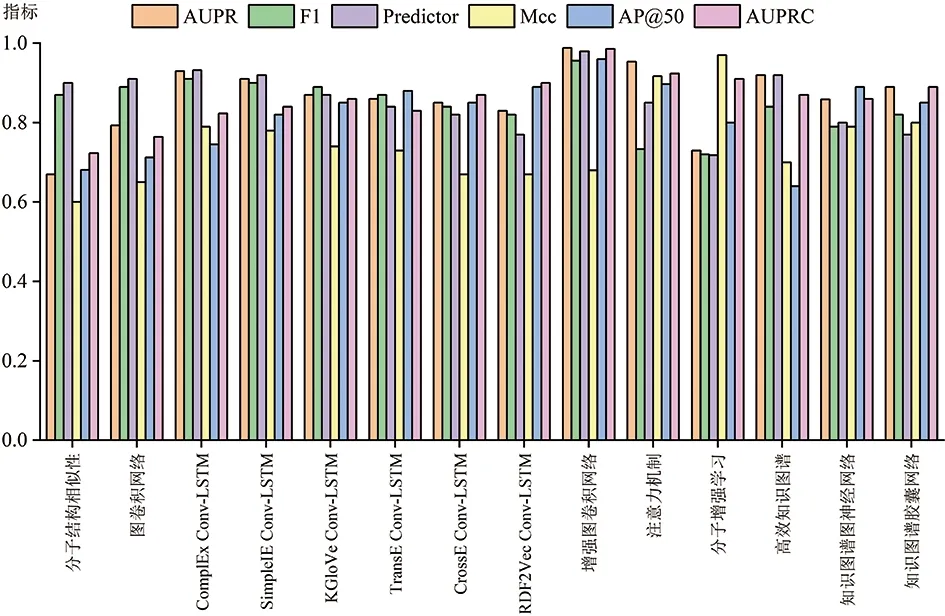
图7 最新方法各个指标对比柱状图
8 结 语
DDIs预测研究是公共卫生和药物安全监测的重要课题。本文围绕药物关联预测的背景,存在的问题及意义对其进行研究。将药物关联预测方法分为五类:基于分子表示的方法、基于机器学习的方法、知识图谱的方法、基于分类的方法及基于其它方法进行DDIs预测。本文对DDIs预测五大类中代表性方法进行阐述与分析。最后,本文讨论了当前DDIs预测研究所面临的挑战和未来发展方向。从国内外近几年研究成果可以看出,越来越多的研究学者们通过多途径、多方法、多角度去进行深刻的DDIs预测研究。确定药物之间的相互作用不仅增强个性化药物治疗方案制定的安全性,还可以大大提高药物研发的效率并为患者推荐个性化的治疗方案。DDIs预测研究对于整个医疗行业,具有重要的研究意义。
