以腰痛为首发症状的肥大细胞白血病1例
2023-03-03李芳蔄雯瑜于雅宁葛凤华孙祥君
李芳 蔄雯瑜 于雅宁 葛凤华 孙祥君
1威海市中心医院检验科,威海 264400;2威海市中心医院病理科,威海 264400;3威海市中心医院血液科,威海 264400
肥大细胞白血病(mast cell leukemia,MCL)是系统性肥大细胞增生症(systemic mastocytosis,SM)的一种少见亚型,占比不到SM的1%,该病在我国罕见[1]。现报道1例,以提高检验人员对该病的认识及诊断水平。
病例资料
患者,女,63岁,腰背部不适2周。患者于2021-10-23因提重物后持续性腰背部疼痛不适,于当地诊所行钢针治疗,未见明显好转,4 d后就诊于当地整骨医院。2021-11-03胸腰段磁共振平扫示:胸腰段退行性变,考虑胸11椎体骨折,建议结合CT检查,胸腰段椎体及附件多发异常信号影,恶性病变可能性大,腰3/4椎间盘膨出。整骨医院给予消肿止痛药物治疗(具体不详,患者不能提供),自诉疼痛较前明显改善。患者于2021-11-05就诊于威海市中心医院肿瘤科门诊,完善相关检查。血常规:白细胞计数2.83×109/L,中性粒细胞百分比65.3%,淋巴细胞百分比27.9%,单核细胞百分百比6.0%,嗜碱性粒细胞百分比0.4%,红细胞计数3.41×1012/L,血红蛋白119 g/L,血小板计数162×109/L。尿常规正常,大便常规正常。肝功能:总蛋白70.7 g/L,白蛋白42.7 g/L,谷丙转氨酶61 U/L,谷草转氨酶41 U/L,谷氨酰转肽酶25 U/L,碱性磷酸酶81 U/L,总胆红素9.2 μmol/L,直接胆红素4.1 μmol/L。2021-11-06肝胆胰脾肾超声:非均匀性脂肪肝(轻度)、肝内钙化灶。全身骨显像:⑴脊柱放射性分布欠均匀,符合退行性变表现;⑵胸1椎体横行条状异常放射性摄取增高区,考虑压缩性骨折改变,病理性?⑶右侧髂骨异常放射性摄取增高区,性质待定;⑷左侧耻骨上支区域似见点状异常放射性增高区,骨骼病变或膀胱内放射性尿液难以分辨。现患者腰背部疼痛可耐受,偶有咳嗽、咳痰,为白色粘痰,少量,无发热及呼吸困难。患者现为进一步治疗入住肿瘤科。
入院查体:体温36.5 ℃,心率80次/min,呼吸频率19次/min,血压143/86 mmHg(1 mmHg=0.133 kPa),身高160 cm,体质量63 kg,Karnofsky功能状态(KPS)评分90分,数字疼痛评分(NRS)3分。全身皮肤黏膜无黄染、皮疹、皮下出血、皮下结节、瘢痕,皮下无水肿,无肝掌、蜘蛛痣。全身浅表淋巴结未触及肿大。双肺叩诊音清,呼吸音清晰,未闻及明显干湿性啰音。心前区无隆起,心尖搏动无移位,无心包摩擦感,心率80次/min,律齐,各瓣膜听诊区未闻及杂音。腹软平坦,无压痛反跳痛,腹部无包块。肝脏未触及,脾脏未触及,Murphy氏征阴性。脊柱正常生理弯曲,四肢自由活动,无畸形、下肢静脉曲张、杵状指(趾),关节无红肿,下肢无浮肿。四肢肌力、肌张力未见异常。双侧Babinski征阴性,脑膜刺激征阴性。生化:K+4.36 mmol/L,Na+138.4 mmol/L,Cl-100.4 mmol/L,HCO3-29 mmol/L,Ca 2.52 mmol/L,P 1.56 mmol/L,尿 素 氮5.0 mmol/L,肌 酐43 mmol/L,尿酸206 mmol/L,血糖6.53 mmol/L,血清淀粉样蛋白22.3 mg/L。肿瘤标志物:癌胚抗原0.74 μg/L,甲胎蛋白3.1 μg/L,糖类抗原(CA)125 7.53 U/L,CA19-9 2 U/ml,CA15-3 4.45 U/ml,CA72-4 1.5 μg/L,细胞角蛋白19片段2.37 μg/L,神经元特异性烯醇化酶5.5μg/L,人附睾蛋白4 57.3 pmol/L。免疫固定电泳血尿免疫球蛋白(Ig)A、M、G、D阴性。影像学检查:胸部CT示右肺中叶炎症,双肺纤维灶。骶髋关节MR示双侧髂骨、骶骨、耻坐骨、股骨上段散在异常信号。PET/CT示胸11椎体、腰2椎体右侧附件、双侧髂骨、骶骨、左侧耻骨上支、左侧股骨上段局部骨质密度不均匀,部分呈溶骨性骨质破坏,代谢增高,最大标准摄取值(SUVmax)6.3,考虑血液系统疾病,多发性骨髓瘤可能性大。胸11椎体病理性骨折;所见骨髓腔弥漫性代谢增高,SUVmax 3.7,肿瘤浸润不除外;左侧第5、6、7前肋走行不自然,轻度代谢增高,SUVmax 4.1,不除外病理性骨折。转入血液科,2021-11-15行骨髓穿刺细胞学检查、流式细胞、基因及病理活检。骨髓细胞学结果:骨髓增生极度活跃,G=4%,E=1%;粒系比值减低,形态未见明显异常;红系比值减低,形态未见明显异常,成熟红细胞未见明显异常;淋巴细胞比值减低,为成熟淋巴细胞;巨核细胞无法清晰识别,血小板较易见;肥大细胞异常增生,约92.5%,胞体大小不一,形态不规则,部分呈撕扯状,部分细胞胞体巨大,胞浆量较丰富,大部分颗粒细小稀疏,少部分颗粒增多粗大,核椭圆形,易见双核、多核和不规则核,核染色质较细致(图1A、B、C)。甲苯胺蓝染色:肥大细胞多数弱阳性,少部分强阳性(图1D)。外周血白细胞数量略低,粒细胞比值形态大致正常,淋巴细胞比值形态大致正常,成熟红细胞形态正常,偶见肥大细胞。诊断意见:考虑MCL,结合病理及免疫组化。骨髓基因检测:B系基因重排IgH、IgK;T系基因重排TCR(TCRγ)、T系基因重排TCR(TCRβ)阴性。C-kit Exon8、C-kit Exon17、FLT3/ITD、-FIP1L1/PDGFR α、FLT3-TK、Jak2/V617F阴性。流式细胞示异常细胞CD117和CD33强阳性,不除外肥大细胞。

图1 1例肥大细胞白血病患者骨髓片。A:瑞吉氏染色,10×100;B:瑞吉氏染色,10×100;C:瑞吉氏染色,10×100;D:甲苯胺蓝染色,10×100
骨髓病理活检:组织1块,体积0.3 cm×0.2 cm×0.2 cm。镜下所见: HE、PAS染色示骨髓增生较活跃(80%),异常细胞广泛增生,胞体中等大,胞浆丰富,胞核梭形或卵圆形,少量粒红系细胞散在分布,巨核细胞可见,少量胞体小。网状纤维染色(MF-2级,灶性)(图2)。免疫组化标记异常细胞示:CD117 +、Tryptase -、CD2 -、CD25 -、CD38 -、CD138 -、CD56 -、CD20 -、CD3 -、CD68 -。诊断结果异常细胞增生,考虑MCL,建议加做C-Kit基因。
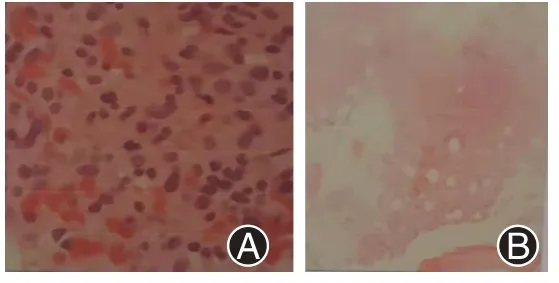
图2 1例肥大细胞白血病患者骨髓活检。A:HE染色,10×40;B:HE染色,10×10
综合骨髓细胞学、病理活检、流式及基因检测,确诊为MCL(非白血病性变异性)。给予哌拉西林他唑巴坦、头孢米诺、拌托拉唑护胃,复方甘草酸甘保肝等治疗,并给子甲泼尼龙治疗原发病。排除禁忌证后2021-11-21开始给予地西他滨25 mg dl~5去甲基化治疗,2021-11-25给CA方案(克拉曲滨8 mg dl~4、10 mg d5+阿糖胞苷50 mg d1~5)化疗,并给予止吐、碱化、水化等治疗。患者本周期化疗结束后无明显不适,2021-11-30出院。2021-12-21患者因铜绿假单胞菌败血症、重度肺部感染、化疗后骨髓抑制、重度粒细胞缺乏、重度血小板减少、重度贫血、紫癜性皮炎再次入院,先后给予头孢米诺、氟康唑、头孢哌酮钠舒巴坦钠、依替米星、利奈唑胺抗感染抗过敏、平喘、补钾、补钙、补充白蛋白等治疗,患者病情恶化,于2021-12-28死亡。
讨 论
肥大细胞起源于骨髓造血干细胞。肥大细胞增多症是肥大细胞克隆性增生,在一个或多个器官中肥大细胞聚集(增多)性浸润所致的异质性疾病。轻者自发消退(如皮肤病损),重者为高度恶性的侵袭性肿瘤伴有多器官衰竭,并可在短时间内死亡[1]。
2017年世界卫生组织将肥大细胞增多症分为皮肤肥大细胞增多症(CM)、SM和肥大细胞肉瘤3大类。SM又分为惰性SM(ISM)、冒烟性SM(SSM)、SM伴相关血液肿瘤(SM-AHN)、侵袭性SM(ASM)、MCL。MCL的诊断标准:⑴符合SM的一般标准;⑵活组织检查示不典型、幼稚的肥大细胞弥散性浸润;⑶骨髓涂片肥大细胞≥20%;⑷经典型病例外周血涂片肥大细胞≥10%,非白血病性变异性(肥大细胞<10%,较常见);⑸常无皮肤病损。
MCL非常罕见,常见的实验室检查结果为血细胞减少[2-3]。身体症状,如体质量减轻、疲劳和盗汗也很常见。此外,1/3的患者还伴有胃肠道症状,特别是腹泻。在一些研究中已经报道了与消化性溃疡密切相关。出血、溶血或弥散性血管内凝血也可能发生[4]。
肥大细胞在肿瘤和反应条件下,表达胰蛋白酶和KIT(CD117)以及某些髓系抗原,包括CD13和CD33。胰蛋白酶、CD117、CD25和CD2(后两种抗原在正常的肥大细胞中不表达)是识别SM中异常肥大细胞的关键标志物。CD117是敏感的,但对肥大细胞没有特异性,而胰蛋白酶则不那么敏感。CD25比CD2更有用,CD2不常表达[5]。MCL表现出与其他类型SM相似的免疫表型反应,然而,1/3的MCL患者已被注意到具有双阴性的CD2/CD25免疫表型[6]。不同比例的MCL患者可能表达CD30[7]。
KIT D816V突变是SM中最常见的突变,在80%~90%的患者中存在,是其主要的表型驱动因素。在侵袭性SM和MCL中,与其他髓系肿瘤相同,一些额外的突变也可能发生。SRF2、ASXL1、RUNX1、TET2、CBL、K/N-RAS和EZH2已经被证明会导致较差的结果[8-9]。与其他类型的SM相比,MCL只有40%~67%的患者携带典型的KIT D816V突变[8-10]。在这些“阴性”的病例中,有一部分可能携带了密码子816 KIT突变而不是D816V或非密码子816 KIT突变[8]。在MCL中,这些非典型KIT突变的组合估计频率为20%[9,11-12]。
从临床病理的角度来看,MCL的鉴别诊断包括胰蛋白酶阳性的急性髓系白血病(AML)和髓母细胞白血病(MML),一种晚期髓样肿瘤伴有部分肥大细胞分化[3]。根据世界卫生组织2017年的标准,这两种情况都可以排除。前者通常至少有20%的成髓细胞表现为弱胰蛋白酶表达。骨髓活检通常显示小于10%的肥大细胞,缺乏致密的弥漫性增殖模式。
本例患者以腰痛为首发症状,无肝脾淋巴结肿大表现,无色素性荨麻疹,骨髓肥大细胞占92.5%,主要为颗粒细小型,甲苯胺蓝染色大部分弱阳性,仅有少数强阳性。免疫表型CD117+,不表达CD2、CD25双阴性,C-kit Exon8、C-kit Exon17均阴性,外周血偶见肥大细胞,结合流式及骨髓病理,符合非白血性MCL。
综上所述,对于MCL,除了进行骨髓形态学及病理学检查外,还应该进行免疫分型和分子生物学等检测,不断提高对此类罕见白血病的诊断水平。
