椎间孔镜下两种不同手术入路治疗单节段巨大型腰椎间盘突出症的疗效比较
2023-01-09胡鉴瑜李京霞刘东颜铭苏玮
胡鉴瑜 李京霞 刘东 颜铭 苏玮
巨大型腰椎间盘突出症通常被定义为影像学资料显示腰椎间盘向后突出超过椎管矢状径1/2,并伴有脊髓或神经受压,患者常表现为剧烈的腰痛并伴有下肢放射性疼痛及麻木[1]。随着微创脊柱外科的发展,通过椎间孔镜对腰椎间盘突出症引起的神经根及硬膜囊精准减压取得了较好的治疗效果,但受限于视野局限,椎间孔镜下摘除巨大脱垂髓核有一定难度。目前,临床上椎间孔镜技术主要采用两种不同手术入路:经皮椎间孔入路腰椎间盘摘除术(percutaneous endoscopic transforaminal discectomy,PETD) 和经皮椎板间入路腰椎间盘摘除术(percutaneous endoscopic interlaminar discectomy,PEID)[2]。而目前对这两种手术入路治疗单节段巨大型腰椎间盘突出症手术疗效的相关研究较少,本研究回顾性分析本院2018 年1 月~2019 年12 月分别采用椎板间入路与椎间孔入路经皮椎间孔镜技术治疗48 例单节段巨大型腰椎间盘突出症患者的临床资料,现报告如下。
1 资料与方法
1.1 一般资料 本研究纳入2018 年1 月~2019 年12 月48 例诊断为单节段巨大型腰椎间盘突出症患者,根据术中采用的手术入路不同分为PETD 组(26 例)及PEID 组(22 例)。其 中,PETD组男15 例,女11 例;平均年龄(62.95±11.69) 岁;L3~4节段突出4 例,L4~5节段突出16 例,L5~S1节段突出6 例。PEID 组男13 例,女9 例;平均年龄(59.53±12.02)岁;L3~4节段突出2 例,L4~5节段突出10 例,L5~S1节段突出10 例。两组患者的性别、年龄、椎间盘突出节段等一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 纳入及排除标准
1.2.1 纳入标准 ①临床表现为单侧下肢麻木或放射痛,伴或不伴腰痛,经非手术治疗3 个月以上无效;或急性发作下肢疼痛,疼痛程度剧烈,严重影响日常生活和工作;②术前CT 和磁共振成像(MRI)显示单节段髓核突出超过椎管矢状径50%,明确诊断为腰椎间盘突出症。
1.2.2 排除标准 ①症状、体征与影像学表现不一致;②合并脊柱肿瘤、结核、感染等病变;③腰椎不稳或腰椎滑脱;④多节段椎间盘突出;⑤一般情况较差无法耐受手术者。
1.3 手术方法
1.3.1 PETD组取侧卧位,患侧向上,腰腹部稳妥固定,C 型臂X 线机透视定位,体表标记穿刺进针点,常规消毒铺巾,用带刻度的穿刺针0.5%利多卡因逐层浸润麻醉直至关节突关节,透视下调整针尖置于目标椎间孔的上关节腹侧,使用导丝插入穿刺针,拔出穿刺针,小尖刀切开皮肤约1 cm,沿导丝置入逐级扩张套管及工作套筒,利用环锯和磨钻去除上关节突腹侧的骨质,椎间孔扩大成形,再次透视定位工作通道位置正确,连接内镜、双极球形射频消融电极,仔细探查神经根、硬膜囊,用髓核钳取出突出或游离的椎间盘组织,减压后用射频刀头止血并修补纤维环,被动活动患侧下肢,观察硬膜囊的搏动及神经根的松弛程度,确认神经根充分松解且没有致压物,拔出工作套管,切口缝合1 针。
1.3.2 PEID组采用静脉复合麻醉或局部浸润麻醉,患者取俯卧位,腰部垫腰桥,C 型臂X 线机透视定位确定病变节段椎板间间隙,于病变节段正中线旁开1~2 cm,确定进针点为上关节突内侧、椎间盘突出侧椎板间隙下方,导丝插入后穿刺到相应节段黄韧带层面,小尖刀切开皮肤、深筋膜约1 cm,经导丝置入工作套管与扩张套管,再次透视定位工作通道位置正确,连接内镜,以椎板内侧缘为参照,篮钳逐层咬除黄韧带,磨钻磨除部分椎板内缘,进入椎管后用髓核钳取出突出或游离的椎间盘组织,减压后用射频刀头止血并修补纤维环,嘱患者咳嗽观察硬膜囊及神经根搏动良好,拔出工作套管,切口缝合1 针。
两组患者均由同一术者主刀完成手术,术中均采用德国Joimax 脊柱内镜系统,术后绝对卧床休息2~3 d,此后指导患者佩带腰围下床活动,术后常规予以甘露醇脱水、小剂量激素等对症治疗,术后7 d 拆线。
1.4 观察指标及判定标准
1.4.1 围手术期指标 包括手术相关并发症发生情况,手术时间、术中出血量、住院时间、术中C 型臂透视次数、透射剂量。
1.4.2 随访时间及术后复发情况 观察并比较两组患者的随访时间及术后复发率。
1.4.3 腰腿痛程度 采用视觉模拟评分法(visual analogue scale,VAS)于术前、术后3 d、术后6 个月、末次随访时评估患者的腰腿痛程度,评分越低,疼痛越轻。
1.4.4 功能障碍情况 采用Oswestry 功能障碍指数(oswestry disability index,ODI)于术前、术后3 d、术后6 个月、末次随访时评估患者的功能障碍情况,评分越低,功能障碍恢复越好。
1.4.5 下肢麻木情况 根据麻木评分表于术前、术后3 d、术后6 个月、末次随访时评估患者下肢麻木症状缓解情况:频发或持续的严重麻木(7~9 分),持续的轻微麻木或偶发严重麻木(4~6 分),偶尔的轻微麻木(1~3 分),无任何麻木(0 分)。
1.4.6 末次随访时腰椎功能优良率 末次随访时按腰椎功能MacNab 标准评估腰椎功能优良率。优:无痛、运动受限,能参加正常工作和活动;良:偶发非神经性疼痛,主要症状减轻,能够参加调整好的工作;可:一定程度的功能改善,仍为残废和(或)失业状态;差:检出持续的神经根受损表现、术后症状反复发作,不得不手术治疗。优良率=(优+良)/总例数×100%。
1.5 统计学方法 采用SPSS22.0 统计学软件进行统计分析。计量资料以均数±标准差()表示,组间比较采用t检验,组内比较采用方差分析;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组患者的围手术期指标比较 两组患者均顺利完成手术,无术后感染、损伤神经、脑脊液漏发生。两组患者的手术时间、术中出血量、住院时间比较,差异无统计学意义(P>0.05);PEID 组患者的术中C 型臂透视次数、透射剂量均少于PETD 组,差异具有统计学意义 (P<0.05)。见表1。
表1 两组患者的围手术期指标比较()
注:与PETD 组比较,aP<0.05
2.2 两组患者的随访时间及术后复发率比较 两组患者随访时间9~20 个月,PETD 组随访时间为(14.88±4.52)个月,PEID 组随访时间为(13.36±3.75)个月,两组随访时间比较,差异无统计学意义(P>0.05)。PETD组1 例患者术后复发行再次椎间孔镜手术治疗,1 例患者术后复发行开放融合手术治疗,术后复发率为7.7%(2/26);PEID 组1 例患者术后1 个月出现下肢疼痛反复,予以卧床休息、理疗及腰椎硬膜外神经阻滞术后疼痛缓解,术后复发率为4.5%(1/22)。两组患者的术后复发率比较,差异无统计学意义(P>0.05)。见表2。
表2 两组患者的随访时间及术后复发率比较(,%)
注:两组比较,P>0.05
2.3 两组患者的VAS 评分比较 两组患者术前、术后3 d、术后6 个月、末次随访时的VAS 评分组内比较,差异具有统计学意义 (P<0.05)。两组患者术后3 d、术后6 个月、末次随访时的VAS 评分低于本组术前,末次随访时的VAS 评分低于本组术后3 d,差异具有统计学意义 (P<0.05) ;两组患者术后3 d 与术后6 个月,术后6 个月与末次随访时的VAS 评分组内比较,差异无统计学意义(P>0.05)。两组患者术前、术后3 d、术后6 个月、末次随访时的VAS 评分组间比较,差异无统计学意义(P>0.05)。见表3。
表3 两组患者的VAS 评分比较(,分)
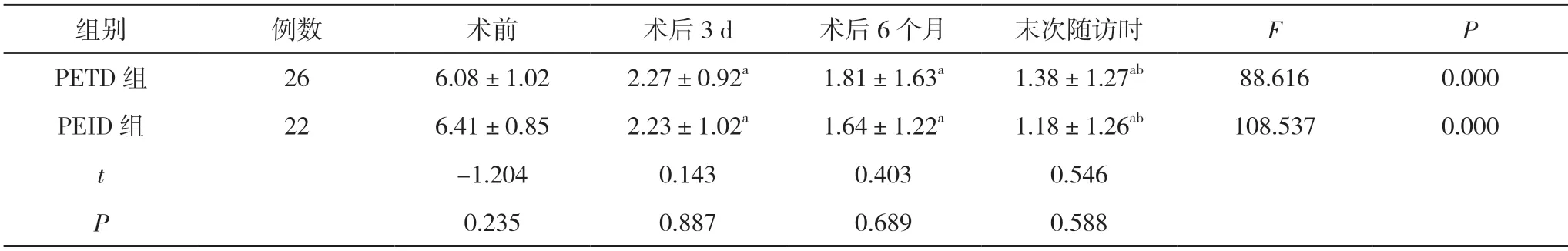
表3 两组患者的VAS 评分比较(,分)
注:与本组术前比较,aP<0.05;与本组术后3 d 比较,bP<0.05
2.4 两组患者的ODI 评分比较 两组患者术前、术后3 d、术后6 个月、末次随访时的ODI 评分组内比较,差异具有统计学意义 (P<0.05)。两组患者术后3 d、术后6 个月、末次随访时的ODI 评分低于本组术前,术后6 个月、末次随访时的ODI 评分低于本组术后3 d,差异具有统计学意义 (P<0.05) ;两组患者术后6 个月与末次随访时的ODI 评分组内比较,差异无统计学意义(P>0.05)。两组患者术前、术后3 d、术后6 个月、末次随访时的ODI 评分组间比较,差异无统计学意义(P>0.05)。见表4。
表4 两组患者的ODI 评分比较(,分)
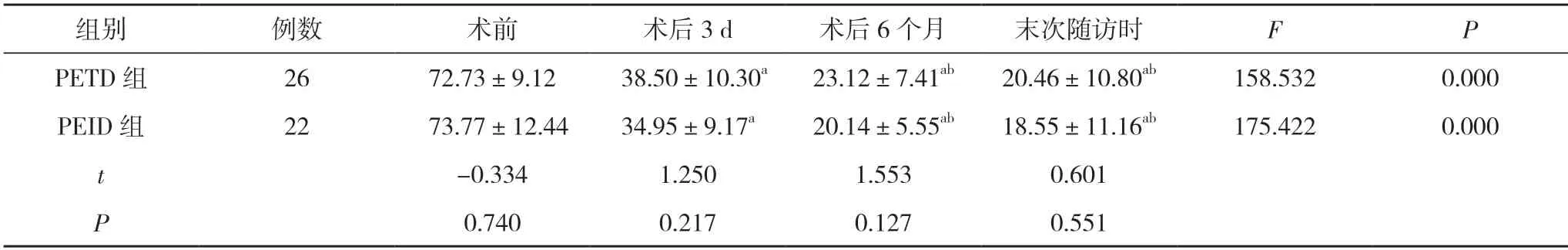
表4 两组患者的ODI 评分比较(,分)
注:与本组术前比较,aP<0.05;与本组术后3 d 比较,bP<0.05
2.5 两组患者下肢麻木评分比较 两组患者术前、术后3 d、术后6 个月、末次随访时的下肢麻木评分组内比较,差异具有统计学意义 (P<0.05)。两组患者术后3 d、术后6 个月、末次随访时的下肢麻木评分低于本组术前,术后6 个月、末次随访时的下肢麻木评分低于本组术后3 d,差异具有统计学意义 (P<0.05) ;两组患者术后6 个月与末次随访时的下肢麻木评分组内比较,差异无统计学意义(P>0.05)。两组患者术前、术后3 d、术后6 个月、末次随访时的下肢麻木评分组间比较,差异无统计学意义(P>0.05)。见表5。
表5 两组患者下肢麻木评分比较(,分)
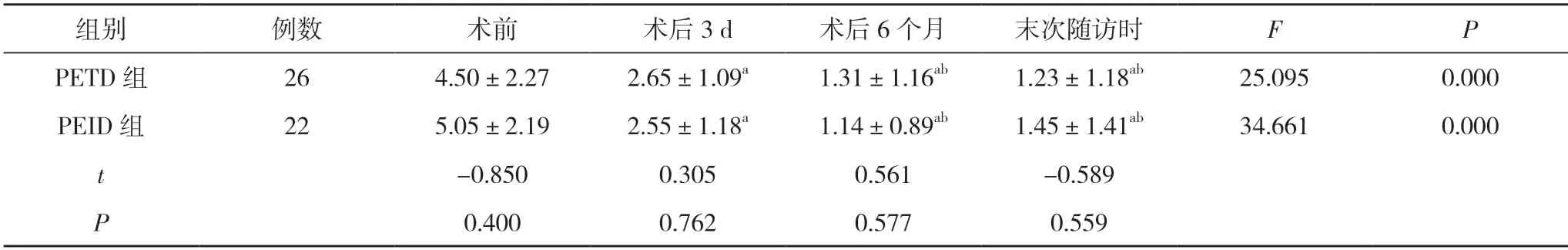
表5 两组患者下肢麻木评分比较(,分)
注:与本组术前比较,aP<0.05;与本组术后3 d 比较,bP<0.05
2.6 两组患者末次随访时腰椎功能优良率比较 末次随访时,按照腰椎功能MacNab 标准,PETD 组优13 例,良9 例,可3 例,差1 例,优良率为84.62%(22/26);PEID 组优11 例,良9 例,可2 例,差0 例,优良率为90.91%(20/22)。两组患者的腰椎功能优良率比较,差异无统计学意义(χ2=0.432,P=0.511>0.05)。典型病例见图1,图2。
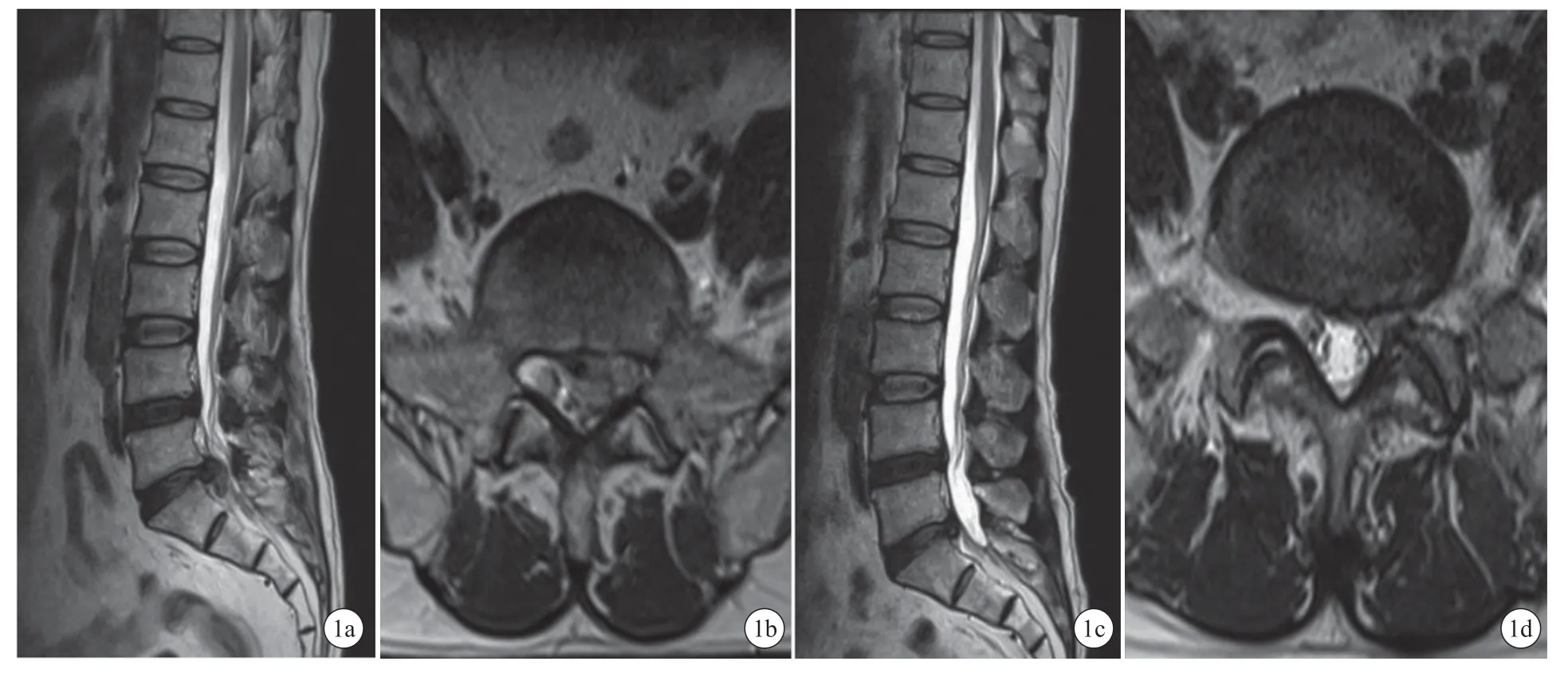
图1 患者男,53 岁,L5~S1 椎间盘突出,行经椎板间入路手术治疗
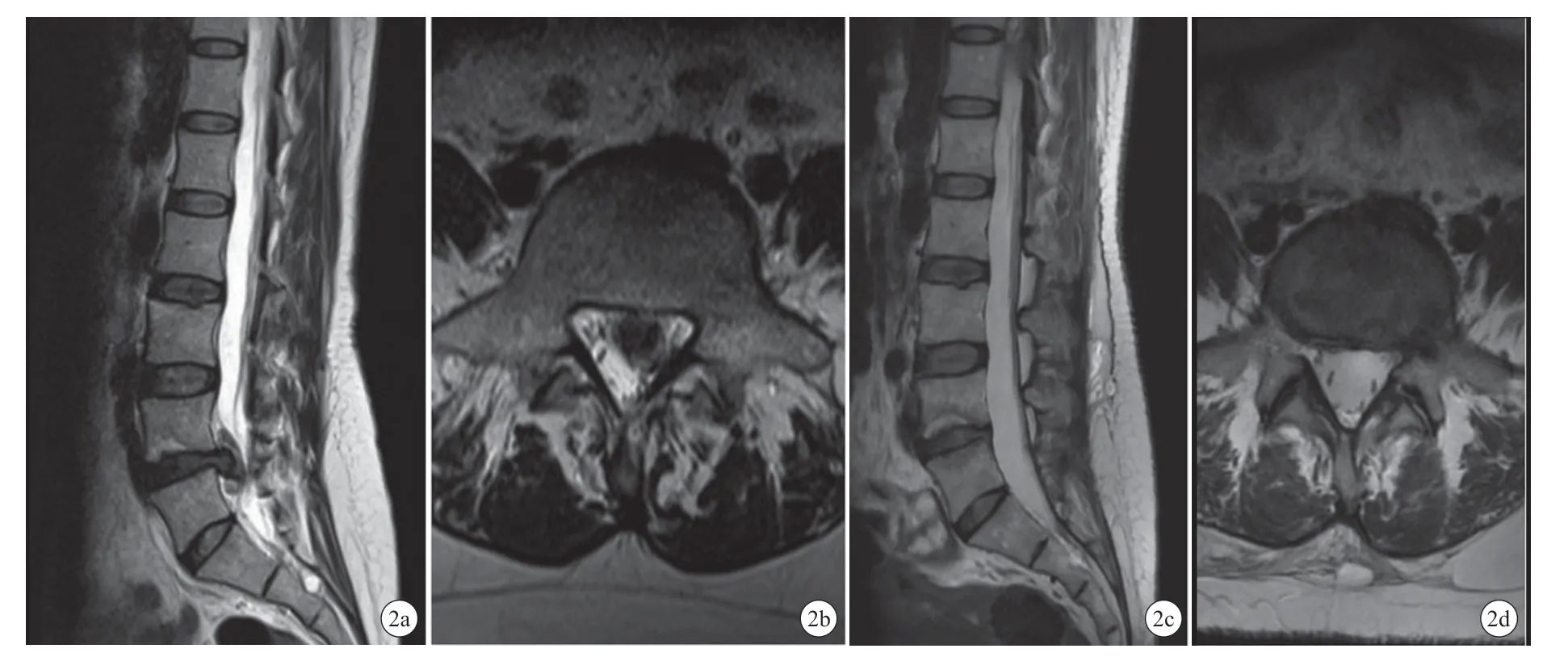
图2 患者女,48 岁,L5~S1 椎间盘突出,行经椎间孔入路手术治疗
3 讨论
巨大型腰椎间盘突出症可对局部硬膜囊与神经根造成严重压迫,影响血液循环和细胞代谢,继而导致相应的神经功能障碍[3]。患者多有腰椎间盘突出症病史,在反复弯腰、剧烈运动、负重等情况下突然出现严重的腰痛及下肢放射痛,疼痛剧烈,常规卧床休息、镇痛、脱水效果欠佳,严重者可表现为双下肢不完全性瘫痪,部分甚至出现鞍区麻木、大小便功能障碍等马尾神经受损现象。因此,明确诊断后应尽早采取手术治疗,彻底解除硬膜囊与神经压迫,预防神经功能永久性损害[4]。
传统开放手术或椎间盘镜手术因其视野宽阔,对手术操作无特殊要求,仅需仔细剥离被顶起的硬膜囊和神经根,取出突出的髓核即可,但存在创伤大、费用高等缺点[5]。在1997 年,Yeung 等开发了脊柱内镜YESS 系统,成为最常见的脊柱微创手术之一,之后逐渐发展为经皮椎间孔入路及经皮椎板间入路脊柱内镜下椎间盘摘除术[6]。通过总结文献,相比传统开放手术而言,椎间孔镜技术通过更小的切口、更少的软组织损伤、有效进行神经根及硬膜囊减压,而且能保留腰椎活动度[7]。根据MacNab 标准,本研究中PETD 组的优良率和PEID 组相似,两组在手术时间、术中出血量、住院时间等方面无显著差异,在最后的随访中,ODI 和VAS 评分明显改善。因此,这两种手术入路治疗巨大型腰椎间盘突出症均获得了满意的疗效。
针对巨大型腰椎间盘突出症,椎间孔镜技术借助脊柱内镜系统在狭小空间内对硬膜囊及神经根致压部位进行精确减压,在最大程度保持脊柱结构和稳定性的条件下,实现减压目的。但与传统开放手术相比,椎间孔镜因其工作通道狭小,视野受限,同时椎管内的血管受到严重挤压后容易破裂出血,导致镜下视野不清,容易造成髓核残留,出现症状不缓解或缓解不彻底,而且盲目操作也会带来神经损伤风险[8]。本研究中虽然没有出现脑脊液漏及硬脊膜损伤,但PETD 组及PEID组均有患者因术后疼痛缓解欠佳行再次手术治疗,这与手术医师的手术经验密切相关。
另一方面,两种入路均有各自的优势及局限性。对于巨大型腰椎间盘突出,PETD 可以避开硬脊膜的阻挡,通过椎管中线而不拉伸神经根,减少了硬脊膜撕裂和术中神经损伤的风险[9]。经椎间孔入路可到达椎间孔外区域,因此椎间孔入路可切除几乎所有类型的腰椎间盘突出,然而,因为工作导管的移动性受到椎间孔大小的限制,在摘除巨大脱垂椎间盘时,PETD 可能不能完全去除突出椎间盘,针对此类患者,可以适当减小穿刺角度,术中采用环钻进行椎间孔成形,为椎间孔留出更多空间,结束手术前一定要进行患侧直腿抬高试验,神经根滑动时注意观察是否有游离髓核,同时术前仔细评估影像学检查是十分必要的。
PETD 行椎间孔成形术的患者手术侧关节突关节部分骨结构破坏,而关节突关节损伤有可能会影响脊柱稳定性,甚至导致术后慢性下腰痛,但这之间的相关性仍需进一步的研究。此外,许多学者认为椎间盘摘除术中椎间盘髓核严重丢失和纤维环大量缺损会增加术后脊柱不稳定和慢性下腰痛的风险。在应用PETD治疗脱垂椎间盘时,部分患者需要切断部分后纵韧带以完全摘除髓核,这是否会影响患者的复发率有待进一步研究[10]。另一方面,治疗L5~S1椎间盘突出时,高髂嵴和狭窄的椎间孔在PETD 术中可能会阻碍手术操作,后外侧入路的穿孔角度有限,需要反复透视,增加了患者和外科医生的辐射暴露[11],本研究中,PETD组的术中C 型臂透视次数及透射剂量均显著高于PEID组,与其他研究相似,PETD 手术对医生健康的长期影响不容忽视。
与PETD 相比,PEID 手术路径与常规开放手术相似,有利于降低学习曲线,同时工作套管在椎板间移动范围较大,可扩大内镜视野,增加椎管内探查面积,减少髓核残留可能性[12]。椎板间入路也存在着一定的技术难点和风险,其中黄韧带的突破技术是首要的技术难题,采用篮钳与射频电极联合应用的方法,逐层突破黄韧带,不仅省时而且可最大限度避免硬膜囊和神经根损伤[13],本研究中PEID 组患者均未出现脑脊液漏。当患者合并巨大中央型腰椎间盘突出时,根据经验,由于硬脑膜和神经根外空间的限制,工作导管很难到达神经根肩,如果将工作导管直接向椎间盘旋转可能会导致进一步神经损伤,局部麻醉下应当严密观察患者下肢疼痛反应[14]。
PEID 术中需要绕过硬脊膜的遮挡:①过度牵拉可能会损伤硬脊膜,硬膜撕裂的风险高于PETD;②虽然在椎间孔镜术中采用局部麻醉有助于保护神经根免受损伤,但局部麻醉手术中PEID 的镇痛效果较差,对于部分患者,严重的疼痛感甚至可能导致致命的心血管事故,所以必要时需转为全身麻醉手术,而与其他全部麻醉操作相比,PEID 的副作用可能更大,而且增加了老年患者麻醉的风险[15]。
椎间孔镜手术仅摘除了突出椎间盘,保留了正常的髓核组织,与其他椎间盘切除术一样,经皮椎间孔镜下腰椎间盘摘除术也有一些复发的危险因素,如男性、肥胖[体质量指数(BMI)≥25 kg/m2]、年龄(≥50 岁)、有外伤史、吸烟、糖尿病等,但椎间孔镜手术也有一些独特的危险因素导致腰椎间盘突出复发。因为椎间孔镜手术有陡峭的学习曲线,当手术医生的手术经验较少(≤200 例)时更容易出现腰椎间盘突出复发。本研究中,PETD 组和PEID 组术后复发率分别为7.7%(2/26)、4.5%(1/22),与其他研究结果相似。术中充分摘除突出椎间盘,使用射频电极修补纤维环,以及减少对后纵韧带及关节突关节的损伤,术后指导如腰肌锻炼、适当的负重和正确的坐姿对减少腰椎间盘突出复发的可能性至关重要[16]。
术后如果患者术前下肢疼痛症状仍然存在甚至恶化,应该考虑残留椎间盘或神经减压不充分,早期可以通过卧床休息以及硬膜外神经阻滞术以进一步观察,若症状持续不缓解,则有必要复查腰椎MRI 评估神经减压情况。
最后,本研究存在一定的局限性:①手术方式和结果统计难以采用双盲设计,难以排除医生主观因素的影响;②本研究样本量较小,随访时间较短,数据具有一定的局限性,长期随访手术效果有待进一步观察。
综上所述,椎间孔镜下治疗巨大型腰椎间盘突出症疗效确切,与椎间孔入路比较,椎板间入路可以明显减少术中透视次数,减少辐射暴露,但术前需要准确评估影像学检查,根据手术医师的手术经验选择合适的手术入路。
