外耳道癌3例报告并文献复习
2022-12-29陈璇王晓茜吴佩娜唐智
陈璇王晓茜吴佩娜唐智
1南方医科大学顺德医院耳鼻咽喉头颈外科(佛山 528308)
2广东省人民医院耳鼻咽喉科(广州 510080)
3南方医科大学顺德医院附属杏坛医院五官科(佛山 528325)
1 病例资料
病例1,患者,男性,39岁,鼻咽癌放化疗后9年,因“反复左耳流脓2月余”就诊,曾在外院病理诊断为“颞骨恶性肿瘤”,未系统诊治,查体可见左侧外耳道后下壁一肉芽样肿物,左侧鼓膜穿孔;纯音听阈示左耳平均听阈88dB,声导抗左耳A型鼓室图;入院后完善全身骨显像提示左侧外耳道软组织影,邻近骨质未见明显破坏,双侧乳突代谢增高,考虑乳突炎;其余骨质未见局灶性活动性骨病变。考虑诊断“左侧颞骨恶性肿瘤(T1N0M0)”,行“左侧颞骨侧切除术+腮腺浅叶切除术(左)+颈淋巴结清扫术(左Ⅱ、Ⅲ区)”。术后病理示左外耳道中分化鳞状细胞癌,镜下可见鳞状上皮异型增生,可见角化珠形成(见图1)。患者术后未放化疗,术后随访2年肿瘤无复发,预后好。
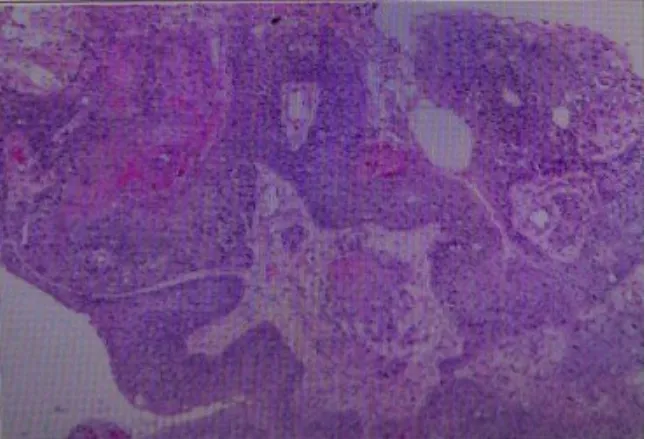
图1 病例1术后病理:左外耳道中分化鳞状细胞癌。镜下可见鳞状上皮异型增生,可见角化珠形成。Fig.1 Case 1 Postoperative pathology:Differentiated squamous cell carcinoma in the left external auditory canal,squamousdysplasia and keratinized beads can be seen under microscope.
病例2,患者,男性,72岁,因“反复左耳流脓数十余年,伴疼痛5月余”就诊,患者曾在外院检查发现外耳道肿物,行“耳内镜下左侧外耳道肿物切除术+左侧中耳探查术”,术后病理示“左外耳道肿物为高-中分化鳞状细胞癌”,术后3个月复查CT示:左外耳道、中耳乳突区不规则软组织密度影伴骨质破坏,局部乳突后壁破坏,邻近颅内未见明确受累征象。中、内耳MRI增强提示左侧外耳道-乳突肿块,考虑恶性肿瘤复发。查体可见左侧外耳道新生物,未窥及鼓膜。考虑诊断“左侧颞骨鳞状细胞癌(T4N1M0)”,术中探查发现肿瘤无被膜,无固定形态,无边界,侵犯范围广,向上侵犯颅中窝硬脑膜,向后侵犯后颅窝硬脑膜,向前侵犯颧弓、下颌窝,向下突破乳突尖浸润胸锁乳突肌肌腱,侵犯茎乳孔、茎突、颈静脉孔,向内侵犯内耳;肿瘤360°包裹颈静脉球,包裹颈内静脉C2段外侧,肿瘤包裹面神经水平段、乳突段、颞外段主干,颈部Ⅰ、Ⅱ、Ⅲ区见多个淋巴结,大者约1.0×0.8×0.6cm,术中切除内耳后见脑脊液漏;行“左侧颞骨次全切除术+颈淋巴结清扫(左Ⅰ、Ⅱ、Ⅲ区)+腮腺全切除术(左)+脑脊液漏修补术”,术后病理提示左外耳道高分化鳞癌,左侧中耳、颅中窝底、关节囊、颈静脉孔、茎乳孔、咽鼓管口、乳突尖、颞下颌关节、颅中窝硬脑膜均可见癌,镜下可见瘤细胞异型性较明显,可见大量角化珠(见图2)。患者术后恢复可,拒绝术后继续化疗并要求出院,术后1个月复查MRI提示左侧颈静脉孔区肿瘤残留,随访11个月后死亡。
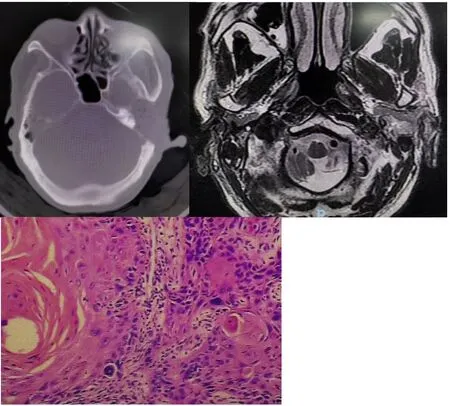
图2 病例2的影像学及病理结果:a.左外耳道、中耳乳突区不规则软组织密度影伴骨质破坏,局部乳突后壁破坏,邻近颅内未见明确受累征象;b.中、内耳MRI增强提示左侧外耳道-乳突肿块,考虑恶性肿瘤复发;c.左外耳道高分化鳞癌,镜下可见瘤细胞异型性较明显,可见大量角化珠。Fig.2 Imaging and pathological results of case 2:a.Irregular soft tissue density shadows in the left external auditory canal and mastoid region of the middle ear with bone destruction,partial destruction of the posterior wall of the ma-stoid,and no clear signs of involvement in the adjacent brain;b.The enhanced MRI of the middle and inner ear ind-icated a left external auditory canal-mastoid mass,and the recurrence of malignant tumor was considered;c.Well-differentiated squamous cell carcinoma of the left external auditory canal,with obvious tumor cell atypia and a large number of keratinized beads under the microscope.
病例3,患者,男性,60岁,鼻咽癌放疗后12年,因“发现外耳道肿物2月余,术后再发1月余”就诊,患者曾于外院行“右侧外耳道肿物切除术”,术后病理活检示“高分化鳞状细胞癌”,术后1个月复发。查体可见右侧外耳道狭窄,右侧外耳道后下壁可见菜花状肿物突起,表面不光滑,无异常渗出,鼓膜完整。MRI提示右侧外耳道癌、双侧腮腺外侧、颈Ⅰ区淋巴结反应性增大。考虑诊断“外耳道恶性肿瘤”,行“右侧颞骨次全切除术+腮腺全切除术(右)+面神经解剖术(右)+颈淋巴结清扫术(右Ⅰ区)”,术中冰冻外耳道肿物切缘阴性,术后病理提示右外耳道高分化鳞状细胞癌,见鳞状上皮被覆的粘膜组织上皮异型增生,可见角化(见图3)。患者出院时右侧颜面部水肿,右眼睑闭合不全,口角向左偏斜,HB面神经评级:Ⅲ级。患者术后未放化疗,术后随访4年肿瘤无复发,预后好。
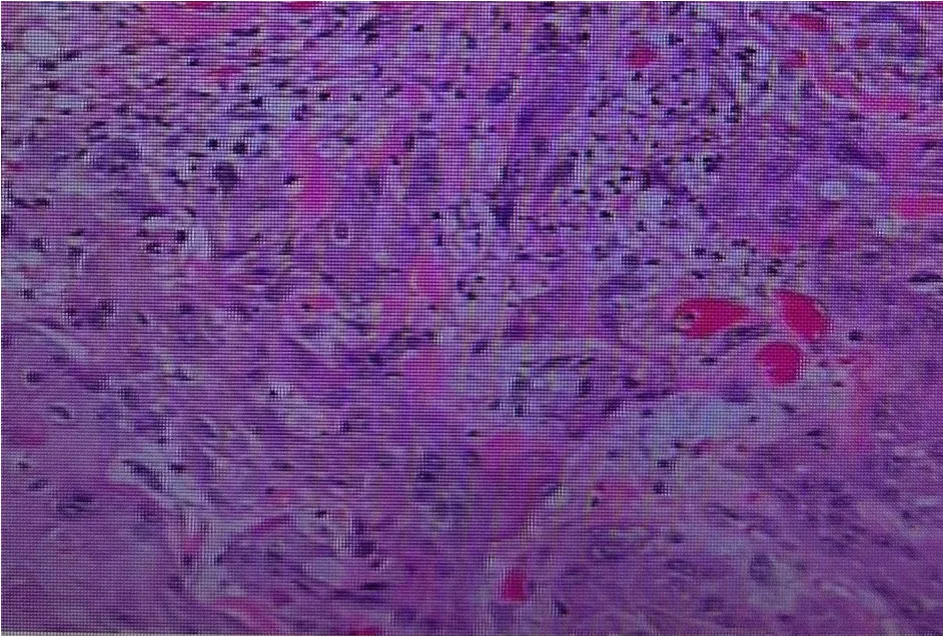
图3 病例3术后病理:右外耳道高分化鳞状细胞癌,见鳞状上皮被覆的粘膜组织上皮异型增生,可见角化。Fig.3 Case 3 Postoperative pathology:Well-differentiated squamous cell carcinoma of the right external auditory canal,with dysplasia of the mucosa covered by squamous epithelium,and keratinization can be seen.
2 讨论
外耳道癌是一类累及外耳道上皮的恶性肿瘤,常见于慢性外耳道炎患者,病例1和2均为慢性外耳道炎并发外耳道癌患者。外耳道癌病理类型以鳞状细胞癌最常见,约占外耳道恶性肿瘤的80%[1],以上3例病理类型均为鳞状细胞癌,中高分化为主。其次是腺样囊性癌,外耳道癌的其他病理类型因发病率低,国内外报道稀少[2]。因外耳道癌初期症状与其他(良性)疾病相似,误诊率高[3],以上3个病例均存在不同程度的耳痛、听力下降、耳流脓、耳堵塞感等非特异性症状[4],与既往报道符合。以上3例早期诊疗过程中均存在误诊误治问题,这与外耳道癌发病率低,专科医生能经治的病例数量有限,很难积累治疗经验有关,可见目前外耳道癌的诊疗规范尚不成熟。
外耳道癌诊断的金标准是病理活检,CT对骨组织的破坏显示清晰,而MRI能显示软组织受侵蚀的范围,故对于高度怀疑病例需反复活检,同时借鉴颞骨高分辨率CT、MRI了解肿瘤部位和范围,确定活检部位并提高活检阳性率[4],但外院在术前均未行病理活检明确肿物性质,未能根据CT、MRI明确外耳道癌的临床分期去制定个体化治疗方案,把外耳道恶性肿瘤当成普通的肿物切除,致使外耳道癌未能完整切除,未能保证切缘阴性,从而导致术后复发,这也影响其预后。
外耳道癌容易向前浸润腮腺,故腮腺的管理对于不同分期的外耳道癌实现无癌浸润至关重要[5]。Katano等[6]回顾分析了39例外耳道鳞状细胞癌患者的临床资料,发现腮腺直接侵犯仅见于晚期患者,而早期和晚期患者术前均有腮腺淋巴结转移。其指出对于所有晚期(T3和T4)患者应强制行腮腺全切除术。治疗上主张早期(T1或T2期)外耳道癌行颞骨侧切除+腮腺浅叶切除术;晚期(T3或T4期)外耳道癌行颞骨次全切除+腮腺全切除+颈部颈淋巴清扫术[4,7]。病例1为早期外耳道癌,行颞骨侧切除+腮腺浅叶切除+颈部颈淋巴清扫术,病例2和3均为晚期外耳道癌,行颞骨次全切除+腮腺全切除+颈部颈淋巴清扫术,均符合外耳道癌的治疗原则。
病例荟萃分析表明,无论是何种外耳道癌病理类型,手术结合术后放疗疗效优于单纯手术或单纯放疗。近年来临床研究发现采用改良TPF(5-氟尿嘧啶)方案对晚期外耳道癌进行放化疗具有良好效果,目前认为外束放疗与手术和/或化疗联合治疗可能是晚期外耳道癌最有效的治疗方案[8]。但根治性放疗同步放化疗的最佳化疗方案仍存在争议[6]。
以往的研究探索光动力治疗在鼻咽癌、喉癌及舌癌的应用,发现可提高患者的生活质量,有其独特优势[9]。Xu,S.,L等学者报道了1例应用光动力治疗早期外耳道基底细胞癌的病例,患者创面愈合,术后随访1年肿瘤无复发[8]。尽管光动力治疗早期外耳道癌效果良好,但关于这方面的文献报道有限,临床上尚不能推崇光动力学治疗。
本文病例1、3既往均存在鼻咽癌放疗病史,其中病例1行放化疗(放疗后9年),病例3单纯放疗(放疗后12年),均在放疗后出现外耳道癌,临床上发现放射治疗头颈部肿瘤尤其是鼻咽癌放疗后会造成放疗后颞骨鳞状细胞癌的发生,尽管放疗后诱发癌症几率很低[10],但病例1和3不排除是放疗后诱发外耳道癌。2019年MaebayashiT报道了一例应用放化疗治疗放射诱导的双侧外耳道癌的病例,且术后肿瘤无复发,这表明放化疗可能是治疗放射诱导癌的有效策略[11],但原则上外耳道癌的治疗以手术为主。此外在头颈部肿瘤中,虽然放射性脑病一般发生于鼻咽癌放疗之后,外耳道癌放疗后发生的脑损伤并不常见,病例1和3鼻咽癌放疗后未出现放射性脑病,术后也未放疗,但在临床工作中应警惕外耳道癌术后放疗患者发生放射性脑病,并及时处理[12]。
目前认为外耳道癌复发最主要原因是切缘阳性,而术中应用冰冻病理是取得安全切缘的保证[4,13],病例1、3术中切除恶性肿瘤后术中冰冻均达到切缘阴性,术后未放化疗,病例1术后随访13个月未复发,病例3术后随访4年未复发。病例2术中探查发现肿瘤浸润范围广,术中冰冻切缘未达阴性,术后患者及家属拒绝放化疗,术后1个月复查MRI提示左侧颈静脉孔区肿瘤残留,随访11个月后死亡。总结以上3例病例,可见术中切缘阳性者预后差,与复发强相关,也影响患者的预后。病例3患者二次手术时术中送检了冰冻病理,结果提示阴性可减少复发可能。远处转移的发生与局部复发显著相关[14],外耳道癌患者复发后生存率明显下降,且再次复发率高[15,16]。外耳道癌的发病率不高,但死亡率高[17],其预后取决于肿瘤的分期,淋巴结转移,面瘫,颅内侵犯硬脑膜以及是否取得安全切缘[18,19]。病理类型对早期外耳道癌患者的预后有直接影响,根据早期肿瘤患者病理恶性程度的不同,制定个体化治疗方案,可延长患者的生存时间[20]。
综上所述,外耳道癌为头颈部少见肿瘤,为数不多的病例资料难以得出有益的临床经验或规范,可供参考的病例分析文献也屈指可数;总的原则都是结合外耳道癌的病理类型、生物学特性及局部侵袭性与转移的方式选择个体化治疗[21]。由于颞骨周围解剖结构复杂,故颞骨高分辨CT和MRI增强对明确肿瘤部位、范围及性质至关重要。治疗方式以手术为主,手术尽可能取得安全切缘。早期患者应行颞骨侧切除+腮腺浅叶切除,晚期患者在手术切除的基础上需要辅助放化疗以期获得较好的预后。同时临床医师未来可继续探索光动力治疗在不同病理类型外耳道癌中的应用疗效,比较光动力学治疗与手术和放化疗的疗效差异。
