不完全性胰腺分裂致慢性胰腺炎1例报告
2022-11-16董美丽张瑞华李腾飞温晓玉
董美丽,张瑞华,李腾飞,王 阳,温晓玉
吉林大学第一医院 肝胆胰内科,长春 130021
慢性胰腺炎(chronic pancreatitis,CP)是一种慢性进行性炎症,胰腺实质被纤维结缔组织取代,最终出现内、外分泌功能不全[1]。目前最常用TIGAR-O系统对CP进行病因分类,其中,引流不畅的胰腺分裂(pancreas divisum,PD)被认为是CP的危险因素[2]。PD是胰腺在发育时,因其背腹侧胰管融合异常而形成的解剖异常,报告发病率为4%~14%。95%的患者不会出现任何症状或体征,但当其与胆结石病、暴饮暴食、饮酒、高甘油三酯血症以及遗传学等危险因素共同作用时,发生急性复发性胰腺炎(acute recurrent pancreatitis,ARP)、CP和慢性腹痛的概率增大。现将本院收治的1例不完全性胰腺分裂(incomplete pancreas divisum,IPD)致CP报告如下。
1 病例资料
患者男性,33岁,主因“间断上腹痛18年,再发伴恶心、呕吐3 d”于2021年12月5日入本院。患者18年前首次因无明显诱因出现上腹疼痛伴恶心、呕吐、腹胀就诊于当地医院,考虑为“胰腺炎”,给予对症治疗后好转。此后约1年发作1次,诱因不明,就诊于北京、当地等多家医院,均按“胰腺炎”对症治疗后好转,但病因不祥。2年前因上腹痛就诊于本院门诊,考虑“胰腺炎”,给予对症治疗好转。3 d前患者再次上腹隐痛,伴恶心、呕吐,为求进一步系统诊治入本院肝胆胰内科。患者起病前无暴饮暴食及大量饮酒。病程中无畏寒发热、无咳嗽咳痰、无脂肪泻等不适。否认服药史,否认胆结石、糖尿病等病史。否认手术外伤史及烟酒史,无遗传性胰腺炎家族史。查体:体温36.5 ℃,心率68次/min,呼吸18次/min,血压125/84 mmHg。BMI 26.9 kg/m2。皮肤及巩膜无黄染,腹部平坦,左上腹压痛阳性,无反跳痛和肌紧张,Murphy征阴性,余无异常。实验室检查:白细胞9.37×109/L,中性粒细胞绝对值7.26×109/L;血淀粉酶156.7 U/L,血清脂肪酶178.16 U/L,尿淀粉酶1042 U/L;CRP 17.77 mg/L;空腹血糖4.03 mmol/L;CA19-9 49.71 U/mL;血清钙离子浓度2.30 mmol/L;甘油三酯2.61 mmol/L,低密度脂蛋白胆固醇3.32 mmol/L,余未见异常。入院诊断为“胰腺炎”,给予禁食水、抑酸、抑制胰酶分泌、补液及对症治疗。因患者胰腺炎反复发作,原因不明,在排除常见的胰腺炎病因后反复阅读腹部CT(图1),发现胰尾部有小钙化影,考虑存在CP,病因不除外自身免疫或解剖异常等罕见因素,遂完善自身免疫性肝病IgG抗体、抗核抗体系列等免疫指标检查,但均为阴性。后行磁共振胰胆管造影(MRCP)(图2)示:脂肪肝;胰腺分离;胰尾部及周围可疑炎性改变。结合患者的病史、临床表现及辅助检查,明确诊断为CP Ⅰ期(IPD)。后转入肝胆外科行经内镜逆行胰胆管造影(ERCP)(图3)、小乳头切开术(EST)和支架植入术,病情好转后出院,随访至今,胰腺炎未复发。
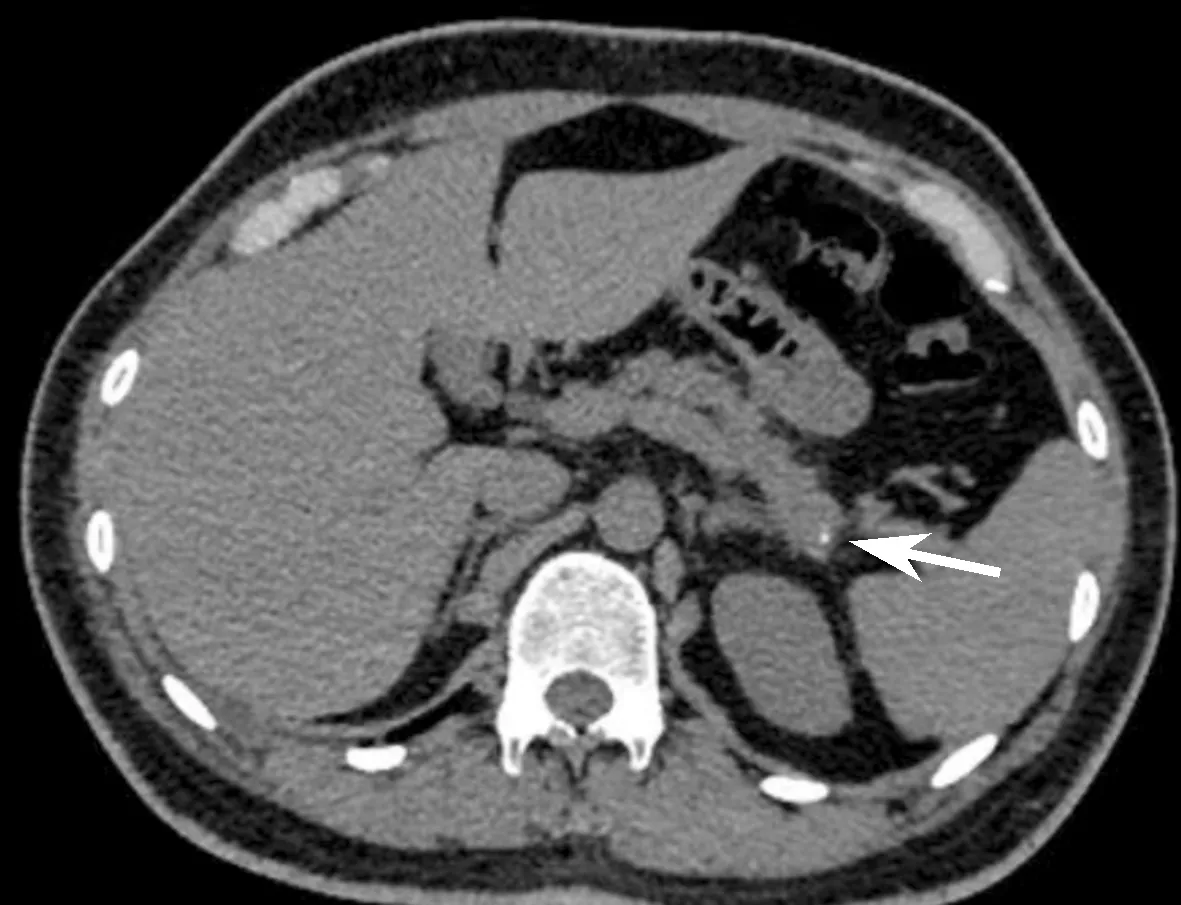
注:肝内外胆管未见扩张,腔内未见异常密度影。胰腺实质密度稍减低,见点状钙化影,边缘毛糙,周围脂肪间隙稍浑浊,见条片状渗出影,胰尾部见结节状钙化影(箭头),大小约0.3 cm,胰管未见扩张。
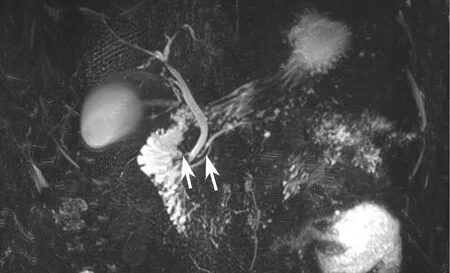
注:胰尾部稍饱满,边界模糊。胰头处可见两个胰管(箭头),主胰管开口于十二指肠小乳头,副胰管开口于大乳头。

注:主副胰管显影(箭头),主副胰管交汇处可见胰管明显狭窄,狭窄远端胰管扩张,最宽处0.5 cm。
2 讨论
PD是因胚胎期胰腺背腹侧胰管融合失败,致使大部分胰液通过背侧胰管经十二指肠副乳头流出[3]。PD分为3类,Ⅰ型(典型PD):背腹侧导管完全不融合;Ⅱ型:腹侧导管缺失,以背侧胰管引流为主;Ⅲ型(IPD):背腹侧导管间存在交通[4]。本例患者主副胰管交汇,符合IPD。PD发病率为4%~14%[4],而IPD在临床中更少见,发生率仅为0.1%~0.9%。大多数患者无症状或体征,只有约5%患者表现为ARP、CP或慢性腹痛,其中腹痛是PD最常见的首发症状[5]。PD的胰腺炎致病性一直存在争议,主流假说认为大量胰液流经微小的副乳头孔时受阻,胰管高压进而发生胰腺炎。这一假说得到了以下证据的支持:ARP或CP患者经小乳头内窥镜和EST解除胰管高压后,临床预后良好;与非手术对照组相比,行背侧导管支架置入术的治疗组患者胰腺炎复发率显著减少,腹痛改善[6]。本例患者行EST和支架植入术后,效果良好,也支持了该假说。然而,PD中只有一小部分患胰腺炎,证明这些患者存在胰腺炎其他易感因素的可能。早期研究[7]表明,在PD背景下,丝氨酸蛋白酶抑制剂Kazal 1型(SPINK1)、阳离子胰蛋白酶原和囊性纤维化跨膜电导调节因子基因多态性与胰腺炎有关,其中SPINK1 rs17107315多态性的相关性最强。可能的解释是PD为胰腺疾病的病理基础,而当PD与胆结石病、暴饮暴食、饮酒、高甘油三酯血症和遗传学等危险因素共同作用时,发生胰腺炎的风险加大[8]。本例患者考虑IPD致胰液流出受阻是胰腺炎反复发作的主要原因,而患者BMI 26.9 kg/m2,胆固醇和低密度脂蛋白水平高于正常范围,因此高脂血症可能也发挥了一定作用。
在临床诊治中,对于反复腹痛,尤其伴有内、外分泌功能不全者,要高度怀疑CP,超声内镜和MRI/MRCP有助于早期诊断,腹部CT等可用于晚期诊断[1,9]。寻找CP病因时,在排除常见病因后,要考虑解剖异常、免疫等罕见因素。PD是最常见的胰腺结构异常,因其症状无特异性,主要依靠影像学检查进行诊断,常用的检查有MRCP、ERCP、胰泌素增强的磁共振胰胆管成像(secretin-enhanced magnetic resonance cholangio-pancreatography,S-MRCP)等。一些PD诊断研究表明MRCP和ERCP结果之间存在良好的相关性,两者均可作出明确诊断。但因MRCP是不需要造影剂的非侵入性检查,能可视化评估胰胆管情况,具有风险小、可重复、可同时显示胰腺和周围结构形态变化等优势,为诊断PD首选[10]。针对本例患者也首选了MRCP来判断是否存在胰腺解剖异常,并得到了明确的结果和确定了分型。ERCP是诊断PD的金标准,但其是涉及辐射的侵入性检查并有10%~15%的并发症发生率,因此限用于诊断难以确定的病例及治疗有症状的患者[11]。S-MRCP是一种新兴检查,通过添加促胰液素来增加导管容积和胰腺外分泌,同时改善先天性胰胆管畸形的可视化[4]。一项系统评价[4]指出,S-MRCP诊断PD的特异性和敏感性与ERCP无显著差异。此外,若多探测器计算机断层扫描显示胰背管和圣托若里尼管之间连续连接,则也可诊断PD[9]。
无症状PD不需治疗或评估,有症状者,先保守治疗。治疗性干预仅适用于急性胰腺炎反复发作或影像改变明显者。ERCP加EST,加或不加支架是症状性PD的首选干预措施[10]。如果ERCP失败且仍有症状,或CP和有局部并发症,可考虑手术优化胰腺引流。最近发表的对1887例PD患者的荟萃分析[12]表明,外科治疗在成功率、降低并发症发生率和再干预率方面可能优于内镜治疗。本例患者胰腺炎反复发作,影像学改变明显,告知其内镜治疗方案的相关风险和效益后,最终决定行ERCP加EST加支架植入术,术后病情明显改善,至今未复发。
PD发病率低,是胰腺炎罕见病因,临床医生可能对其缺乏了解,因而容易漏诊。本病例患者提示在临床实践中,对于反复腹痛者,如果明确诊断为胰腺炎而病因不明,则应考虑有症状的PD。同时,在诊治过程中,应详细追问病史,避免遗漏与疾病相关的重要信息,并沿着辅助检查中发现的蛛丝马迹,抽丝剥茧寻找致病因素,从而提高诊断的准确率,提供个体化治疗,改善患者预后。
伦理学声明:本例报告已获得患者知情同意。
利益冲突声明:所有作者均声明不存在利益冲突。
作者贡献声明:董美丽负责课题设计,资料分析,撰写论文;张瑞华、李腾飞参与收集及分析数据;王阳指导撰写文章并修改论文;温晓玉负责拟定写作思路并最后定稿。
