副猪嗜血杆菌的分离鉴定与灭活疫苗的初步研制
2022-09-07温树桦曹华斌王承宝
肖 敏,刘 建*,卢 昌,任 华,温树桦,曹华斌,王承宝,王 闯
(1.江西正邦养殖有限公司,江西南昌 330096;2.江西正邦农业科学院,江西南昌 330096;3.江西农业大学,江西南昌 330045;4.西北农林科技大学,陕西杨凌 712100)
副猪嗜血杆菌(Haemophilusparasuis,HPS)是巴氏杆菌科(Pasteurellaceae)的一种革兰氏阴性菌,体积较小,不具有运动性,形态多样(从单球杆菌到丝状链)[1],在生长过程中需要V因子(烟酰胺腺嘌呤二核苷酸,NAD)[2-3]。副猪嗜血杆菌是4周龄~8周龄仔猪上呼吸道的早期寄居菌,母源免疫水平、菌落定居情况及机体免疫系统的变化可以引起猪多发性浆膜炎和关节炎[4],临床症包括高热(41.5℃)、咳嗽、腹式呼吸、关节肿胀伴有跛行以及侧卧、四肢划动和震颤等[5]。在感染猪场内,副猪嗜血杆菌病的发病率和死亡率存在着很大的变化,一般猪群副猪嗜血杆菌病发病率可能从5%~10%不等,在阴性猪群中可达到75%[6]。
副猪嗜血杆菌是猪上呼吸道内的寄生菌,鼻腔和气管的病原菌检测并不能对该病菌进行诊断。可以从纤维素渗出物、发病猪的内脏器管实质和肺炎病猪的肺脏病变部位对副猪嗜血杆菌进行分离鉴定,从而对该病进行诊断[7]。该菌生长条件十分苛刻,在室温下仅少量可以存活,对分离得到的病原菌进行抗生素敏感性的测定和病原菌的分型十分重要[8]。本研究主要从副猪嗜血杆菌感染症状比较典型的30日龄~50日龄病猪的肺脏组织、关节积液、腹腔积液、胸腔积液进行细菌分离,然后用PCR方法对分离菌株进行初步鉴定及血清型分型,为黑龙江、江西和广东地区部分猪场副猪嗜血杆菌的研究提供流行病学数据。同时初步研制了副猪嗜血杆菌的单价灭活疫苗,为副猪嗜血杆菌的多联多价疫苗研制奠定了一定的基础。
1 材料与方法
1.1 材料
1.1.1 实验动物 6周龄~8周龄Balb/c小鼠购自江西中医药大学实验动物中心。20日龄~25日龄仔猪购自江西某猪场,该猪场未发生过猪链球菌病和副猪嗜血杆菌病,未免疫过猪链球菌疫苗和副猪嗜血杆菌疫苗,仔猪无猪链球菌病和副猪嗜血杆菌病临床症状。试验方案和实验动物福利与伦理均符合相关规定。
1.1.2 主要试剂 胰蛋白胨大豆肉汤培养基和大豆酪蛋白琼脂培养基,广东环凯微生物科技有限公司产品;特级新生牛血清,草原绿野生物工程材料有限公司产品;氧化辅酶Ⅰ(NAD),北京索莱宝科技有限公司产品;商品化猪链球菌病、副猪嗜血杆菌病二联灭活疫苗,武汉科前生物股份有限公司产品。
1.1.3 主要仪器 分光光度计,上海精科科学仪器有限公司产品;生化培养箱,上海博讯医疗生物仪器股份有限公司产品;全自动核酸提取仪,西安天隆科技有限公司产品;PCR仪,赛默飞世尔科技(中国)有限公司产品。
1.2 方法
1.2.1 病料采集 从黑龙江、江西、广东3个省12个发病猪场采集疑似副猪嗜血杆菌病料,发病猪为30日龄~50日龄,主要临床症状为呼吸困难、关节肿胀、跛行、皮肤及黏膜发绀、站立困难甚至瘫痪。病猪停药后5 d~10 d,剖检取病猪完整肺部,如有关节积液、腹腔积液、胸腔积液等病料,用一次性注射器吸取,4℃保存用于实验室细菌分离。
1.2.2 细菌分离 用无菌棉签将肺部病变部位、肺支气管黏液和其他积液涂布于含有NAD的大豆酪蛋白琼脂培养基上,同时蘸取金黄色葡萄球菌划线,37℃培养24 h~48 h后观察;挑取沿金黄色葡萄球菌“卫星生长”的菌落,再次在巧克力琼脂培养基上,同时蘸取金黄色葡萄球菌划线,37℃培养24 h~48 h。挑取沿金黄色葡萄球菌“卫星生长”的菌落,接种胰蛋白胨大豆肉汤培养基中37℃、220 r/min培养12 h~16 h,用于后续菌落鉴定。
1.2.3 生化鉴定 无菌条件下用接菌环刮取多个菌落,进行革兰氏染色,并分别接种过氧化氢酶、吲哚、蔗糖、乳糖、七叶苷和甘露醇等微量生化鉴定管中,随后加入3 μL~5 μL的NAD,并设置对照组,37℃培养24 h~48 h,按照试剂盒说明书进行判定。
1.2.4 PCR鉴定及血清型分型 根据GenBank公布的猪副猪嗜血杆菌序列,结合Ologo6.0及Primeer Premier软件自行设计1对副猪嗜血杆菌16S rRNA引物以及15对分型引物,引物由上海英俊生物技术有限公司合成(表1)。副猪嗜血杆菌基因组DNA模板提取及PCR反应参照文献[3]。
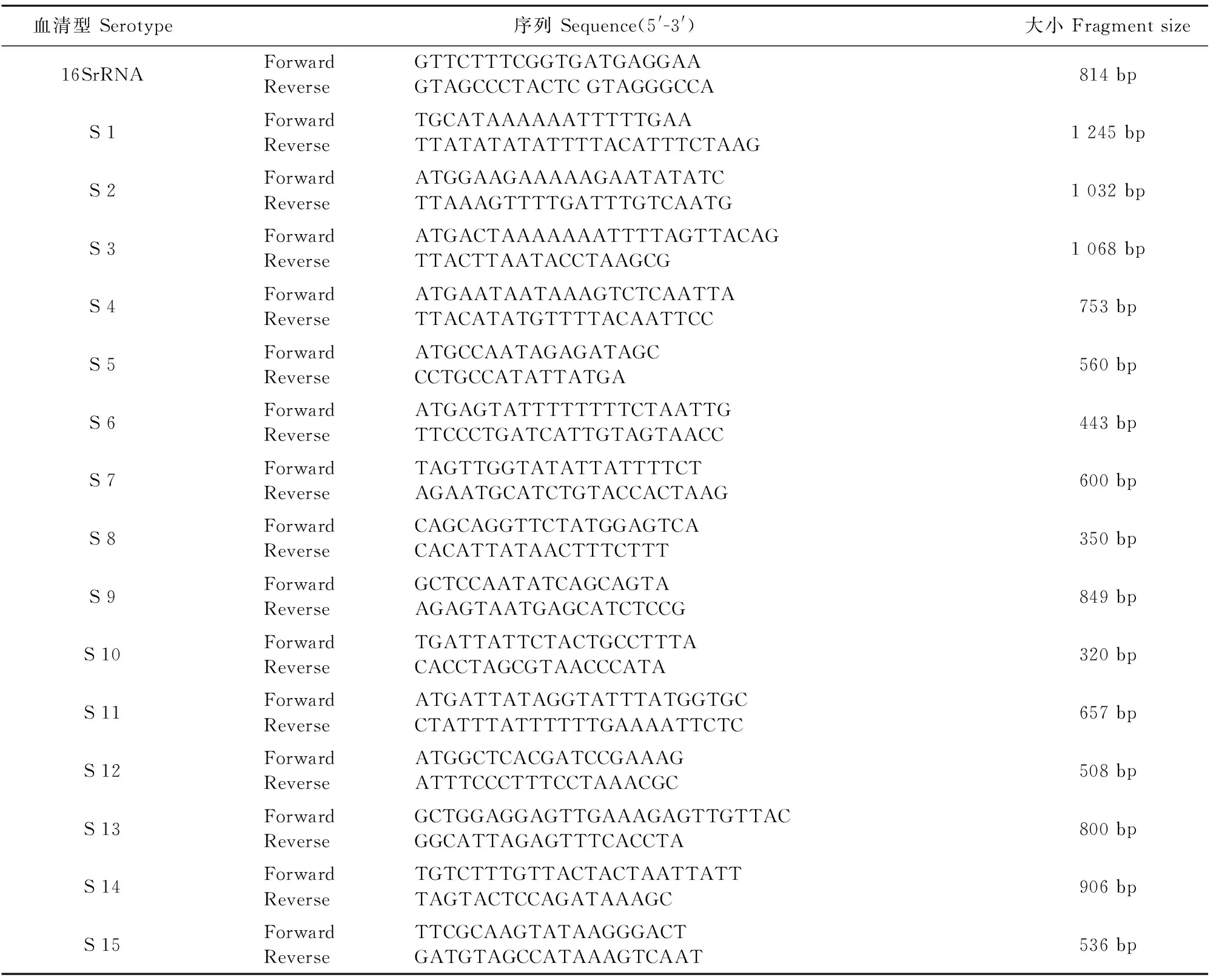
表1 副猪嗜血杆菌血清型引物核苷酸序列
1.2.5 副猪嗜血杆菌的毒力试验 选取25只6周龄~8周龄Balb/c小鼠,随机分成5组,每组5只,分别设置不同活菌浓度组6×109、6×108、6×107、6×106CFU/mL和未攻毒对照组,皮下注射0.2 mL菌液,未攻毒对照组注射0.2 mL生理盐水。连续观察7 d,记录小鼠死亡情况。按照Reed&Muench氏法计算副猪嗜血杆菌的LD50。
1.2.6 疫苗制备 副猪嗜血杆菌菌种(2型、7型、13型)分别接种含有50 mL/L新生牛血清和10 g/L NAD的胰蛋白胨大豆肉汤培养基中,37℃培养10 h。培养的菌液6 000 r/min离心5 min,弃上清,用无菌磷酸缓冲盐溶液将沉淀重悬至1.2×109CFU/mL。按体积比加入1 mL/L甲醛溶液,37℃静置灭活24 h~48 h,期间每隔4 h搅拌1次。取灭活后的菌液涂布于大豆酪蛋白琼脂培养基平板,进行活菌检验,以确保灭活彻底。然后与水包油包水佐剂充分混匀,使得副猪嗜血杆菌的终浓度为6×109CFU/mL。疫苗适用于4周龄~8周龄仔猪,免疫剂量为每头份2.0 mL。
1.2.7 疫苗安全性试验 选取20日龄~25日龄仔猪15头,随机分成3组,每组5头,试验分组分别为试验Ⅰ组(本试验疫苗)、试验Ⅱ组(佐剂组)、试验Ⅲ组(空白组),试验Ⅰ组颈部肌肉注射2 mL的本试验疫苗,试验Ⅱ组注射2 mL佐剂,试验Ⅲ组注射2 mL无菌磷酸缓冲盐溶液。连续观察仔猪7 d,对仔猪体温、饮食、精神状况、死亡情况进行记录,评价疫苗的安全性。
1.2.8 疫苗攻毒保护试验 选取20日龄~25日龄仔猪40头,随机分成4组,每组10头,试验分组分别为试验Ⅰ组(本试验疫苗)、试验Ⅱ组(商品疫苗组)、试验Ⅲ组(不免疫组)、试验Ⅳ组(未免疫不攻毒组)。免疫组仔猪颈部肌肉免疫2次,首免后35 d进行二免,每次免疫剂量为1 mL/头。二免后2周,所有免疫组和攻毒对照组口服4 mL(5×109CFU/mL)的副猪嗜血杆菌活菌。在免疫前、攻毒前和攻毒后7 d分别采集仔猪血清和鼻腔拭子。
2 结果
2.1 菌落和细菌形态
大豆酪蛋白琼脂培养基培养基上,离金黄色葡萄球菌菌苔越近长势越好,越远菌落较小甚至未出现菌落(图1A)。阴性对照组在大豆酪蛋白琼脂培养基上培养24 h~48 h后,可以观察到金黄色葡萄球菌附近无“卫星生长现象”(图1B)。

图1 副猪嗜血杆菌的卫星生长现象

M.DNA标准DL 2 000;1~10.样品;+.阳性对照;-.阴性对照
2.2 菌株生化鉴定结果
取副猪嗜血杆菌疑似菌落进行革兰氏染色,在显微镜下可以观察到革兰氏阴性细小杆菌,具有多种不同形态,从单个球杆菌到长的、细长的、甚至丝状的菌体。将疑似菌落接种于过氧化氢生化鉴定管中,肉眼可见鉴定管中产生明显的气泡,而阴性对照组无气泡产生;接种于蔗糖、乳糖、七叶苷、吲哚和甘露糖微量生化鉴定管中,蔗糖生化鉴定管由淡色变为黄色,乳糖、七叶苷、吲哚和甘露糖生化鉴定管颜色没有变化。
2.3 副猪嗜血杆菌PCR鉴定和分型鉴定结果
根据NCBI公布的副猪嗜血杆菌16S rRNA序列设计引物,对上述分离获得的副猪嗜血杆菌进行PCR扩增,得到的PCR产物经琼脂糖凝胶电泳验证。由琼脂糖凝胶电泳结果可以看出,PCR扩增的目的片段位于750 bp~1 000 bp,与预期PCR扩增产物片段814 bp大小一致(图2)。利用15对副猪嗜血杆菌分型引物对上述细菌进行分型鉴定,部分副猪嗜血杆菌分型琼脂糖电泳结果(图3),黑龙江H猪场和I猪场副猪嗜血杆菌利用12型引物扩增出508 bp大小的片段,黑龙江G猪场副猪嗜血杆菌利用13型引物扩增出800 bp大小的片段。13个猪场副猪嗜血杆菌的血清型分型情况(表2)。

A.副猪嗜血杆菌12型检测结果,M.DNA标准DL 2 000;+.阳性对照;-.阴性对照;1.黑龙江F猪场Hps;2.黑龙江G猪场;3.黑龙江H猪场
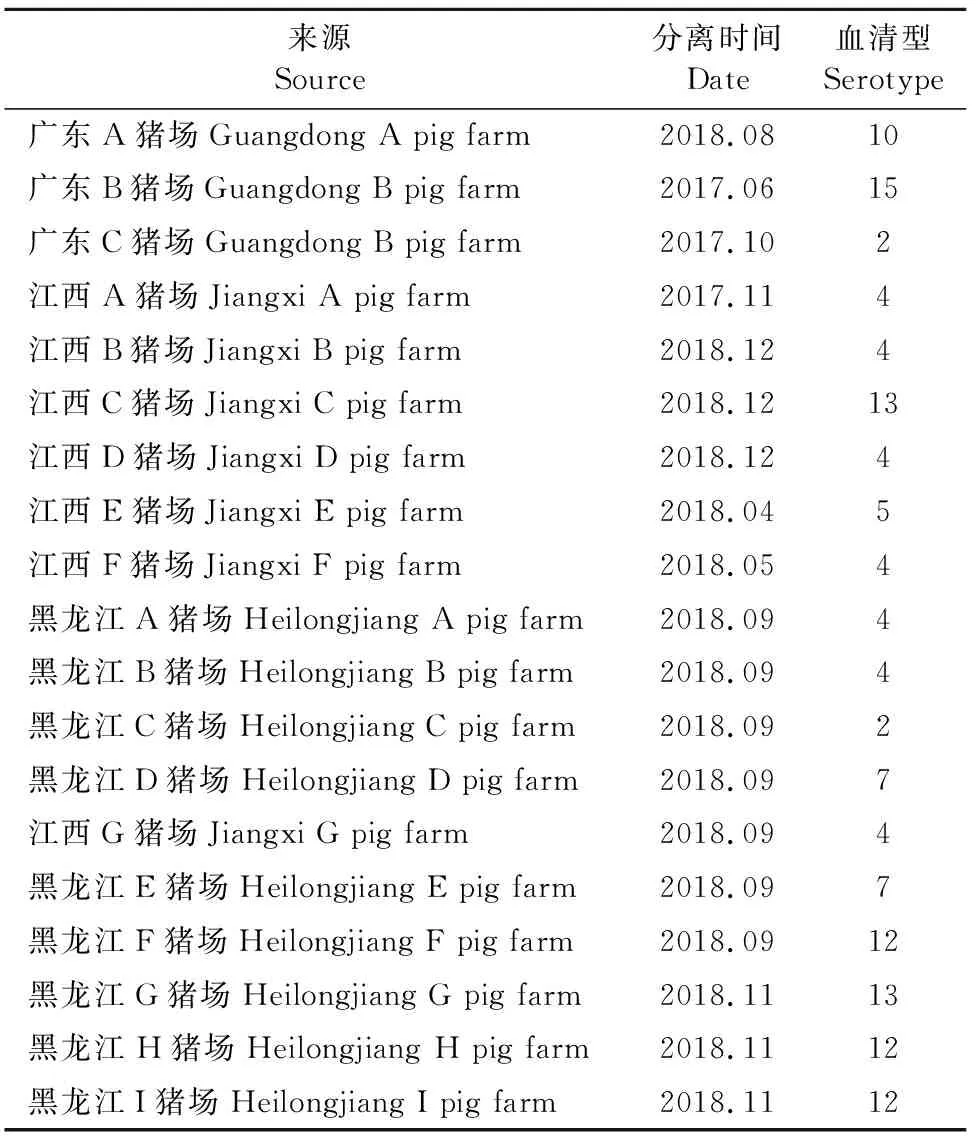
表2 各猪场副猪嗜血杆菌血清型分型情况
2.4 副猪嗜血杆菌的小鼠毒力试验
Balb/c小鼠皮下接种6×109、6×108、6×107、6×106CFU/mL副猪嗜血杆菌后,均出现精神不振,试验组小鼠于48 h内都出现死亡(图4)。用Reed &Muench氏法计算副猪嗜血杆菌的50%感染致死量(LD50),不同血清型副猪嗜血杆菌的50%感染致死浓度为5.0×107CFU/mL~1.0×108CFU/mL。
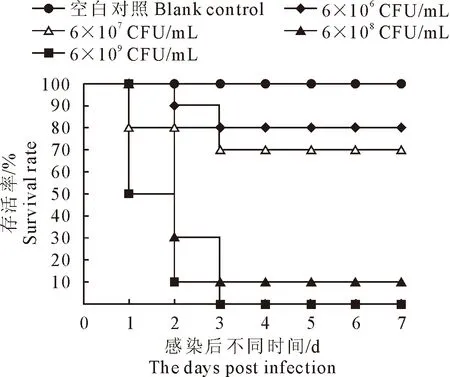
图4 小鼠感染副猪嗜血杆菌后的存活情况
2.5 副猪嗜血杆菌灭活疫苗对仔猪免疫保护结果
副猪嗜血杆菌2型、7型、13型单价灭活疫苗分别经颈背部肌肉免疫2 mL(6×109CFU/mL),随后逐日观察仔猪的精神状态及死亡情况。副猪嗜血杆菌灭活疫苗免疫组、佐剂免疫组和空白对照组仔猪体温均正常、精神状态良好,没有死亡情况。副猪嗜血杆菌单价灭活疫苗免疫组利用同源菌株攻毒后没有出现仔猪死亡情况,鼻腔拭子未检测出Hsp核酸;而未免疫攻毒组出现仔猪死亡情况,且鼻腔拭子的Hsp核酸为阳性。用副猪嗜血杆菌间接血凝诊断试剂盒对仔猪免疫前和二免后14 d的血清抗体进行检测,二免后14 d疫苗免疫组仔猪抗体水平较免疫前明显升高,且副猪嗜血杆菌单价灭活疫苗的抗体水平与商品苗的抗体水平差异不显著(P>0.05)(图5)。
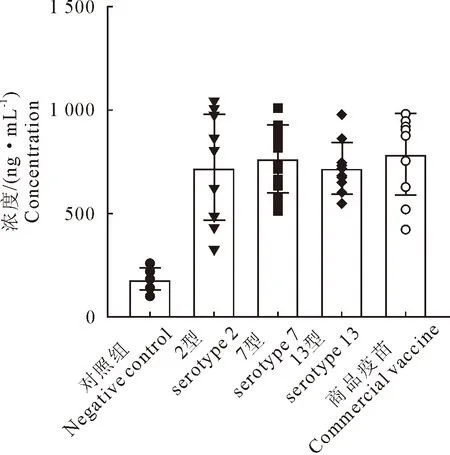
图5 二免后14 d仔猪免疫后抗体水平
3 讨论
近年来随着我国养猪业的发展,规模化猪场猪群受猪繁殖与呼吸综合征病毒、猪圆环病毒、伪狂犬病毒等病毒感染后,可以继发副猪嗜血杆菌病[9-13]。副猪嗜血杆菌是猪上呼吸道寄生细菌,在健康猪群中该细菌的分离率为0~51.6%,其中仔猪群的分离率高达22.6%[14]。副猪嗜血杆菌有15个血清型,不同血清型的致病力也不相同,其中1型、2型、3型、4型、5型、8型、10型、12型、13型、14型和15型的致病力较强,而6型、7型、9型和11型没有致病力[15]。副猪嗜血杆菌的流行病学调查显示,我国猪群中主要的流行血清型为4型、5型、12型、13型和14型[16]。本研究对我国黑龙江、江西和广东地区部分猪场的副猪嗜血杆菌疑似病猪进行副猪嗜血杆菌分离,从发病猪中分离得到19株副猪嗜血杆菌,其中2型2株、4型7株、5型1株、10型1株、12型3株、13型2株、15型1株及低毒力株7型2株。这为黑龙江、江西和广东地区副猪嗜血杆菌的防控提供了流行病学数据。
疫苗接种和抗生素是用于副猪嗜血杆菌感染的预防和控制手段,但是抗生素的长期使用使副猪嗜血杆菌的耐药性越来越强,疫苗接种成为该病防治最为有效的措施[17]。我国商品化副猪嗜血杆菌以灭活疫苗为主,主要包含血清型1型、4型、5型、12型和13型。副猪嗜血杆菌不同菌株和不同血清型之间仅有部分交叉保护或无交叉保护,这使得目前商品化的灭活疫苗保护效果较差,不能有效的控制猪场副猪嗜血杆菌的流行[18]。
本研究从黑龙江、江西、广东3个省12个发病猪场分离得到19株副猪嗜血杆菌,包括2型2株、4型7株、5型1株、7型2株、10型1株、12型3株、13型2株、15型1株,由于广东、黑龙江、江西副猪嗜血杆菌均有多种血清型流行,且我国的商品化副猪嗜血杆菌灭活疫苗以1、4、5、12、13型为主,故初步研究了副猪嗜血杆菌2、7、13型单价灭活疫苗。本次研制的副猪嗜血杆菌单价灭活疫苗免疫仔猪14 d后,血清中副猪嗜血杆菌抗体浓度达到700 ng/mL,对同血清型的副猪嗜血杆菌的免疫保护率达到100%。副猪嗜血杆菌单价灭活疫苗产生的抗体水平与商品苗的抗体水平之间没有显著差别,为副猪嗜血杆菌多联多价疫苗的研制奠定了基础。
