顶空-气相色谱法测定生活饮用水中三氯甲烷和四氯化碳的方法探讨
2022-08-09刘谨菲
刘谨菲
(山西省检验检测中心食品与粮食检验技术研究所,山西太原 030012)
氯化消毒技术成熟、效果较好、作用持久,是国内集中式供水最为常用的消毒方式。然而该方式在消毒过程中容易产生三氯甲烷、四氯化碳等不利于人体健康且有“三致”作用的消毒副产物[1-3]。GB 5749—2006[4]中将三氯甲烷、四氯化碳列为水质常规指标,规定其限值分别为0.060 mg/L 和0.002 mg/L;GB 5750.8—2006[5]中顶空毛细管柱气相色谱法则是当前检验检测机构测定饮用水中三氯甲烷和四氯化碳最为常用的方法。在日常检测中发现,配制标准使用液溶剂、配制标准系列用水、实验室环境以及配制标准系列方式等对顶空气相色谱检测结果的影响较大。本研究通过对相关检测条件进行优化,建立了顶空-气相色谱测定生活饮用水中三氯甲烷和四氯化碳的分析方法。
1 材料与方法
1.1 材料与试剂
市售预包装纯净水;甲醇中三氯甲烷溶液标准物质[编号GBW(E)080239-3,10.0 mg/L]、甲醇中四氯化碳溶液标准物质[编号GBW(E)080240-3,1.00 mg/L],均由中国计量科学院提供;甲醇,色谱纯,美国Fisher 试剂。
1.2 仪器与设备
6890N 气相色谱仪(配微电子捕获检测器μ-ECD)、7697A 顶空自动进样器,20 mL 钳口顶空瓶及瓶盖、10 μL、100 μL 微量进样针,均由美国Agilent 公司提供;5 mL 移液枪,德国Eppendorf 公司;Synergy 超纯水机,德国Milli-Q 公司;LT-VBX50真空干燥箱,立德泰勀(上海)科学仪器有限公司。
1.3 试验方法
1.3.1 标准溶液配制
(1)混合标准使用液。分别吸取0.25 mL 质量浓度为10.0 mg/L 的三氯甲烷标准溶液、1.25 mL 质量浓度为1.00 mg/L 的四氯化碳标准溶液于5 mL 容量瓶中,用甲醇稀释、定容至刻度,配制成三氯甲烷质量浓度为500 μg/L、四氯化碳质量浓度为250 μg/L的混合标准溶液。
(2)混合标准工作系列。取6 个20 mL 顶空瓶(超纯水清洗后于120 ℃烘箱中烘烤2 h,冷却至室温),用移液枪准确加入5 mL 超纯水(于通风橱中用电炉煮沸30 min 后冷却至室温),用微量进样针分别吸取2 μL、4 μL、10 μL、20 μL、40 μL 和100 μL 混合标准溶液,将针头伸入顶空瓶中水面下1 ~2 mm 处注入混合标准溶液,盖好、压紧顶空瓶盖,轻摇混匀,即配制成三氯甲烷质量浓度为0.2 μg/L、0.4 μg/L、1.0 μg/L、2.0 μg/L、4.0 μg/L 和10.0 μg/L,四氯化碳质量浓度为0.1 μg/L、0.2 μg/L、0.5 μg/L、1.0 μg/L、2.0 μg/L、5.0 μg/L 的混合标准工作系列。
1.3.2 水样处理分析
在100 mL 蓝盖试剂瓶(于120 ℃烘箱中烘烤2 h,冷却至室温)中加入0.3 ~0.5 g 抗坏血酸,取水样至满瓶,密封低温保存,24 h 内进行检测。
用移液枪准确吸取5 mL水样于20 mL顶空瓶中,盖好、压紧顶空瓶盖,上机测试。
1.4 仪器工作条件
(1)顶空条件。加热箱温度:40 ℃;定量环/阀温度:60 ℃;传输线温度:80 ℃;循环时间:6 min;平衡时间:60 min;压力平衡时间:0.1 min;进样时间:0.5 min;进样量:1 mL。
(2)色谱条件。色谱柱:DB-5MS(30 m×0.25 mm,0.25 μm);载气:高纯氮,流量为2.2 mL/min;柱温:60 ℃,保持4 min;进样口温度:215 ℃;进样方式:分流进样,分流比为100 ∶1;μ-ECD 温度:250 ℃;尾吹气:高纯氮,流量为60 mL/min;色谱峰保留时间定性,色谱峰面积定量。
2 结果与分析
2.1 配制标准使用液溶剂考察
按照1.3.1 中混合标准使用液配制方法,分别用甲醇和超纯水作为溶剂配制三氯甲烷和四氯化碳的混合标准使用液,再使用100 μL 微量进样针各吸取20 μL 混合标准使用液于装有5 mL 超纯水的顶空瓶中,盖好、压紧顶空瓶盖,在1.4 仪器工作条件下平行测定2 次,计算平均峰面积。由表1 可看出,以甲醇为溶剂配制的混合标准使用液经稀释配成标准溶液浓度点后,测得三氯甲烷和四氯化碳的峰面积均大于以超纯水为溶剂同样操作配制的标准溶液。这是由于两种目标组分在甲醇中的溶解度都远远大于其在水中的溶解度,从而减少了标准使用液配制过程中的挥发损失,使得试验结果更为准确可靠;同时标准使用液稳定性增加,可贮存更长时间,避免了频繁配制增加实验成本,也提升了检测效率。

表1 甲醇和超纯水作溶剂配制标准使用液比较
2.2 配制标准系列用水本底消除
按照1.3.2 中水样处理分析步骤,分别测定实验室超纯水、3 种品牌预包装纯净水、煮沸后放凉的超纯水中两种目标组分的含量,对比测得的本底值,考察配制标准系列用水的本底消除方式。
由表2 可知,实验室超纯水、某品牌饮用天然水、某品牌饮用纯净水以及某品牌蒸馏水都检测出两种目标物组分,存在本底干扰,煮沸后放凉的超纯水中未检测到目标组分,可以用作配制标准系列用水。由此可见,虽然各种知名品牌纯净水经过多道工序处理与净化,但仍然存在痕量或超痕量的消毒副产物残留,不能直接作为本试验配制标准系列用水,而实验室超纯水经煮沸30 min放凉后无本底值干扰。同时由于三氯甲烷和四氯化碳挥发性很强,为避免实验过程中的环境因素影响,超纯水的煮沸放凉过程应在通风橱中进行或通入氮气。
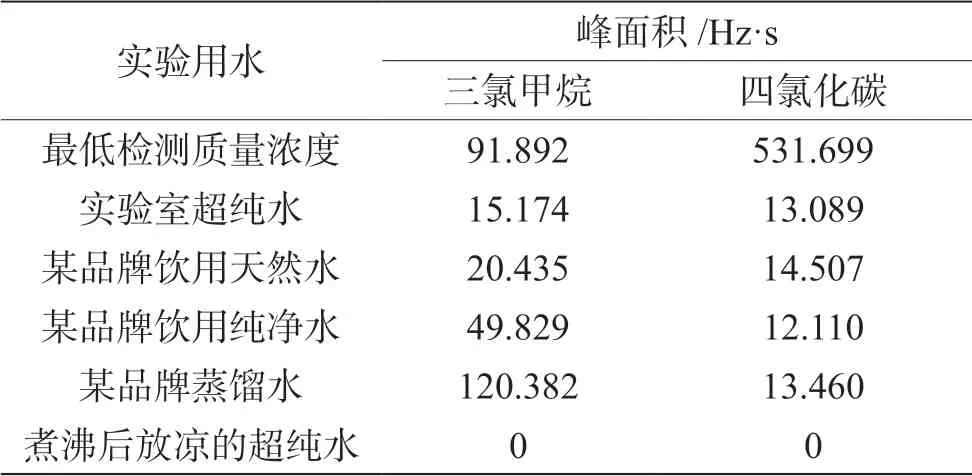
表2 配制标准系列用水的本底值测定结果
2.3 配制标准系列方式差异影响
按照GB 5750.8—2006 中的标准系列配制方式,三氯甲烷和四氯化碳的标准曲线线性较差,重现性低,原因在于三氯甲烷沸点为61 ~62 ℃,四氯化碳沸点为76.8 ℃,两者在水中的溶解度也较低,极易在配制、转移过程中因挥发而影响实验测定结果。本研究比较了在5 mL 容量瓶中加入标准溶液配制标准系列再转移至顶空瓶,以及直接在预装5 mL 实验用水的顶空瓶中液面上方与下方加入标准溶液3 种不同配标方式的差异。
由表3 可看出,在容量瓶中配标再转移至顶空瓶中的方式,两个目标物标准曲线线性最差,色谱峰面积也较小;在顶空瓶中液面上方加标的方式次之,这是由于加入的标准溶液浓度较高,使用微量进样针打入顶空瓶瞬间也会有部分挥发;当进样针伸入顶空瓶中试验用水液面下1 ~2 cm 注入标准溶液时,两个目标物的线性均达到0.999 以上。注入的混合标准溶液体积较小,对20 mL 顶空瓶的横截面积影响不大,因此可忽略加入标准溶液的体积影响。
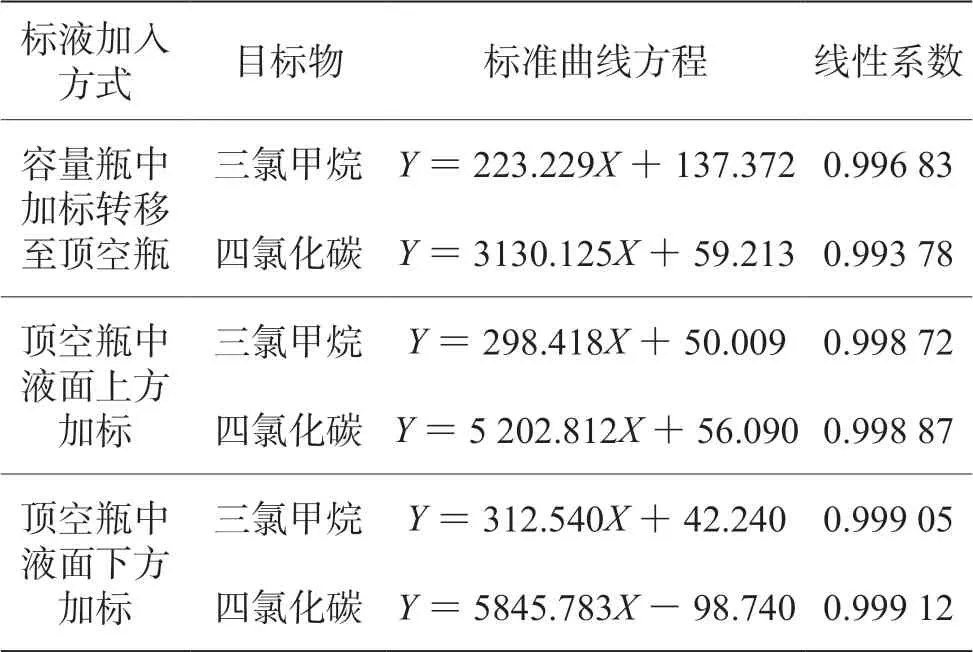
表3 标准溶液配制方式对标准曲线的影响
2.4 方法的最低检测质量浓度
最低检测质量浓度即为方法的测定下限,按照3倍仪器噪声(S/N=3)计算方法检出限,10 倍仪器噪声(S/N=10)计算方法的最低检测质量浓度,三氯甲烷和四氯化碳的最低检测质量浓度分别为0.2 μg/L、0.1 μg/L。
2.5 方法的加标回收率与精密度
选用在通风橱中煮沸30 min 后放凉的实验室超纯水进行加标试验,结合方法线性范围与生活饮用水中三氯甲烷和四氯化碳的浓度范围,分别向试验用水中加入低、中、高3 个浓度水平的混合标准溶液进行6 次平行测定,计算方法的回收率与精密度。由表4可知,三氯甲烷的平均回收率为90.60%~98.31%,RSD 为0.98%~2.67%,四氯化碳的平均回收率为94.50%~99.57%,RSD 为1.05%~2.12%,均符合相关标准的规定。
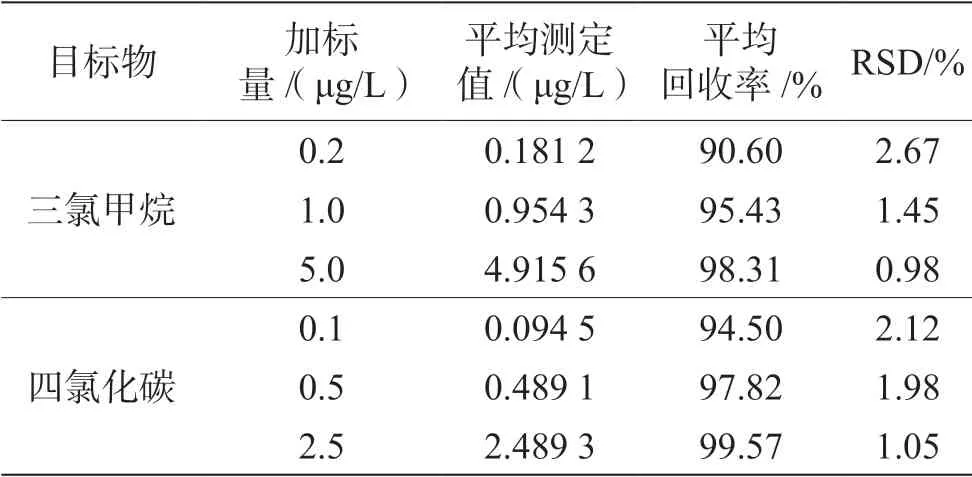
表4 三氯甲烷和四氯化碳的回收率与精密度
3 结论
本研究通过对配制标准使用液溶剂、配制标准系列用水及配制标准系列方式的优化,建立了顶空-气相色谱法测定生活饮用水中三氯甲烷和四氯化碳的分析方法。结果表明,采用甲醇(色谱纯)配制标准使用液,煮沸30 min 后放凉的超纯水作配制标准系列用水,在顶空瓶中液面下方加标的配标方式,三氯甲烷和四氯化碳的线性范围、最低检测质量浓度、加标回收率与精密度均满足相关标准要求,可满足生活饮用水中三氯甲烷和四氯化碳的日常检测需求。
