硫酸盐类型对杨木燃料乙醇蒸馏废水厌氧消化特性的影响
2022-08-05邓萍萍闫晓帆刘瑞霞丁婷婷陈介南吴志平
邓萍萍,闫晓帆,刘瑞霞,丁婷婷,陈介南,吴志平
(中南林业科技大学 材料科学与工程学院,湖南 长沙 410004)
1 实验部分
1.1 试剂与仪器
杨木燃料乙醇蒸馏废水,是实验室通过预处理糖化发酵制备燃料乙醇蒸馏出来的残液,冷藏4 ℃冰箱中备用;接种物(污泥),取自学校环境研究所的污水处理池,在(35±1)℃密封驯化20 d后所得;硫酸钠、硫酸亚铁、硫酸铁皆是分析纯。实验材料的理化性质见表1。
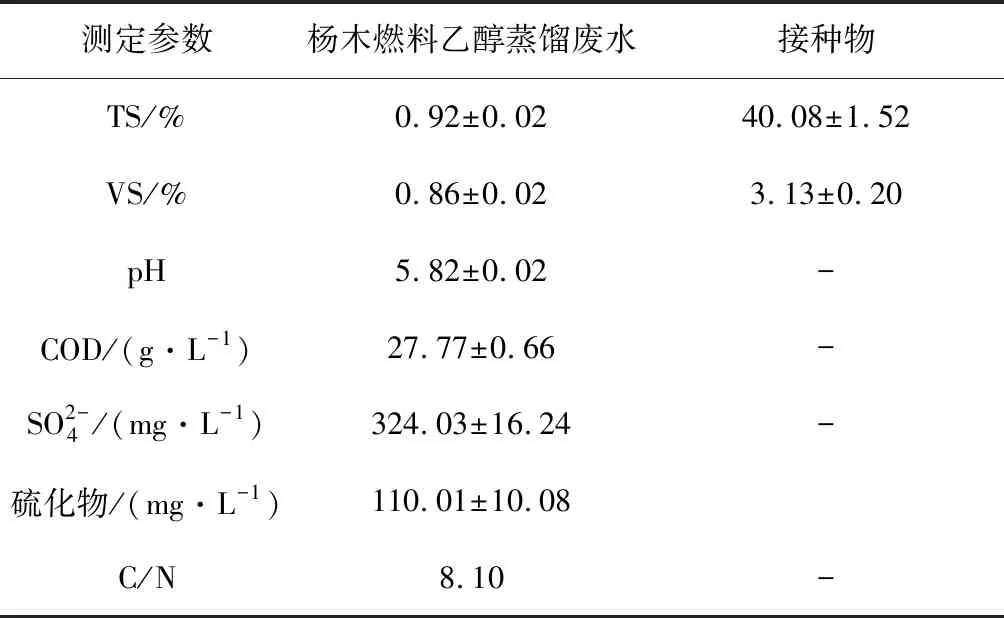
表1 实验材料基本性质
DZKW-4恒温水浴锅;雷磁pHS-3E型pH计;连华科技COD消解仪;岛津LC-20A型液相色谱仪;安捷伦7890 B气相色谱仪;UV-5100紫外-可见光分光光度计;Liqui TOCⅡ总有机碳分析仪;K1100凯氏定氮仪。
1.2 实验方法

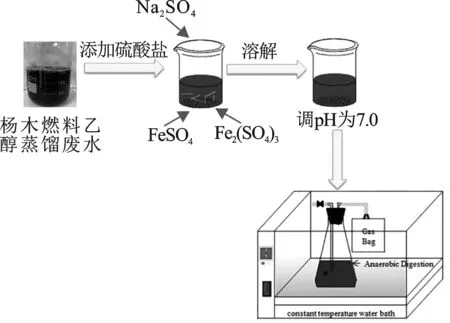
图1 不同类型硫酸盐废水厌氧消化装置Fig.1 Anaerobic digestion equipment of different types of sulphates wastewater

表2 实验设计
1.3 分析方法
1.3.1 水质分析 根据GB 11901—89重量法测定杨木燃料乙醇蒸馏废水和接种物的TS,采用灼烧法和GB 11901—89测定废水和接种物的VS;根据HJ 84—2016铬酸钡分光光度法测定废水的硫酸盐浓度;根据HJ 501—2009燃烧氧化-非分散红外吸收法测定废水的总有机碳含量;根据HJ 636—2012碱性过硫酸钾消解紫外分光光度法测定废水的总氮含量;根据 HJ 60—2000 碘量法测定废水的硫化物含量。
1.3.2 液相成分及气相成分测定 取出的发酵液以10 000 r/min离心15 min,上清液用以测定液相成分(pH、COD及VFAs)。采用pH计测定pH值;采用连华科技COD消解仪测定COD值;通过LC-20A液相色谱仪测定微生物代谢产生的挥发性脂肪酸(VFAs)含量。色谱条件为C18色谱柱,流动相为乙腈∶0.1%磷酸=5∶95,柱温为30 ℃,紫外波长为210 nm,挥发性脂肪酸的浓度和组成用外标法测定,每个标准样品的保留时间用乙酸、丙酸和丁酸测定。制备乙酸、丙酸和丁酸的混合标准溶液,并用超纯水稀释至几种不同浓度。将混合溶液的保留时间与单一样品的保留时间进行比较,根据已知标准样品的浓度计算发酵液乙酸、丙酸和丁酸的含量,用6 mol/L 硫酸溶液调节上清液pH值为2.0,上清液通过0.45 μm滤膜,取10 μL滤液进行测定。
厌氧发酵过程中的每日产气量采用排水法测量。气体的主要成分是氢气、氮气、甲烷和二氧化碳。气相组分采用外部标准方法测定气体成分和含量,通过GC-7890 B五阀八柱三通道快速炼厂气分析系统测定。色谱条件为:程序升温(60 ℃,保持1 min,然后以20 ℃/min升至80 ℃,再以25 ℃/min升至190 ℃,保持0.3 min),进样口(温度为250 ℃,压力为9.994 9 psi,总流量为145 mL/min,隔垫吹扫为3 mL/min,分流比为70 ∶1),FID检测器(温度为250 ℃,空气流量为350 mL/min,氢气流量为40 mL/min,尾吹气氮气流量为27 mL/min),TCD2、TCD3检测器(温度为250 ℃,参比流量为45 mL/min,尾吹气流量为2 mL/min)[6]。
将累积产甲烷量实验数据拟合到修正的Gompertz方程中(式1)[7],产甲烷速率通过对修正的Gompertz方程进行微分得到(式2)[8],当V达到Rm时,由式(2)得到Tmax的方程(式3)。参数Pm、Rm、t和λ采用Curve Expert 1.4 版软件确定,实验数据和拟合曲线使用origin软件8.5(origin software,Inc,USA)绘制。
(1)
(2)
(3)
式中P(t)——反应时间t(d)内的累计产甲烷量,mL/gVS;
Pm——最大产甲烷量,mL/gVS;
Rm——最大产甲烷率,mL/gVS·d;
λ——产甲烷滞后时间,d;
e——常数,2.718;
Tmax——最大产甲烷速率时的时间,d。
2 结果与讨论
2.1 硫酸盐类型对杨木燃料乙醇蒸馏废水的产甲烷性能的影响
图2为硫酸盐类型对杨木燃料乙醇废水厌氧消化产甲烷的影响。通过Gompertz模型拟合得出,添加Fe2(SO4)3、FeSO4、Na2SO4实验组拟合值R2分别是0.996 1,0.991 6,0.995 3,说明曲线与实测值拟合效果好。
由图2(A)可知,添加Fe2(SO4)3实验组累计甲烷产量为543.0 mL/gVS,比添加FeSO4和Na2SO4实验组分别高29.72%,35.82%,添加FeSO4比Na2SO4实验组高4.70%,说明含铁硫酸盐可以改善产甲烷性能,原因是添加含铁离子可以促进厌氧消化反应器中微生物之间的电子传递,加速电子传递效率[9-10]。在0~8 d厌氧消化反应过程中,添加Fe2(SO4)3比FeSO4实验组的累计产甲烷量低,原因是过量的三价铁离子可作为电子与MPA竞争电子,从而影响厌氧体系中电子的再分配过程,弱化产甲烷菌活性[11]。在8~18 d,添加Fe2(SO4)3比FeSO4实验组的累计产甲烷量高,原因是部分Fe3+还原为Fe2+,Fe2+能够与硫酸盐还原产生的S2-形成沉淀物,从而抑制H2S的产生,使得产甲烷菌能够有效利用底物,另一部分Fe3+可以促进厌氧消化反应器中微生物之间的电子传递,加速电子传递效率,改善产甲烷性能[10,12]。
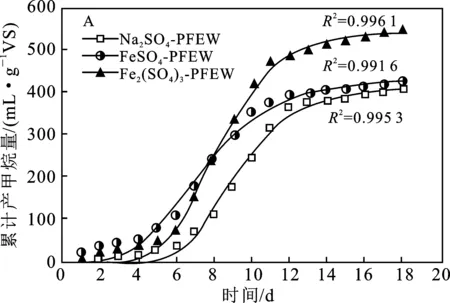

图2 硫酸盐类型对厌氧消化累计产甲烷量的影响(A),对产甲烷速率的影响(B)Fig.2 Effect of sulfate types on the cumulative methane production of anaerobic digestion (A),the rate of methane production of anaerobic digestion (B)
由图2(B)可知,添加Fe2(SO4)3、FeSO4、Na2SO4各实验组产甲烷最大速率分别是98.79,64.35,70.02 mL/gVS·d,厌氧微生物中的产甲烷菌对铁的需求量较高,提高铁的生物利用性,能够显著提高厌氧产甲烷菌活性[13]。添加FeSO4的最大产甲烷速率出现的时间最早但值最小,出现最大产甲烷速率时间最早的原因是Fe2+会提高水解酸化酶活性[14],能快速有效的降解有机质,这与COD含量变化相符合;产甲烷速率最小原因是SRB活性最强,这与硫酸盐去除率相符合,因此发酵体系中SRB与MPA竞争底物能力更强,导致厌氧消化产甲烷速率减小[15]。
2.2 硫酸盐类型对VFAs含量和pH的影响
硫酸盐类型对杨木燃料乙醇蒸馏废水的VFAs含量的影响见图3(A)。
由图3(A)可知,各实验组前6 d厌氧消化以乙酸含量为主,前4 d不同类型硫酸盐实验组乙酸含量相差不大,但在第6 d各组乙酸含量相差较大,添加Fe2(SO4)3、FeSO4、Na2SO4实验组乙酸含量分别是2.302 5,1.027 9,1.900 0 g/L,表明添加Fe2(SO4)3为厌氧微生物提供丰富的营养基质,从而增强产甲烷菌在微生物菌群的活跃度。在8~18 d厌氧消化过程中,添加Fe2(SO4)3类型的厌氧消化过程中VFAs含量最高,说明Fe2(SO4)3能有效提高酸化过程,提高乙酸含量,这是由于在酸化过程中,Fe3+可以富集异化铁还原菌,该类细菌可以通过异化铁还原过程参与到复杂有机物的降解过程中,转化为更多酸类物质,为产甲烷菌提供了良好的底物[16]。


图3 硫酸盐类型对VFAs含量的影响(A),厌氧发酵体系pH变化(B)Fig.3 Effect of sulfate types on the content of VFAs (A) and the pH change of anaerobic digestion (B)
pH值是反映厌氧消化稳定运行的重要指标,反映厌氧微生物的生存环境[17]。各实验组pH值随时间变化趋势见图3(B)。
由图3(B)可知,各实验组pH值先上升,随后下降,再缓慢升高,最后趋向于平衡过程。pH值下降的原因是厌氧消化过程中水解酸化速率大于产甲烷速率。添加Fe2(SO4)3实验组厌氧消化过程中pH值只有一个阶段下降,而添加Na2SO4实验组厌氧消化过程中pH值有2个阶段下降,原因是Fe2(SO4)3的添加,使微生物、底物和Fe3+三者的接触几率变大,加快反应器中微生物对有机物的消耗,进而加快反应器达到稳定状态[18]。
2.3 硫酸盐类型对厌氧消化COD去除的影响
COD是影响厌氧消化过程的关键参数,图4(A)显示厌氧消化过程中反应器COD含量的变化过程。


图4 COD含量随厌氧消化过程的变化(A),硫酸盐类型对COD去除率的影响(B)Fig.4 COD content changes with anaerobic digestion process (A),the effect of sulfate types on COD removal rate (B)
由图4(A)可知,各实验组COD含量先快速下降,再升高,再下降,最后趋于稳定,厌氧消化结束后,添加Fe2(SO4)3、FeSO4、Na2SO4各实验组COD含量分别是0.5,0.42,0.60 g/L。当厌氧发酵4~6 d 时,COD含量升高,原因是水解酸化速率大于产甲烷速率,导致体系中存在大量的小分子物质。图4(B)是硫酸盐类型对COD去除率的影响。
由图4(B)可知,添加Fe2(SO4)3、FeSO4、Na2SO4的实验组COD去除率分别是97.74%,98.11%,97.30%,COD去除率没有显著差异,原因是反应结束后COD作为碳源(<0.6 g/L)已被消耗完[19]。添加Fe2(SO4)3、FeSO4比Na2SO4实验组的COD去除率略高。有研究表明,Fe3+的添加有助于促进厌氧消化系统中蛋白酶和葡萄糖苷酶的活性,加速了蛋白质和碳水化合物的分解,从而加快COD的去除[20],而添加FeSO4对COD去除率效果更好,这是由于Fe2+存在会提高水解酸化酶的活性[14],使得有机物降解得更彻底。
2.4 硫元素平衡分析
硫酸盐类型对杨木燃料乙醇蒸馏废水厌氧消化结束后硫酸盐含量的影响见图5(A)。
由图5(A)可知,添加Fe2(SO4)3、FeSO4、Na2SO4各实验组厌氧消化结束后,硫酸根含量分别是0.099,0.041,0.066 g/L,硫酸根含量均<0.1 g/L,达到排放标准,添加Fe2(SO4)3实验组硫酸盐去除率最低,原因是发酵液中含有一定量游离的Fe3+会对硫酸盐还原过程中的关键酶——亚硫酸盐还原酶活性产生明显抑制,导致硫酸盐还原过程受影响[21]。图5(B)显示厌氧消化结束后沼液中硫化物的含量。

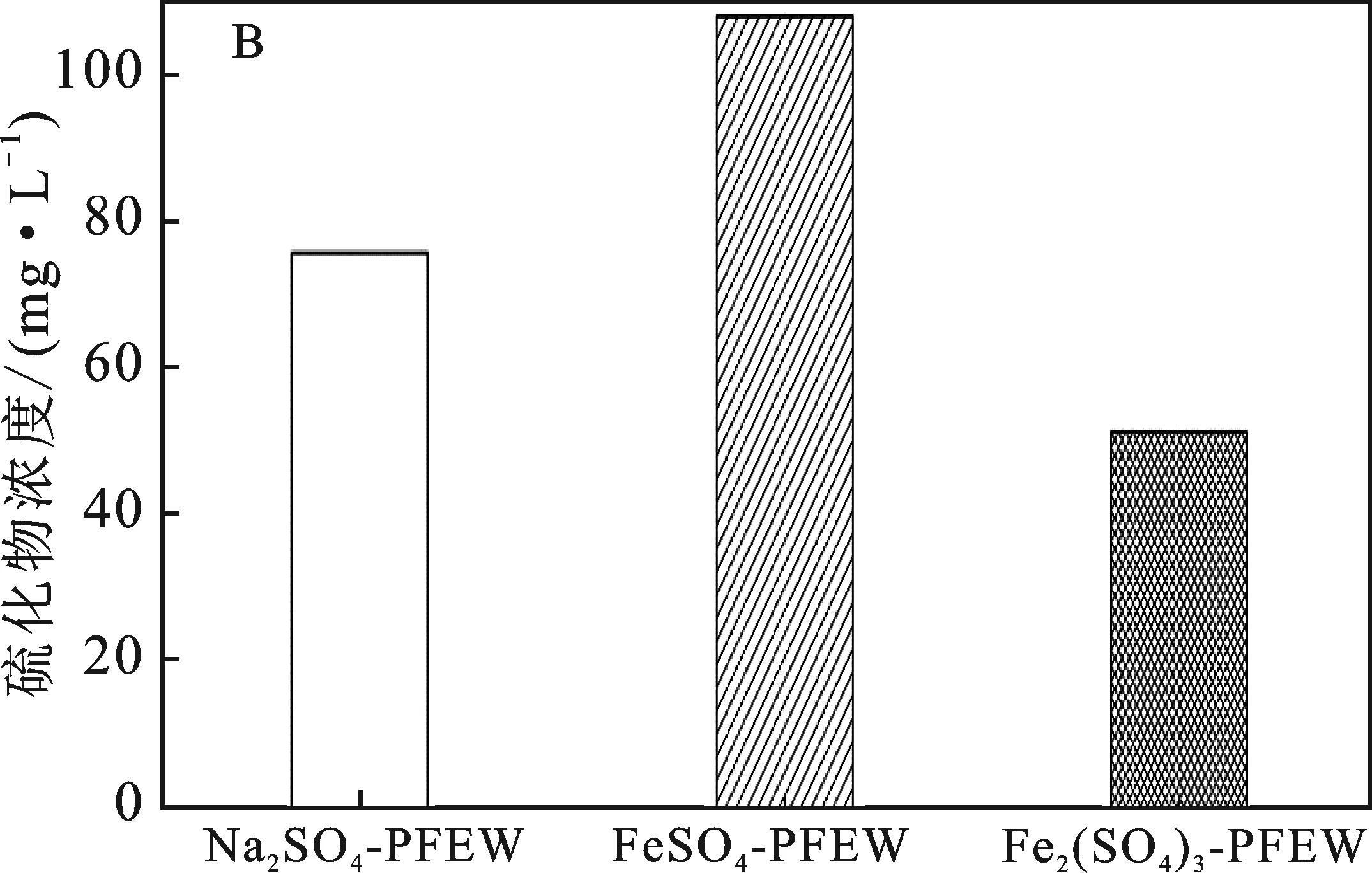
图5 硫酸盐含量厌氧消化结束前后变化(A),厌氧消化结束后沼液中硫化物浓度(B)Fig.5 The change of sulfate content before and the end of anaerobic digestion (A) and the concentration of sulfide in the biogas slurry at the end of anaerobic digestion (B)
由图5(B)可知,由于厌氧消化过程pH为7.0~8.2,不利于H2S气体的排出,因此在气相中未检测出H2S物质,产生的硫化物主要以HS-和S2-的形式存在,它们对厌氧微生物的毒性较低,不会抑制产甲烷过程。理论上硫酸盐还原菌还原的硫酸盐含量应等于液相中硫化物的含量和气相中硫化氢的量之和。添加Fe2(SO4)3、FeSO4、Na2SO4各实验组厌氧消化结束后,液相硫化物含量分别是51.40,107.56,75.53 mg/L,皆低于硫酸盐还原过程理论产生的硫化物量,一方面是微生物自身代谢作用消耗部分硫酸盐,将硫酸盐还原成不溶性硫化物;另一方面是微生物具有吸附作用,活性污泥吸附 S元素[22]。添加Fe2(SO4)3实验组液相中硫化物含量最少,这是由于添加Fe2(SO4)3促进S元素的成矿作用,对固定发酵液中的硫化物有重要影响[23-24]。
3 结论
(1)添加Fe2(SO4)3的杨木燃料乙醇蒸馏废水厌氧消化产甲烷量最高,比添加FeSO4和Na2SO4分别提高了29.72%和35.82%;添加Fe2(SO4)3的VFAs含量最高,Fe3+可以富集异化铁还原菌,能够提高乙酸含量,为产甲烷菌提供更多基质,增强甲烷菌活性。