ECMO联合应用期间CRRT非计划性下机的预测模型构建
2022-07-13万娜于洋王淑芹张春艳张小建袁庆伶贾燕瑞
万娜,于洋,王淑芹,张春艳,张小建,袁庆伶,贾燕瑞
体外膜肺氧合治疗(Extracorporeal Membrane Oxygenation, ECMO)作为一种有效的心肺支持手段,已广泛应用于心肺衰竭患者救治。ECMO 期间易发生急性肾损伤和容量超负荷[1],连续性肾脏替代治疗(Continuous Renal Replacement Therapy,CRRT)能最大限度地模拟肾脏对水和溶质的清除模式,持续、大量、缓慢地清除体内水和溶质,稳定内环境和减轻肺水肿[2],ECMO联合CRRT治疗作为救治危重患者的新手段安全有效,但其联合应用期间的治疗管理经验尚处于探索阶段。CRRT治疗中由于各种原因导致的非计划性下机会使治疗终止,不仅影响危重患者的治疗效果,与ECMO联合进行CRRT管路的连接操作复杂,反复进行CRRT上下机增加患者发生导管相关血流感染的概率及护理人员工作量[3]。如何减少CRRT非计划性下机,保障ECMO联合CRRT治疗的顺畅进行是管理重点及难点。有关CRRT非计划性下机已有较多相关报道[4-6],但ECMO联合应用期间发生的CRRT非计划性下机有哪些影响因素需进一步深入探讨。本研究对ECMO联合应用期间CRRT非计划性下机的影响因素进行分析,建立预测模型并评估其效能,以期对ECMO联合CRRT患者进行有效管理提供依据。
1 对象与方法
1.1对象 采用连续入组方便取样的方法,选择2017年7月至2021年7月在北京市某三级甲等医院呼吸重症监护病房行ECMO联合CRRT治疗的患者为研究对象。纳入标准:年龄>18周岁;接受ECMO联合CRRT治疗;CRRT治疗模式为连续性静脉-静脉血液滤过(Continuous Veno-venous Hemofiltration,CVVH)。排除临床资料不完善者。本研究所有研究对象或家属均知情同意,愿意参与本研究。本研究经医院伦理委员会批准(伦理号:2017-科-129)。共纳入患者45例,男33例,女12例;年龄23~72岁,中位年龄53(41,66)岁。其中重症肺炎呼吸衰竭38例,绒毛膜癌肺转移1例,多发伤1例,重症心力衰竭5例。
1.2方法
1.2.1ECMO联合CRRT实施方案 ECMO联合CRRT的连接方式多样,本组患者均采用CRRT管路与ECMO管路并联的方式,利用ECMO管路预留接口作为CRRT的引血端及回血端,连接口的选择遵循体外膜式氧合治疗成人重症呼吸衰竭推荐意见[7]中建议的膜肺后引血膜肺前回血的连接方式。ECMO装置采用德国迈柯唯公司的Rotaflow或Cardiohelp,均采用微创穿刺进行体内置管留置,治疗模式根据患者疾病类型选择静脉-静脉体外膜肺氧合(VV-ECMO)或静脉-动脉体外膜肺氧合(VA-ECMO),血泵转速为1 510~5 370 RPM,血流量为1.43~6.39 L/min。CRRT采用瑞典金宝Prismaflex 或德国费森Multifiltrate及其配套装置,治疗模式为CVVH(连续性静-静脉血液滤过),置换液采用青山利康公司生产的血液滤过置换基础液,根据患者检验结果进行电解质添加,置换液速度为2 000 mL/h,临床上依据患者病情、生命体征、凝血情况确定CRRT上机时间、频次、是否应用抗凝剂及类型、置换液稀释方式、血泵及脱水速度,给予个体化治疗方案。
1.2.2ECMO联合应用期间CRRT非计划性下机的指征 对未完成CRRT治疗目标或未达到CRRT计划时间而终止治疗的界定为CRRT非计划性下机,反之称为CRRT计划性下机[8]。查阅文献结合临床确定ECMO联合应用期间CRRT非计划性下机的标准:以滤器凝血 Ⅱ 级或以上、压力上升速度明显,机器提示管路凝血,各种报警不能排除导致下机为标准。滤器凝血以《血液净化治疗标准手册》[9]Ⅲ 级凝血为标准:0级,无凝血或数条纤维凝血;Ⅰ 级,<10%纤维凝血;Ⅱ 级,<50%纤维凝血;Ⅲ 级,>50%纤维凝血。
1.2.3资料收集方法 在参照相关文献[2-5,10]并咨询重症医学、护理学专家的基础上制订ECMO联合CRRT资料收集表。记录项目包括患者一般资料、ICU住院时间、ECMO联合应用期间CRRT运行总时间及例次、ECMO治疗模式及血流速度、CRRT血流速度及脱水速度、抗凝方式、稀释方式、CRRT机型、治疗时长、血常规、血气分析、感染及凝血指标、下机原因、是否使用血制品等。其中检验指标为每次治疗前的测量值,包括红细胞计数、血红蛋白、红细胞压积、血小板、活化部分凝血活酶时间、凝血酶原时间、国际标准化比值、降钙素原、血气分析中的pH值、游离钙离子及乳酸水平。由经科室资质授权的ECMO护士实施ECMO联合CRRT监测与护理,并据实填写ECMO联合CRRT资料收集表。资料收集完成后由经培训的研究小组成员进行复核,确认无误后行计算机录入。
1.2.4统计学方法 采用SPSS22.0软件进行统计分析,计数资料用频数及百分比表示,计量资料用均数±标准差或中位数与四分位间距表示,采用独立样本t检验、Mann-WhitneyU检验、χ2检验。采用logistic回归方程构建预测模型,运用ROC曲线下面积检验模型预测效果,采用Hosmer-Leme show检验对模型一致性进行评判。检验水准α=0.05。
2 结果
2.1ECMO联合应用期间CRRT治疗完成情况 45例患者完成ECMO联合CRRT治疗343例次。因达到治疗目的或治疗时间CRRT下机92例次(26.8%);因患者放弃治疗、死亡下机11例次(3.2%);因撤除ECMO、更换膜肺、外出CT检查等治疗相关因素下机22例次(6.4%);因滤器凝血Ⅱ级或以上、机器提示管路凝血及各种报警不能排除导致的非计划性下机218例次(63.6%)。218例次中无明确诱因212例次,运行时间19.0(12.0,29.0)h,≤24 h内下机的占57.1%;有明确诱因6例次,包括血滤机故障被迫下机2例次,滤器破膜1例次,ECMO膜肺血栓导致血滤机血泵多次停转下机3例次。
2.2ECMO联合应用期间CRRT非计划性下机的单因素分析 见表1。
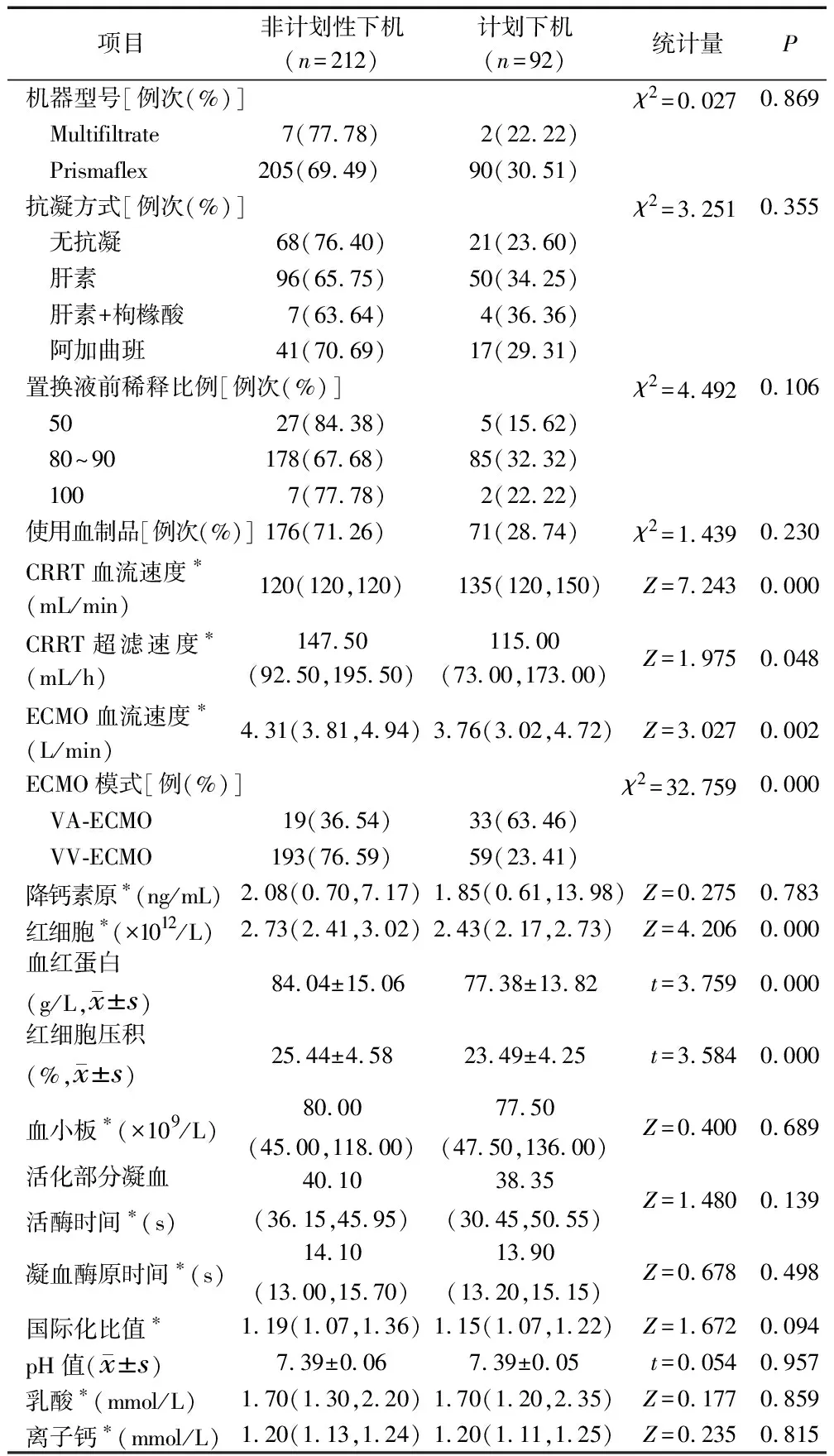
表1 ECMO联合应用期间CRRT非计划性下机的单因素分析
2.3ECMO联合应用期间CRRT非计划性下机的多因素分析 以是否发生非计划性下机为因变量(否=0,是=1),单因素分析有统计学意义的因素为自变量行多因素logistic回归分析,结果见表2。

表2 ECMO联合应用期间CRRT非计划下机的logistic回归分析
2.4预测模型及效果评价 ECMO联合应用期间CRRT非计划性下机的风险因素计算公式为:Logit(P)=7.599-0.079×CRRT血流速度+0.534×ECMO血流速度+1.561×ECMO模式,根据预测模型计算绘制ROC曲线(见图1),最终得到ROC曲线下面积为0.812,95%CI(0.754,0.869),约登指数最大值为0.521,最佳诊断值为0.694,灵敏度为0.825,特异度为0.696。该预测模型使用Hosmer-Leme show检验,χ2=10.113,P=0.257,拟合度较好。

图1 预测ECMO联合应用期间CRRT非计划性下机的ROC曲线
3 讨论
3.1构建ECMO联合应用期间CRRT非计划性下机预测模型的临床意义 ECMO联合CRRT的主要技术难点是连接方式的选择、抗凝药物的调整和管路相关并发症的监测与处理[11]。国外相关研究就ECMO联合CRRT的开始时机、不同连接方式的对比及抗凝剂的选择进行了有益的探索[12-14],国内相关文章多为经验性总结,缺乏高质量的数据支持[2]。本研究采用前瞻性队列研究的形式观察分析ECMO联合应用期间CRRT非计划性下机的影响因素并构建预测模型,为临床早期预警识别CRRT非计划性下机高危患者,减少ECMO联合CRRT治疗期间管路相关不良事件提供了一定数据支撑。本预测模型将ECMO联合应用期间CRRT非计划性下机风险因素直观的展现在公式中,针对现存风险因素进行积极干预,如适当调整ECMO血流速度及CRRT血流速度,有利于减少ECMO联合应用期间CRRT非计划性下机发生,提高医疗资源利用率,减轻家属负担及医务人员工作量。
3.2ECMO联合应用期间CRRT非计划性下机影响因素分析
3.2.1CRRT血流速度 本研究发现,ECMO联合应用期间CRRT血流速度是CRRT非计划性下机的保护因素,CRRT血流速度越快越不容易发生非计划性下机,与单独行CRRT治疗的多项研究结果一致[4,8]。本研究中计划下机组血流速度中位数为135 mL/min,非计划性下机组为120 mL/min,两组比较,差异有统计学意义(P<0.01)。单独行CRRT 治疗时最佳血流速度推荐为150~200 mL/min[15],本研究中两组血流速度均低于推荐值,虽然充足的血流量是CRRT顺利实施的保障,但ECMO联合CRRT治疗患者病情危重,CRRT血流速设定要依据患者血流动力学、ECMO运行情况及抗凝方式的选择等多方面因素考虑综合确定。
3.2.2ECMO血流速度 ECMO血流速度是ECMO联合应用期间CRRT非计划性下机的风险因素,ECMO血流速度越快越易发生CRRT非计划性下机,这与Pelenc等[16]研究结果一致。ECMO的高流速会使CRRT各压力阈值超范围,易导致CRRT压力紊乱,反复停机从而影响运行效率,甚至出现极端情况破膜发生[17]。本研究中也出现1例次因管路压力过高导致滤器破膜下机。单独行CRRT治疗时常根据滤器前压(PFP)、跨膜压(TMP)及静脉压(PV)数值判断管路凝血[18],ECMO并联后CRRT压力参数并不能真正反映管路凝血情况,需更关注压力上升趋势,如压力上升明显,机器提示管路凝血及时下机,避免滤器或静脉壶完全阻塞无法回血造成血液丢失。针对如何减少ECMO血流速度对CRRT管路压力影响可借鉴文献经验选择相应方法。许程飞等[19]通过旋转ECMO与CRRT连接处三通,降低血液流经三通时流速,使三通起到限流作用,降低ECMO血流速度对CRRT引血压力影响。陈丽花等[20]通过选用可正负压调节CRRT机器,使用正压控制模式避免CRRT高压报警。有学者研究显示,在CRRT引血端、回血端使用额外的压力控制线可提高CRRT管路寿命[21]。
3.2.3ECMO模式 本研究结果显示,VV-ECMO模式下CRRT非计划性下机发生率是VA-ECMO模式的4.764倍,与Na等[21]研究结果一致,其研究发现ECMO联合应用期间CRRT管路72 h内更换概率VV-ECMO模式是VA-ECMO模式的1.33倍。考虑可能与ECMO模式不同的适用人群特点有关。VV-ECMO模式主要针对呼吸衰竭患者,支持力度高且运行时间长,而VA模式主要针对心脏衰竭患者,支持力度相对低且运行时间短。支持力度、运行时间等不同可能对CRRT运行产生影响,后期需要进一步研究加以证实,本研究结果提示医务人员在VV-ECMO模式下更应关注CRRT运行情况。
3.3ECMO联合应用期间CRRT非计划性下机预测模型的预测效能较好 本研究采用Hosmer-Lemeshow评价模型的拟合优度.验证结果显示差异无统计学意义,说明该模型预测结果与实际发生率吻合度较高。当ROC曲线下面积为0.5~0.7时,表示预测效果低;当曲线下面积为0.7~0.9时,表示预测效果中等;当曲线下面积>0.9时,表示预测效果好[22]。本研究模型的ROC曲线下面积为0.812,约登指数最大值为0.521,最佳诊断值为0.694,灵敏度为0.825,特异度为0.696,证明该模型预测和鉴别ECMO联合应用期间CRRT非计划性下机的效果良好。当预测模型评分≥0.694分时,表明患者极可能发生CRRT非计划性下机,应引起医护人员的重视,必要时进行治疗参数调整;当评分接近临界值时,医护人员也应提高警惕,根据患者病情制订前瞻性干预方案,最大限度地避免CRRT非计划性下机的发生。
4 小结
本研究通过收集ECMO联合CRRT治疗患者住院期间相关数据构建ECMO联合应用期间CRRT非计划性下机预测模型,该模型具有较好的预测性能,为临床医护人员早期识别CRRT非计划性下机高危患者提供了便捷的筛查工具。但本研究为单中心研究,且缺乏外部验证,未来需要进行多中心、更大样本的前瞻性队列研究,以完善模型预测效能。此外,相关研究显示ECMO联合CRRT的不同连接方式对CRRT的运行有明显影响,本研究并未采取多种连接方式,未来可在不同的中心采取不同的ECMO联合CRRT连接方式,评估不同连接方式对CRRT非计划性下机的影响,构建更完善的预测模型。
