Fe2O3修饰CaSO4/Ben载氧体化学链燃烧反应特性
2022-07-06穆丽颖肖慧霞张志丰蔡志阳王亦飞于广锁
穆丽颖, 肖慧霞, 张志丰, 蔡志阳, 王亦飞, 于广锁
( 华东理工大学资源与环境工程学院,上海市煤气化工程技术研究中心,上海 200237)
化学链燃烧(Chemical Looping Combustion,CLC)是一种具有CO2内分离特性的高效无火焰燃烧技术,是减少化石燃料CO2排放的有效方法之一[1]。CLC技术中载氧体在两个相互连通的燃料反应器和空气反应器之间循环[2],或在单个流化床内间歇运行循环[3]。载氧体在燃料反应器中为燃料供氧,随后进入空气反应器中氧化再生[4],如此循环以避免燃料与空气直接接触,提高尾气中CO2的富集程度,并抑制NOx的生成,从而降低CO2捕集成本。
寻找具有载氧量高、热稳定性能好、氧化还原反应性高和价廉易得、环境友好的载氧体是发展CLC技术的关键[5]。CaSO4因载氧量高、成本低和环境友好被广泛关注,但应用时存在机械强度弱、反应活性差等问题[6]。研究表明,可通过添加惰性载体提高载氧体的机械强度,增加使用周期。惰性载体如膨润土(Ben)[7]、海泡石[8]、Al2O3[9]、SiO2[10]等,其中膨润土的添加能够明显提高CaSO4载氧体的机械强度[7];引入活性组分如Fe2O3[11]、CuO[12]、CoO[13]和Mn2O3[14]可在一定程度上提高钙基载氧体的反应活性,其中Fe2O3修饰效果最佳。Fe2O3不仅是促进煤气化动力学的活性组分,而且对CaSO4载氧体的还原反应具有催化作用[15]。但有关Fe2O3对添加惰性载体的CaSO4载氧体的催化作用和机理研究得较少。
本文在已添加Ben的CaSO4/Ben载氧体的基础上,添加活性助剂Fe2O3制备了系列复合载氧体。在间歇式流化床反应器中进行循环实验,评估Fe2O3修饰CaSO4/Ben载氧体的反应活性和稳定性;利用热重分析仪测试反应活化能,从而验证Fe2O3对CaSO4/Ben与CO反应的催化作用,为改善CaSO4/Ben载氧体性能提供了一种可行方法。
1 实验部分
1.1 药品与仪器
硫酸钙(CaSO4·2H2O),w≥99%,上海麦克林生化科技有限公司;膨润土(Al2O3·4SiO2·H2O),w≥99%,上海阿拉丁生化科技有限公司;硝酸铁(Fe(NO3)3·9H2O),w≥99%,上海润捷化学有限公司。磁力搅拌器,上海司乐仪器有限公司,B11-1型;电热恒温鼓风干燥箱,上海精宏实验设备有限公司,DHG-9140A型;手动粉末压片机,上海精胜仪器公司,JSP-24S型;马弗炉,德国Nabertherm公司,P330型;热重分析仪(TGA),德国NETZSCH公司,STA2500 Regulus型;
1.2 载氧体制备
将硫酸钙与Ben按照m(CaSO4)∶m(Al2O3·4SiO2)=6∶4进行机械混合。将混合物CaSO4/Ben浸渍于不同浓度的硝酸铁溶液中,经搅拌(80 ℃)、烘干(105 ℃)、造粒(10 MPa)、煅烧(900 ℃)、粉碎筛分(粒径180~250 μm),制得Fe2O3负载量(质量分数,以Fe元素质量分数计,下文提及的修饰剂含量均以此计)分别为0、2.5%、5.0%、7.5%、10.0%、12.5%、15.0%、17.5%和20.0%的载氧体颗粒CaSO4/Ben-iFe(i表示Fe元素质量分数)用于流化床实验。将膨润土浸渍于硝酸铁溶液中,通过改变膨润土和硝酸铁比例,使载氧体中因硝酸铁煅烧而生成的Fe2O3与Al2O3·4SiO2的质量比控制为6∶4,混合物经搅拌、烘干、造粒、煅烧、粉碎筛分后制得Fe2O3/Ben载氧体。
1.3 实验装置及性能测试方法
1.3.1 实验装置 间歇式流化床化学链燃烧系统实验装置如图1所示,主要由配气控制系统、间歇式流化床反应器和气体在线检测系统三部分构成。配气控制系统中CO、N2以及空气由钢瓶供给,以质量流量计控制气体流量。流化床反应器主体为不锈钢管(310S, ϕ 32 mm×1050 mm),多孔陶瓷分布板设置于其底部515 mm处,通过加热反应器外部包覆的带有温控程序的电阻炉以提供反应所需的热量。气态产物经过冷却、除尘和干燥后进入西门子实验室在线分析系统(Ultramat 23,Calomat 6,Oxymat 61),检测组分包括CO、CO2以及O2。
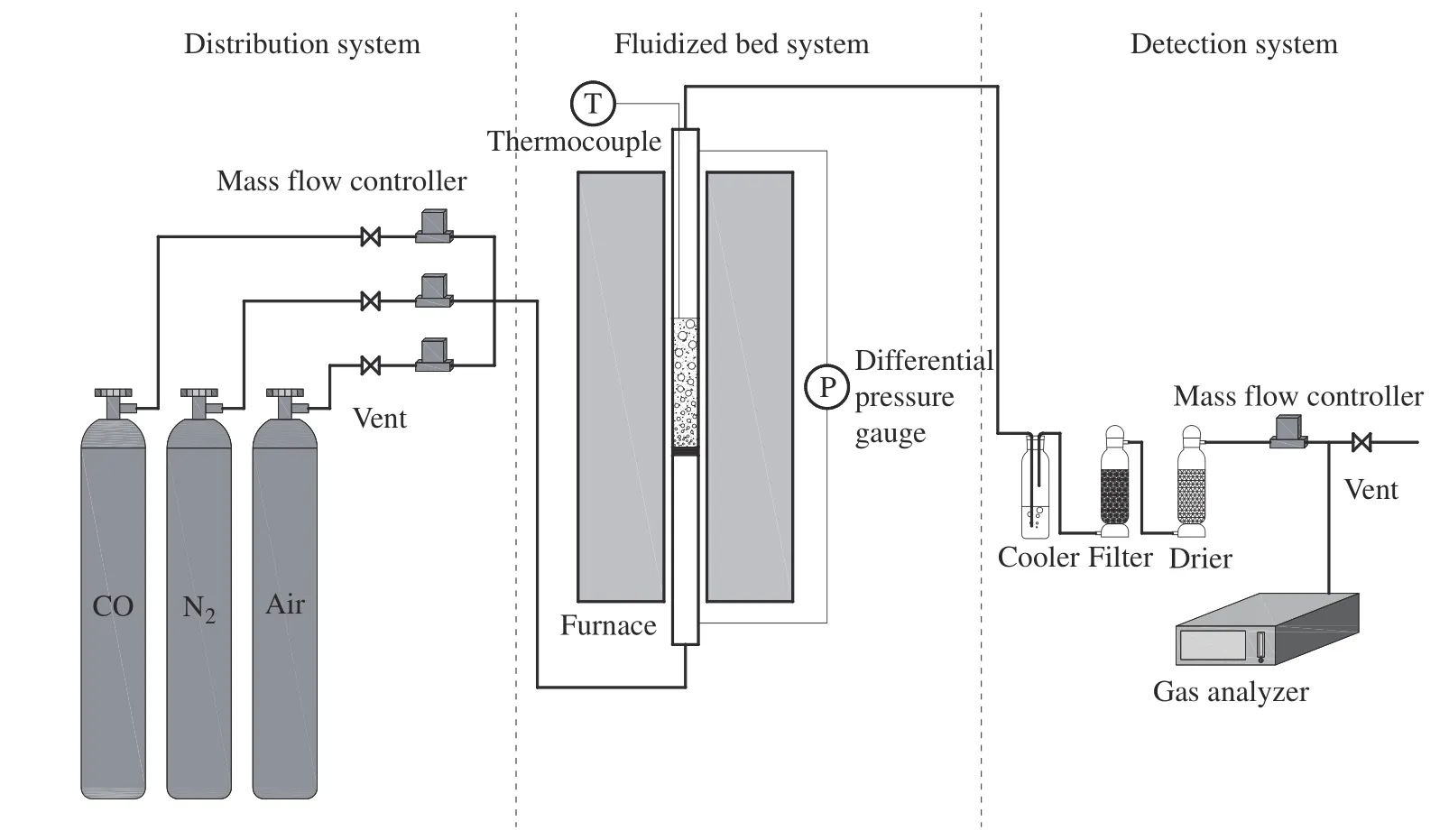
图1 间歇式流化床化学链燃烧系统Fig. 1 Chemical looping combustion system of batch fluidized bed
1.3.2 循环性能测试 称取30 g载氧体置于分布板上,检测系统的气密性后,在N2气氛下将反应器加热至900 ℃进行还原-吹扫-氧化-吹扫循环实验。还原阶段反应时间设置为20 min。吹扫时,通入N2直至完全置换系统内的气体,避免还原气体与氧化气体接触。在氧化阶段,由于载氧体的氧化反应为放热反应,为维持反应器内温度恒定,使用O2、N2体积比为9∶1的混合气体替代空气,氧化至尾气中O2体积分数恢复至初始水平(10%)时停止。各载氧体分别进行12次氧化还原循环,最后一次循环反应结束时,载氧体被氧化至氧化态。
1.3.3 反应性能测试 称取约20 mg载氧体置于氧化铝坩埚中,利用热重分析仪测试载氧体的反应性能。在N2气氛下,以30 ℃/min升温速率升温至设定温度(800、850、900、950 ℃)后,以100 mL/min的速率通入CO与N2混合气(体积比为1∶4)。当载氧体质量稳定时反应结束,并在N2气氛中冷却至室温。
1.4 数据处理
以CO作为燃料,其与载氧体在还原阶段发生1个主反应(式(1))和3个副反应(式(2)~式(4)),反应后气体流量增加。

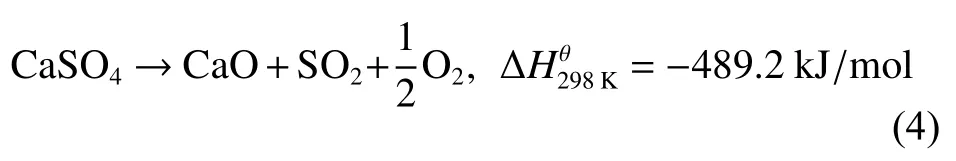
因此根据N2质量守恒[16]计算得到出口气体的流量Qout:
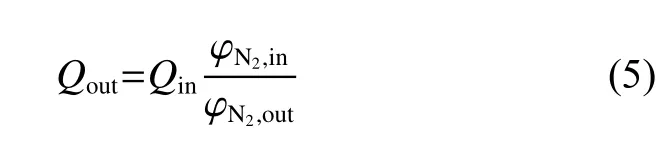
定义反映载氧体反应性能的重要指标CO平均转化率(XCO)为:
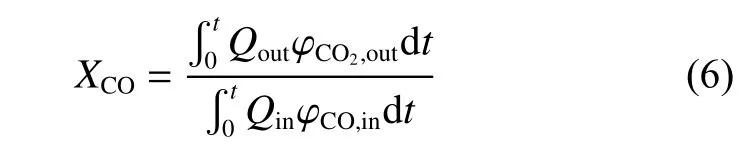
为量化多次循环(n)中载氧体反应活性的衰减速率,定义CO平均转化率衰减比δ,其与CO平均转化率的关系为:
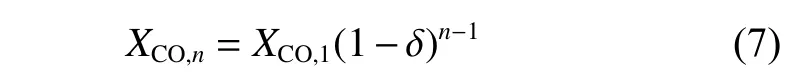
载氧体还原度(R0)定义为:

2 结果与讨论
2.1 Fe2O3负载量对燃料转化的影响
为探究Fe2O3负载量对CaSO4/Ben载氧体与CO反应活性的影响,图2示出了初次还原阶段不同Fe2O3负载量对CaSO4/Ben载氧体的CO平均转化率的影响。由图2可见,随着Fe2O3负载量增加,CO平均转化率显著增加。当Fe2O3负载量增加至15.0%时,CO平均转化率由原来的0.83提高至0.97,表明Fe2O3对CaSO4/Ben载氧体与CO的还原反应有明显的促进作用,可有效提高CO的燃烧效率;但当Fe2O3负载量从15.0%增加至20.0%时,CO平均转化率增幅仅为2.5%。因此,综合考虑反应性与经济性,在本文实验条件下,初次反应时Fe2O3负载量为15.0%时最佳。主要原因有两点:(1)Fe2O3在CaSO4与CO的还原反应中起催化作用,Fe2O3在反应过程中先被CO还原生成单质Fe,随后与CaSO4结合形成中间体CaFeSO,中间体在与CO反应时又重新生成Fe2O3[17-18];(2)由于载氧体煅烧时前驱体Fe(NO3)3分解并释放气体,促进了载氧体孔隙的发展。利用BET方法测试新制备的CaSO4/Ben和CaSO4/Ben-15.0%Fe载氧体颗粒孔径特性,结果如表1所示,表明添加15.0%Fe2O3后的载氧体颗粒其比表面积(SBET)与孔容(VP)均有所增加,有利于气固反应的进行。
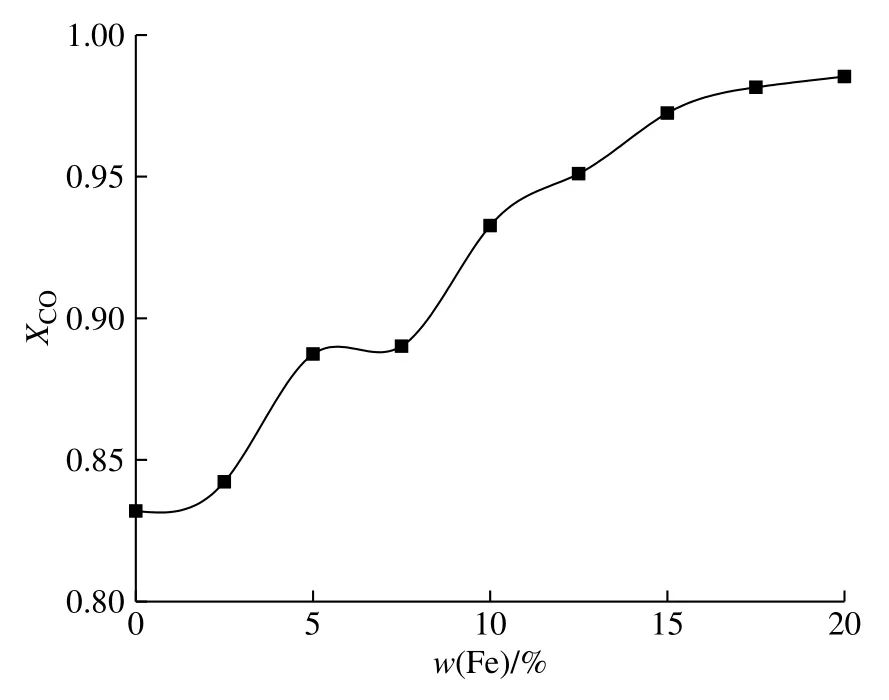
图2 Fe2O3负载量对CO平均转化率的影响Fig. 2 Effect of Fe2O3 content on CO average conversion

表1 CaSO4/Ben和CaSO4/Ben-15.0%Fe载氧体颗粒孔径特性Table 1 Pore size characteristics of CaSO4/Ben and CaSO4/Ben-15.0%Fe oxygen carriers
为验证Fe2O3对CaSO4/Ben载氧体与CO反应的强化作用,对比CaSO4/Ben与CaSO4/Ben-15.0%Fe载氧体在初次还原过程中出口CO2和CO体积分数,结果如图3所示。从图3可以看出,在CaSO4/Ben与CO反应初期,由于成核和生长特征[19-20],因此有约3 min的诱导期,随后CO体积分数持续升高;而CaSO4/Ben-15.0%Fe的诱导期缩短为2 min,且诱导期后CO体积分数趋近于0。加入Fe2O3后,产生的CO2体积分数峰值也从CaSO4/Ben的16.70%增至CaSO4/Ben-15%Fe的18.70%。说明Fe2O3的添加提高了CaSO4/Ben载氧体与CO反应速率,使通入反应器的CO气体充分反应,因而CO2浓度持续升高。
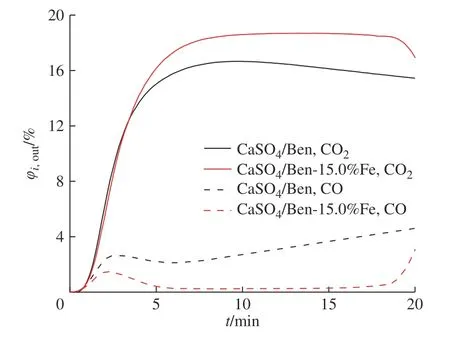
图3 反应器出口气体浓度与反应时间的关系曲线Fig. 3 Relationship of reactor outlet gas concentration with reaction time
2.2 载氧体循环特性
为了研究Fe2O3修饰的CaSO4/Ben载氧体与CO的反应活性和稳定性,对各载氧体进行12次循环实验,结果如图4所示。CaSO4/Ben载氧体在多次循环反应(图中虚线表示不同循环次数的间隔)过程中,CO2体积分数峰值在15.0%~16.6%范围内变化较为稳定,但达到峰值后的衰减速率增加;CO体积分数的峰值则在前6次循环过程中逐渐增加,后趋于平缓。CaSO4/Ben-15.0%Fe载氧体从第2次循环起CO和CO2体积分数的峰值就比较稳定。由此可见,添加质量分数为15.0%的Fe2O3后,载氧体与CO反应的稳定性得到了提高。
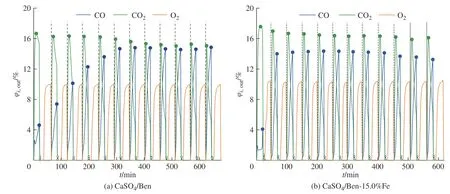
图4 载氧体化学链燃烧反应物及产物浓度曲线Fig. 4 Concentration curves of reactants and products in CLC of oxygen carriers
12次循环实验中各载氧体的CO平均转化率如图5所示,可见各载氧体CO平均转化率总体呈下降趋势,且前2次循环时下降趋势显著,原因是副反应式(2)~(4)的发生,使CaSO4转化为CaO时释放含硫气体,从而导致载氧体中的有效组分减少,载氧体颗粒的可回收性降低。在第2次循环后,CO平均转化率衰减速率变缓,副反应产生的CaO在反应器中累积,从而抑制副反应的发生[21],且Fe2O3可抑制副反应式(4)的发生[18]。纵向对比可知,CO平均转化率基本上随Fe2O3负载量的增加而增加。CaSO4/Ben与CaSO4/Ben-15.0%Fe经12次循环反应后,CO平均转化率分别由原来的0.83下降至0.66,以及由原来的0.97下降至0.87。由此可见,Fe2O3可显著提高载氧体的反应活性和稳定性。当Fe2O3负载量为15.0%~20.0%时,Fe2O3对CaSO4/Ben载氧体反应活性及稳定性的改善程度相近。

图5 CO平均转化率随循环次数的变化Fig. 5 CO average conversion rate varies with the cycle numbers
为了研究载氧体反应性能下降的原因,对比了CaSO4/Ben-15.0%Fe载氧体12次循环反应前后的微观形貌,如图6所示。可见在12次循环反应后,CaSO4/Ben-15.0%Fe载氧体颗粒表面由于循环过程中发生放热反应导致轻微的熔融团聚现象,从而使CaSO4/Ben-15.0%Fe载氧体表面孔隙与比表面积减少,阻碍CO向载氧体内部扩散,并会导致CO平均转化率下降,这与图5结果一致。

图6 CaSO4/Ben-15.0%Fe载氧体12次循环反应前后的SEM分析Fig. 6 SEM analysis of CaSO4/Ben-15.0%Fe oxygen carriers before and after the 12 th cycles
通过BET测试得到CaSO4/Ben-15.0%Fe载氧体颗粒反应前后孔径分布情况及孔径特性,分别如图7和表2所示。经过12次循环反应后,CaSO4/Ben-15.0%Fe载氧体孔径与孔容均有所减小。在2~10 nm段反应前后孔径分布变化不大;在10~70 nm段的40 nm左右处,反应后孔容的峰值强度减弱,主要是CaSO4/Ben-15.0%Fe载氧体颗粒表面发生了轻微的烧结团聚所致。
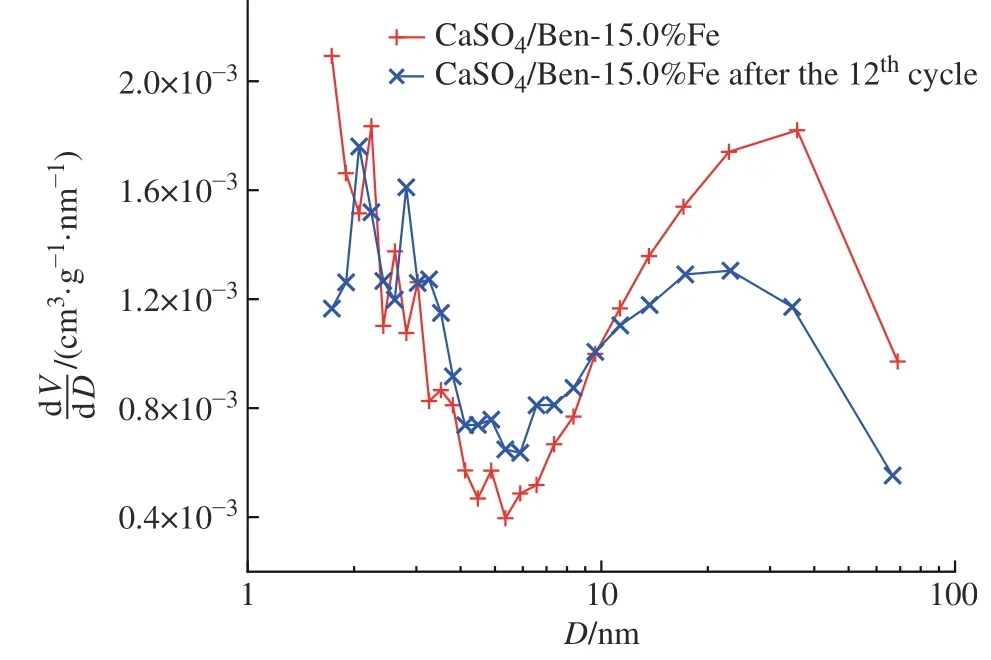
图7 CaSO4/Ben-15%Fe载氧体颗粒在12次循环反应前后孔径分布情况Fig. 7 Pore size distribution of CaSO4/Ben-15%Fe oxygen carrier particles before and after the 12th cycles

表2 CaSO4/Ben-15.0%Fe载氧体颗粒在12次循环反应前后孔径特性Table 2 Pore size characteristics of CaSO4/Ben-15.0%Fe oxygen carriers before and after the 12th cycles
为了衡量多次循环化学链燃烧过程中各载氧体反应的稳定性,借助CO平均转化率的衰减比进行对比,其变化曲线如图8所示。由图8可以看出,随着Fe2O3负载量的增加,CO转化率的平均衰减比总体呈下降趋势,CaSO4/Ben载氧体反应的稳定性也随之得到改善。因此在本文的实验条件下,当载氧体中Fe2O3的负载量为15.0%时,载氧体即可维持良好的循环反应活性和稳定性。
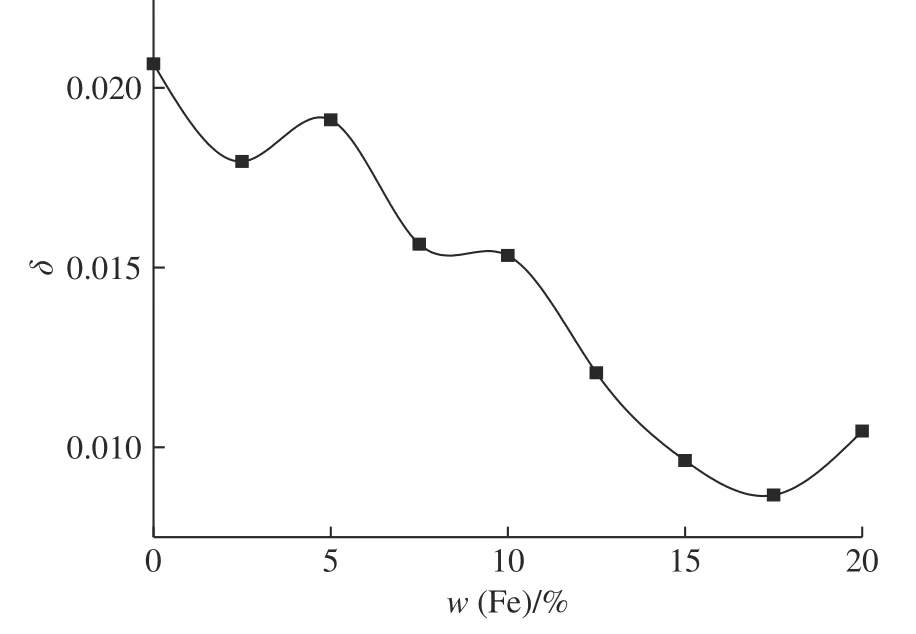
图8 CO平均转化率的衰减比Fig. 8 Attenuation ratio of CO average conversion
2.3 Fe2O3对反应活化能的影响
图9示出了不同载氧体在800 ℃下的热重(TG)和微分热重(DTG)曲线。图9(a)反映了CaSO4在载氧量上的显著优势。Fe2O3/Ben样品的质量损失约为18%,与样品中Fe2O3完全还原成Fe的质量损失一致,表明样品中的Fe2O3与CO反应时最终被还原为单质Fe。CaSO4/Ben-5.0%Fe样品的质量损失约为30%,其中Fe2O3被还原后造成的质量损失仅为2.2%,CaSO4的还原则是造成样品失重的主要原因。由图9(b)的DTG曲线可以看出,与CaSO4/Ben和Fe2O3/Ben相比,添加Fe2O3修饰的CaSO4/Ben载氧体反应性得到显著改善。此外,由图9(a)还可以看出,CaSO4/Ben样品反应90 min时仍未完全还原,而Fe2O3/Ben仅在20 min内即完全还原,其反应性优于CaSO4/Ben。添加的Fe2O3加速了CaSO4的还原,Fe2O3负载量为5.0%、10.0%、20.0%的CaSO4/Ben载氧体分别在26 min、21 min、14 min内完全转化。CaSO4/Ben-5.0%Fe的最高还原反应速率约为CaSO4/Ben和Fe2O3/Ben的两倍;随着Fe2O3负载量的增加,反应速率虽然没有明显变化,却可相对缩短完全反应所需的时间。因此,Fe2O3对CaSO4具有良好的协同促进作用。
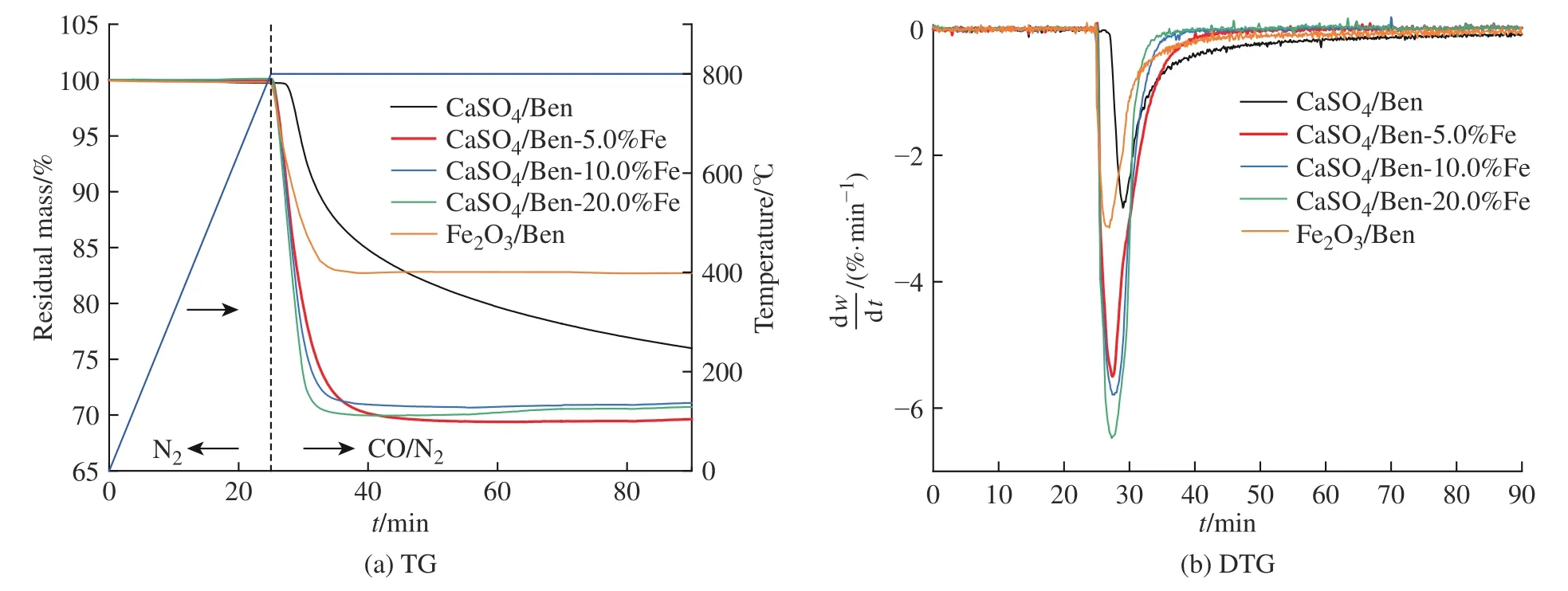
图9 不同载氧体在800 °C下的TG和DTG曲线Fig. 9 TG and DTG curves of different oxygen carriers at 800 °C
2.3.1 反应动力学模型验证 如前所述,Fe2O3修饰剂对CaSO4和CO的反应具有催化作用。基于特征分析,进行以下假设[22]:(1)忽略载氧体样品颗粒的孔隙率;(2)忽略副反应;(3)忽略外部传质;(4)不考虑结构变化及烧结;(5)热效应最小化,假定为等温反应;(6)反应处于伪稳状态。
反应初期CaSO4与CO经诱导期后进入快速反应期,体现出成核和生长过程的特征。反应时CO吸附在CaSO4表面活性点位,高温下部分原子核分散在CaSO4表面。因此在假设条件下,结合TGA分析,采用缩合模型模拟载氧体转化数据。恒定温度下的动力学方程为:
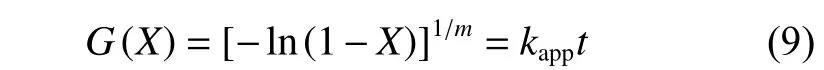
其中kapp是表观反应速率常数,如式(11)所示:

考虑到反应式(1)产生CaS后,发生固固反应(式(3))对b没有影响,因此根据反应式(1),取b=0.25。CO还原CaSO4可以认为是一阶反应,取n=1[22]。
化学反应速率常数k随温度的变化遵循Arrhenius表达式:
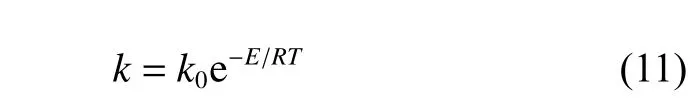
2.3.2 活化能拟合 借助TGA分析Fe2O3负载量不同的载氧体在不同温度下的转化率变化。由式9可看出ln[−ln(1−Xr)]和lnt的曲线是以m为斜率的线性曲线,且当lnt=0时的截距为mlnkapp。表3所示为不同反应温度对应的最佳拟合值,由表可见在不同反应温度下CaSO4/Ben颗粒的最佳拟合值为1.711~1.756,数据拟合的线性因子在0.946~0.991之间变化。对同一材料使用单一的m值,这与使用的形核与生长动力学模型的解释是一致的。因此,所有的拟合曲线以平均值m=1.734进行绘制。
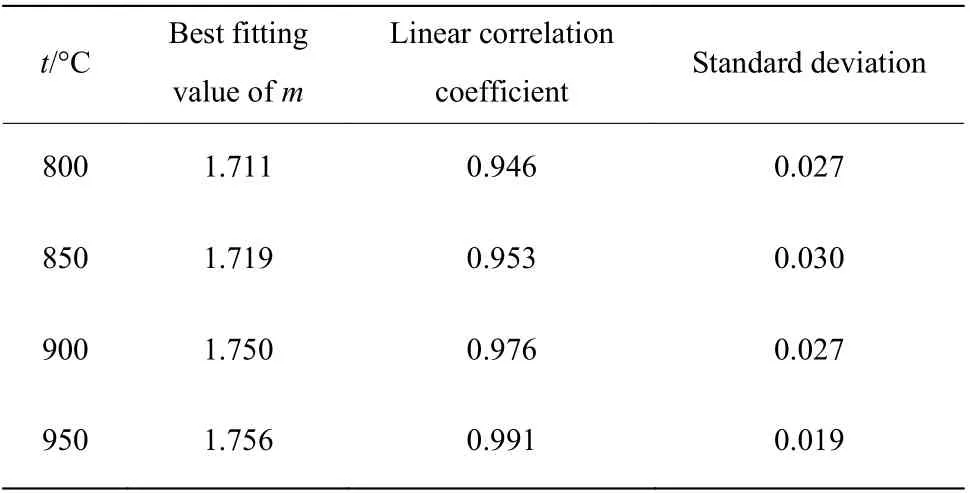
表3 不同反应温度对应的最佳拟合值mTable 3 Best fitting value m corresponding to different reaction temperatures
图10示出了CaSO4/Ben转化率的动力学模型数据与实验数据的比较结果,可见二者吻合较好,主要在800 ℃和850 ℃中的低转化率时存在一定的偏差。

图10 不同反应条件下CaSO4/Ben载氧体转化率的实验数据和模型数据比较Fig. 10 Comparison of experimental and model data of conversion of CaSO4/Ben oxygen carrier with different reaction conditions
由式(10)分别求得对应的化学反应速率常数k值,并根据式(11)变式(lnk=lnk0−E/RT)线性化拟合得到对应的活化能E。图11所示为温度与CaSO4/Ben载氧体化学反应速常数关系曲线,拟合的线性相关系数为0.992,计算得到反应活化能为88.27 kJ/mol。

图11 ln k与1/T的Arrhenius图Fig. 11 Arrhenius diagram of ln k and 1/T
图12示出了不同Fe2O3负载量的CaSO4/Ben载氧体与CO反应活化能的变化曲线。结果表明,与CaSO4/Ben载氧体相比,添加Fe2O3后载氧体的反应活化能均有所降低,即Fe2O3对CaSO4/Ben载氧体的催化作用随Fe2O3负载量的增加而增强,这与图2结果一致,Zhang等[23]也获得了相似的结果,证实Fe2O3对CaSO4/Ben载氧体反应具有催化作用,可降低CaSO4与CO反应的活化能,提高CaSO4晶格氧释放速率,从而提高载氧体转化率。
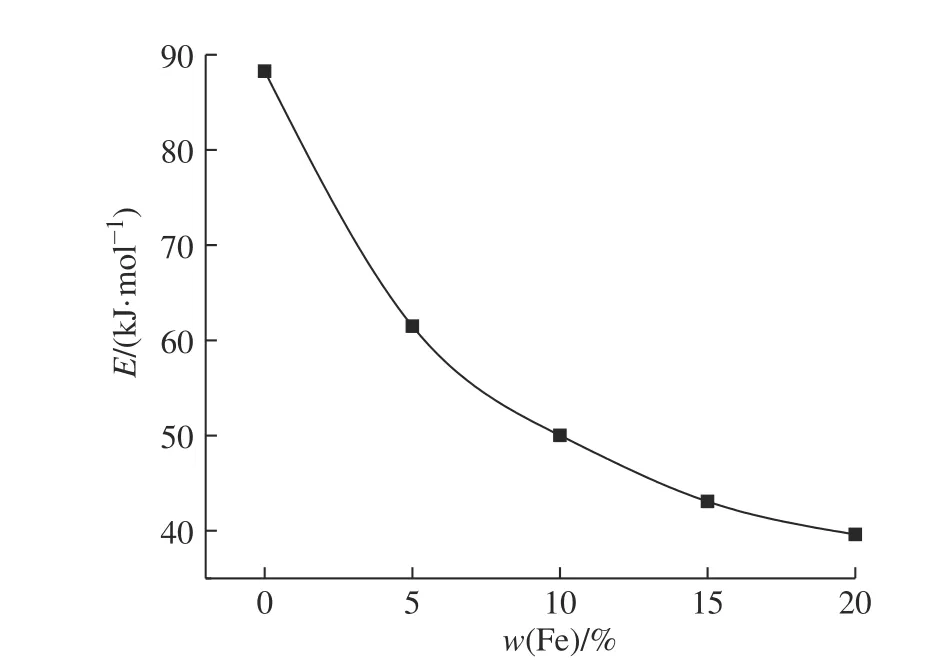
图12 活化能随Fe2O3负载量的变化曲线Fig. 12 Change curve of activation energy with Fe2O3 content
3 结 论
通过在CaSO4/Ben载氧体中添加不同质量分数的Fe2O3,借助间歇式流化床反应器与TGA分析仪,研究Fe2O3修饰CaSO4/Ben载氧体的化学链燃烧特性,得到以下结论:
(1)Fe2O3的添加可增加载氧体的比表面积和孔容,有利于提高载氧体反应活性,但导致载氧体表面轻微烧结团聚,从而影响燃料气体向载氧体内部扩散的过程,不利于燃料转化。
(2)载氧体在多次循环反应中,部分CaSO4生成CaO与含硫气体,导致其有效组分减少,在最初2次循环时的稳定性较差。当Fe2O3负载量为15.0%~20.0%时载氧体反应稳定性最佳,有利于维持化学链燃烧系统长时间运行。
(3)Fe2O3对CaSO4/Ben载氧体与CO反应起催化作用,能显著提高其反应速率,提高CO燃烧效率。通过计算反应活化能,并对比各载氧体中CO平均转化率,发现Fe2O3的最佳负载量为15.0%。
符号说明:
b——还原的化学计量系数
D——孔径, nm
E——化学反应的活化能,J/mol
G(Xr)——载氧体积分函数
kapp——表观反应速率常数
k——化学反应速率常数
k0——为指前因子,m/s
m0——反应前反应物质量,g
mt——t时刻反应物质量,g
mre——反应后残留质量,g
m——阿夫拉米指数
n——反应级数
pCO——气体中的CO分压,kPa
Qin——进口气体流量,L/min
Qout——出口气体流量,L/min
R0——载氧体还原度
R——理想气体常数,8.314 J/(mol·K)
SBET——BET比表面积, m2/g
t——反应时间,min
T——反应温度,K
Vp——孔容, cm3/g
XCO——CO平均转化率
XCO,n——第n次循环反应的CO平均转化率
φi,in——还原阶段流入系统的i气体的体积分数,%
φi,out——还原阶段流出系统的i气体的体积分数,%
δ——衰减比
