基于指纹图谱探讨白芍不同炮制品成分的差异
2022-07-05马向慧姜恒丽曹丽娟
刘 烨,马向慧,姜恒丽,曹丽娟
(盛实百草药业有限公司,天津市中药饮片炮制技术企业重点实验室,天津 300301)
白芍为毛茛科植物芍药Paeonia lactifloraPall.的干燥根,味苦、酸,性微寒,归肝、脾经;具有养血调经,敛阴止汗,柔肝止痛,平抑肝阳的功效;可用于治疗血虚萎黄,月经不调,自汗,盗汗,胁痛,腹痛,四肢挛痛,头痛眩晕等症[1]。2020年版《中国药典》收载有白芍、炒白芍和酒白芍三种炮制规格的饮片。白芍的化学成分复杂,主要有单萜及其苷类、三萜类、黄酮类、鞣质类和多糖类等[2-5],但目前多只以芍药苷作为考查指标对白芍的不同炮制品进行质量控制,不能全面地反映白芍的质量和不同炮制品之间的成分变化。
指纹图谱是一种表征中药内在质量整体变化的评价手段,对中药饮片质量控制的全面性具有重要意义[6-8],同时用化学计量法加以辅助评价,能更全面地表现中药饮片的内在品质。本次研究采用高效液相色谱法建立了白芍不同炮制品(各10批)的指纹图谱方法,并通过相似度分析、聚类分析和主成分分析比较其差异性,以期为规范白芍饮片的炮制工艺提供依据,并为白芍不同炮制品的质量控制提供参考。
1 仪器与材料
1.1 仪器 Waters2695高效液相色谱仪(美国沃特世科技有限公司);XP205电子天平[梅特勒-托利多仪器(上海)有限公司];ME-204/02电子天平[梅特勒-托利多仪器(上海)有限公司];KQ-600DB数控超声波清洗器(昆山市超声仪器有限公司);DZKW-110恒温水浴锅(STWK有限公司);H130冷却水循环装置(莱伯泰科有限公司)。
1.2 试剂 超纯水(娃哈哈有限公司);乙腈(德国默克股份有限公司)、磷酸(和光纯药工业株式会社)均为色谱纯。
1.3 对照品 芍药苷(批号110736-201943,纯度为95.1%)、没食子酸(批号110831-201605,纯度为90.8%)、儿茶素(批号110877-202005,纯度为95.1%)均购自中国食品药品检定研究院;芍药内酯苷(批号PS011455,纯度为97.52%)购自成都普思生物科技股份有限公司;五没食子酰葡萄糖(批号ZZS19101116,纯度为99.39%)购自上海甄准生物科技有限公司。
1.4 药材 10批次白芍药材分别购自安徽、四川、浙江,均来源于毛茛科植物芍药Paeonia lactifloraPall.的干燥根,经盛实百草药业有限公司参照2020年版《中国药典》(一部)检验合格。
1.5 饮片 取白芍药材,参照2020年版《中国药典》(一部)“白芍”炮制方法,洗净,润透,切薄片,干燥,得白芍生品饮片(编号:B1~B10);参照“炒白芍”炮制方法,取净白芍片,照清炒法(2020年版《中国药典》通则0213)炒至微黄色,得炒白芍饮片(编号:CB1~CB10);参照“酒白芍”炮制方法,取净白芍片,照酒炙法(2020年版《中国药典》通则0213)炒至微黄色,得酒白芍饮片(编号:JB1~JB10)。白芍、炒白芍和酒白芍的样品详细信息见表1。

表1 30批白芍不同炮制品样品明细
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液的制备 分别精密称取儿茶素、没食子酸、芍药苷、五没食子酰葡萄糖和芍药内酯苷对照品适量,加稀乙醇制成每1 ml含儿茶素0.916 8μg、没食子酸43.40μg、芍药苷93.01μg、五没食子酰葡萄糖12.82μg、芍药内酯苷49.54μg的混合对照品溶液。
2.1.2 供试品溶液的制备 精密称取白芍(或炒白芍,或酒白芍)粉末(过四号筛)0.2 g,置50 ml量瓶中,加稀乙醇35 ml,超声30 min,放置至室温,加稀乙醇至刻度,摇匀,滤过,取续滤液,即得。
2.2 色谱条件 色谱柱:TSKgel ODS-80TS(150 mm×4.6 mm,5μm);流动相:乙腈(A)-0.1%磷酸(B)溶液;梯度洗脱(0~10 min,5%→7%A;10~15 min,7%→13%A;15~25 min,13%A;25~40 min,13%→25%A;40~65 min,25%→55%A);进样量:10μl;流速:1.0 ml/min;柱温:30℃;检测波长:230 nm。
2.3 精密度试验 取“2.1.2”项下供试品溶液(B1号)1份,按照“2.2”项下色谱条件连续进样6次,以芍药苷为参照峰,记录各共有峰的相对保留时间和相对峰面积。结果,各共有峰的相对保留时间RSD<1.0%,相对峰面积RSD<3.0%,表明本方法精密度良好。
2.4 重复性试验 取“2.1.2”项下供试品溶液(B1号)6份,按照“2.2”项下色谱条件进样分析,以芍药苷为参照峰,记录各共有峰的相对保留时间和相对峰面积。结果,各共有峰的相对保留时间RSD<1.0%,相对峰面积RSD<3.0%,表明本方法重复性良好。
2.5 稳定性试验 取“2.1.2”项下供试品溶液(B1号)1份,分别在0、2、4、8、12和24 h按照“2.2”项下色谱条件进样检测,以芍药苷为参照峰,记录各共有峰的相对保留时间和相对峰面积。结果,各共有峰的相对保留时间RSD<1.0%,相对峰面积RSD<3.0%,表明样品在室温下放置24 h内稳定性良好。
3 不同炮制品HPLC指纹图谱的测定
3.1 指纹图谱的建立 取“2.1.1”项下混合对照品溶液按“2.2”项下色谱条件进样,得对照品色谱图,见图1。分别取白芍(B1~B10)、炒白芍(CB1~CB10)、酒白芍(JB1~JB10)按“2.1.2”项下方法制备供试品溶液,按“2.2”项下色谱条件进样检测,记录数据并导入《中药色谱指纹图谱相似度评价系统》(2012年版)软件,采用平均数法和多点校正法,时间宽度0.10 min,分别生成白芍、炒白芍和酒白芍对照指纹图谱,见图2-4。

图1 混合对照品HPLC色谱图
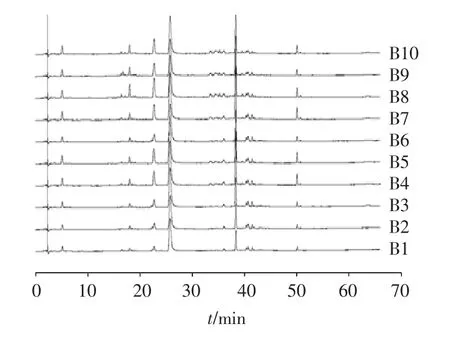
图2 10批白芍样品的HPLC指纹图谱叠加图
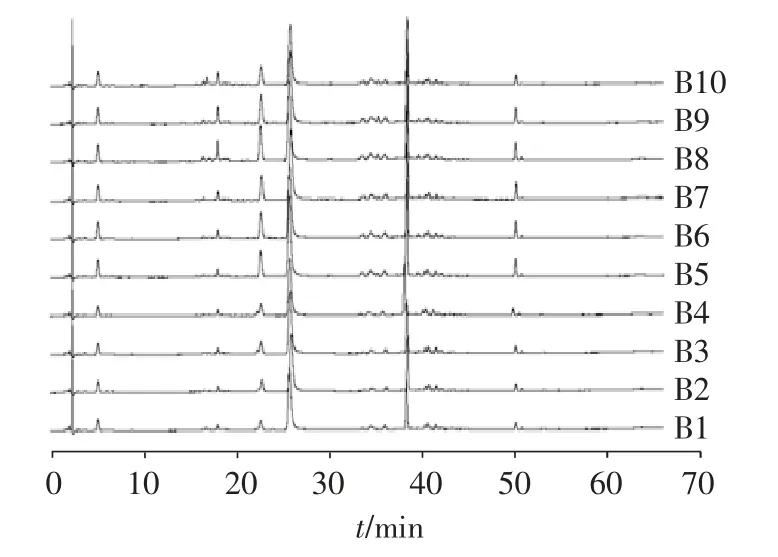
图3 10批炒白芍样品的HPLC指纹图谱叠加图
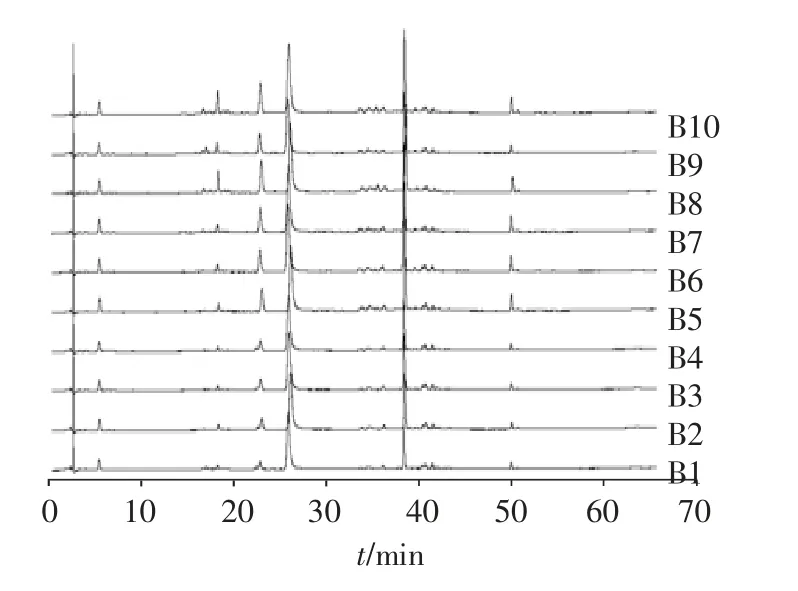
图4 10批酒白芍样品的HPLC指纹图谱叠加图
综合上述图谱,共标定10个共有峰,其中4号峰峰面积稳定、分离度良好,故选择其为参照峰。通过与对照品比对,共指认了5个色谱峰,分别为1号峰(没食子酸)、2号峰(儿茶素)、3号峰(芍药内酯苷)、4号峰(芍药苷)、6号峰(五没食子酰葡萄糖),见图5。

图5 白芍(A)炒白芍(B)酒白芍(C)HPLC对照图谱
以4号峰为参照峰,计算3种白芍炮制品的共有峰的相对峰面积,结果见表2,各共有峰的RSD范围为16.204%~52.877%。

表2 白芍、炒白芍和酒白芍的指纹图谱相对峰面积分析结果
3.2 相似度分析 分别通过10批次白芍、炒白芍和酒白芍生成的共有模式为对照指纹图谱,计算各批次之间的相似度,结果见表3。可见10批次白芍的相似度均>0.986,10批次炒白芍的相似度均>0.989,10批次酒白芍的相似度均>0.985,表明白芍及其炮制品质量稳定,炮制工艺稳定,且经炮制后化学成分并未发生质的变化。
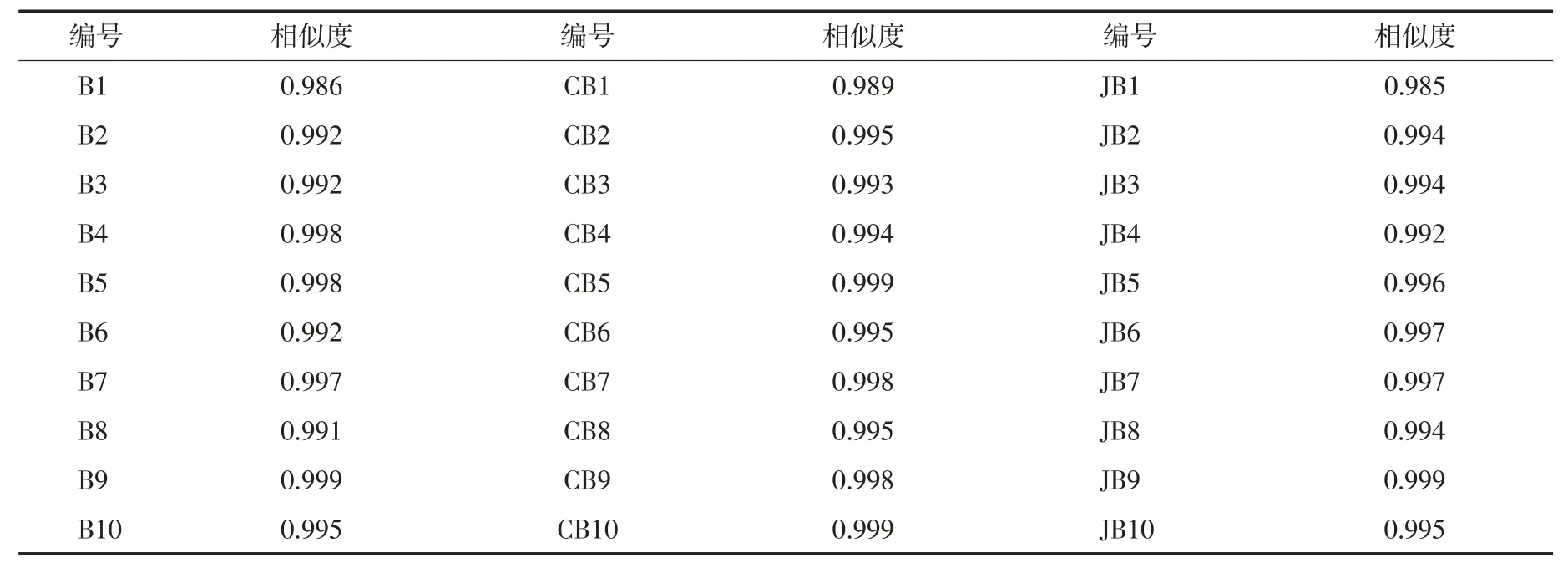
表3 30批白芍不同炮制品相似度结果
3.3 白芍与炒白芍、酒白芍各共有峰相对峰面积差异分析 比较3种白芍炮制品的共有峰的相对峰面积可知,与白芍生品相比较,炒白芍和酒白芍的1号峰、3号峰、6号峰的相对峰面积均有不同程度的增加,其中1号峰具有显著性差异;2号峰、8号峰、9号峰的相对峰面积均有不同程度的减小,其中8号峰和9号峰有显著性差异;炒白芍中7号峰的相对峰面积也出现显著性减小;10号峰和5号峰的相对峰面积均无明显的变化,结果见表4和图6。
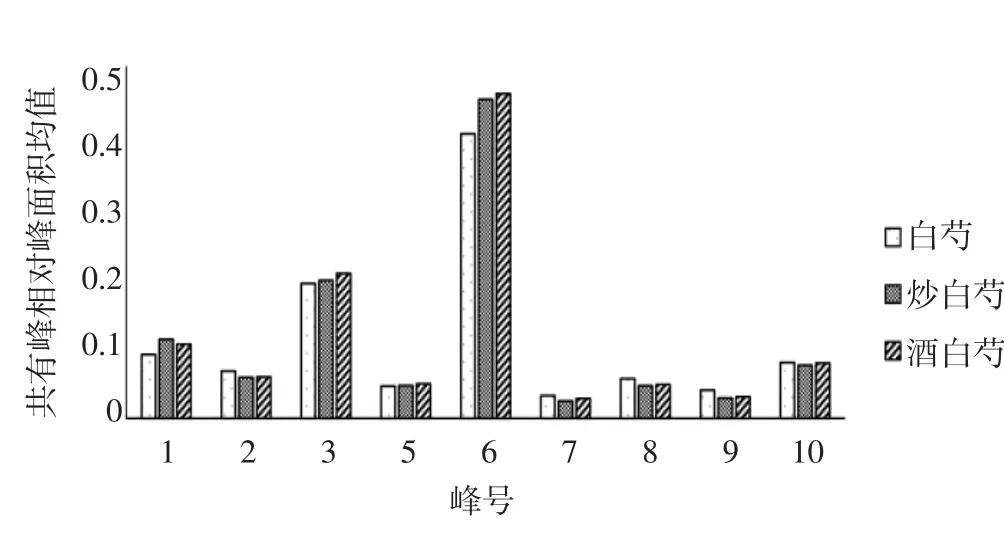
图6 白芍与炒白芍、酒白芍的相对峰面积均值对比图

表4 白芍与炒白芍、酒白芍共有峰相对保留时间和相对峰面积(n=10)
3.4 指标性成分定量分析 分别取白芍、炒白芍和酒白芍样品(各10批)参照2020年版《中国药典》一部[1]白芍项下含量测定方法进行检测,计算炮制前后芍药苷的含量变化,结果见表5和表6。由表5可知,白芍中芍药苷含量为2.5%~3.1%,平均含量为2.7%;炒白芍中芍药苷含量为2.2%~3.0%,平均含量为2.5%;由表6可知,酒白芍中芍药苷含量为2.2%~2.9%,平均含量为2.5%。炒白芍含量变化平均值为-0.2%,酒白芍含量变化平均值为-0.2%,说明炒制、酒制会影响芍药苷的含量。
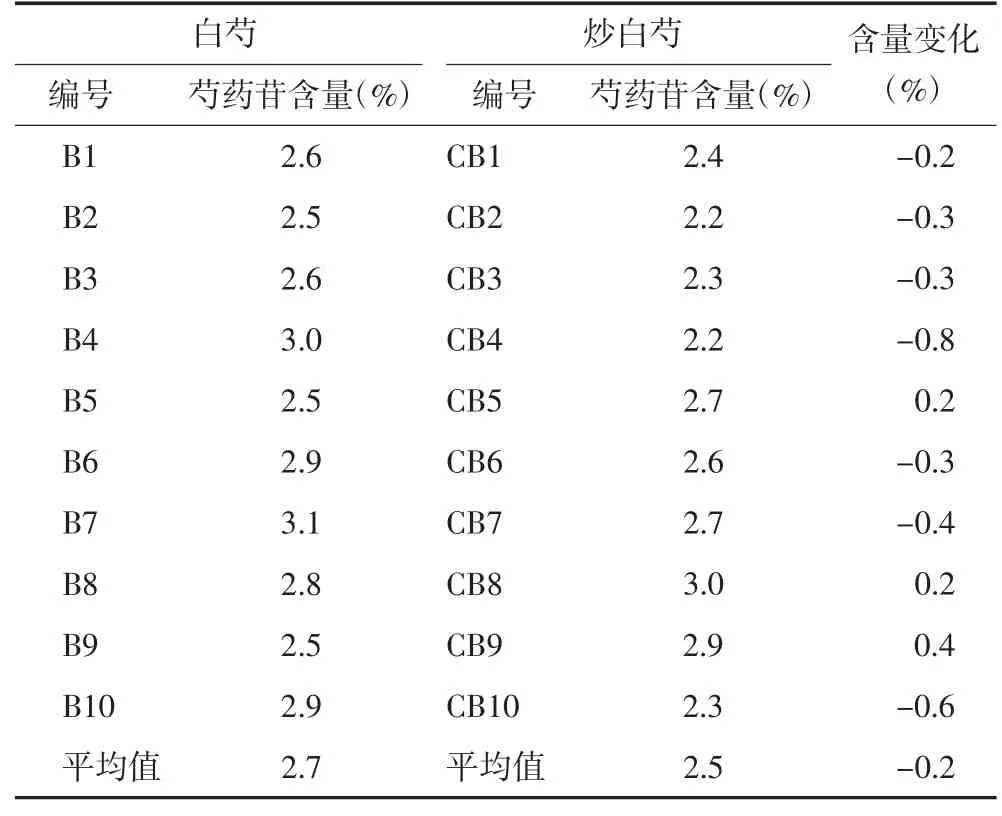
表5 白芍及炒白芍中芍药苷质量分数及变化
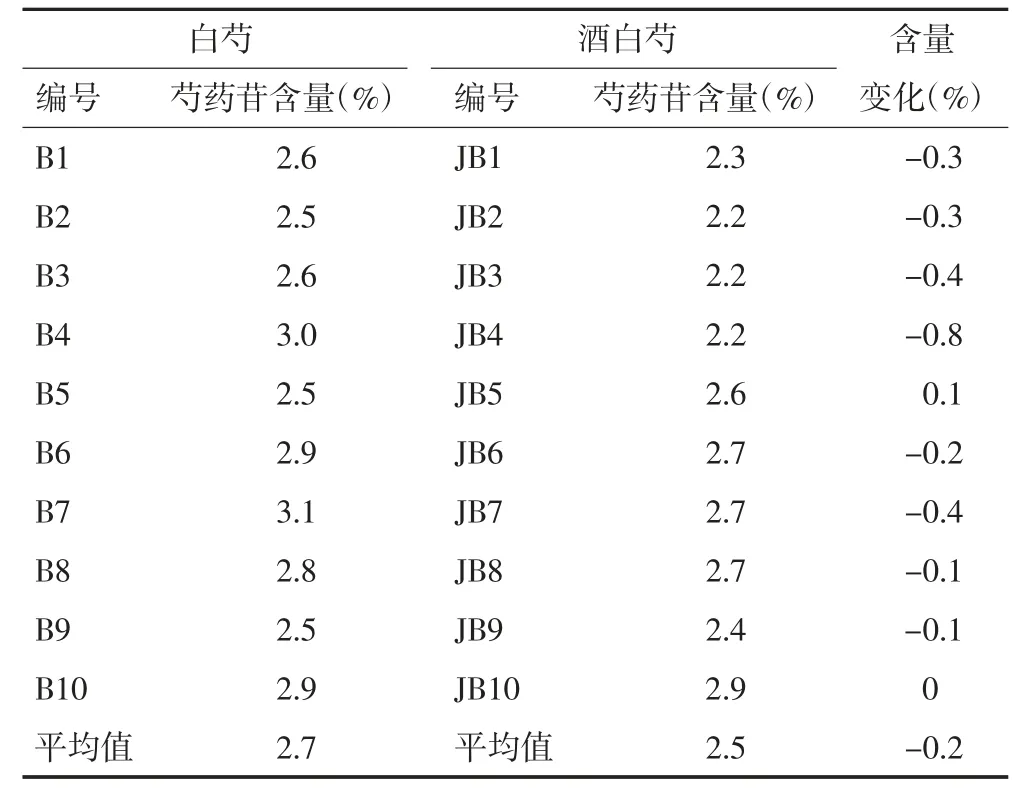
表6 白芍及酒白芍中芍药苷质量分数及变化
3.5 系统聚类分析 将各批次白芍饮片共有峰的峰面积导入SPSS 17.0系统软件,进行标准化处理后,采用组间连接法,以余弦距离作为样品间距离计算方法进行系统聚类分析,结果见图7。当余弦距离为25时,样品可聚为两大类,B1~B7为一类,B8~B10为另一类;当余弦距离为15时,样品聚为三大类,B1、B2、B3、B6为一类,B4、B5、B7为一类,B8、B9、B10为一类。

图7 10批白芍样品聚类分析图
3.6 主成分分析 采用SPSS 17.0软件对白芍不同炮制品(各10批)的共有峰峰面积进行标准化处理后,对指纹图谱所得的10个共有峰进行主成分分析,所得累计方差贡献率和特征值结果见表7、图8。以特征值>1为提取标准,得到2个主成分因子,方差百分比分别为58.67%和31.70%,累积贡献率为90.37%,说明提取的2个主成分可以代表原始色谱峰峰面积90.37%的信息,具有很好的代表性,提示主成分因子1、2可作为白芍不同炮制品的评价指标。
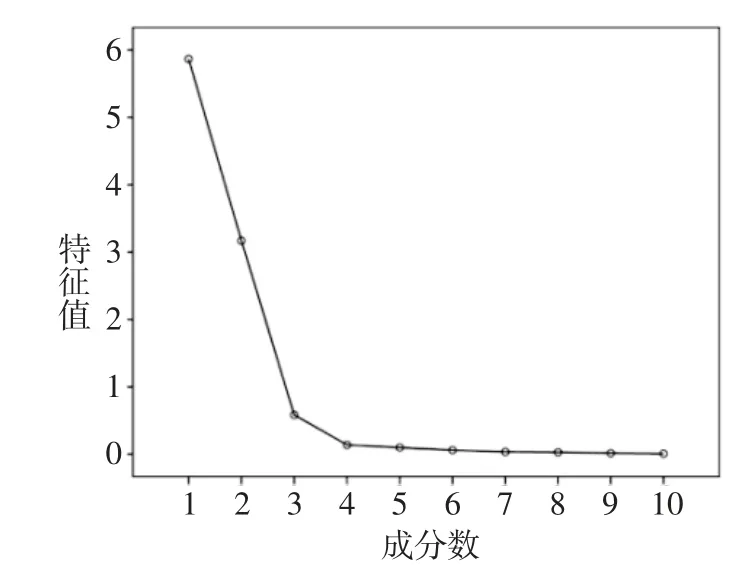
图8 主成分分析碎石图

表7 特征值及方差贡献率
主成分载荷矩阵(表8)反映了各变量对主成分的贡献大小和作用方向,对其分析可知7个变量与主成分因子1呈正相关,其中以峰1(没食子酸)、峰3(芍药内酯苷)、峰5、峰6和峰10对其贡献较大;7个变量与主成分因子2呈正相关,其中峰7、峰8和峰9对其贡献较大,与不同白芍炮制品各共有峰相对峰面积差异分析结果基本一致。
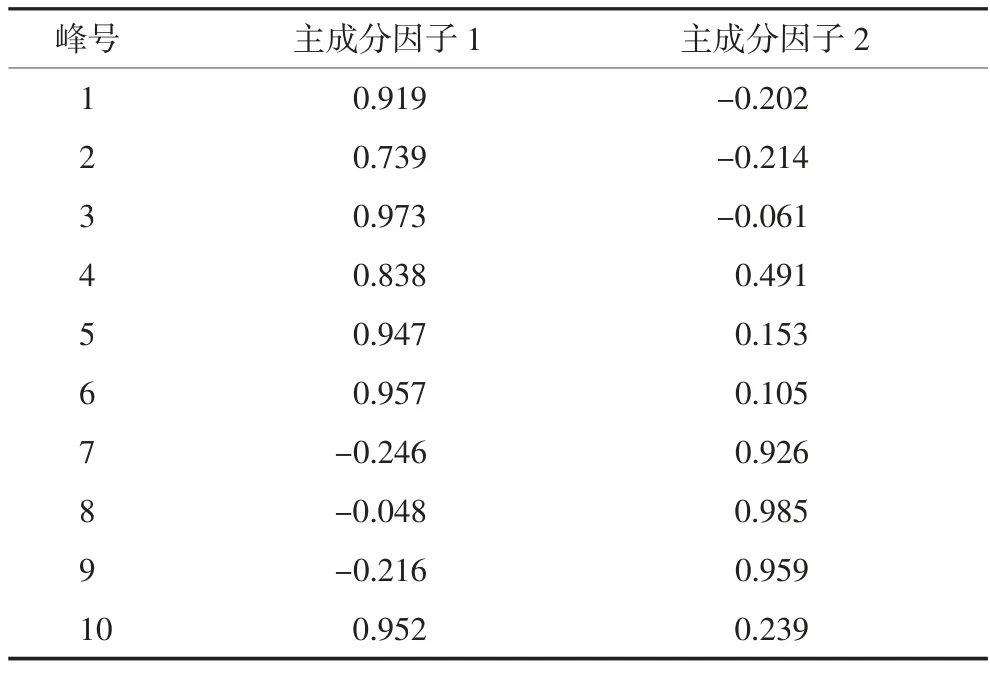
表8 主成分载荷矩阵
对上述主成分载荷值进行计算,得出各主成分的线性模型:F1=0.38×Z峰1+0.31×Z峰2+0.4×Z峰3+0.35×Z峰4+0.39×Z峰5+0.4×Z峰6-0.10×Z峰7-0.02×Z峰8-0.09×Z峰9+0.39×Z峰10;F2=-0.11×Z峰1-0.12×Z峰2-0.03×Z峰3+0.28×Z峰4+0.09×Z峰5+0.06×Z峰6+0.52×Z峰7+0.55×Z峰8+0.54×Z峰9+0.13×Z峰10。其中,F1、F2分别表示第1、2个主成分因子,Z峰1~Z峰10分别表示10个共有峰峰面积的标准化数据。
将各样品数据代入上述计算模型后,可得其主成分得分,结果见表9,以两个主成分因子的得分值分别为横纵坐标建立散点图,结果见图9。其可直观表现出各样品间的差异,B4、B5、B7分布较集中,B1、B2、B3、B6分布较集中,与聚类分析结果一致。
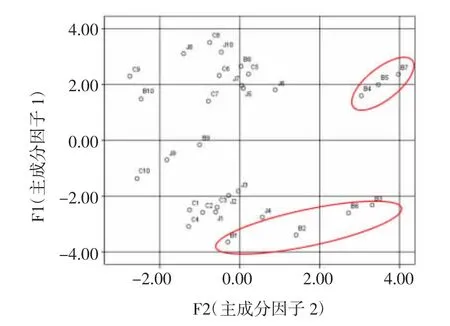
图9 30批白芍不同炮制品的主成分因子得分图
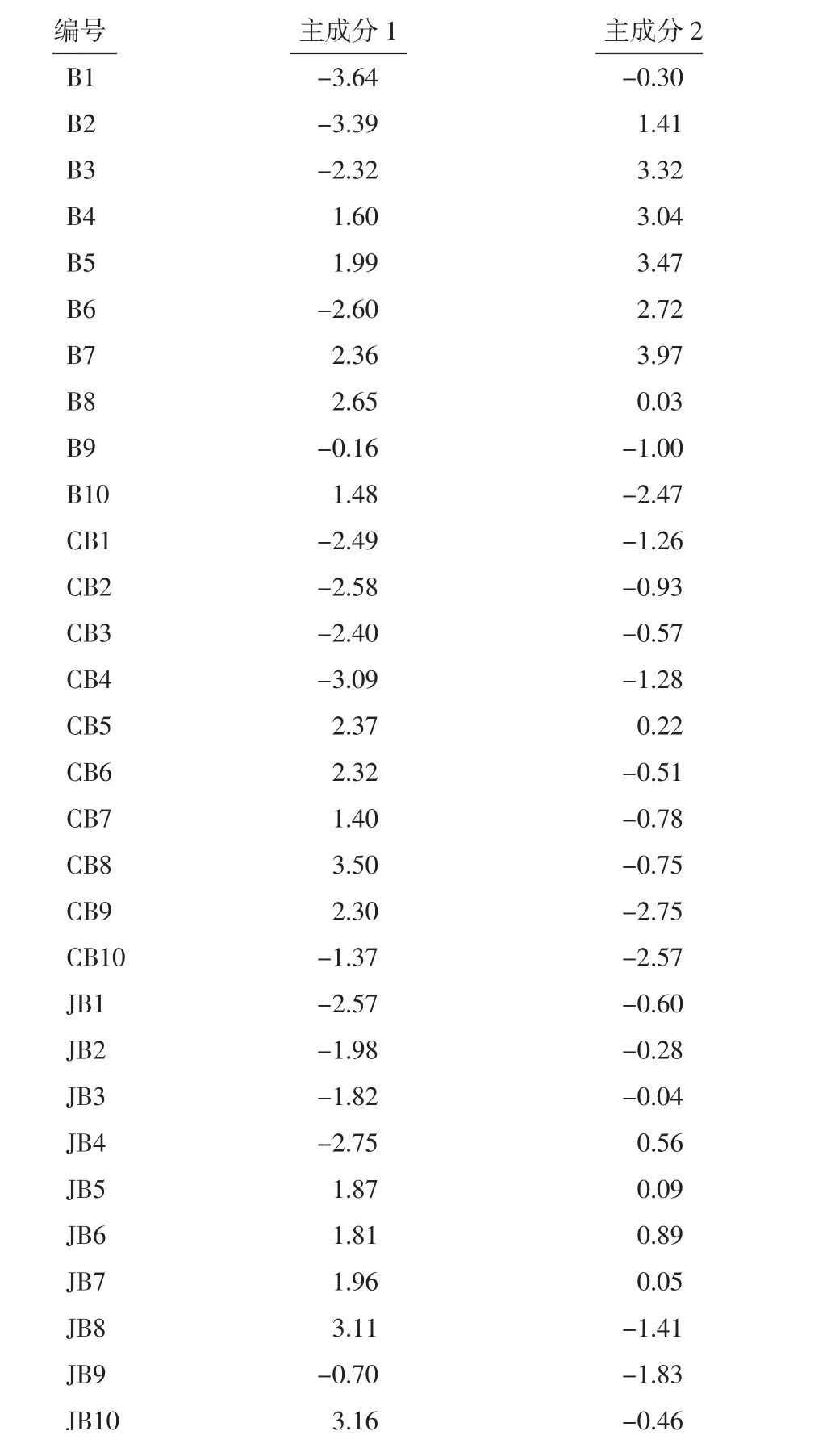
表9 30批白芍不同炮制品的主成分因子得分表
4 讨论
本研究前期采用DAD检测器对白芍样品进行全波长扫描,综合对比后,230 nm波长下,色谱图基线平稳,色谱峰数量较多且吸收强度均匀,因此选用其为检测波长。
分析比较了甲醇-水、乙腈-水、甲醇-0.1%磷酸和乙腈-0.1%磷酸四种不同的流动相系统,乙腈-0.1%磷酸条件下图谱基线平稳,色谱峰分离度良好,受干扰因素影响小,因此选择其作为最佳流动相系统。
对不同提取方式、不同提取溶剂和不同提取时间进行了考查,从提取的全面性、稳定性,操作的便捷性等方面考虑,选择稀乙醇作为样品提取溶剂,超声法提取30 min。
白芍、炒白芍和酒白芍(各10批)的指纹图谱相似度均大于0.98,证明其炮制前后化学成分种类未发生变化,同时,相对峰面积的RSD为16.204%~52.877%,证明白芍炮制前后化学成分含量变化较大。含量测定结果表明,白芍炒制前后指标性成分芍药苷含量变化为-0.8%~0.4%,整体呈下降趋势;酒制前后指标性成分芍药苷含量变化为-0.8%~0.1%,整体也呈下降趋势。
聚类分析结果与主成分分析结果互相印证,即B1、B2、B3、B6聚为一类,B4、B5、B7聚为一类,B8、B9、B10聚为一类。由此可知,虽然产地一致,但受生长环境等其他因素影响,白芍饮片的质量也有差异。主成分分析结果与白芍不同炮制品共有峰相对峰面积差异分析结果基本一致,色谱峰1(没食子酸)、3(芍药内酯苷)、5、6(五没食子酰葡萄糖)、7、8、9、10对炮制前后化学成分差异的贡献较大,与白芍生品相比较,炒白芍和酒白芍的1号峰、3号峰、6号峰的相对峰面积均有不同程度的增加,其中1号峰具有显著性差异;2号峰、8号峰、9号峰的相对峰面积均有不同程度的减小,其中8号峰和9号峰有显著性差异;炒白芍中7号峰的相对峰面积也出现显著性减小。
芍药内酯苷具有镇静、镇痛、抗惊厥及护肝等作用[9]。炒白芍、酒白芍与白芍相比,寒性减弱,镇痛能力增强,推测其与芍药内酯苷的含量增加有一定的关系。
