一种混酸槽液的分析方法研究
2022-06-14吕淑芳郑付华
吕淑芳,郑付华
(成都航利实业有限公司,四川 成都 611930)
目前,随着新装备修理能力的不断发展,为适应新装备维修保障的需要,开发了大量表面处理新工艺,硝酸、氢氟酸的混酸溶液作为新开发的腐蚀检查溶液,其分析方法无参考依据。而本文提出的分析方法,不仅能够填补此溶液无分析方法的空白,解决此溶液只能通过换新来满足工艺要求的弊端,而且能够对表面处理现场使用的硝酸、氢氟酸的溶液提供技术支撑,增强整个表面处理的槽液使用控制能力。
本文重点分析了混酸溶液中氢氟酸的分析原理及方法,且测试结果准确可靠。
1 原 理
在卤素元素中,最不易测定的就是元素氟。但是氟离子F-和氯离子Cl-能与Pb2+生成在水溶液中性条件下生成白色沉淀PbClF[1]。通过测定Cl-来间接测定F-。由于PbClF形成分子式的比值为Pb2+:Cl-:F-=1:1:1,溶解后Cl-是一种可测定的物质,加入硝酸银标准溶液生成氯化银沉淀,过量的硝酸银选择铁铵钒做指示剂,利用KCNS返滴定[2]。
1.1 PbClF的定性检测
(1)加水100 mL至300 mL烧杯中。
(2)加入氯化钠2 g,加入氟化纳2 g,搅拌至完全溶解。
(3)加入硝酸铅20 g,搅拌使之完全反应,水浴加热,温度80~90 ℃,20 min,冷却,静置1 h。
(4)静置后过滤,用去离子水清洗7~8次,将沉淀物移入500 mL烧杯中,加入100 mL去离子水,用玻璃棒充分搅拌,让 PbClF充分溶解。过滤后(不冲洗)弃去沉淀,滤液保留,往滤液中加入1滴0.1 mol/L硝酸银溶液,观察是否有白色沉淀产生,如果没有,过量加入1 mL的0.1 mol/L硝酸银溶液,如果此次仍旧没有白色沉淀产生,则证明PbClF的溶解度小于0.2 mg/L,满足重量分析的要求。
(5)计算
PbClF溶解度<硝酸银定性含量<2×10-4mg。
(6)数据计算

PbClF溶解度<1.25×10-5g/L<2×10-4g/L
式中:MPbClF=251.7
10-3×0.1×0.05——硝酸银物质的量
0.01——溶液体积
0.2 mg——重量分析的沉淀溶解的上限值
试验证明: PbClF的溶解度小于0.2 mg/L,满足重量分析的要求。
1.2 试验方法的可靠性分析
1.2.1 氟化钠作为氢氟酸的标液
由于硝酸溶液和氢氟酸溶液的百分含量是一个较大的范围值,因此不能配制和槽液一样的标准液,因此选择氟化钠作为氢氟酸的标液,来验证方法的可靠性。
经查[3],氟化纳的溶解度为20 ℃/4.06 g,30 ℃/422 g,其分子量为49.99。
试验方法如下:
(1)称取0.4199 g氟化纳溶解于100 mL容量瓶中,其浓度为0.1038 mol/L。
(2)依次称取10 mL氟化纳标准溶液于1#、2#、3#、4#、5#、6#烧杯中,分别加水80 mL。
(3)加入氯化钠1.5 g搅拌溶解完全,在搅拌的情况下加入2.5 g Pb(NO3)2,使之完全溶解并与F-和Cl-生成沉淀,水浴加热,温度80~90 ℃,20 min,冷却,静置1 h。1 h后过滤,用热水洗涤3~4遍,滤液弃之。
(4)将滤纸和沉淀一起转移到300 mL(1#、2#、3#、4#、5#、6#)烧杯中,加水10 mL,加浓硝酸20 mL,搅拌使沉淀完全溶解,分别准确加入25 mL硝酸银标准溶液,搅拌均匀。
(5)待反应完全后过滤,用少量去离子水洗涤3~4遍,收集滤液(这时滤液中只含有硝酸和硝酸银),在滤液中加入铁铵钒指示剂1 mL,用0.1 mol/L KCNS返滴定其中的硝酸银至溶液出现稳定的微红色为终点。
(6)空白实验:使用的去离子水中的氯离子≤0.05 mg/L,因此可以将空白值设为0。
试验数据如表1所示。
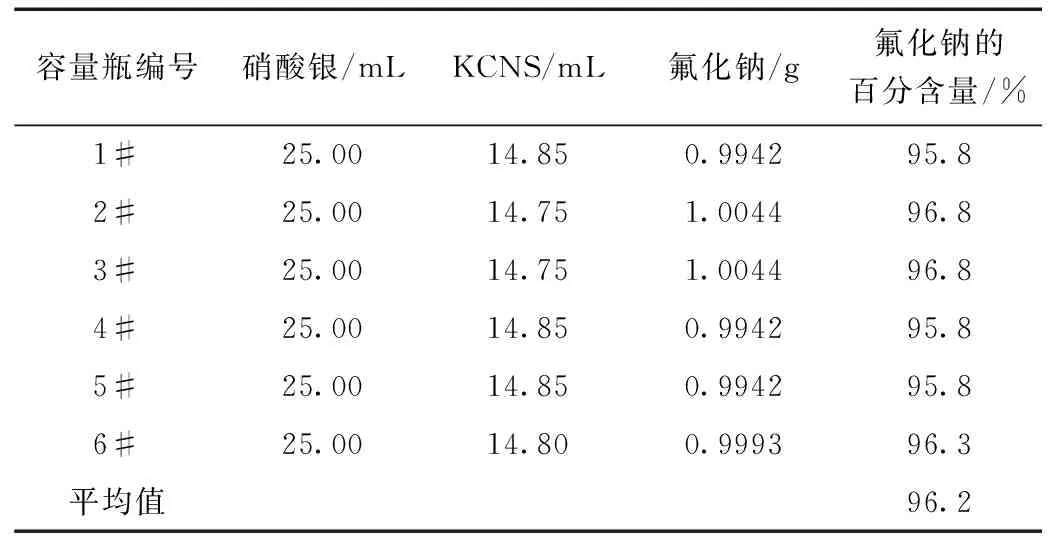
表1 试验数据(氟化钠)
由表1可知,氟化纳(分析纯)的百分含量大于98%,实验结果为96.2%,因此实验结果略小于理论数值,其主要原因在于氟化纳没有基准物质因此需选用一种基准物质代替氟化纳。
1.2.2 氯化钠作为氢氟酸的标液
选择以氯化钠工作基准物质试剂替代氟化纳。同理,Pb2+:Cl-:F-=1:1:1。利用测定氟氯化铅中氯离子的含量来测定氟离子[4]。试验步骤如下:
(1)称取0.5932 g已烘干的工作基准试剂氯化钠,溶解于100 mL容量瓶中,摇匀,其浓度为0.1015 mol/L。
(2)取氯化钠标准溶液10 mL于300 mL烧杯中,加水50 mL加入2 g氟化纳,搅拌均匀,在搅拌的过程下加入Pb(NO)23 g使之完全溶解并与F-和Cl-生成沉淀,水浴加热,温度80~90 ℃,20 min,冷却静置1 h。1 h后过滤,用热水洗涤3~4遍,滤液弃之。将滤纸和沉淀一起转移到300 mL烧杯中,加水10 mL,加入浓硝酸20 mL,充分搅拌,使PbClF溶解,静置5 min后再充分搅拌,确保 PbCIF全溶解。
(3)在上述烧杯中准确加入硝酸银标准溶液25 mL,搅拌均匀,待反应完全后过滤,用少量去离子水洗涤3~4遍,收集滤液,在滤液中加入铁铵钒指示剂1 mL,用0.1 mol/L KCNS返滴定其中的硝酸银至溶液出现稳定的微红色为终点。
(4)空白实验:使用的去离子水中的氯离子≤0.05 mg/L,因此可以将空白值设为0。
试验数据如表2所示。
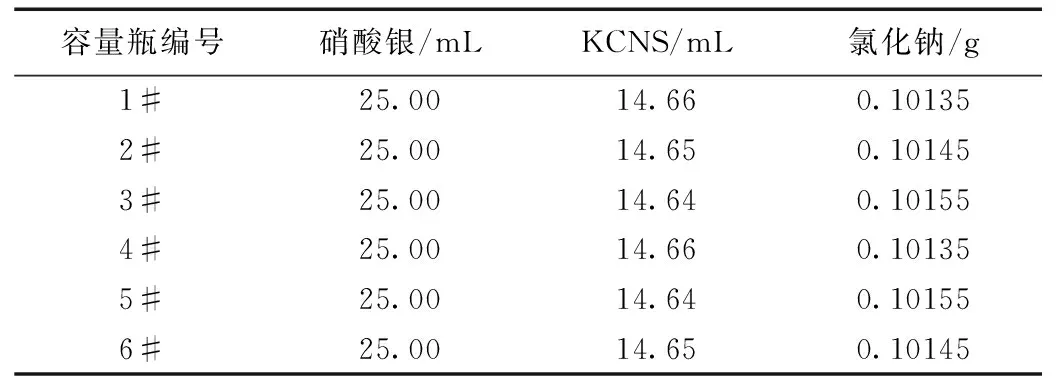
表2 试验数据(氯化钠)
由表2可知,氯化钠工作基准试剂中氯化钠的百分含量为99.95%~100.05%,虽然我们有两个测定值不在范围内,但误差仍然远远小于1‰。试验结果合格,证明了方法的可靠性。
2 氢氟酸的测定
2.1 样品,试剂与设备
硝酸:127~169 mL/L、氢氟酸:120~130 mL/L。
硝酸银标准溶液、氯化钠标准溶液、氯化钠工作基准试剂、铁铵矾指示剂、硫氰化钾。
电子秤、烧杯、漏斗、水浴锅、电位滴定仪。
2.2 测定方法
(1) 取1 mL混酸溶液,加水50 mL,使用电位滴定仪,选择pH挡用0.1 mol/L的氢氧化钠中和至pH为7.0~7.4之间为终点。
(2) 加入氯化钠1.5 g,搅拌至完全溶解,加入硝酸铅3 g,搅拌使反应完全后在,水浴加热,温度80~90 ℃,20 min,冷却静置1 h后过滤,用热水洗涤3~4遍,滤液弃之。将滤纸和沉淀一起转移到300 mL烧杯中,加水10 mL,加入浓硝酸20 mL,充分搅拌,使PbClF溶解,静置5 min后再充分搅拌,确保PbClF完全溶解。
(3) 在上述烧杯中准确加入硝酸银标准溶液45 mL,搅拌均匀,待反应完全后过滤,用少量去离子水洗涤3~4遍,收集滤液。在滤液中加入铁铵钒指示剂1 mL,用0.1 mo/L KCNS返滴定其中的硝酸银至溶液出现稳定的微红色为终点。其主要反应如下[5]:
HF+NaOH=NaF+H2O
Pb(NO3)2+NaF+NaCl=PbFClF↓+2NaNO3
PbClF+2HNO3=Pb(NO3)2+HF+HCl
Cl-+Ag+=AgCl↓
Ag++CNS-=AgCNS↓
Fe3++6KCNS=K3Fe(CNS)6(红色)+3K+
(4) 计算公式
其中:C1——硝酸银溶液的浓度,mol/L
V1——硝酸银溶液的体积,mL
C2——KCNS溶液的浓度,mol/L
V2——KCNS溶液的体积,mL
20——HF的分子量
其中:1.14——HF的比重
40%——HF的百分含量
3 结 论
本文建立了混酸中氢氟酸的测定方法,通过向溶液中加入氯化钠,测定溶液中的氯离子的含量间接测定氟离子的含量,从而得出混酸溶液中氢氟酸的含量。其方法操作简单,数据可靠,填补此溶液无分析方法的空白,解决此溶液只能通过换新来满足工艺要求的弊端,大大提高了此类溶液的管控能力。
