锂皂石/壳聚糖纳米复合支架的制备及相关生物学性能的初步研究*
2022-05-29樊雪敏郭安捷陈志兴莫水学方善宝
樊雪敏,徐 雯,郭安捷,陈志兴,莫水学△,方善宝△
(1.广西医科大学附属口腔医院,南宁 530021;2.广西口腔颌面修复与重建研究自治区级重点实验室,南宁 530021;3.广西颅颌面畸形临床医学研究中心,南宁 530021;4.颌面外科疾病诊治研究重点实验室广西高校重点实验室,南宁 530021)
慢性牙周病引起牙周组织破坏,造成牙槽骨缺损,长期缺牙继发牙槽骨废用性吸收等是临床口腔治疗中常见的疑难问题[1]。近年来,骨组织替代材料如人工骨粉在牙槽骨缺损修复中取得了较好的成骨效果,但目前骨粉价格较高,诱导成骨效果欠佳,机械性能不足,且伴有成骨后骨再吸收等问题,使得人工骨粉的临床应用受到一定限制[2]。因此,采用组织工程学技术,研究更经济实惠且成骨效果优良的骨替代支架材料仍在探索中。
复合材料是指通过物理或化学方法,从分子水平上复合两种或两种以上不同性质的成分,合成具有不同功能的新型材料。纳米复合材料指的是复合材料中添加了具有纳米尺寸(直径小于100 nm)的材料。纳米粘土锂皂石(laponite,LAP)是一种人工合成的层状硅酸盐材料,由直径约为25 nm、厚度为1 nm 的层状圆盘纳米颗粒组成,是一种具有高孔隙率、高比表面积和大长径比等优点的纳米材料[3-4]。Laponite-XLG 可形成凝胶级产品的成品锂皂石之一,具有高纯度、低重金属及低微生物含量等特性,易溶于水,可与其他成分相互作用生成新的纳米复合物,被证明具有促进成骨的作用效果[5-8]。
壳聚糖(chitosan,CS)是一种天然带正电荷的碱性多糖,具有良好的生物相容性、抗菌性和可降解性,被广泛研究应用于支架材料、伤口愈合等领域[9-11]。基于LAP和CS在成骨领域表现出的优秀潜能,本研究拟构建LAP/CS纳米复合支架载体,分析其理化性能表征,以人牙周膜干细胞作为种子细胞,观察LAP/CS 纳米复合支架对细胞的黏附能力及细胞毒性,探讨其后期应用于牙槽骨组织工程修复的可行性。
1 材料与方法
1.1 纳米复合支架的制备
使用原位聚合法和冷冻干燥法制备LAP/CS纳米复合支架。CS 溶于1 wt%的乙酸溶液中,获得2%CS溶液。将不同质量的LAP粉末溶于纯水中,分别制取1 wt%、3 wt%、5 wt%、7 wt%、10 wt%的LAP 溶液。在CS溶液中缓慢加入不同浓度的LAP溶液,磁力搅拌器搅拌混匀。将LAP/CS 溶液浇铸在直径15 mm、高度2 mm 的圆柱形模具中,振荡30 min,置于-20 ℃冰箱中冷冻过夜。使用冷冻干燥机将材料在低温、真空状态下进行冷冻干燥。用0.1%NaOH溶液对材料进行中和,去离子水反复清洗以去除多余的盐分,再次冻干备用。
按不同LAP 浓度进行分组,即CS 组(未添加LAP)、1% LAP/CS 组、3% LAP/CS 组、5% LAP/CS组、7% LAP/CS 组、10% LAP/CS 组,同时设未添加支架材料的空白对照组。
1.2 人牙周膜干细胞的分离培养
收集因正畸治疗需要被拔除的离体前磨牙{伦理审查编号:2018 年伦申[科]第(914)号}。患者纳入标准:(1)无牙周系统疾病,牙齿无龋坏,无根尖病变;(2)牙齿被完整拔除;(3)年龄12~18 岁。本研究所有患者及家属均知情同意。采用组织块法[12]分离培养人牙周膜干细胞(human periodontal ligament stem cells,hPDLSC),进行细胞传代,取第3 代hPDLSC作为种子细胞用于后续实验。
1.3 纳米复合支架的理化性能检测
1.3.1 形貌观察 将制备好的各组材料进行喷金镀膜,用扫描电镜(SEM,日本,Hitachi SU8220)观察材料表面形态结构。
1.3.2 材料元素分析 X 线能谱分析(energy dispersive X-ray,EDX)观察材料的硅、镁、氧、钠等元素的分布情况。
1.3.3 支架材料的吸水性 每组支架材料采用专用模具制备成直径为15 mm、高度为2 mm 的圆柱形材料,称量干燥的支架重量,记为Wd,浸泡于5 mL去离子水中,次日取出,用滤纸吸干表面水分,称量支架的湿重,记为Ws。计算支架的吸水率,即(Ws-Wd)/Wd×100%。
1.3.4 支架材料的降解率 取各组制备好的支架材料,用万分之一天平进行称重,初始质量记为W1;然后将支架材料浸泡于5 mL PBS 溶液中,37 ℃、100 r/min 持续振摇,去离子水冲洗,冷冻过夜、干燥,用万分之一天平进行称重,质量记为W2。计算材料的降解率,即(W1-W2)/W1×100%。
1.3.5 支架的细胞毒性 首先制备LAP/CS支架材料的浸提液:在超净工作台中将消毒好的支架材料置于无菌12孔板中,加入细胞培养基,37 ℃培养箱中静置过夜,即可得到材料的浸提液。取hPDLSC,按2×103个/孔的密度接种在96 孔板中,分组处理后,培养24 h,加入浸提液,空白对照组仅加入含10%血清的普通培养基,在细胞培养箱中静置培养。分别在1 d、3 d、5 d、7 d采用CCK8法检测支架材料对hPDLSC的毒性,用酶标仪检测450 nm处各孔的吸光度(OD)值。
1.3.6 支架对细胞的黏附能力 取hPDLSC,按2×104个/孔的密度接种于LAP/CS纳米复合支架上,细胞培养箱中静置培养2 h后加入培养基。次日去除培养基,PBS 清洗,胰蛋白酶消化、计数。计算细胞黏附率,即黏附细胞数/接种细胞数×100%。
细胞接种后置于细胞培养箱中静置培养24 h,去除培养基,PBS清洗,4%多聚甲醛固定30 min,置于-20 ℃冰箱中,次日使用冷冻干燥机进行干燥,喷金镀膜后在电镜下观察细胞在材料上的黏附情况。
1.4 统计学方法
采用SPSS 24.0 统计软件分析数据。计量资料以均数±标准差(±s)表示,组间比较采用独立样本t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 支架形貌
肉眼观察(图1)各组支架,表现为多孔海绵状结构,CS 组颜色较LAP/CS 组偏黄,呈黄白色。LAP/CS组支架呈白色疏松多孔的海绵状结构。电镜观察支架的表面形态(图2),各组支架均表现为疏松多孔结构,各孔隙之间相互连通。

图1 不同支架形貌大体观

图2 电镜观察LAP/CS支架形貌(×200)
2.2 EDS元素分析
各组支架分布着氧、钠、镁、硅等元素。CS组大部分为氧元素,几乎不含镁、硅元素。LAP/CS各组镁、硅元素含量较高。各组材料元素的平面分布见图3。

图3 元素分布平面图
2.3 支架材料的吸水率与降解率
CS 组吸水率和降解率最高,随着LAP 含量升高,支架材料的吸水率和降解率均下降;CS 组吸水率超过600%,其余各组吸水率均低于CS组;在18 d时CS 组、LAP/CS 组、3% LAP/CS 组、5% LAP/CS组、7% LAP/CS 组、10% LAP/CS 组降解率分别为12.96%、9.96%、9.56%、8.62%、7.05%、6.85%,见图4。
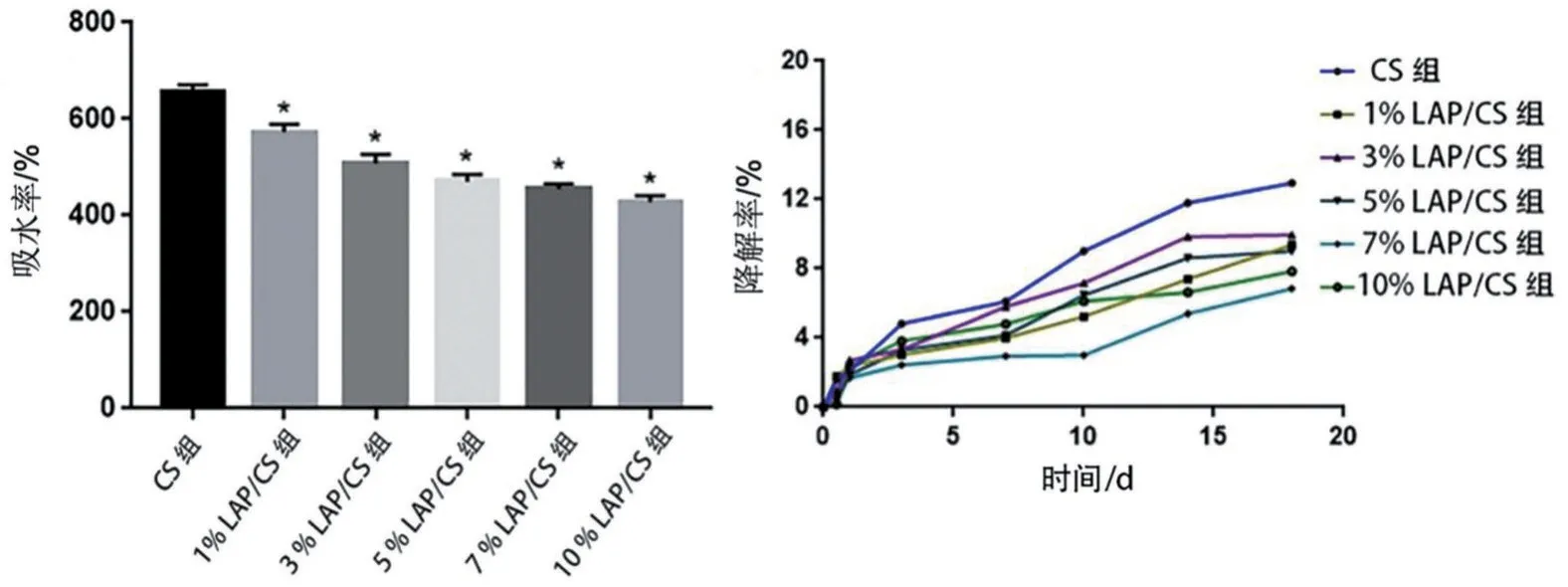
图4 支架材料吸水率和降解率
2.4 支架材料的细胞相容性
2.4.1 各组支架材料对hPDLSC 的毒性 在1 d、3 d、5 d、7 d 时各组OD 值比较,差异无统计学意义(P>0.05),表明各组支架材料无细胞毒性,见图5。

图5 CCK8细胞毒性检测
2.4.2 细胞黏附能力 扫描电镜下可见CS 组支架孔径较小,表面黏附凝聚成团状的细胞;添加了LAP的支架孔径相对较多,在孔径之间的材料表面可见细胞均匀分散,局部可见细胞聚集成团,亦可见多处单个细胞分布,细胞的分散性优于CS 组。1% LAP/CS 组、3% LAP/CS 组、5% LAP/CS 组细胞较少且分散,而7%LAP/CS组、10%LAP/CS组细胞较多且密集。
1% LAP/CS 组细胞黏附率为72.22%,低于CS组的86.11%;5% LAP/CS 组和7% LAP/CS 组细胞黏附率分别为94.44%和97.22%,均高于CS 组;3%LAP/CS 组、10% LAP/CS 组细胞黏附率分别为88.89%、90.02%,与CS 组比较差异无统计学意义,见图6。

图6 细胞黏附情况
3 讨论
支架材料修复组织缺损时承担恢复缺损组织形态,提供临时机械性能和传递生物因子等作用[13]。具有多孔结构的支架材料可提供细胞黏附生长的空间,有利于细胞的黏附和迁移,为细胞外基质的形成提供模板,也为再生的组织提供结构支持[14]。本研究中,添加了LAP 的支架具有网格状的结构,这种网格状结构提供了种子细胞生长和黏附的空间。
镁元素被证明与骨的代谢密切相关,Mg2+可通过多种途径影响成骨与破骨的作用[15]。Mg2+可通过多种途径调控成骨分化,包括增强细胞的黏附和增殖功能,促进细胞的成骨分化[16-17]。研究表明,以LAP 制备的支架材料在作用过程中可缓慢释放一定量的Mg2+,通过Mg2+激活细胞成骨分化,从而促进成骨效果[18]。本研究结果表明,LAP/CS支架含有镁元素,进一步提示本实验构建新型支架材料可能具有诱导干细胞成骨分化的潜能。
良好的吸水性可充分保证支架材料对培养基及生长因子等物质的吸附能力,为细胞在材料上生长及植入体内提供有利的条件[19]。CS 基复合材料可维持较高的吸水率,同时延缓材料的降解率,提高机械性能,如CS-纳米羟基磷灰石、CS-明胶复合物等[20-21]。CS 组支架表现出较高的吸水率,添加LAP 后复合支架的吸水率稍有降低,但仍保持在400%以上,表明LAP/CS 支架仍具有良好的吸水性。
骨组织工程支架材料的降解率与成骨的过程密切相关,过快的降解速率无法为新骨的形成提供支持作用,过慢的降解率则可能会限制新生骨组织的生长空间[22-23]。本研究材料降解实验证明LAP/CS支架材料在18 d时的降解率约10%左右,为缓慢降解型材料。CS组降解率较添加了LAP的各组降解率稍快,可能原因是LAP 与CS 相互作用形成的三维多孔结构具有较高的稳定性,使其降解速率降低。LAP/CS 支架的降解率较低,可能导致在体内成骨过程中影响新生骨组织的生长。
良好的生物安全性和细胞相容性是支架材料最基本的性能要求。本研究CCK8 实验证明LAP/CS纳米复合支架无细胞毒性,细胞黏附实验和扫描电镜观察均可证明LAP/CS支架具有良好的细胞黏附能力,表明支架具有较好的细胞相容性。
综上,LAP/CS 纳米复合支架的制备方法较为简单,具有多孔结构,良好的吸水性,含成骨相关的微量镁元素,体外细胞实验证明LAP/CS 支架具有良好的细胞相容性,具备成骨诱导支架材料的结构基础。但该支架材料的降解率较低,仍待进一步研究如何改良支架材料的降解率,以提升支架的骨传导性能。
