4种评分系统对HBV相关慢加急性肝衰竭合并食管胃底静脉曲张出血患者短期预后的评估价值
2022-05-12王爱民梅雪郭红英袁伟张宇一钱志平王介非刘玉
王爱民 梅雪 郭红英 袁伟 张宇一 钱志平 王介非 刘玉
慢加急性肝衰竭(acute-on-chronic liver failure,ACLF)是指在慢性肝病基础上,由各种诱因引起的。以急性黄疸加深、凝血功能障碍为肝衰竭表现的综合征,可合并包括消化道出血、肝性脑病、腹水、感染、肝肾综合征等并发症。在我国ACLF患者的病因主要是乙型肝炎病毒(hepatitis B virus,HBV)感染,其中在肝硬化基础上的ACLF患者常常合并门静脉高压食管胃底静脉曲张破裂出血(esophageal gastric variceal bleeding, EGVB),是导致其死亡的主要原因之一。研究哪种评分对HBV相关慢加急性肝衰竭并发EGVB的预测更准确,对患者进行早期预警和指导治疗均意义重大。本研究回顾性分析HBV相关慢加急性肝衰竭合并EGVB患者的短期预后,进一步探讨LSPS、ALBI、MELD及CTP评分系统的预测价值。
资料与方法
一、研究对象
选取上海市公共卫生临床中心2018年12月18日至2021年9月6日收住入院的HBV相关慢加急性肝衰竭患者。诊断标准符合《肝衰竭诊治指南(2018年版)》[1]。入组标准:符合 HBV相关慢加急性肝衰竭诊断标准,经内镜检查证实为 EGVB。排除标准:①年龄<18 岁或>75 岁;②合并其他肝炎病毒感染、酒精、药物、中毒等其他原因导致的肝衰竭;③伴有弥漫性血管内凝血;④心脑梗死非稳定期;⑤伴有肾脏基础疾病引起的肾功能不全;⑥妊娠晚期;⑦由于其他疾病而需要长期抗凝治疗的患者;⑧肝癌或其他恶性肿瘤发生肝脏转移;⑨既往曾行经颈静脉肝内门体分流术、脾脏切除术或联合贲门周围血管离断术者;⑩病例资料缺失者。
二、研究方法
回顾性分析52例患者的人口学特征、临床特征、实验室指标、影像学检查等,并记录患者随访期间的治疗措施以及入组后的生存时间,随访截止时间为2021年9月6日。所有纳入患者均在内科治疗的基础上,出血后立即予以禁食、补充血容量、血管活性药物、预防性使用抗生素等治疗,排除禁忌后行内镜治疗。
三、预后评分系统
计算LSPS、ALBI、MELD及CTP评分并分级。LSPS=肝硬度值×脾脏直径/血小板计数(109/L)[2];ALBI=-0.085 ×[Alb(g/L)]+ 0.66 × lg[TBil(mg/dl)],依据ALBI评分可将其分为3级,1级:≤-2.6,2 级:>-2.6且≤-1.39,3 级:>-1.39[3];MELD=9.57 × ln[Cr(mg/dl)]+ 3.78 × ln[TBil(mg/dl)]+ 11.2 × ln[INR]+ 6.43 × (酒精性、胆汁淤积性为 0,其余为1)[4];根据患者在出血前1周内TBil、Alb、INR的水平以及有无腹腔积液及肝性脑病的相关严重程度,进行CTP评分并分级[5]。
四、统计学方法
采用 SPSS26.0统计学软件进行分析。非正态分布的计量数据采用M(P25,P75)表示,组间比较采用非参数检验;正态分布的计量数据以均数±标准差表示,组间比较采用t检验;计数资料以例数(百分比)表示,组间比较采用卡方检验。采用ROC曲线下面积(AUC)评估4种评分系统的预测效能。P<0.05为差异有统计学意义。
结 果
一、死亡组和存活组基本特征、实验室指标比较
随访期间,28 d死亡患者17例(32.69%),存活35例(67.31%)。90 d死亡22例(42.31%),存活30例(57.69%)。入组患者男性46例(88.46%)。28 d死亡组TBil、门静脉内径、脾直径、肝性脑病、肝肾综合征、感染等指标高于存活组,且差异有统计学意义(均P<0.05);其他指标两组差异无统计学意义(均P>0.05)。见表1。
二、28 d死亡组和存活组评分的比较
死亡组ALBI、MELD、CTP评分高于存活组,ALBI和CTP分级低于存活组(P<0.05),LSPS评分两组差异无统计学意义(P>0.05)。见表2。
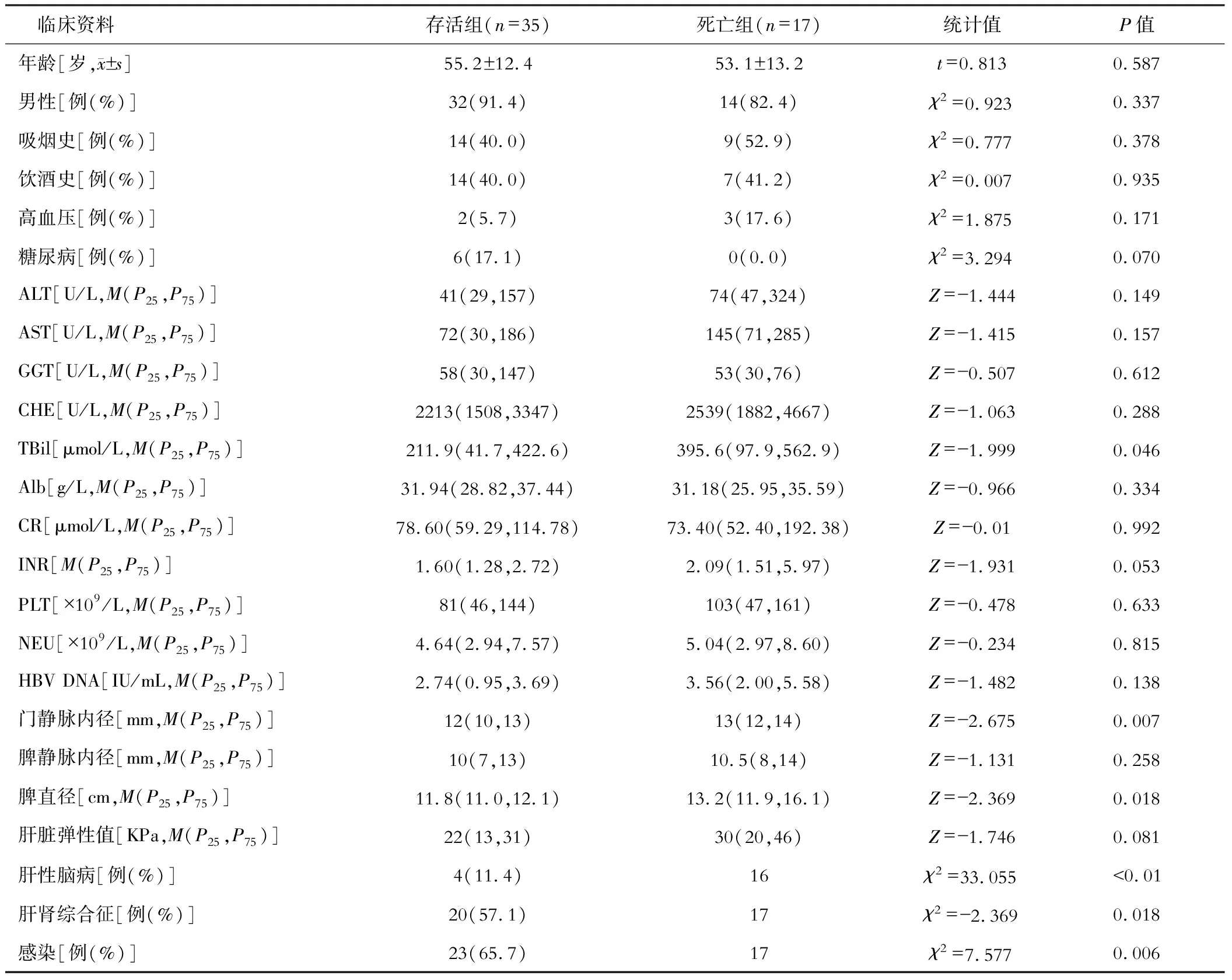
表1 28 d死亡组与存活组临床资料比较

表2 存活组和死亡组评分比较
三、4种评分系统对28 d和90 d死亡风险的预测效能比较
28 d死亡风险的ROC曲线分析显示,LSPS评分、ALBI评分、MELD评分及CTP评分ROC 曲线下面积分别为0.533(95%CI: 0.368~0.698),0.620(95%CI: 0.457~0.782),0.664(95%CI: 0.505~0.823),0.848(95%CI: 0.731~0.964),CTP评分对HBV相关慢加急性肝衰竭并发EGVB患者28 d的预测效能最好。
90 d死亡风险的ROC曲线分析显示,LSPS评分、ALBI评分、MELD评分及CTP评分ROC 曲线下面积分别为0.633(95%CI: 0.478~0.789),0.586(95%CI: 0.426~0.747),0.656(95%CI: 0.500~0.812),0.805(95%CI: 0.678~0.931),CTP评分对HBV相关慢加急性肝衰竭并发EGVB患者90 d的预测效能较高。
讨 论
我国最为常见的肝衰竭类型系HBV相关ACLF,是在慢性乙型肝炎或乙型肝炎相关肝硬化的基础上短期内急性加重引起的。美国一项研究显示,失代偿期肝硬化患者中,1/4发生ACLF,其中1/4的ACLF患者在28 d内死亡[6]。肝衰竭合并食管胃静脉曲张破裂出血病情更加凶险,1年内的再出血率高达70%[7]。Guo等[8]研究显示,ACLF并发出血事件时血小板减少、纤维蛋白原降低。代琴棋等[9]研究显示,ACLF合并上消化道出血时并发症(包括肝性脑病、肝肾综合征)的发生率、胃底静脉曲张、纤维蛋白原降解产物、门静脉宽度等指标差异显著。本研究显示与存活组比较,死亡组TBil、门静脉内径、脾直径、并发症的发生率、ALBI、MELD及CTP评分明显偏高,与既往研究一致。
随着影像检查的开展,LSPS评分作为一种无创手段评估食管胃底静脉曲张程度和门静脉高压。文献报道,LSPS评分是一种无创并准确的判断慢性肝病患者食管静脉曲张的指标[10-11]。但本研究显示LSPS评分无法预测HBV相关ACLF并发EGVB患者28 d和90 d死亡风险,可能与纳入的病例数偏少有关。
ALBI评分是一种新型肝功能评估模型,研究发现其与多种慢性肝病的预后相关[12-13]。Liu等[14]研究显示ALBI评分可较好地预测ACLF患者28 d病死率,而MELD评分预测性较差。Li等[15]研究显示ALBI评分、MELD评分均可准确预测HBV-ACLF 30 d和90 d的病死率。Lei[16]的研究显示,ALBI分级是评估HBV相关终末期肝病患者严重程度的一种简单适用的方法,与CTP和MELD评分呈现平行趋势。Xavier等[17]研究显示,肝硬化合并上消化道出血患者,ALBI评分可准确预测住院和30 d病死率,而CTP和MELD评分不能预测。Zou等[18]研究显示,ALBI、CTP和MELD评分均能很好预测肝硬化急性胃肠出血住院病死率。Voicu等[19]回顾性分析367例肝硬化静脉曲张出血患者发现 MELD评分是病死率唯一预测因子。美国15个中心的一项静脉曲张出血的肝硬化队列研究显示,CTP评分在预测6周病死率方面效能优于MELD评分[5]。Yang等[20]一项系统回顾和荟萃分析显示在确定急性静脉曲张出血的患者在医院的高死亡风险方面,CTP优于其他风险评分。本研究显示,CTP评分的预测效能优于LSPS、ALBI和MELD评分。
本研究系单中心、小样本、回顾性研究。今后进一步开展包括基因组学、蛋白质组学、代谢组学等多组学研究以及联合并发症的评分系统,有可能提高该类患者早期死亡风险预测的准确性。
综上所述,HBV-ACLF并发EGVB患者,CTP评分预测短期预后效能最佳。临床需早期评估患者预后,积极探索该类患者的临床特征,早期给予卡维地洛改善短期预后[21],条件允许早期行胃镜检查或干预,尽早建议患者行肝移植挽救生命。
