变换波长高效液相色谱法测定茵栀黄口服液中防腐剂的含量
2022-04-29王云霞张苗苗谢志民
王云霞,张苗苗,谢志民
茵栀黄口服液是2019年国家评价性抽检品种,具有清热解毒,利湿退黄,用于肝胆湿热所致的黄疸,症见面目悉黄、胸肋胀痛等;由茵陈提取物12 g、栀子提取物6.4 g、黄芩苷40 g 和金银花提取物8 g按照工艺制成1 000 mL,质量标准中制法项规定添加有0.3%的苯甲酸钠作为防腐剂[1],以防止茵栀黄口服液在储存过程中发生霉变,2015 年版《中国药典》(四部)通则0181 合剂[2]项下规定苯甲酸的用量不得超过0.3%,添加防腐剂过少起不到防腐作用,口服液在储存过程中会变质,添加过量防腐剂,容易导致人体摄入防腐剂过多,会对人体造成一定危害,过量摄入苯甲酸和苯甲酸钠,会造成肝毒性及肾毒性,有研究表明还会造成染色体分裂异常甚至致癌,故苯甲酸和苯甲酸钠的过量摄食是不合适的[3],这就必须严格控制工艺,严格控制处方中的加入量,防止少加,多加及乱加别的防腐剂,才能保证药品的安全有效。
目前检测防腐剂方法主要有高效液相色谱法[4-12]和高效液相色谱-质谱联用法[13]。高效液相色谱-质谱联用法所用仪器较昂贵,不易普及,为了满足普通实验室的检测需求,本实验拟采用变换波长高效液相色谱法,筛选出6种防腐剂作为目标物,并对来自全国抽检的32 批次茵栀黄口服液进行相关检测,为茵栀黄口服液的安全性评价提供一定的参考依据。
1 材料与方法
1.1 材料
1.1.1 仪器 1260 型高效液相色谱仪(美国Agilent科技有限公司);SPD-M10AVP 二极管阵列检测器(日本岛津公司);BT124S 型电子分析天平(北京赛多利斯仪器有限公司)。
1.1.2 药品与试剂 32 批次样品均为国家评价性抽检样品,均来自于北京华润高科天然药物有限公司(独家产品,最早生产批号2721247,生产日期是2017 年10 月;最晚生产批号181216,生产日期是2018年12月,1个规格:10毫升/支,服用剂量为一次10 mL)。
苯甲酸对照品(中国食品药品鉴定研究院,批号100419-201703,含量99.9%)、山梨酸钾对照品(中国食品药品鉴定研究院,批号101075-201602,含量99.7%)、羟苯甲酯对照品(中国食品药品鉴定研究院,批号100278-201705,含量100.0%)、羟苯乙酯对照品(中国食品药品鉴定研究院,批号100847-201604,含量99.9%)、羟苯丙酯对照品(中国食品药品鉴定研究院,批号100444-201804,含量99.6%)、羟苯丁酯对照品(中国食品药品鉴定研究院,批号110792-200503,含量100.0%);乙腈、甲醇均为色谱纯,水为超纯水,其他试剂均为分析纯。
1.2 方法
1.2.1 色谱条件色谱柱:Agilent C18(250 mm×4.6 mm,5µm);流动相:甲醇(A)-0.02 mol/L磷酸二氢钠溶液(B)(用磷酸调pH值3.7)(V/V),梯度洗脱(洗脱程序详见表1);流速:1.0 mL/min;柱温:30 ℃;紫外检测器;苯甲酸以228 nm 为检测波长,山梨酸、羟苯甲酯、羟苯乙酯、羟苯丙酯及羟苯丁酯以255 nm 为检测波长;进样体积10µL。
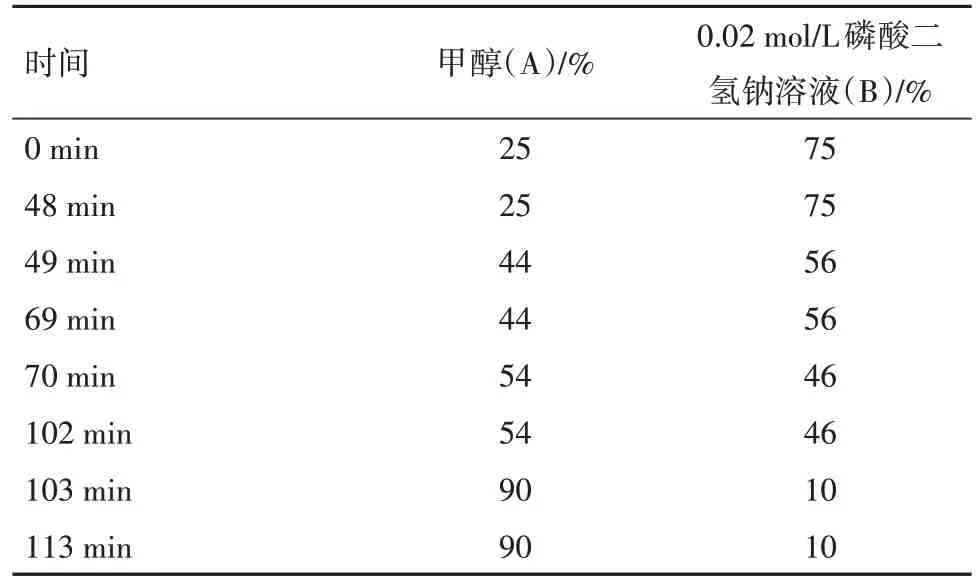
表1 梯度洗脱顺序
1.2.2 溶液的制备
1.2.2.1 对照品溶液的制备精密称取苯甲酸、山梨酸钾、羟苯甲酯、羟苯乙酯、羟苯丙酯、羟苯丁酯适量,分别加50% 甲醇制成240、80、10、10、10、10 mg/L的溶液,即得。
1.2.2.2 供试品溶液的制备精密吸取样品1 mL,置50 mL 量瓶中,加50%甲醇稀释至刻度,摇匀,用微孔滤膜滤过,取续滤液即得。
1.2.3 系统适用性试验精密称取山梨酸钾对照品215.24 mg、羟苯甲酯对照品22.88 mg、羟苯乙酯对照品22.72 mg、羟苯丙酯对照品19.88 mg、羟苯丁酯20.88 mg,置同一50 mL 量筒中,加茵栀黄口服液(批号181206)使溶解至40 mL,摇匀,即得茵栀黄口服液模拟阳性样品,精密吸取茵栀黄口服液模拟阳性样品、茵栀黄口服液阴性样品(未加防腐剂),分别按照“1.2.2.2”项下制备茵栀黄口服液模拟阳性样品供试品溶液及茵栀黄口服液阴性样品供试品溶液。精密吸取以上2 种溶液及“1.2.2.1”项下对照品溶液,按“1.2.1”项下条件进行测定,记录色谱图。结果,相邻色谱峰的分离度均大于1.5;苯甲酸的理论塔板数为20 655、山梨酸的理论塔板数为20 417、羟苯甲酯的理论塔板数为19 988、羟苯乙酯的理论塔板数为193 447、羟苯丙酯的理论塔板数为442 048、羟苯丁酯的理论塔板数为165 648;阴性无干扰;同时对生产批号2721247,生产日期为2017 年10月;生产批号272538,生产日期为2018年4月;生产批号272848,生产日期为2018 年6 月的三批次产品也做了加标模拟阳性试验,目标峰与杂质峰均能很好分离且无干扰。以二极管阵列检测器测定,茵栀黄口服液模拟阳性样品中6种防腐剂色谱峰的紫外吸收图谱与对照品溶液色谱峰的紫外吸收图谱一致。结果见图1。
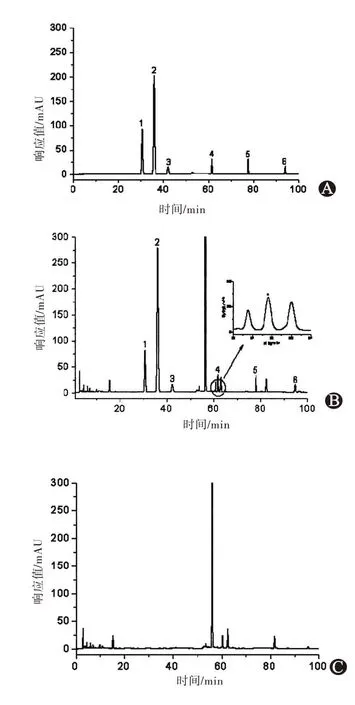
图1 茵栀黄口服液HPLC图:A为对照品,B为模拟阳性样品,C为阴性样品
1.2.4 方法学考察
1.2.4.1 线性关系考察精密称取羟苯甲酯对照品10.18 mg、羟苯乙酯对照品10.02 mg、羟苯丙酯对照品9.97 mg、羟苯丁酯对照品10.29 mg,置同一50 mL量瓶中,加50%甲醇使溶解至刻度,摇匀,作为对羟基苯甲酸酯类的对照品储备溶液;精密称取苯甲酸对照品12.35 mg、山梨酸钾对照品16.14 mg,置同一25 mL 量瓶中,精密加入对羟基苯甲酸酯类的对照品储备溶液10 mL,用50% 甲醇使溶解,并加至刻度,摇匀,作为6 号对照品溶液;精密吸取6 号对照品溶液5 mL,置10 mL 量瓶中,加50%甲醇稀释至刻度,摇匀,作为5 号对照品溶液;精密吸取5 号对照品溶液5 mL,置10 mL 量瓶中,加50%甲醇稀释至刻度,摇匀,作为4 号对照品溶液;精密吸取4 号对照品溶液5 mL,置10 mL 量瓶中,加50% 甲醇稀释至刻度,摇匀,作为3 号对照品溶液;精密吸取3号对照品溶液5 mL,置10 mL 量瓶中,加50% 甲醇稀释至刻度,摇匀,作为2号对照品溶液;精密吸取2号对照品溶液5 mL,置10 mL量瓶中,加50%甲醇稀释至刻度,摇匀,作为1 号对照品溶液;精密吸取1号对照品溶液5 mL,置10 mL 量瓶中,加50% 甲醇稀释至刻度,摇匀,作为0号对照品溶液。吸取上述7种不同质量浓度溶液各10µL注入液相色谱仪,按“1.2.1”项下条件进行测定。以进样质量(C,ng)为横坐标、峰面积(A)为纵坐标绘制标准曲线,标准曲线方程和线性范围见表2。

表2 标准曲线方程及线性范围
1.2.4.2 精密度试验精密吸取“1.2.4.1”项下1、3、6 号对照品溶液各10µL,按“1.2.1”项下色谱条件连续进样测定6 次,记录峰面积。结果,6 种防腐剂峰面积的RSD 均小于0.6 %(n=6),表明仪器精密度良好。
1.2.4.3 重复性试验由本实验室的两名实验员取“1.2.3”项下的茵栀黄口服液模拟阳性样品在不同时间按照“1.2.2.2”项下方法制备供试液,用“1.2.4.1”项下3 号对照品溶液作为对照,用不同仪器按“1.2.1”项下条件进行测定,结果6 种防腐剂的含量的RSD 均小于0.90%(n=12),表明该方法的重复性良好。
1.2.4.4 稳定性试验精密吸取“1.2.4.3”项下茵栀黄口服液模拟阳性供试品溶液(第一次实验员制备的供试液),放置0、2、4、8、12、16、20、24 h 后按“1.2.1”项下色谱条件进行测定。结果,6 种防腐剂峰面积的RSD 均小于0.6%(n=8),表明该样品在24 h内有很好的稳定性。
1.2.4.5 加样回收率试验精密称取苯甲酸对照品62.85 mg、山梨酸钾对照品91.64 mg、羟苯甲酯对照品14.13 mg、羟苯乙酯对照品13.08 mg、羟苯丙酯对照品12.48 mg、羟苯丁酯对照品15.37 mg,置同一50 mL 量瓶中,加50%甲醇使溶解至刻度,摇匀,作为加样对照品溶液。精密吸取重复性试验项下的模拟阳性样品1 mL,6 份,分别置100 mL 量瓶中,分别精密加入上述对照品溶液2 mL,加50%甲醇使溶解至刻度,摇匀,用微孔滤膜滤过,取续滤液作为供试品溶液。取“1.2.4.1”项下3 号对照品溶液作为对照,按“1.2.1”项下色谱条件进行测定,结果6种防腐剂平均加样回收率分别为100.69%、98.44%、101.21%、104.18%、103.95%、103.55%,RSD 分别为0.24%、0.29%、0.72%、0.71%、0.44%、0.34%(n=6)结果见表3。
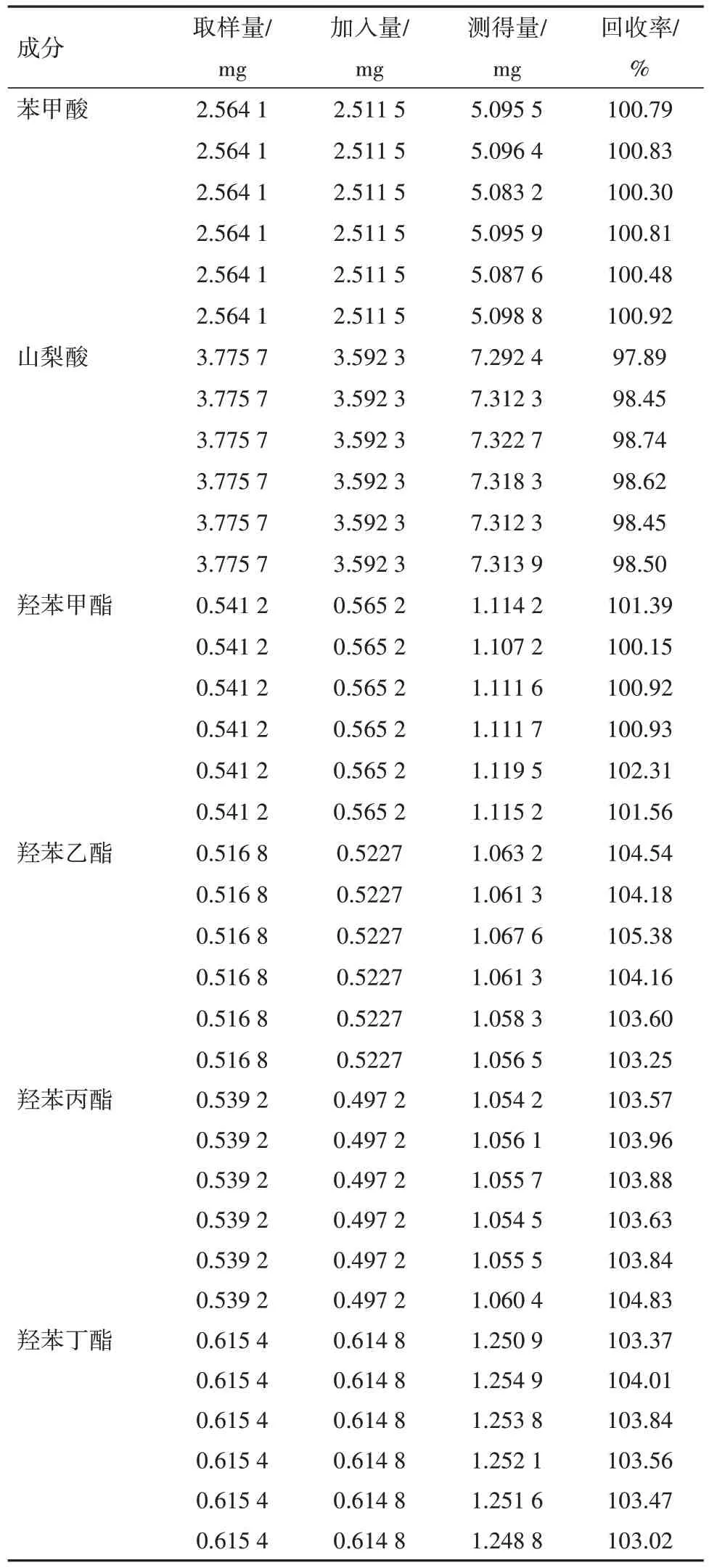
表3 6种防腐剂的回收率测定结果(n=6)
1.2.4.6 最低方法检出限和定量限精密称取羟苯甲酯对照品9.07 mg、羟苯乙酯对照品4.39 mg,置5 mL 量瓶中,加50%甲醇溶解至刻度,摇匀,作为1号储备溶液;精密称取羟苯丙酯对照品7.99 mg、羟苯丁酯对照品6.58 mg、山梨酸钾对照品5.39 mg,置50 mL量瓶中,加50%甲醇溶解至刻度,摇匀,作为2号储备溶液;精密称取苯甲酸对照品8.04 mg,置50 mL量瓶中,精密加入1 号储备溶液3 mL、2 号储备溶液3 mL,加50%甲醇溶解至刻度,摇匀,作为1 号加样对照品溶液。精密量取1 号加样对照品溶液1.5 mL,置5 mL 量瓶中,加水至刻度,摇匀,作为2 号加样对照品溶液。精密量取“1.2.3”项下模拟阴性样品1 mL,4 份,分别置50 mL 量瓶中,分别精密加入上述1号对照品溶液0.7 mL、1.3 mL和2号对照品溶液0.7 mL、1.3 mL,各加50%甲醇至刻度,摇匀,用0.45 µm 滤膜滤过,取续滤液作为定量限和检测限供试品溶液。按“1.2.1”项下色谱条件进行测定,按色谱峰峰高与基线噪声的比值计算,基线噪音3 倍量峰高时的含量为最低检出限、基线噪音10倍量峰高时的含量为最低定量限。结果苯甲酸的最低检出限为0.600 ng,最低定量限为2.400 ng;山梨酸钾的最低检出限为0.015 ng,最低定量限为0.140 ng;羟苯甲酯的最低检出限为0.025 ng,最低定量限为0.330 ng;羟苯乙酯的最低检出限为0.090 ng,最低定量限为0.270 ng;羟苯丙酯的最低检出限为0.010 ng,最低定量限为0.040 ng;羟苯丁酯的最低检出限为0.022 ng,最低定量限为0.080 ng。
2 结果
对抽检的32 批次茵栀黄口服液按照“1.2.2.2”项制备方法制备供试液,按照“1.2.2.1”项浓度配制对照品溶液浓度,按“1.2.1”项色谱条件进行测定,32批均检出苯甲酸,含量范围2.393 0~2.591 9 g/L,32批均未检出其他5种防腐剂。对于苯甲酸限度的确定,根据2015 年版《中国药典》(四部)通则0181合剂项下规定苯甲酸的用量不得超过0.3%,根据茵栀黄口服液处方及工艺,每1 000 毫升加苯甲酸钠3 g,换算为苯甲酸2.54 g,按照工艺偏差±10%计算,暂拟定每1 mL 含苯甲酸钠以苯甲酸计,应为2.29~2.79 mg。
3 讨论
3.1 波长的确定在进行液相色谱法测定时,一般选取目标物的最大吸收波长来进行检测,此时检测灵敏度最高,但在多组分测定时单一波长很难满足测定需求,故选用变换波长法。用二极管阵列检测器通过全波长光谱扫描得出苯甲酸的最大吸收为228 nm,山梨酸的最大吸收为252 nm,羟苯甲酯的最大吸收为255 nm,羟苯乙酯的最大吸收为255 nm,羟苯丙酯的最大吸收为255 nm,羟苯丁酯的最大吸收为256 nm,除苯甲酸外,其余5种成分最大吸收波长差距不大,为了减少变换波长的频次,并且对山梨酸检测波长在252 nm 和255 nm、羟苯丁酯检测波长在256 nm和255 nm下的峰面积进行比较,差异不大,最终进行组合,确定了6种防腐剂的最大吸收,确定了正文中的检测波长。
3.2 色谱条件的确定在预试验中,笔者分别选用了等度洗脱和梯度洗脱两种类型进行试验,等度流动相有甲醇-0.15%乙酸铵(20∶80,V/V)、甲醇-乙腈-0.15%乙酸铵(10∶5∶80,V/V/V),结果是基线较平,出峰过快,苯甲酸和山梨酸色谱峰不能完全分离,达不到改变波长的要求,目标物色谱峰出峰时间漂移。梯度洗脱程序①:流动相(A)甲醇-(B)0.02 mol/L 磷酸二氢钠溶液(用磷酸调pH 值3.5),程序(V/V)0~30 min(A)20%→80%,(B)80%→20%,30~40 min
(A)80%,(B)20% ,梯度洗脱程序②:流动相(A)甲醇-(B)0.02 mol/L 磷酸二氢钠溶液(用磷酸调pH 值3.5),程序(V/V)0~40 min(A)20%→80%,(B)80%→20%,40~50 min(A)80%,(B)20%,结果是山梨酸和羟苯甲酯的色谱峰完全重合,无法分析;梯度洗脱程序③:流动相(A)甲醇-(B)0.02 mol/L 磷酸二氢钠溶液(用磷酸调pH 值3.7),程序(V/V)0~40 min(A)
20%→80%,(B)80%→20%,40~50 min(A)80%,(B)20%,结果对照色谱峰能够完全分离,供试品色谱峰除羟苯乙酯色谱峰前后有干扰之外,其余均能完全分离,继续在此基础上调整流动相,在49~69 min 期间采用过流动相(A)由25%逐步升至50%、由25%逐步升至48%,色谱图分离效果不如49~69 min(A)44%,(B)56% ,在系统适用性过程中采用在49~69 min(A)43%,(B)57%、(A)45%,(B)55%,均能达到分离效果,分析原因,4 号峰左右侧杂质峰与4 号目标物极性相似,利用梯度洗脱改变了流动相配比,出峰速度不能达到恒速,故效果不如等度洗脱。最终确定梯度洗脱程序④:流动相(A)甲醇-(B)0.02 mol/L 磷酸二氢钠溶液(用磷酸调pH 值3.7),程序(V/V)0~48 min(A)25%,(B)75%,48~49 min(A)25%→44%,(B)75%→56%,49~69 min(A)44%,(B)56%,69~70 min(A)44%→54%,(B)56%→46%,70~102 min(A)54%,(B)46%,102~103 min(A)54%→90%,(B)46%→10%,103~113 min(A)90%,(B)10%,结果6 种防腐剂峰形对称,无干扰,分离度好。与乙酸铵系列流动相比,优势在于流动相配置好后,流动相的pH 值不会发生变化,色谱峰的时间不会漂移,在配制流动项时需要注意的是0.02 mol/L磷酸二氢钠溶液用磷酸调pH 值时,一定要准确用酸度计调至3.7,否则山梨酸和羟苯甲酯色谱峰会完全重合,在此条件下进行测定用三个厂家色谱柱试验均能达到较好的分离效果。
3.3 小结茵栀黄口服液目前所执行的标准无防腐剂检测项,并且本品还会在新生儿黄疸中使用,考虑到安全性,故建议增加防腐剂检查项。本实验建立的方法,6 种防腐剂色谱峰的分离度较高,回收率平行性较好,最大优点是正文中的流动相可以将目标峰与周围杂质峰完全分离,避免造成假阳性结果,该方法可以为茵栀黄口服液中防腐剂的检查提供一定的依据,也可以为其他口服液在防腐剂的检查中提供一定的参考价值。
