注射用头孢西丁钠的质量评价
2022-03-18王强李香荷韩彬张冬田兰高燕霞
王强 李香荷 韩彬 张冬 田兰 高燕霞
( 河北省药品医疗器械检验研究院,石家庄 050000)
头孢西丁钠(cefoxitin sodium)是β-内酰胺类药物,由链霉菌产生的甲氧头孢菌素C经半合成制得,属于第二代头孢菌类药物。1974年由默沙东公司(Merck Sharp &Dohme)开发上市[1],1993年进入我国市场销售。临床主要用于敏感菌所致的呼吸道感染、心内膜炎、腹膜炎等感染,最主要的不良反应为皮疹等过敏反应[2]。
2020年国家食品药品监督管理总局将注射用头孢西丁钠列为国家药品抽验计划品种。注射用头孢西丁钠由无菌原料直接分装制成。经查询国家药品监督管理局网站,国内现有注射剂生产企业49家,批准文号101个,有0.5、1.0、2.0和3.0 g 4种规格。注射用头孢西丁钠收载于《中国药典》2020年版[3]及USP43[4]版。本文在完成法定标准检验的基础上,结合探索性研究结果进一步分析,进而对全国范围内注射用头孢西丁钠的质量现状进行评价,并从安全性和有效性角度对企业生产工艺和现行标准提出建议。
1 仪器与试药
1.1 仪器
LC-20AT高效液相色谱仪(日本岛津公司),Sciex Atrap6500质谱仪(AB Sciex公司),WITT PA7.0残氧分析仪(德国WITT公司),Mettler Toledo XS205型电子天平(瑞士Mettler Toledo公司);YB-II型澄明度测定仪。
1.2 试药
头孢西丁钠对照品(130572-201603,95.1%)由中国食品药品检定研究院提供。Cefoxitin EP impurity A(批号04107,含量95.78%)、cefoxitin impurity D(批号04102,含量97.04%)均由BenPharmas公司提供。
试剂均为分析纯,水为超纯水。
1.3 样品
本次抽验共抽到样品202批次,涉及生产企业23家,批准文号39个。抽样覆盖全国31个省/自治区/直辖市,抽样最多的省份为海南省,为26批次,占全部抽样量的12.9%。抽验样品能代表国内本品种目前的生产和使用状况,对其进行检验和统计分析,结果能较好地反映注射用头孢西丁钠的质量现状。
2 试验方法
2.1 法定标准检验
本次抽验涉及的23家生产企业中,11家企业执行《中国药典》2020年版;2家企业执行国家药品标准(注册标准);10家生产企业执行双标准,即不同项目分别执行《中国药典》和相关国家药品标准。各标准的主要区别在于溶液的澄清度与颜色、有关物质、聚合物以及含量测定。
2.2 有关物质质谱分析
色谱柱:Agilent 120 PFP(100 mm×2.1mm,2.7 μm);流动相:甲醇-水(0.1%甲酸);流速:0.4 mL/min;柱温:40℃;离子源:APCI;采集模式:负离子;电压:3.5 kV;离子源温度:350℃;脱溶剂气流量:35 mL/min。
2.3 头孢西丁聚合物分析
聚合物含量测定:用球状亲水改性硅胶为填充剂(TSK-GEL G2000swxl,7.8 μm×30 cm,5 μm的色谱柱),流动相为磷酸盐缓冲液(pH7.0)[0.005 mol/L磷酸氢二钠溶液-0.005 mol/L磷酸二氢钠溶液(61:39)]-乙腈(95:5,V/V),柱温为25℃,流速为0.9 mL/min,检测波长为235 nm,限度为不得过1.0%。
聚合物的质谱分析:采用二维色谱法分析头孢西丁聚合物的可能结构。
一维液相色谱条件:色谱柱:T S K G E LG2000swxl(7.8 mm×30 cm,5 μm);流动相:0.005 mol/L磷酸盐缓冲液(pH7.0)-乙腈(95:5);流速:0.8 mL/min;柱温:30℃。
二维液相色谱条件:色谱柱:Agilent Elicpse C18(150 mm×4.6 mm,5 μm);流动相:水-乙腈(70:30,V/V);流速:0.3 mL/min;柱温:30℃。
离子源:ESI(+);检测器电压:1.6 kV接口电压:4.5 kV;脱溶剂管温度:200℃;加热模块温度:200℃。
3 结果与讨论
3.1 产品总体质量总结
依据现行标准检验,本次抽验的202批次注射用头孢西丁钠全部符合规定。该品种2013年曾被列为国家评价性抽验品种,当时检验合格率为93.4%,不符合规定项目为溶液的颜色、细菌内毒素和含量,共涉及6家生产企业[5];提示注射用头孢西丁钠产品总体质量近年来有所提升。
对本次抽验的含量测定结果进行分析,其以无水物计为91.0%~98.2%,按平均装量计为95.0%~107.1%。企业A样品含量按无水物计为93.0%~97.7%,按平均装量计为98.0%~107.1%,批间差异相对较大,提示对个别企业的生产稳定性应引起关注。
3.2 有关物质
注射用头孢西丁钠共检出13个杂质(图1)。各企业产品无明显差异。采用对照品定位结合LC-MS/MS分析,推测主要杂质(杂质含量≥0.05%)有5 个:杂质1,杂质5(去甲酰胺基头孢西丁酸,EP杂质A)、杂质6(头孢西丁内酯,EP杂质D)、杂质7及杂质13。通过酸、碱、氧化、热、光和紫外强制降解试验,分析各杂质在不同条件下的相应变化(表1),确定降解杂质及工艺杂质。
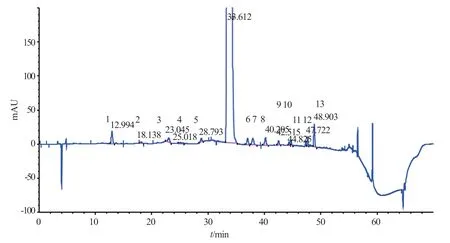
图1 注射用头孢西丁钠有关物质典型HPLC图谱Fig.1 HPLC chromatogram of cefoxitin sodium for injection in related substances

表1 强制降解实验结果Tab.1 Results of degradation test
对202批次样品中的有关物质含量进行分析,单个杂质含量为0.1%~0.5%,杂质总和为0.3%~1.5%,见图2(抽样6批次以上企业)。最大单个杂质为杂质1、杂质6、杂质7或杂质13。分析不同企业产品的差异。企业F、企业I和企业J均使用同一厂家的原料,企业I和企业J共13批次样品的最大杂质均为杂质13,质量较为稳定;而企业F不同批次样品中的最大杂质为杂质1、杂质6或杂质13。企业C和企业N虽然使用不同厂家的原料,但最大杂质均为杂质7或杂质13。提示产品的杂质不仅与原料来源有关,且与生产过程和储存过程有关。

图2 有关物质检测结果箱式图Fig.2 Boxplots of the related substances
进一步比较同一企业产品的批间差异。企业D的产品,单个杂质和总杂质含量分别为0.1%和0.4%,且杂质批间差异小;其他企业的产品,杂质含量与溶液的颜色(简称颜色)呈明显正相关:颜色为黄色7号的样品,总杂质含量为0.6%~1.1%,高于颜色低的样品。企业C的1批次样品(本次抽验所有批次中杂质含量最高的样品),最大单个杂质达到0.5%(杂质13),总杂质含量达到1.5%,其颜色为黄色8号。
《中国药典》2020年版注射用头孢西丁钠各论规定,单个杂质不得过0.5%,总杂质不得过4.0%。本次抽验结果提示,注射用头孢西丁钠总杂质的限度有进一步提升的空间,建议为“不得过3.0%”,并增加对已知杂质A和杂质D的控制(不得过0.2%),以使检验结果更真实的反映产品质量。
3.3 头孢西丁聚合物
《中国药典》2020年版未收载头孢西丁聚合物的检测方法。结合文献报道[6-7],采用球状亲水改性硅胶测定注射用头孢西丁钠中的聚合物含量。在TSK高效凝胶色谱系统中,供试品可检出3个聚合物峰(图3),对202批次抽验样品的检测结果表明,聚合物含量为0.1%~1.0%(图4)。企业F和企业P的聚合物含量达到1.0%。
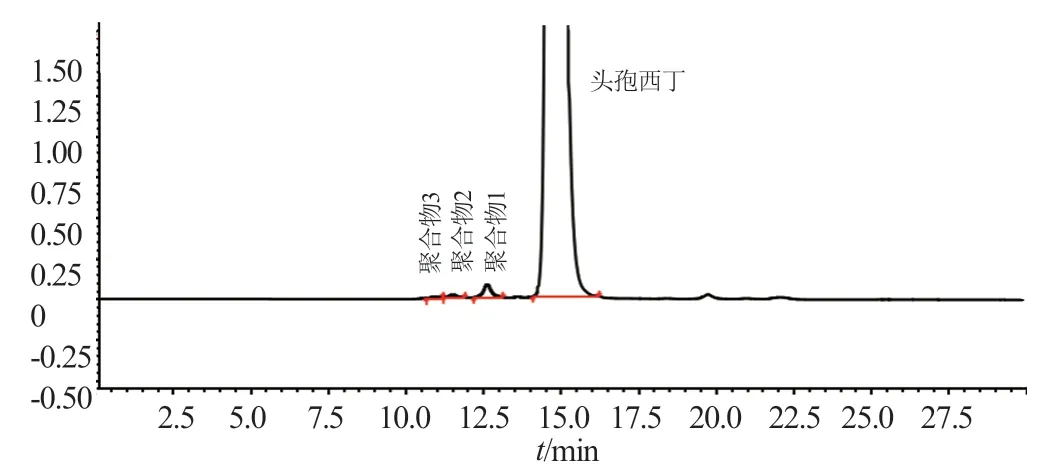
图3 注射用头孢西丁钠聚合物典型HPLC图谱Fig.3 HPLC chromatogram of cefoxitin sodium for injection in polymer

图4 聚合物检测结果箱式图Fig.4 Boxplots of the polymer
采用LC-MS/MS对实际样品中(图3)两个主要聚合物杂质的结构进行推测,可能的结构(表2)。聚合物1的一级质谱图中m/z855.0648为[M+H]+,m/z877.0425为[M+Na]+,分子量为854.1016,分子式推测为C32H34N6O14S4。二级质谱图中主要的裂解碎片为m/z472.0192、m/z428.0407、m/z411.0052、m/z383.0034、m/z335.0007和m/z287.0099(图5)。聚合物2的一级质谱图中分子离子峰m/z833.0922为[M+Na]+,m/z832.0915、m/z834.0789和m/z835.0662为分子离子峰的同位素峰,分子量为809.0801,分子式推测为C31H31N5O13S4。二级质谱图中主要的裂解碎片为m/z472.0193和m/z411.0082(图6)。
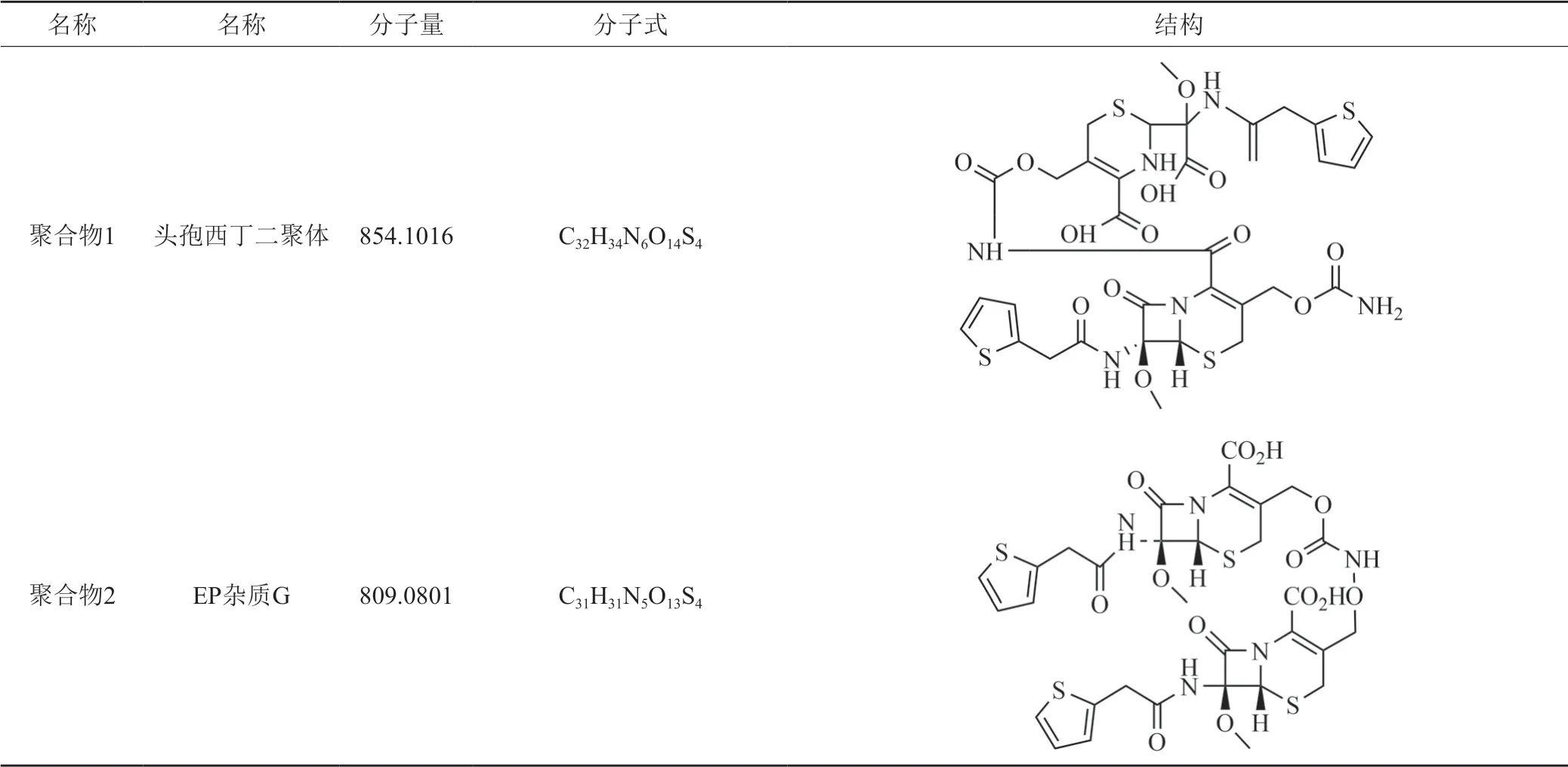
表2 聚合物结构推测Tab.2 Speculation on the structure of polymer
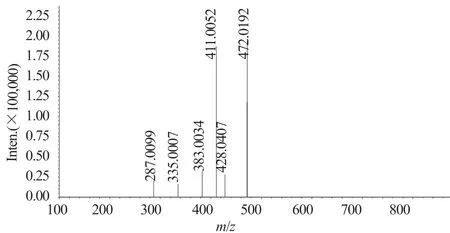
图5 聚合物1二级质谱图Fig.5 The MS2 spectra of polymer 1
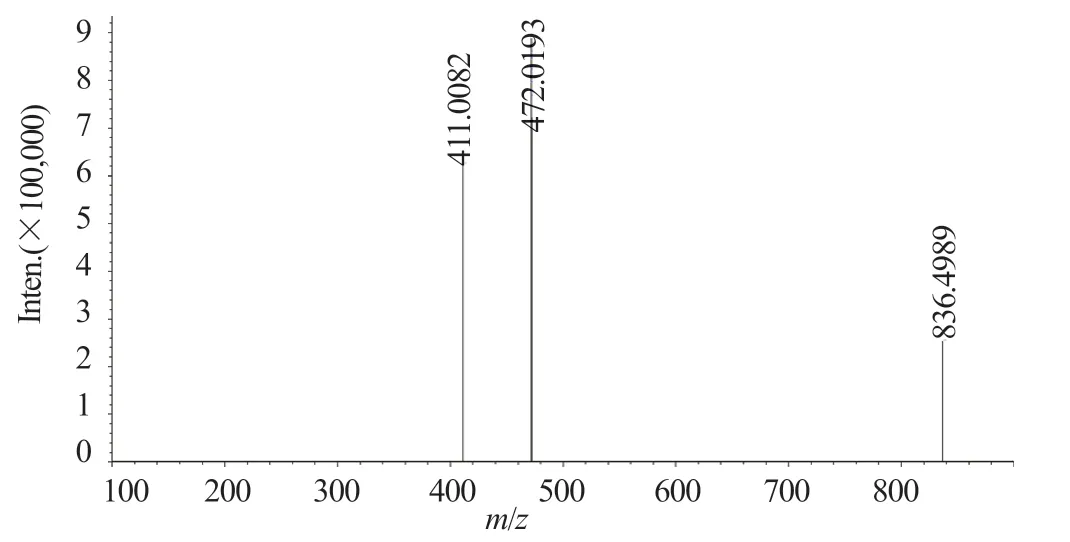
图6 聚合物2二级质谱图Fig.6 The MS2 spectra of polymer 2
3.4 溶液的颜色
《中国药典》2020年版规定,注射用头孢西丁钠颜色不得深于黄色或黄绿色8号标准比色液;国家药品标准YBH02162013、YBH11862008等规定,颜色不得深于黄色或黄绿色7号标准比色液。根据2014—2016年国家局发布的质量公告,注射用头孢西丁钠抽样不合格的主要项目为溶液的颜色。对本次抽验结果进行分析,颜色不深于Y6(黄色6号)共191批次样品,占94.6%;部分企业样品颜色较深,且批间差异较大(Y2~Y7);企业F的全部5批次样品颜色均为Y7,企业K、O、P和Q分别有1批次样品的颜色达到Y7。企业C的1批次颜色达到了Y8,质量状况不理想。
3.4.1 残氧量的影响
采用WITT-PA7.0残氧仪对202批次样品进行检测。结果表明,202批次样品的残氧量在0.4%~16.7%(图7)。企业D、J、L和N样品的残氧量控制在2%以下,样品溶液的颜色均不深于Y5。企业F的5批次样品残氧量在7.0%~15.3%(颜色均为Y7),企业P的残氧量在12.7%~16.7%(2批次颜色为Y4、1批次颜色为Y6,1批次颜色为Y7),可见残氧量与头孢西丁钠的溶液颜色呈明确的正相关性(图8)。
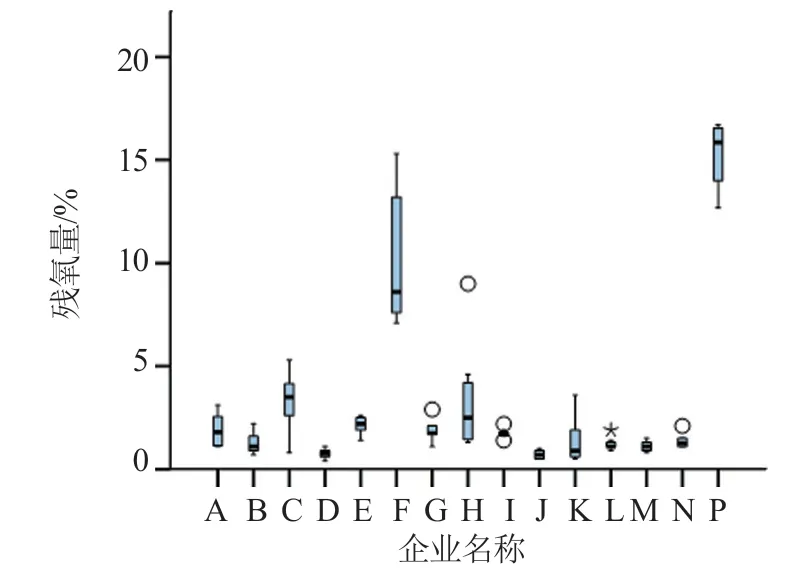
图7 残氧量测定结果统计Fig.7 Boxplots of the residual oxygen
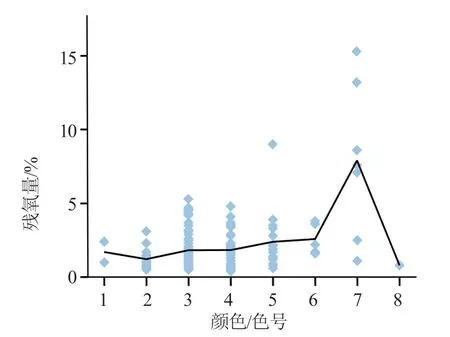
图8 残氧量与颜色的相关性Fig.8 The correlation between residual oxygen and color of solution
3.4.2 杂质与颜色的相关性
相关性分析显示,杂质1和杂质13与溶液的颜色均呈正相关(P<0.01)(图9a和9b)。聚合物含量与溶液的颜色也呈正相关性(P<0.01)(图9c)。
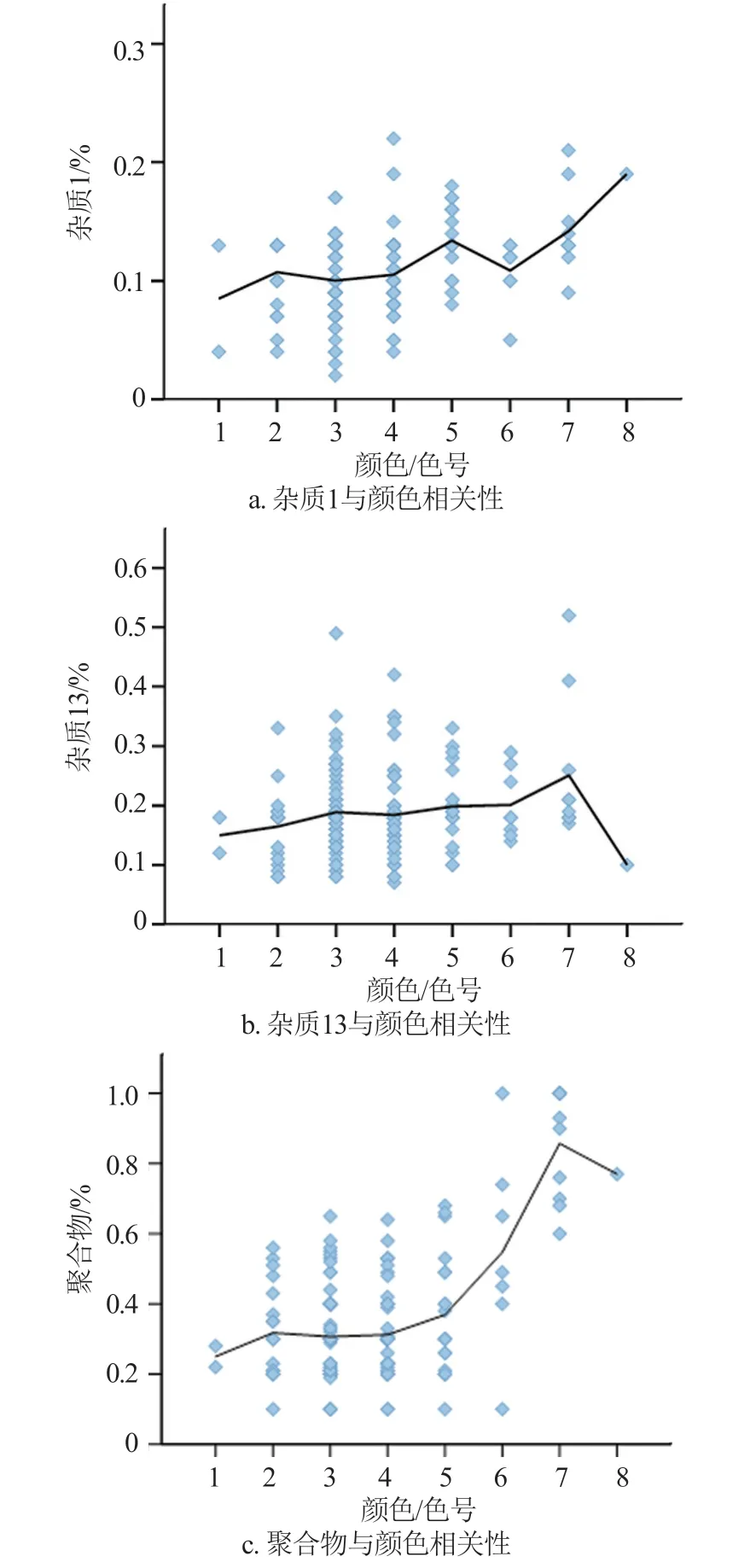
图9 杂质与颜色相关性Fig.9 The correlation between impurity and color of solution
3.4.3 储存条件的影响
对溶液颜色达到Y7的11批次样品进行分析,其储存温度均为20℃以下,符合说明书中规定的储存温度,但储存湿度在60%以上的有7批次。头孢西丁钠易潮解,相关文献报道储存湿度会对溶液的颜色产生一定影响[5]。
文献[8]表明,头孢类抗生素与制剂瓶中残留氧气发生反应是溶液颜色变深的主要原因,氧气残留量与生产工艺中的充氮环节的控制有关。本次抽验的结果进一步印证了文献的结论。此外,注射用头孢西丁钠易吸潮,贮存及运输条件控制不当也是导致颜色加深的原因。
3.5 结论
本次评价性抽验结果显示,依照法定标准检验202批样品均符合规定,提示国产注射用头孢西丁钠总体质量状况“较好”。
注射用头孢西丁钠由原料直接无菌分装制成,生产中的充氮环节控制不足,易造成瓶中残氧量偏高,严重影响产品的溶液颜色,是生产工艺的风险点。由于产品中的特定杂质与溶液颜色呈正相关,提示保证制剂在贮存期的稳定性也是控制产品质量的关键。
本次抽验结果提示,现行《中国药典》标准有待进一步完善。建议:①提高原料和注射剂的有关物质的控制水平,增加杂质A和杂质D的控制。②结合企业加强对充氮工艺的控制,合理制定溶液颜色的限度。③增加聚合物的检查。
