锂金属负极的改性策略的研究进展*
2021-12-14彭钰函薛丽红张五星严有为
张 航,彭钰函,薛丽红,张五星,严有为
(华中科技大学 材料科学与工程学院,材料成形与模具技术国家重点实验室,武汉 430074)
0 引 言
能源和环境危机是阻碍现代社会发展的两大障碍,而解决这两大危机的根本办法是大规模使用清洁能源。在使用清洁能源的过程中,二次电池是核心技术之一,是我国在2060年实现“碳中和”战略目标的重要保障。
锂离子电池具有高功率、高能量密度、低自放电、长循环寿命等优势,已成为目前最广泛使用的二次电池技术[1- 2]。目前,商用锂离子电池的能量密度可达260 Wh/kg,但远未达到电动汽车对动力电池的超长续航要求,其主要原因之一在于当前使用的石墨或石墨/硅负极的比容量较低(小于500 mAh/g),因此亟待开发能量密度更高的负极材料[3-5]。金属锂拥有高理论容量(约3 860 mAh/g)和最低的电化学电势(-3.040 V,SHE),可以提供高的能量密度和宽的电压窗口,是下一代高能量密度二次电池的理想负极材料之一[6-7],有望突破锂离子电池400 Wh/kg的能量密度瓶颈。
锂作为碱金属,最外层仅有一个电子,具有很高的反应活性和还原性,易与电解液反应生成固态电解质界面(SEI),SEI膜能让电解液中的Li+自由通过,但不允许电解液的其他成分进出,这有效阻止了电解质的分解;另外,SEI膜能够使电场下的Li+均匀分布,减少浓差极化。可见,SEI膜对稳定电池循环性能和延长循环寿命有着非常重要的作用[8-11]。但是金属锂在沉积/溶解过程中存在较大的体积变化,造成SEI膜不断地发生破裂和重构,这种现象将持续消耗Li+,形成较厚的SEI膜,导致电池内阻增大,并使得金属锂负极结构粉化,电池稳定性发生恶化。
由于锂金属电极表面存在粗糙度和SEI膜不稳定等因素,可导致锂离子在锂金属负极表面的不均匀沉积,并形成锂枝晶。锂枝晶的形成和生长,将消耗电解液,并形成额外SEI膜,导致库伦效率降低。另外,连续生长的锂枝晶将刺穿隔膜,致使电池短路,产生大电流放电,在短时间内热量积累,出现热失控等安全隐患。此外,锂枝晶在活性点位附近的不均匀溶解可能导致锂枝晶从基体脱落,脱落的锂枝晶将被厚厚的SEI膜包覆,形成无法传输Li+、电子和无法提供容量的“死锂”,甚至出现锂的粉化,造成巨大容量损失。因此,解决锂枝晶问题也是推动金属锂负极商业化进程的关键因素之一[12-13]。
为了解决上述问题,研究者分别从锂负极、隔膜、人工SEI膜、电解液和固体电解质等方面提出了改进方法,并取得了良好的效果。本文将对这些方法进行综述,并对其未来的研究方向进行展望。
1 锂负极改性
为了解决金属锂负极的锂枝晶生长,体积变化以及SEI膜的反复破裂等问题,研究者提出了以具有框架结构的材料作为金属锂“host”的设想,这种框架结构具有以下优点[14-20]:(1)导电框架可以提供电子电导,有效降低局部电流密度,从而抑制锂枝晶的生长和“死锂”的产生;(2)有利于锂负极表面的Li+均匀分布,从而使Li发生均匀沉积/剥离;(3)框架结构将锂的沉积/剥离限制在结构内部,保持了锂负极的体积稳定,从而避免体积变化引起的SEI膜的反复破裂,降低容量损失。
Lin等[21]以氧化石墨烯(rGO)为框架,与金属锂复合,制得复合金属锂负极Li-rGO,如图1所示。rGO表面的官能团与金属锂有较高的结合能,使rGO有良好的亲锂性,在充放电过程中Li-rGO仅有20%的体积变化。由于石墨烯价格昂贵,人们尝试采用低廉的多孔碳为框架。Liang等[22]采用化学气相沉积(CVD)法在碳框架表面包覆Si以改善其亲锂性,然后灌入熔融的锂,制备的复合负极的容量可达2 000 mAh/g。Zhang等[23]通过电镀法在碳纤维表面镀Ag,然后灌锂,制得复合负极(CF/Ag-Li),装配的Li‖S电池在0.5 C倍率下循环400圈后仍有785 mAh/g的容量。Jiang等[24]在碳纸上原位生成Co3O4后,灌锂,制得复合锂负极,对电池在循环1 000 h后,过电位仅18 mV。Sun等[25]以碳纸为框架,电化学沉积金属锂后,以LiFePO4为正极,装配全电池,在0.5 C电流下循环250圈,容量保持99.8%。Liu等[26]以碳化棉花为框架,电化学沉积锂后制得复合负极,以LiFePO4为正极,0.5 C电流下循环200圈后容量保持91.3%。

图1 Li-rGO复合负极的制备过程示意图 [21]Fig 1 Schematic of the synthetic procedures of a layered Li-rGO composite film
Zhou等[27]通过机械压力将碳布与锂箔结合在一起,制备出复合金属锂负极,在5 mA/cm2的电流密度下,Li||Li对电池的极化仅150 mV,并稳定循环200圈。Shi等[28]将金属锂与碳框架进行轧制,制备出卷对卷的复合金属锂负极, Li||Li对电池能够在50%的深度放电下,以120 mV的较小极化循环90 h以上。
除碳材料外,金属、有机物也可以作为框架材料。Ke等[29]将多孔铜作为3D框架沉积锂,Li||Li对称电池在0.5 mA/cm2稳定地循环620 h。Li等[30]采用冲压机对金属锂与铜网施加机械压力,使金属锂均匀分布在铜网中,制备出以铜网为框架的锂金属复合负极,装配的Li/Li4Ti5O12半电池表现出良好的倍率性能和长循环稳定性。Wu等[31]将Cu网表面氧化成CuO,再与锂复合制成负极,以LiFePO4为正极,装配的全电池在5 C下,循环了1 000圈。Chi等[32]在3D泡沫Ni中灌入熔融锂制备出复合负极,Li||Li对电池在5.0 mA/cm2循环100圈,保持200 mV的低过电位。另外,该课题组将Li与B合金化,形成Li7B6的微纳米尺寸框架,Li7B6对Li+的吸附能力强于金属锂晶粒,可诱导Li在Li7B6上优先形核,从而有效抑制锂枝晶生长[33]。
Cheng等[34]将网状玻璃纤维作为框架,玻璃纤维的Si-O、O-H、O-B等官能团能降低Li+扩散的表面能,使Li+均匀分布,在10.0,2.0 mAh/cm2下稳定循环500圈,无明显锂枝晶产生。
Liu等[35]在聚酰亚胺表面采用ALD法制备ZnO层,并将熔融锂灌入,制备出厚度仅为85 μm的复合金属锂负极。对电池在5 mA/cm2下循环100圈,保持约110 mV的过电位。
2 隔膜改性
传统锂离子电池的隔膜多为聚乙烯(PE)、聚丙烯(PP)等聚烯烃隔膜。聚烯烃隔膜的Li+传输性能好,不与电解液反应,耐强氧化性与强还原性,且与电解液润湿性好,有较低的内阻。但其也存在许多问题:Li+在隔膜附近分布不均,导致金属锂异质形核、沉积,生成锂枝晶;聚烯烃隔膜的力学性能差,锂枝晶会刺破隔膜,导致电池短路;在Li||S电池中,无法抑制多硫化物的穿梭效应;热稳定性差,有热失效的风险[36-40]。为了解决这些问题,常常采用具有高热稳定性、高电压稳定性、高机械强度的Al2O3、TiO2、SiO2等氧化物作为隔膜的增强相,另外,这些氧化物具有较高的硫化物结合能,能够抑制Li||S电池中多硫化物的穿梭效应[41-45]。
为了进一步提高隔膜的离子电导率,研究者也采用快离子导体作为隔膜的改性材料。Yu等[46]将Li1.3-Al0.3Ti1.7(PO4)3(LATP)陶瓷膜与PP隔膜复合,抑制了锂枝晶生长和多硫化合物的穿梭效应。接着,采用对金属锂更稳定的Li1+xYxZr2-x(PO4)3(LYZP)替代LATP,装配的Li||S电池在0.2 C的电流下循环,首圈容量可达1 000 mAh/g,循环150圈后,还能保持90%的容量[47]。Zhao等[48]在PP隔膜上涂覆一层Al掺杂Li6.75La3Zr1.75Ta0.25O12(LLZTO)膜,改善了隔膜的Li+分布,如图2所示,装配的Li||LFP软包电池的电化学性能得到明显提高。
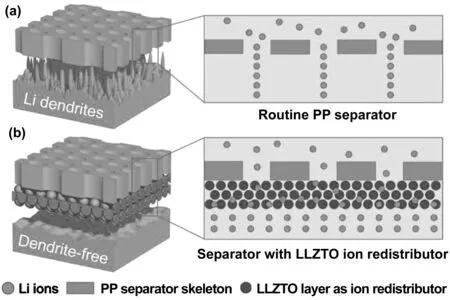
图2 采用(a)PP和(b)LLZTO/PP为隔膜的锂金属阳极的电化学沉积行为示意图[48] Fig 2 Schematic illustration of the electrochemical deposition behaviors of the Li metal anodes using (a) a routine PP separator and (b) a composite separator with the LLZTO/PP layer [48]
研究者还采用氟化物、氮化物和有机物来改善PP隔膜。Li等[49]在PP隔膜上涂敷SrF2微球,SrF2表面比金属锂更容易吸附Li+,从而提高了Li+的分散性,有效抑制了Li负极上Li枝晶的生长。Luo等[50]将六方氮化硼(BN)涂覆在隔膜表面,利用BN的高导热性使热分布变得均匀,促使Li+均匀形核,避免锂枝晶的产生。Liu等[51]将纳米碳(FNC)涂覆在隔膜表面,在循环过程中,锂枝晶在金属锂负极和FNC改性层上相对生长,当两侧锂枝晶接触时,轴向机械力转化为径向机械力,阻止锂枝晶刺穿隔膜。
Ryou等[52]受到蚌的仿生结构启发,在PE隔膜表面涂覆聚多巴胺(PD)膜,使金属锂负极与隔膜紧密粘合,提高Li+的分散性,减小金属锂的表面张力,从而抑制锂枝晶的生长。Li等[53]利用催化反应,在隔膜表面原位生成聚吡咯(Ppy)层,Ppy吸附大量电解液,从而使隔膜附近的Li+均匀化,提高了电化学性能。Nie等[54]利用与电解液良好润湿的生物质膜提高Li+传输数,制备的Li|| Li1.2Mn0.6Ni0.2O2电池能够在20 C的超高倍率下循环。Huo等[55]在PP隔膜表面制备了一层Li6.4La3Zr1.4Ta0.6O12/PVDF复合固态电解质(PLLZ)层,PLLZ层具有大量3D快离子通道和高的Li+传输数,不仅能控制Li+浓度梯度,而且能抑制锂盐的阴离子传输,对称电池稳定循环1 000 h后过电位仅40 mV。
3 人工SEI膜
人工SEI膜是直接在金属锂负极表面制造一层人造保护膜,以提高金属锂负极的电化学性能。
Peng等[56]采用浇注法在金属锂负极表面制备了Al2O3保护层,具有高机械强度的Al2O3阻碍了锂枝晶生长,将金属锂的生长限制在保护层内。Luo等[57]在Li负极表面制备了高极性的β-聚偏二氟乙烯(β-PVDF)SEI膜,使Li+均匀分布,在5.0,4.0 mA/cm2条件下锂可均匀沉积/剥离。Xu等[58]制备出 (聚偏氟乙烯-六氟丙烯)共聚物(PVDF-HFP)和LiF复合的人工SEI膜,兼具良好的机械强度、柔性和Li+电导率,使Li||LiFePO4电池的寿命提高了2.5倍。Liu等[59]在金属锂表面构建Cu3N纳米颗粒/丁苯橡胶复合保护层,如图3所示。Cu3N与金属锂反应,形成快离子导体Li3N,而丁苯橡胶可提供柔性界面,从而提高了电池的电化学性能和安全性能。
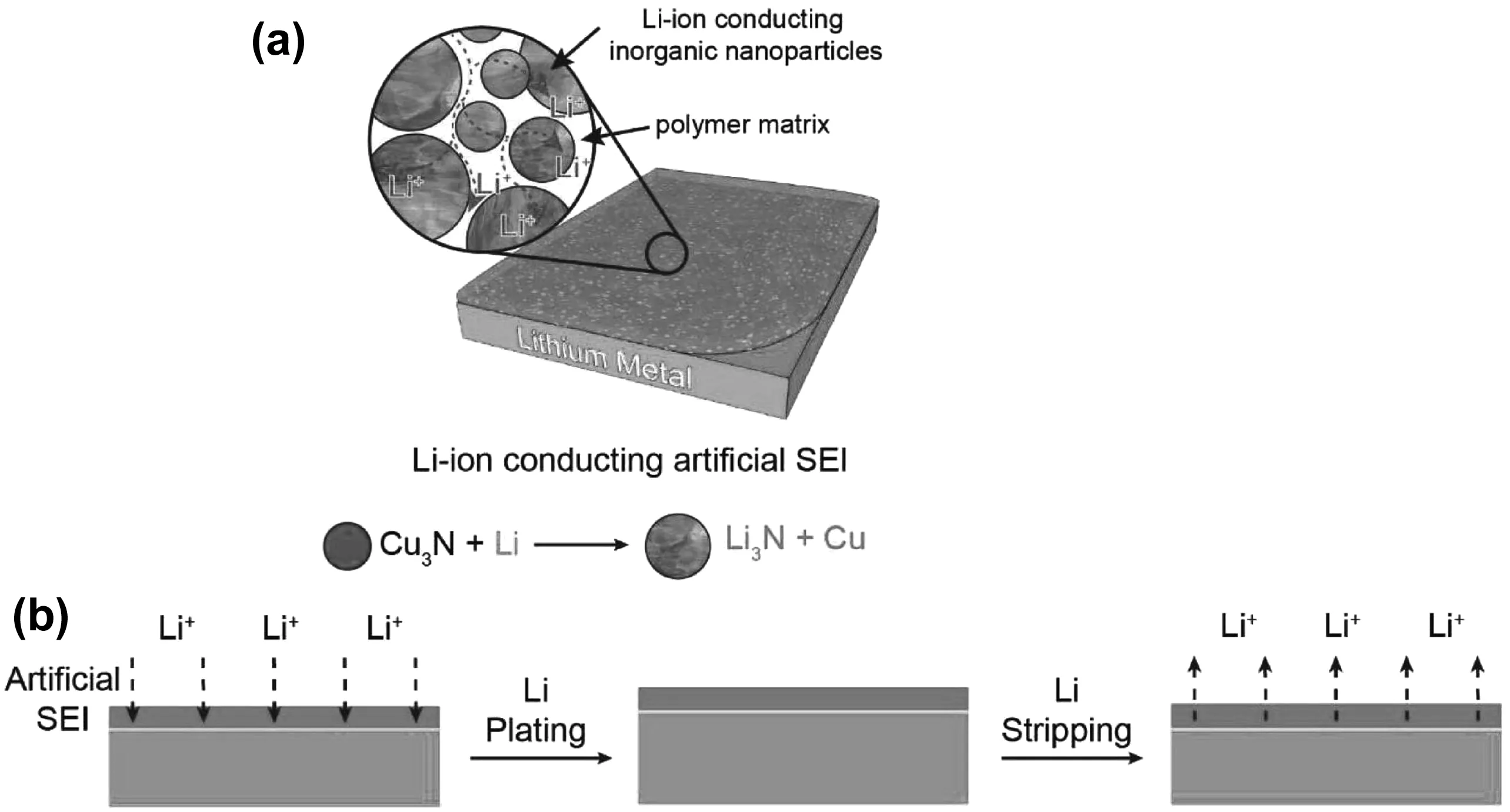
图3 (a)Cu3N纳米颗粒/丁苯橡胶复合人工SEI膜示意图,(b)人工SEI膜保护锂负极的沉积/剥离过程的示意图[59]Fig 3 (a) Structural diagram of Cu3N nanoparticles/SBR artificial SEI film, (b) schematic illustration of the Li plating/stripping behavior of the artificial SEI protected Li[59]
气相沉积法可以实现原子级厚度、高致密、高均匀的人工SEI膜的制备。Xie等[60]通过CVD法将石墨烯和六方氮化硼的复合保护层沉积在Cu箔上,得到超薄二维金属锂保护界面层,有效抑制了副反应,在2.0,5.0 mAh/cm2的条件下,稳定地循环了50圈。Liu等[61]通过CVD制得无机/有机硅酸盐复合的人工SEI膜,其中无机LixSiOy既充当锂离子导体,又作为硬质相阻止锂枝晶的生长,而有机甲基苯丙胺起到增韧、增塑的作用。Kozen等[62]采用原子层沉积(ALD)法在金属锂表面制备出仅14 nm厚的Al2O3人工SEI膜。Cha等[63]通过磁控溅射制备了厚度10 nm的MoS2层,二维MoS2诱导Li原子进入层间,控制了Li+的均匀流入/流出,从而有效控制了Li的沉积/脱出过程。
与非原位人工SEI膜相比,原位人工SEI膜与金属锂负极结合地更紧密,对锂更稳定。Li等[64]利用金属锂与聚丙烯酸发生氧化还原反应,原位制备出具有高柔性、高稳定性、与金属锂结合紧密的聚丙烯酸锂作为人工SEI膜,Li||Li对电池能够稳定循环700 h。Lu等[65]利用金属锂与P2S5、S的四氢呋喃混合溶液进行反应,形成以Li3PS4为主要成分的保护层,稳定了负极界面,抑制多硫化合物的穿梭效应。Liang等[66]利用金属锂还原金属氯化物,形成LixM合金(M为In、Zn、Bi或As)及LiCl组成的保护层。LiCl有良好的电子绝缘性,而LixM合金层提高了Li+传输性,使Li的沉积/剥离过程均匀化。Li||Li对电池在2.0 mA/cm2电流下,可以稳定、连续循环1 400 h。
Cheng等[67]将金属锂负极在三盐电解液(其中以DOL/DME为混合溶剂,LiTFSI、LiNO3、Li2S5为溶质)中预循环形成SEI膜后,分别搭配S和LiNi0.5-Co0.2Mn0.3O2(NCM523)两种正极,电化学性能均有明显提高。Wang等[68]在稀释的离子液体中,对金属锂进行电化学循环预处理后,金属锂负极体现出高稳定性,在5.0 mA/cm2的高电流密度下,表现出大于99.98%的高库伦效率。
4 电解液改性
电解液一般由有机溶剂、锂盐和添加剂组成。传统锂离子电池主要采用碳酸酯为有机溶剂,如碳酸乙烯酯(EC)、碳酸二乙酯(DEC),碳酸丙烯酯(PC)、碳酸二甲酯(DMC)等。碳酸酯类电解液也可用于锂金属电池,但循环寿命不理想[69-70]。Markevich等[69]提出在酯类电解液中加入氟代碳酸乙烯酯(FEC),FEC能够使负极和正极的表面分别形成一层致密SEI膜和CEI膜,提升了电池的综合性能。
醚类有机溶剂,如1, 3-二氧乙烷(DOL)、1, 2-二甲基乙烷(DME)等,可以提高金属锂电池循环寿命,且还原电位更低,但其耐高电压性能较差,难以匹配LiCoO2、LiFePO4等商用正极材料,限制了其应用[71-73]。Miao等[74]以1, 4-二氧烷(DX)和1, 2-二氧乙烷(DME)为混合有机溶剂,DX中的六元子环对称分子结构具有抗氧化能力,使溶剂可在4.87 V的高电压下保持稳定。
离子液体不易燃,与金属锂负极相容性好,但黏度过高,离子电导率低。Lu等[75]采用SiO2纳米颗粒改性离子液体(IM-TFSI 和 PP-TFSI),并将其与PC、LiTFSI配制成电解液,其离子电导率可达1×10-3S/cm,电化学性能有了显著的提高。
理想的锂盐应不仅能够高效传输Li+,还能够促进薄而稳定SEI膜的形成。目前常用的锂盐包括LiClO4、LiAsF6、LiTFSI。LiClO4对金属锂稳定,但其强氧化性易产生安全问题;LiAsF6具有剧毒性,难以广泛应用;LiTFSI易解离、高压稳定性好、热稳定性好,但对锂枝晶的抑制能力差。Suo等[76]研究发现,提高锂盐浓度能够改善Li的沉积行为、抑制锂枝晶生长。Qian等[77]制备出一种7.0 mol/L LiTFSI的超高浓度电解液,电解液中的锂盐接近饱和状态,锂盐在Li+的传输中起到主导地位,Li+传输数提高至0.73,并降低了锂枝晶的产生和对金属锂的腐蚀。Chen等[78]设计出LiTFSI和LiBOB的双盐电解质,LiBOB有利于形成更薄、更稳定的SEI膜,以弥补LiTFSI性能上的不足之处。Zhao等[79]制备出LiTFSI、LiNO3和Li2S5的三盐电解质,通过协同作用使金属锂负极表面的SEI膜电导率提高了一个数量级。
添加剂能够有效降低金属锂负极与电解质间的界面阻抗,减少副反应,稳定SEI膜。LiNO3是醚类电解液的常用添加剂,能够钝化金属锂负极,形成稳定而致密的SEI膜,然而LiNO3在SEI膜中形成的LiNxOy会导致电池内阻增大[80-81]。Li2Sn和LiNO3联合使用,两者的协同作用使金属锂负极表面形成平整、稳定的SEI膜[81]。Choudhury等[82]在电解液中加入0.5%(质量分数)的LiF,形成富LiF的SEI膜,LiF的Li+电导率是Li2CO3的30倍,促进了Li+均匀沉积,抑制了锂枝晶生长。锂的卤化物(LiF、LiCl、LiBr、LiI)能够降低Li在SEI膜界面处的活化能,稳定金属锂的沉积过程。Lu等[83]将锂的卤化物作为添加剂,发现Li||Li对电池循环数百周期后,金属锂仍均匀沉积。金属阳离子也可以作为电解质添加剂,Ding等[84]向电解液中添加低浓度的Cs+或Rb+。锂沉积过程如图4所示,Cs+和Rb+的还原电位比Li+低,在金属锂表面形成了静电屏蔽,一旦有锂枝晶形成,Cs+、Rb+将优先堆积于锂枝晶尖锐处,形成带正电的静电场以排斥Li+,诱导Li+在其他区域沉积,获得无锂枝晶、自修复的平滑Li沉积层。

图4 基于SHES机理的锂沉积过程示意图[84]Fig 4 Illustration of Li deposition process based on the SHES mechanism
5 固态电解质
固态电解质具有高机械强度和高的Li+迁移数,这使固态电解质能够抑制锂枝晶生长,此外,固态电解质无多硫化物的穿梭效应。固态电解质主要包括无机和有机两大类。

有机固态电解质是以聚合物为基体,锂盐为锂离子导体。有机固态电解质比无机固态电解质柔软,便于成型,与金属锂负极的界面电阻小,但存在着离子导电率差、易结晶等亟待克服的问题。聚氧化乙烯(PEO)作为最广泛使用的有机固态电解质,室温电导率仅有10-6~10-8S/cm。降低有机物的结晶度,可大幅提高其离子电导率。Yuan等[92]在PEO中加入Zn的金属有机框架(Zn基MOF-5),MOF-5上的路易斯酸位与PEO链段作用,降低了PEO的结晶度,促进Li+的迁移,25 ℃离子电导率提高至3.16×10-5S/cm。有机固态电解质的Li+传输数低,严重影响Li+传输效率。Chen等[93]将聚(4-苯乙烯磺酰基(三氟甲基磺酰基)酰亚胺)(PSTFSI)与PEO制备共聚物,PSTFSI缔合锂盐中的阴离子,仅允许Li+移动,从而提高了Li+传输数。Zhou等[94]采用拥有高氧化电位的聚(N-甲基-丙二酰胺)(PMA)与PEO制成双层电解质,能够与高电压的LCO进行匹配。
为了兼具无机电解质和有机电解质的特点,常将两者复合使用。Huo等[95]将LLZO粉末分散到PEO中,降低了PEO的结晶度,提高了Li+电导率。Liu等[96]研究发现,在PEO为主体的无机/有机复合固态电解质中,Li+优先在无机/有机的界面进行传输。Fu等[97]将静电纺丝制备的LLZO纤维填入PEO中,其室温Li+电导率提升至2.5×10-4S/cm,Li||Li对称电池在最高电流密度为0.5 mA/cm2的条件下,稳定循环了1 000 h。Zhou等[98]制备了PEO/LLZO/PEO 3层电解质,如图5所示。LLZO阻挡了PEO中阴离子的扩散,提高了整体Li+传输数,柔性的PEO与电极接触良好,电场分布均匀,降低了局部电流密度,从而抑制锂枝晶生长。
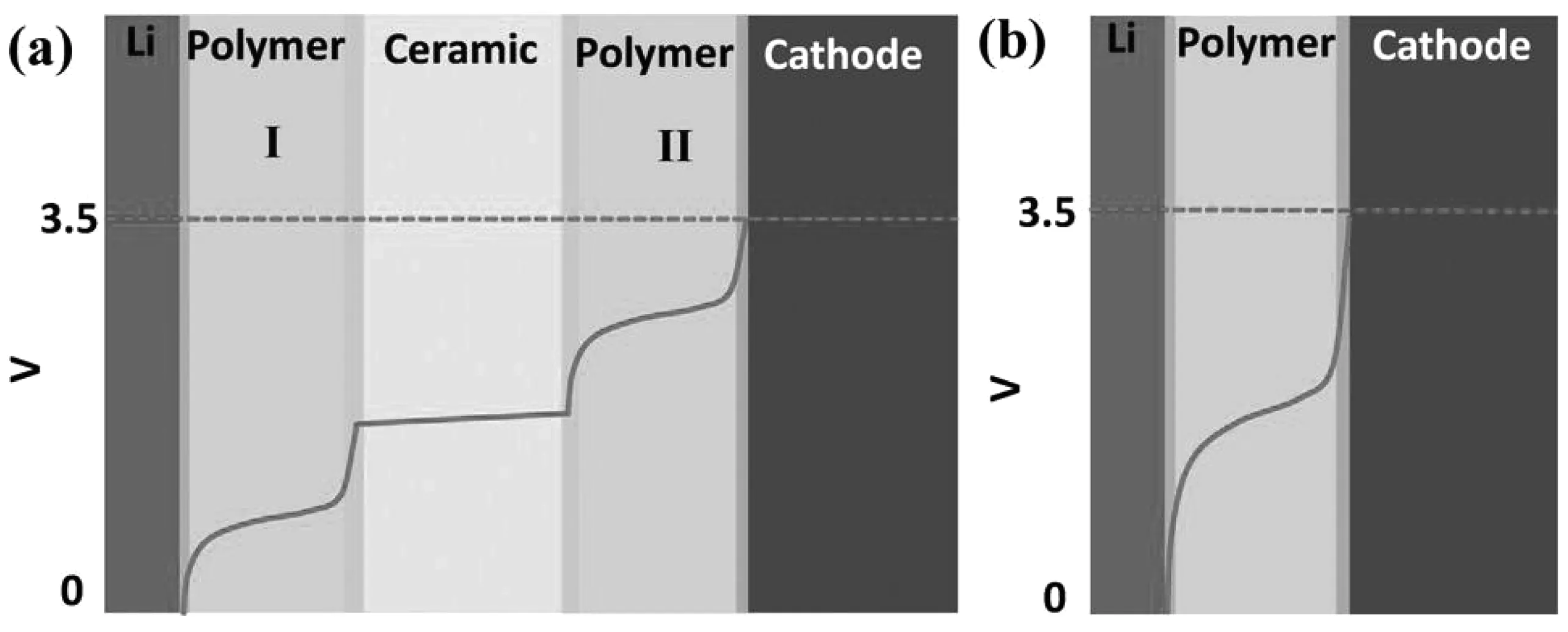
图5 (a)PEO/LLZO/PEO 3层电解质的电压曲线分布示意图;(b)单层PEO中的电压曲线分布示意图[98]Fig 5 Illustration of the electric potential profile across the sandwich electrolyte (a) and individual polymer electrolyte (b) in the charge process of a Li/LiFePO4 cell[98]
6 结 语
金属锂作为负极是未来锂电池发展的必然趋势。但高活泼的锂造成了SEI膜不稳定,锂枝晶生长和体积膨胀效应等问题。
研究者从锂负极、隔膜、电解液、人工SEI膜和固体电解质这5个方面对金属锂负极的保护开展了大量的研究工作,虽然取得令人瞩目的成果,但仍然存在以下不足:(1)廉价的多孔碳常用作金属锂的“host”,但它的亲锂性差,需要在其表面引入其他元素进行改性,因此复合金属锂负极的表面在制备过程中会形成复杂的SEI膜,该SEI膜可能无法与电解质系统兼容。另外,金属锂与电解液的接触而产生的问题尚未解决。(2)粉末作为隔膜的增强相,在提高隔膜的力学性能和物理化学性能上仍有局限性,而多层隔膜使隔膜的厚度增加,内阻变大,在一定程度上会造成电池的容量衰减和能量密度降低。(3)电解液的组分会影响锂金属负极表面SEI膜的组成和结构,从而影响锂金属负极的性能。由于SEI膜敏感易被破坏,采用常规的非原位测试技术难以获得其相关信息,因此,难以揭示其形成机理。(4)不能准确控制人工 SEI 膜的厚度及锂离子传导能力,锂离子在人工SEI膜/负极界面以及SEI膜内的扩散、迁移、被还原过程及相应的机理等难以阐明。(5)使用固态电解质的锂电池的性能仍不如商业化的液态电解质锂电池。这是因为无机固态电解质与电极的界面容易形成较高的阻抗,而有机固态电解质的Li+电导率、Li+传输数、电化学窗口仍然不尽人意。此外,人们对固体电解质与电极的界面机理认识还不统一。
因此,锂金属电池的未来研究及发展有以下几个方面:
(1)发展非破坏的、原位测试技术及模拟计算深入研究SEI膜的成分、结构、形成过程以及锂离子在SEI膜内的行为等基础科学问题,为未来电解液体系和人工SEI膜的设计和发展提供理论基础。
(2)综合考虑SEI膜的稳定性、机械强度、锂离子的输运、与金属锂和电解质的兼容性等关键因素,能对人工SEI膜进行精准的设计和调控。
(3)深入研究固态电解质与电极之间的界面机理,提高固态电解质与电极的界面结合能力和导锂离子能力,开发柔性一体化的固态电解质,减小电池的体积,提高电池的能量密度。
(4)单一的改性策略还不能够从根本上解决锂负极面临的难题,应将不同的改性策略结合起来,进一步提高金属锂负极的物理力学性能和电化学性能,推进金属锂电池的实际应用。
