眼部转移性透明细胞肾细胞癌的临床病理分析
2021-11-07毕颖文蔡蓉蓉王纾宜朱雄增
毕颖文,蔡蓉蓉,王纾宜,朱雄增
(1.复旦大学附属眼耳鼻喉科医院病理科,上海 200031;2.复旦大学附属肿瘤医院病理科,上海 200032)
肾细胞癌约占所有成人恶性肿瘤的3%,透明细胞肾细胞癌(clear-cell renal cell carcinoma,CCRCC)是肾细胞癌最常见的类型。据统计33%的肾细胞癌会发生转移[1],转移至眼部的肾细胞癌虽然比较少见,但有时眼部转移灶可以先于原发肿瘤被发现,其眼部临床表现也往往不具有特异性,常会被临床医生忽视。本研究回顾性分析5例确诊的眼部转移性CC-RCC,旨在归纳其临床病理特点,以期为早期准确诊断提供依据。
1 对象与方法
1.1 对象
收集复旦大学附属眼耳鼻喉科医院眼科2010年1月至2020年12月11年间收治的经病理诊断为眼部转移性CC-RCC的患者共5例(5只眼)。收集临床资料包括患者年龄、性别、眼位、发病过程、既往病史、术前眼部及全身检查、影像学检查,包括眼部B超、CT和MRI、正电子发射计算机断层显像(positron emission tomography CT,PET-CT),治疗方法及随访结果等。
1.2 方法
手术取出组织用10%甲醛固定,石蜡包埋、切片、HE染色。免疫组织化学染色采用EnVision二步法。所用抗体CK、CK7、CK8、CK19、CK20、CAM5.2、EMA、34βE12、CEA、VIM、PAX8、CD10、TTF-1、S-100、CD56、SYN、HMB45、DES、MSA、SMA、LCA、CD68、Ki-67购自基因科技有限公司和福州迈新生物技术开发有限公司。所用的免疫组织化学仪器为罗氏的Ventana Ultra全自动免疫组化仪。PAS(Periodic Acid-Schiff)染色试剂盒购自珠海贝索生物技术有限公司。
2 结果
2.1 临床特点
2.1.1 脉络膜转移性CC-RCC
3例脉络膜转移性CC-RCC均为男性,例1和例3均为62岁,例2为51岁,平均58岁,均表现为右眼前黑影伴视力下降,病程分别为6月,1月和4月。术前检查视力均为右眼前手动,右眼底见视网膜下隆起肿块伴视网膜脱离。3例B超均显示右眼球内隆起肿物,例1和例2位于后极部,例3位于鼻侧球壁,中等回声,大小7.1~8.4 mm×15.5~ 18.2 mm,均伴表面视网膜脱离,例3伴挖空征及脉络膜凹陷征,考虑脉络膜黑色素瘤(图1)。例2两年前行左肾癌手术,1年前右肺上叶转移,术前胸部CT显示双肺多发结节,右侧为著,大者 2 cm×2 cm。例1术前胸部CT显示两肺内多个小结节影,大部分位于两肺外带,结节边界尚清晰,符合肺转移瘤表现。3例均在我院眼科全身麻醉下进行了右眼球摘除及义眼座的植入(表1)。
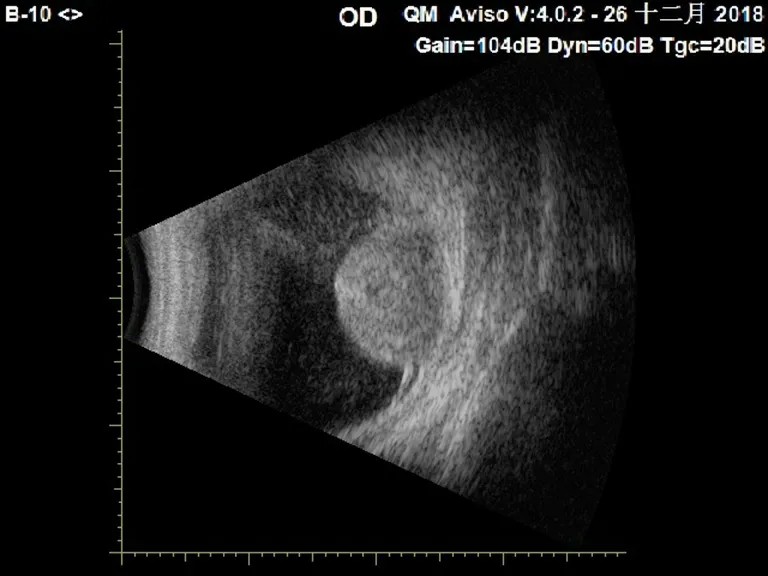
图1 右眼脉络膜转移性CC-RCC患者(例3):B超检查示右眼鼻侧球壁前探及8.4 mm×15.53 mm半球形中高回声,伴挖空征及脉络膜凹陷征,考虑脉络膜黑色素瘤Figure 1 Choroidal metastatic CC-RCC (case 3):B-scan ultrasound demonstrated an intraocular mass with medium to high internal reflectivity suspected of choroidal melanoma
2.1.2 眼眶转移性CC-RCC
2例眼眶转移性CC-RCC中例4为女性,56岁,右眼红肿伴眼球突出2 个月,2 个月前外院行右肾CC-RCC切除手术,术前CT显示右眶外上方 3 cm×4 cm软组织肿块,涉及眶顶及外侧肌锥外与中颅底,伴眶顶壁、外侧壁与蝶骨大翼骨质破坏 (图2)。PET-CT提示右肾癌术区未见明显肿瘤复发,右眼眶外侧壁转移并侵及右侧额骨。术前右眼矫正视力0.6,右眼球突出,上转运动受限,眼球下移。例4在我院全身麻醉下行右眶颅联合肿物摘除术(表2)。
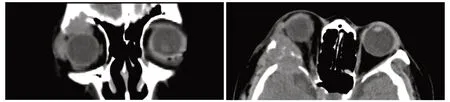
图2 右眼眶转移性CC-RCC患者(例4):冠状位和水平位CT显示右眶外上方3 cm×4 cm软组织肿块,涉及眶顶及外侧肌锥外与中颅底,伴眶顶壁、外侧壁与蝶骨大翼骨质破坏Figure 2 Orbital metastatic clear-cell renal cell carcinoma (case 4):coronal and axial CT scan showed superotemporal 3 cm×4 cm mass of the right orbit with bone destruction
例5,男性,65岁,左眉弓肿物3年,渐大。7年前左肾CC-RCC切除术,术后靶向药物(多吉美)治疗,半年前“肾癌肺部转移”行胸腔镜手术。术前MRI示左眶顶上眼睑皮下一椭圆形结节肿块影,大小2.2 cm×2.4 cm×2 cm,紧贴眼球前上壁,眼球向下移位。术前左眼视力0.1,左眼眉弓处扪及质硬隆起肿物2 cm×1 cm,界清,眼球下移伴上睑下垂。例5在我院全身麻醉下行左眼眶肿物摘除术(表2)。
2.2 病理学特点
2.2.1 脉络膜转移性CC-RCC
3例眼球摘除标本经固定后均根据术前检查显示的肿瘤部位,行肿瘤最大面切开眼球,肿瘤切面呈黄白色,镜下见肿瘤均位于脉络膜内,伴表面视网膜脱离,网膜下渗出(图3A),肿瘤内血管丰富,呈裂隙状,肿瘤细胞细胞质透亮,多呈实性片巢状排列,部分呈腺管、腺泡状排列,大部分细胞细胞质透明,部分细胞细胞质呈嗜伊红颗粒状(图3B),核小,形状不一,核仁不明显,部分核空泡状,可见核分裂象(图3C),部分区可见肿瘤细胞坏死(图3D)。肿瘤细胞细胞质PAS染色(+),不耐淀粉酶消化(图3E)。免疫组织化学染色显示肿瘤细胞CK、VIM、CK8、CD10、PAX8阳性(图3F~3H),CK7、CK19、CK20、CEA、TTF-1、S-100、CD56、SYN、HMB45、DES、MSA、SMA、LCA、CD68均为阴性,增殖活性ki-67指数在5%~40%。例1和例3结合形态及免疫组织化学,考虑为转移性CC-RCC,建议在肾脏等处寻找原发灶。例2结合形态、免疫组织化学及病史,符合脉络膜转移性CC-RCC(表1)。

图3 光镜下观察例3脉络膜转移性CC-RCC患者肿瘤组织Figure 3 Choroidal metastatic CC-RCC of Case 3
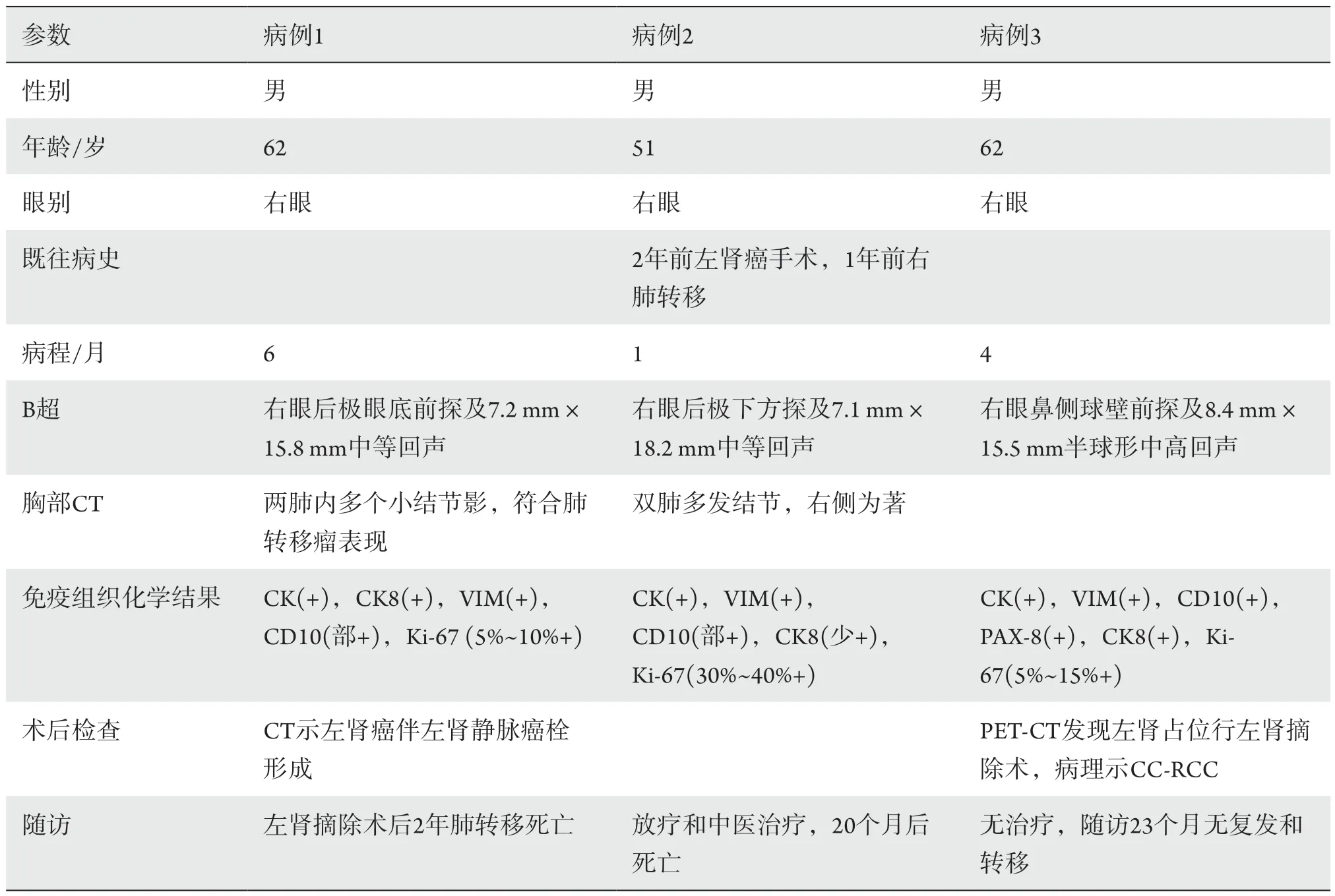
表1 3例脉络膜转移性CC-RCC的临床病理资料Table 1 Clinicopathologic data of 3 patients of choroidal metastatic clear-cell renal cell carcinoma
2.2.2 眼眶转移性CC-RCC
2例眼眶肿物切除标本镜下见大部分肿瘤细胞细胞质透亮,呈实性片巢状、腺管状、腺泡状排列(图4),核小,形状不一,部分核空泡状,可见核仁和核分裂象,例4可见肿瘤侵犯骨组织(图5)。肿瘤细胞质特殊染色PAS(+),不耐淀粉酶消化。免疫组织化学染色显示肿瘤细胞CK、VIM、CK8、EMA、CD10、PAX8阳性,CK7、CK19、CK20、S-100、SYN、CHG、HMB45、SMA、LCA、CD 68 均为阴性,增殖活性Ki-67 指数为20%~30%。例4和例5结合形态、免疫组织化学及病史,符合转移性CC-RCC(表2)。

图4 光镜下观察例5患者左眼眶转移性CC-RCC,部分区肿瘤细胞呈腺泡状排列,并见核分裂象(箭头;HE,×400)Figure 4 Orbital metastatic CC-RCC (case 5) showed some tumor cells with alveolar architecture and mitotic figure (arrow;IHC,×400)

图5 光镜下观察例4患者右眼眶转移性CC-RCC,图示肿瘤侵犯骨组织(HE,×100)Figure 5 Orbital metastatic CC-RCC (case 4) showed bone destruction (HE,×100)

表2 2例眼眶转移性CC-RCC的临床病理资料Table 2 Clinicopathologic data of 2 patients of orbital metastatic clear-cell renal cell carcinoma
2.3 治疗和随访
2.3.1 脉络膜转移性CC-RCC
例1术后腹部CT示左肾下部见一椭圆形软组织影,大小6.5 cm×5.8 cm×8.9 cm,左肾门下部肾静脉内见充盈缺损影,诊断左肾癌伴左肾静脉癌栓形成,后在当地医院行左肾摘除术,病理检查证实为左肾CC-RCC。术后2年患者因肺转移死亡。例2眼部手术后因同时肺部转移行放疗和中医治疗,20个月后死亡。例3术后PET-CT检查发现左肾占位,在当地医院行左肾摘除术,术后病理示左肾CC-RCC,肿瘤大小约4.5 cm×4 cm×3 cm。术后未行特殊治疗,随访至今23个月无复发和转移(表1)。
2.3.2 眼眶转移性CC-RCC
例4眼部手术后在肿瘤医院行靶向治疗,52个月后因出现转移死亡。例5眼部术后继续靶向药物治疗,1年后因心脏并发症死亡(表2)。
3 讨论
眼部转移性肿瘤是眼部重要的恶性肿瘤之一,约12%的癌症患者会发生眼部的转移[2]。在眼部转移癌中,73.6%仅转移至眼球,12.3%仅转移至眼眶,而14.1%同时或先后转移至眼球和眼眶[3]。
因为葡萄膜组织血供丰富,葡萄膜是全身其他部位恶性肿瘤最常见的经血液播散的眼部转移部位,其次是眼眶、眼睑和结膜[4]。1997年Shields等[5]在520例葡萄膜转移性肿瘤的总结分析中,转移性肾癌占2%,仅次于乳腺癌(47%)、肺癌(21%)和胃肠道癌(4%),位于第四位。34%的患者在发现眼内转移癌时没有肿瘤病史,眼部症状为首发。2018年Shields等[4]总结的Wills眼科医院眼肿瘤中心过去44年(1974年1月至2017年6月)的1 111例葡萄膜转移性肿瘤是迄今为止最大的一个研究队列,其中肾癌46例(4%),仅次于乳腺癌416例(37%)和肺癌295例(26%),位于第三位,可见近年来葡萄膜转移性肾癌的发病率有上升趋势。46例葡萄膜转移性肾癌的患者平均年龄为66岁,85%为单眼转移。
在2001年Shields等[6]的100例眼眶转移性肿瘤的总结分析中,肾癌及肉瘤有5例,其中肾癌 4 例,肉瘤1 瘤,均为男性,单眼,仅次于乳腺癌、前列腺癌、肺癌和皮肤黑色素瘤,位于第五位。而在男性患者中,发生率仅次于前列腺癌和皮肤黑色素瘤,位于第三位。
肾细胞癌是来源于近端肾小管上皮的恶性肿瘤,约占成人恶性肿瘤的3%。CC-RCC又称经典型肾细胞癌,是肾细胞癌最常见的类型,占肾脏肿瘤的70%~80%,多见于老年人,平均发病年龄 61岁,男性多见,男女比例为1.6:1~2:1。临床主要表现为血尿,肾区疼痛和肾区肿块;影像学检查显示为肾实质性肿物。巨检肿瘤切面黄色,易见出血坏死及囊性变。组织病理学特征为癌细胞呈立方、柱状或楔形,细胞质内含大量糖原和脂类物质,使之呈透明状,故细胞质PAS染色(+),不耐淀粉酶消化。癌细胞核呈圆形、卵圆形或不规则形,核仁可大可小,病理核分裂象不常见。癌细胞多呈实性巢索状排列,部分呈管状、腺泡状或乳头状排列,间质毛细血管丰富[7]。一般情况下肿瘤细胞表达广谱CK,低分子量上皮标记CK8、CK18和CAM5.2,同时表达VIM、CD10和PAX8。脂肪分化相关蛋白Adipophilin常阳性提示肿瘤内富含脂质[2]。Fuhrman根据癌细胞核的形态特点,将肾细胞癌分为4级(I~IV级),分级越高,细胞核的异型越大,预后越差[7]。
据统计33%的肾细胞癌会发生转移,最常见的转移部位是肺、肝、骨和脑[1],转移至眼内和眼眶非常少见。Shome等[8]总结并回顾了自1934年以来英文文献报道的68例眼内及眼眶的转移性肾细胞癌,年龄38~77(平均60)岁;男性63例,女性 5例;单眼64例,双眼4例。30例有肾细胞癌病史,发生眼部转移的时间为5~216(平均96)个月。31例转移至眼内(45.6%),31例转移至眼外(45.6%),未指明部位6例。眼内31例中,转移至脉络膜20例,虹膜7例,睫状体4例;眼外31例中,转移至眼眶25例,泪腺2例,结膜1例,眼外肌1例,眼睑1例,眉毛部位1例。在确诊眼部转移时,同时伴有全身转移的18例,其中肺13例,脑9例,骨8例,肝1例,都是肾细胞癌常见的转移部位。本组5例患者年龄51~65(平均59.2)岁,男:女为4:1。病程1~36(平均9.8)个月。例1、例2和例5都出现肺部转移,例4眼眶骨转移。5例均为单眼病变,有趣的是其中例1~3均为左肾CC-RCC转移至右眼脉络膜,为对侧转移;例4为右肾CC-RCC转移至右眼眶,例5为左肾CC-RCC转移至左眼眶,为同侧转移。文献[9]中报道部分原发肾细胞癌手术后因出现眼部转移的时间较长,在10年以上,被称为迟发的孤立性转移,常使人忽略了转移的可能性。
60%的肾癌患者与von-Hippel-Lindau综合征(VHL综合征)有关,VHL综合征是由VHL肿瘤抑制基因失活引起的遗传性肿瘤综合征,常染色体显性遗传,表现为家族多发性多器官良恶性肿瘤症候群,包括中枢神经系统和视网膜血管母细胞瘤、内淋巴囊肿瘤、肾癌、肾囊肿、肾上腺嗜铬细胞瘤、胰腺囊肿或肿瘤等。约40%的VHL综合征患者在他们一生中会发生CC-RCC。Rai等[2]曾报道1例伴有眼内视网膜血管母细胞瘤和肾癌的VHL患者发生了眼内和眼眶的CC-RCC的转移的罕见病例。本组的5例患者均无VHL综合征相关的病史。
眼内转移性肿瘤最常见累及的部位是脉络膜(88%),其次为虹膜(9%)和睫状体(2%)[5]。因眼内转移性肿瘤常引起视网膜脱离和网膜下积液,患者常表现为视物模糊、眼前黑影、闪光感及眼前漂浮物,部分因继发性青光眼引起疼痛,但也有病人没有症状仅在眼部检查时发现[10]。结合本组研究,转移至眼内的肾细胞癌较易累及脉络膜,表现为眼前黑影伴视力下降,眼底见视网膜下隆起肿块伴视网膜脱离,通常肿物可呈黄色,部分因血管丰富或出血而呈桔红色。本组3例B超均显示球内中等回声隆起肿物,厚度7.1~8.4 mm,基底宽15.5~18.2 mm,可伴有挖空征和脉络膜凹陷,故术前考虑脉络膜黑色素瘤可能大。Shields等[4]的2018年总结的46例葡萄膜转移性肾癌的肿瘤平均基底长度为9.1 mm,平均厚度为4.4 mm,高于乳腺癌(2.4 mm),肺癌(3.6 mm)和胃肠道癌 (4.0 mm),故转移性肾癌因肿物隆起较高,术前通常被诊断为无色素黑色素瘤[11]。
眼眶转移性肿瘤常表现有下述4个特点:肿物效应、浸润性生长、功能影响和炎症表现[12]。转移至眼眶的肾细胞癌多累及眼眶脂肪、肌肉和骨组织,常表现为弥漫的眼眶肿物,伴视力下降,眼球突出,眼球移位,运动受限,可扪及眼眶肿物及疼痛等。本组例4肿瘤边界不清,累及眼眶外上方伴骨质破坏,表现为眼球红肿突出,上转受限,眼球下移;例5累及眶顶眼睑皮下,为一椭圆形结节样肿块,体检可扪及皮下界清质硬肿物,伴眼球下移和上睑下垂。例5患者眼部肿物生长时间长,病史有3年,边界尚清,可能与患者一直在进行靶向药物治疗有关。
眼内和眼眶内转移性CC-RCC的病理形态接近于原发的肾细胞癌,癌细胞细胞质透明或颗粒状,呈实性片巢状和腺样分布,间质血管丰富。但有时转移灶的细胞分化可以更差或表现出不同的形态,这时免疫组织化学检查将有助于诊断,一般肿瘤细胞表达广谱CK,低分子量CK如CK8、表达VIM、CD10和PAX8。PAX8是配对盒基因家族(paired box gene family)成员,对肾的发育很重要,表达在肿瘤细胞核上。同时表达VIM和CK是它的重要特点,说明具有中胚层来源和上皮形态的特点,有助于缩小诊断的范围。另外形态上也需要和其他具有透明细胞特征的眼部原发和转移性肿瘤相鉴别,主要有具有透明细胞形态的葡萄膜黑色素瘤,软组织透明细胞肉瘤和血管周上皮样细胞肿瘤(PEComa)。1)具有透明细胞形态的无色素葡萄膜黑色素瘤中的气球状瘤细胞(balloon-cell)常见于色素膜黑色素瘤放疗后肿瘤细胞的退变,核固缩变小,细胞质呈泡沫状,免疫组织化学染色呈S-100(+)、HMB45(+)、Melan-A(+)。2)软组织透明细胞肉瘤是一种具有色素细胞分化的软组织肿瘤,组织学和免疫学表型类似黑色素瘤,表达S-100、HMB45和Melan-A,瘤细胞胞质透亮,但其具有特异性染色体易位t(12;22)(q13;q12)产生EWSR1-ATF1融合基因,可行分子病理检测证实。3)血管周上皮样细胞肿瘤(PEComa)是一种间叶性肿瘤,肿瘤内同样含丰富纤细血管网,瘤细胞胞质透亮或嗜伊红色,但瘤细胞核多较一致,核分裂象罕见,通常表达色素细胞标记HMB45和平滑肌标记SMA,上皮标记CK阴性可以鉴别。
目前肾细胞癌的治疗包括手术切除、放疗、化疗、免疫治疗(白介素和干扰素)及靶向药物(酪氨酸激酶抑制剂)的治疗。眼部转移性肾细胞癌的治疗[8]包括眼内肿物局部切除、眼球摘除、眼眶肿物切除、眼内容剜除、外放射治疗[6,8]及斑块状放疗[11],也有局部行质子治疗有效的报道[9]。
眼部转移性肾癌的预后较差,在Shields等[4]的2018年总结的46例葡萄膜转移性肾癌的平均生存期仅8.6个月,2年的生存率26%,5年生存率为零。Shome等[8]总结的随访到的39例眼部转移性肾癌病人中,13例存活(1/3),26例死亡(2/3)。本组5例患者中4例已死亡,生存时间12~52个月,平均生存期27个月,优于先前的研究报道,可能得益于目前多种靶向治疗药物的使用。
综上所述,CC-RCC可以转移至眼内或眼眶,眼部症状可以是其首发表现,眼部的临床表现和影像学检查常无特异性,有时会出现10年以上的迟发转移,需要警惕,确诊和鉴别诊断需要结合组织学形态、免疫组织化学及相关病史。早期诊断可以使患者尽早得到合适的治疗,改善预后。
开放获取声明
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。详情请访问:
https://creativecommons.org/licenses/by-nc-nd/4.0/。
