超声鉴别诊断恶性外周神经鞘瘤与神经纤维瘤
2021-10-28金珍珍王丹丹何靖楠魏凌飞
金珍珍,郭 稳,陈 涛,王丹丹,何靖楠,魏凌飞
(北京积水潭医院超声科,北京 100035)
恶性外周神经鞘瘤(malignant peripheral nerve sheath tumor,MPNST)指任何起源于外周神经施万细胞或神经鞘呈不同分化的恶性肿瘤,除外起源于神经外膜或外周神经血管系统的肿瘤[1]。MPNST预后极差,常见远处转移,原位复发风险可达40%~65%,5年生存率约20%~50%[1-3]。1型神经纤维瘤病(neurofibromatosis type 1,NF1)是MPNST最重要的风险因素,约40%的MPNST由NF1恶变形成,其中30%由深部丛状神经纤维瘤发展而来[3-4]。目前,影像学鉴别诊断MPNST与神经纤维瘤(尤其是NF1相关型)仍较为困难。本研究评价超声鉴别诊断MPNST和神经纤维瘤的效能。
1 资料与方法
1.1 研究对象 回顾性分析2010年4月—2020年4月143例于北京积水潭医院经病理证实为MPNST或神经纤维瘤的患者,MPNST组45例,男29例,女16例,年龄10~82岁,中位年龄52.0(39.5,63.5)岁,均为单发病灶,累及头颈部8例、胸背部5例、腹盆腔2例、上肢15例(腕部6例)、下肢15例(足踝1例),其中13例为NF1相关型;神经纤维瘤组98例,男46例,女52例,年龄5~77岁,中位年龄39.0(29.0,54.3)岁,均为单发病灶,累及头颈部11例、胸背部4例、腹盆腔4例、上肢57例(腕部43例)、下肢22例(足踝2例),其中5例为NF1相关型。排除标准:①复发病灶;②起源于大脑、脊髓或脊神经根;③丛状神经纤维瘤;④超声检查于病理学检查后进行。检查前患者或其监护人均签署知情同意书。
1.2 仪器与方法 采用GE Logiq E9彩色多普勒超声诊断仪,凸阵探头,探头频率1.0~5.0 MHz;线阵探头,探头频率6~15 MHz。由2名具有10年以上工作经验的超声科医师独立评估病灶二维灰阶超声声像图,意见不同时通过讨论达成一致,观察病灶位置[表浅/深在(以脂肪层与肌层间的深筋膜为界)]、大小、最大径/最小径比值、形态、边界、包膜、回声、回声均匀性、囊性成分、内部钙化、靶征(外周相对中心呈低回声)及后方回声,判断病灶是否与神经相连,以及相对神经的位置[中心型(位于神经中央),外周型(位于神经旁)];参照Alder分级法[5]评价病灶内血流丰富程度:无血流信号为0级;可见1~2条点状血流,且血管管径<1 mm为1级;可见一条主要血管且长度超过病灶的半径,或者同时可见2~3条小血管为2级;可见4条及以上血管或血管相互连通交织成网状为3级。见图1~4。
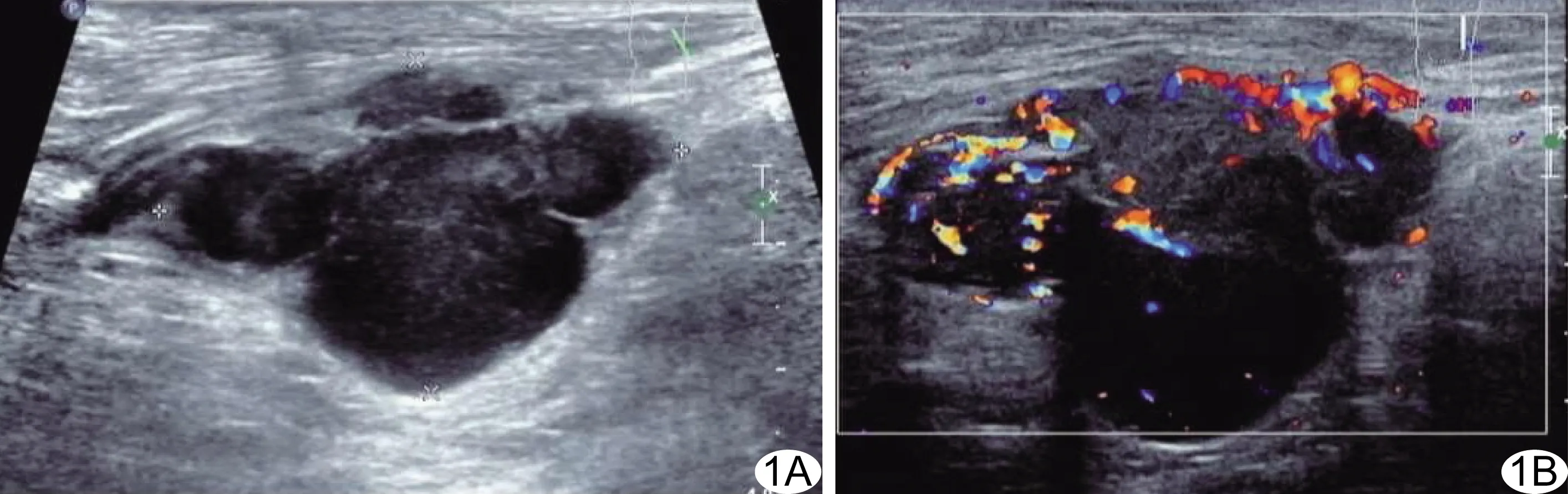
图1 患者女,55岁,MPNST A.二维超声声像图示右腘窝4.0 cm×2.7 cm×2.2 cm分叶状实性低回声肿物,位置深在,形态不规则,边界不清晰,无包膜,内部回声不均匀;B.CDFI显示血流分级为3级
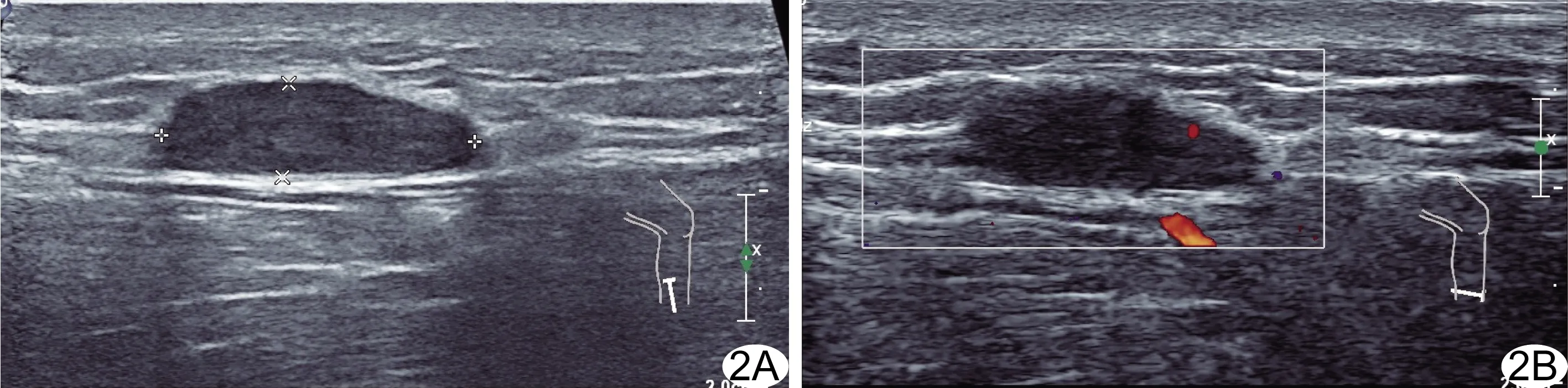
图2 患儿男,17岁,神经纤维瘤 A.二维超声声像图示左小腿下段外侧腓浅神经1.6 cm×0.7 cm×0.5 cm实性低回声肿物,位置表浅,形态规则,边界清,有包膜,内部回声均匀;B.CDFI显示血流分级为1级
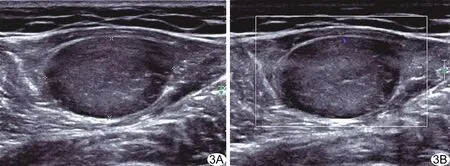
图3 患者男,34岁,神经纤维瘤 A.二维超声声像图示右大腿股内侧肌内5.9 cm×2.8 cm×1.8 cm实性低回声肿物,可见“靶征”;B.CDFI显示血流分级为1级

图4 患者女,29岁,神经纤维瘤 A.二维超声声像图示右上臂正中神经2.2 cm×1.7 cm×1.6 cm实性低回声肿物,两侧均与正中神经相连;B.CDFI显示血流分级为3级
1.3 统计学分析 采用SPSS 24.0统计分析软件。以频数表示计量资料,组间比较行χ2检验或Fisher精确概率法;以±s表示符合正态分布的计量资料,组间比较行独立样本t检验;以中位数(上下四分位数)表示不符合正态分布的计量资料,组间比较行秩和检验。将差异具有统计学意义的一般资料及超声表现纳入二元Logistic回归分析,分析鉴别MPNST与神经纤维瘤的独立因素。绘制受试者工作特征(receiver operating characteristic,ROC)曲线,并计算曲线下面积(area under the curve,AUC)评价回归模型及各超声表现鉴别MPNST与神经纤维瘤的效能,采用Delong检验评价诊断效能差异。P<0.05为差异有统计学意义。
2 结果
MPNST组患者年龄显著大于神经纤维瘤组(Z=2.670,P=0.008);组间性别差异无统计学意义(χ2=3.789,P=0.052)。
2.1 超声表现 MPNST组与神经纤维瘤组病灶位置、最大径、最小径、形态、边界、囊性成分、靶征及血流分级差异均有统计学意义(P均<0.05),见表1。
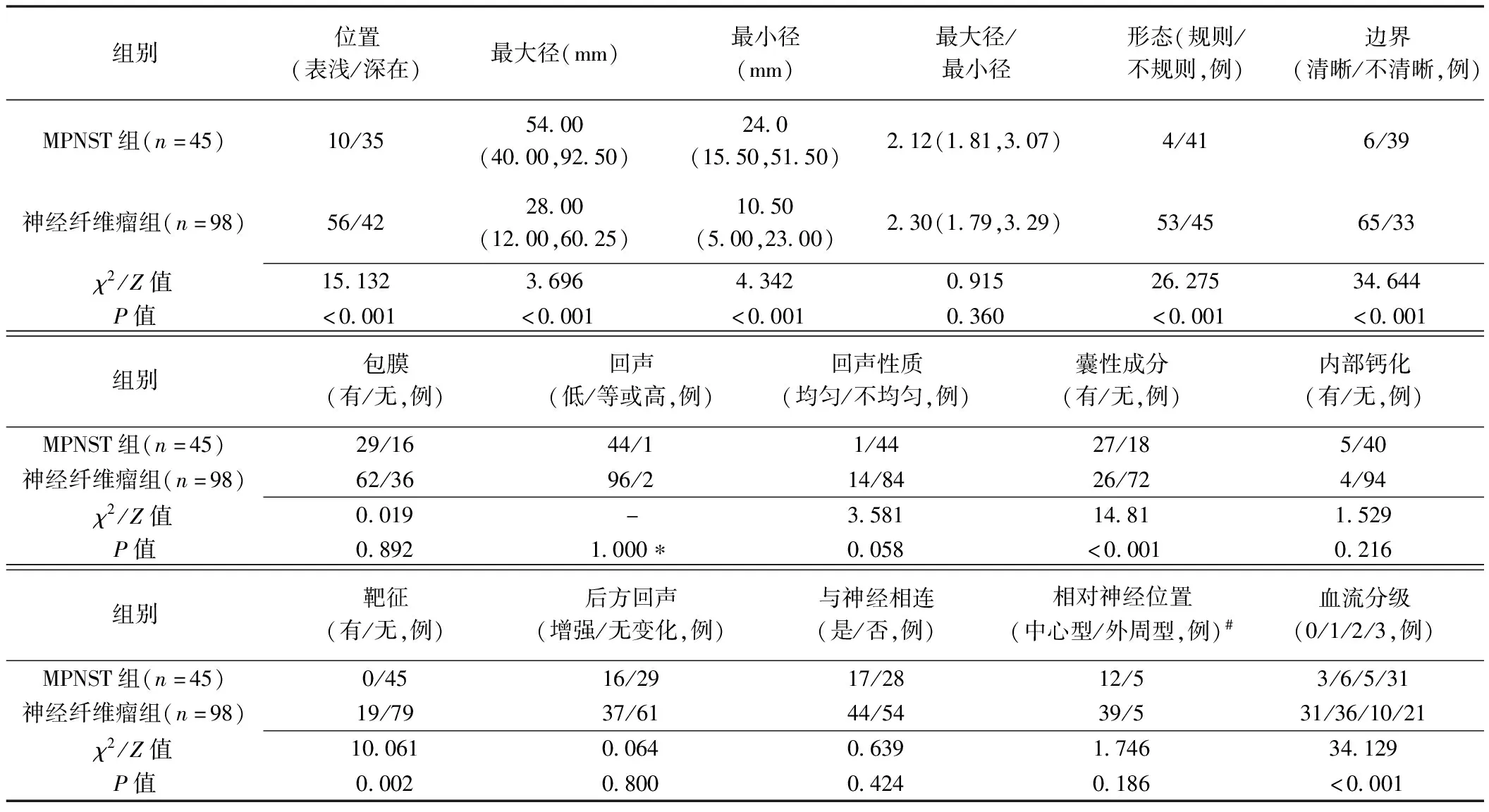
表1 MPNST与神经纤维瘤超声表现比较
2.2 回归分析 多因素Logistic回归分析结果显示,病灶位置、形态、边界及血流分级是鉴别MPNST与神经纤维瘤的独立因素(P均<0.05),见表2。回归模型公式为:Logit(P)=-5.249+1.669×位置+1.880×形态+1.743×边界+1.720×血流分级(位置:表浅=0,深在=1;形态:规则=0,不规则=1;边界:清晰=0,不清晰=1;血流分级:0/1级=0,2/3级=1)。模型系数综合检验显示模型总体有意义(χ2=74.276,P<0.001);似然比检验显示模型拟合效果较好(Cox&Snell R2=0.405,Nagelkerke R2=0.569);Hosmer-Lemeshow检验提示模型拟合优度较高(χ2=3.493,P=0.745)。

表2 Logistic回归模型鉴别诊断MPNST与神经纤维瘤
2.3 鉴别效能Logistic回归模型鉴别MPNST与神经纤维瘤的AUC为0.895,诊断效能显著高于单一根据病灶位置(AUC=0.765)、形态(AUC=0.726)、边界(AUC=0.765)及血流分级(AUC=0.742)进行鉴别(Z=5.093、5.530、5.053、4.366,P均<0.001)。将>0.164判断为MPNST,≤0.164判断为神经纤维瘤,回归模型鉴别二者的准确率、敏感度、特异度、阳性预测值及阴性预测值分别为83.92%、86.67%、82.65%、69.60%及93.10%。见图5。

图5 Logistic回归模型及超声表现鉴别MPNST与神经纤维瘤的ROC曲线
3 讨论
本研究发现MPNST组与神经纤维瘤组患者年龄、病灶位置、最大径、最小径、形态、边界、囊性成分、靶征及血流分级均存在显著差异。MPNST超声多表现为位置深在、形态不规则、边界不清的不均匀低回声肿物,多见囊性成分,后方无声影,富血供;神经纤维瘤则多为位置表浅、形态规则、边界清且有包膜的均匀低回声肿物,后方多无声影,可见靶征,与神经相连病灶多为低血供中心型,与既往研究[1,6]结果基本相符;但既往关于神经纤维瘤血供的报道[6-8]不尽相同,可能与研究对象及样本量有关。
本研究多因素Logistic回归分析结果显示,病灶位置、形态、边界及血流分级是鉴别MPNST与神经纤维瘤的独立因素;病灶大小、回声均匀性及囊性成分组间差异虽具统计学意义,但并非鉴别二者的独立因素,可能与MPNST生长较缓慢且多无明显疼痛,患者就诊时肿瘤大多已较大,而确诊MPNST较为耗时有关。回声不均多与病灶内部出血、坏死及钙化相关,也可与内部骨、软骨及脂肪组织等异源性成分有关,本组97.78%(44/45)MPNST和85.71%(84/98)神经纤维瘤回声不均匀。RYU等[6]报道,神经纤维瘤多无囊性变,认为据此可鉴别MPNST与神经纤维瘤。囊性变多因病灶内部坏死、出血或囊肿而形成,本组MPNST多见囊性成分,而神经纤维瘤较少见。
靶征反映病灶的组织学表现,其中央区由紧密排列的嗜酸性纤维(内富含细胞)和稀疏的非纤维基质(如黏液样物质)组成,周围由松散排列的嗜酸性纤维(内细胞稀少)和丰富的非纤维性基质组成。本研究中19.39%(19/98)的神经纤维瘤可见靶征,与既往报道中靶征显示率11.5%~29.0%[7-8]相符,但低于MRI的47.0%~70.0%[9],可能与MRI组织对比度高于超声有关。本组MPNST均未见靶征,提示该征象有助于鉴别良恶性神经肿瘤,但并非独立因素。此外,本研究中出现靶征的神经纤维瘤超声均表现为中央低回声、周围呈低-无回声,即周围相对中央回声更低,与RYU等[6,10]描述的神经纤维瘤中央呈高回声、周围呈低回声不同,可能与病灶内嗜酸性纤维(内富含细胞)与非纤维基质所占比例不同有关。
综上,超声可为临床鉴别诊断MPNST与神经纤维瘤提供依据。但本研究样本量偏小,且NF1相关型病例较少,未能实行对比研究,有待完善。
