持续性肺动脉高压新生儿行吸入性一氧化氮治疗后死亡的危险因素▲
2021-10-27赵钰玮刘光辉戴立英盛卫婷
赵钰玮 刘光辉 戴立英 郑 洪 王 燕 王 磊 盛卫婷
(安徽省儿童医院新生儿科,合肥市 230051,电子邮箱:zyw3257@sina.com)
新生儿持续性肺动脉高压(persistent pulmonary arterial hypertension,PPAH)是由于新生儿出生后胎儿型循环无法正常过渡到正常“成人”型循环而导致的严重心肺并发症,是危重新生儿致死的主要病因之一。一氧化氮被认为是血管舒张因子,能够选择性扩张肺动脉血管进而降低肺动脉压力,同时不影响体循环。近年来,吸入性一氧化氮(inhaled nitric oxide,iNO)技术被应用于治疗足月儿及近足月儿PPAH,但仍有30%的患儿在iNO治疗后效果不佳而生命受到威胁[1]。本研究回顾性分析在我院新生儿重症监护病房(neonatal intensive care unit,NICU)使用iNO技术治疗的PPAH患儿的临床资料,探讨PPAH患儿iNO治疗后死亡的风险因素。
1 资料与方法
1.1 临床资料 回顾性分析2018年1月至2019年12月我院NICU收治的39例PPAH患儿的临床资料。纳入标准:符合《新生儿肺动脉高压诊治专家共识》[2]中关于PPAH的诊断标准;出生胎龄≥34周,出生后3 d内进行iNO治疗。排除复杂性先天性心脏病、中枢性呼吸暂停、出血性疾病或严重贫血、先天性膈疝、遗传代谢性疾病、先天性多发畸形、iNO治疗前已使用血管扩张药或治疗时间不足24 h、放弃治疗而死亡的患儿。其中,男婴30例、女婴9例,出生胎龄(38.93±1.84)周,出生体重(3421±752)g。根据日龄28 d时是否存活将患儿分为存活组29例和死亡组10例。
1.2 临床资料收集 记录患儿胎龄、体重、性别、母亲年龄、分娩方式、围生期疾病史(胎膜早破史、新生儿窒息史、新生儿呼吸窘迫综合征、肺炎、胎粪吸入性综合征、先天性心脏病、败血症)、肺表面活性物质的使用情况;经iNO治疗前动脉血pH、PaO2、PaCO2数值,以及iNO治疗时机械通气模式及iNO最大剂量;iNO、机械通气、氧疗使用时间及住院时间。所有数据由2名临床医生进行校对录入。
1.3 iNO治疗方法 根据患儿病情采用常频或高频机械通气模式进行iNO治疗,以开始吸入一氧化氮作为治疗起点,初始剂量为20 ppm,吸入30 min后如患儿皮肤青紫改善,则根据经皮氧饱和度变化调节一氧化氮吸入流量,如皮肤青紫改善不明显可予以调高一氧化氮吸入流量。治疗用一氧化氮经专用质量流量控制仪调节适合流量后接入呼吸机供气管道中,在近患儿气道端 Y 形管接口处使用一氧化氮治疗仪(英国SLE公司,型号:SLE3600)监测气道中一氧化氮和二氧化氮浓度。气体由复旦大学附属儿童医院提供。治疗期间使用全自动血气、电解质和生化分析仪(美国i-STAT公司,型号:i-stat300)监测动脉血气分析及高铁血红蛋白浓度,其中高铁血红蛋白浓度均未见异常。
1.4 统计学分析 应用SPSS 17.0软件进行统计分析。符合正态分布的计量资料以(x±s)表示,组间比较采用t检验,不符合正态分布的计量资料以中位数(四分位数)表示,组间比较采用非参数检验;计数资料以例数(百分比)表示,组间比较采用χ2检验或Fisher精确检验;纳入单因素分析中P<0.1的因素进行二元Logistic回归分析,以P<0.05为差异有统计学意义。
2 结 果
2.1 两组患儿一般资料、围生期疾病和治疗史的比较 死亡组新生儿窒息发生率高于存活组,肺表面活性物质使用率低于存活组(均P<0.1)。两组患儿的出生时胎龄、体重、性别、母亲孕龄、分娩方式、其他围生期疾病史比较,差异均无统计学意义(均P>0.05)。见表1。
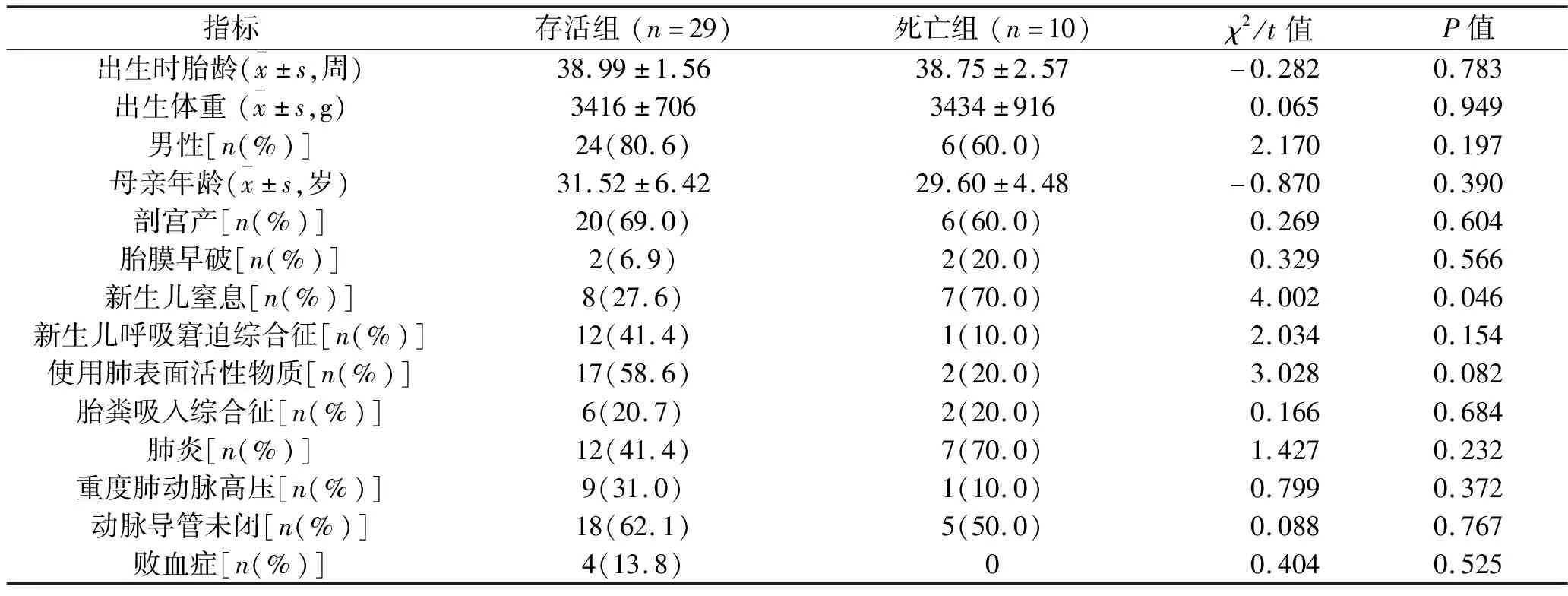
表1 两组患儿一般资料、围生期疾病和治疗史的比较
2.2 两组患儿行iNO治疗前血气分析指标和治疗情况的比较 死亡组患儿iNO治疗前动脉血pH值低于存活组(P<0.1),但两组治疗前其他血气分析指标、iNO治疗时高频机械通气情况及使用iNO最大剂量比较,差异均无统计学意义(均P>0.1)。存活组iNO吸入时间、机械通气时间、氧疗使用时间及住院时间均长于死亡组(均P<0.05)。见表2。
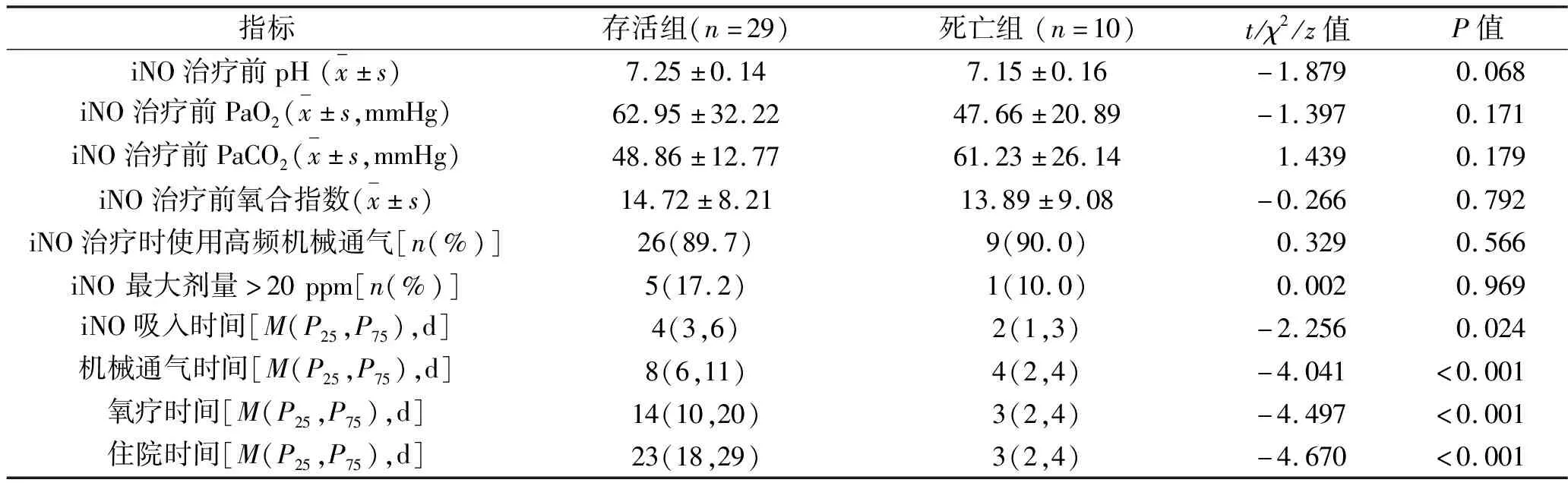
表2 两组患儿iNO治疗前血气分析指标和治疗情况的比较
2.3 PPAH患儿iNO治疗后死亡危险因素的多因素分析 将新生儿窒息(无=0,有=1)、使用肺表面活性物质(应用=0,未用=1)及iNO治疗前pH值[以正常值上下限(7.35~7.45)作为分界标准,7.35~7.45=0分,<7.35 或>7.45=1]作为自变量,患儿日龄28 d时存活情况(存活=0,死亡=1)作为应变量,纳入二分类Logistic回归模型并进行分析,iNO治疗相关数据未列入多因素分析。结果显示,新生儿窒息、未使用肺表面活性物质是影响PPAH患儿行iNO治疗后死亡的独立危险因素(P<0.05),见表3。
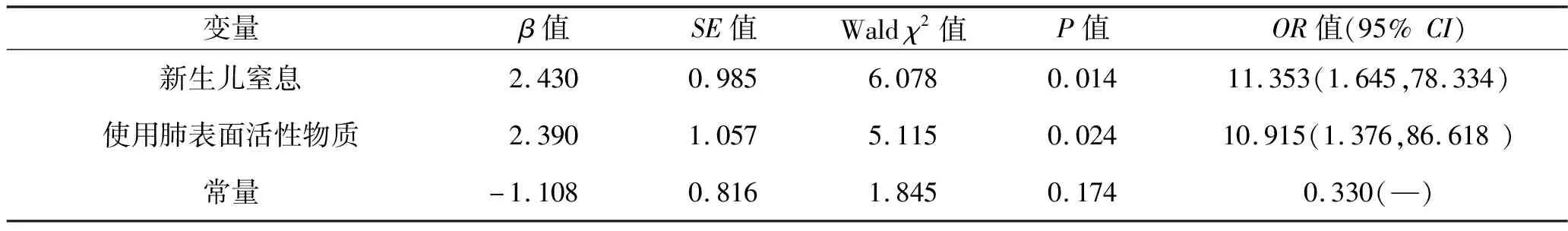
表3 PPAH患儿行iNO治疗后死亡危险因素的多因素分析
3 讨 论
新生儿PPAH是指新生儿出生后胎儿型循环过渡到正常“成人”型循环发生障碍,导致肺循环压力持续增高,大量血流经卵圆孔和(或)动脉导管水平由右向左分流,从而出现严重的低氧血症和发绀的病理状态。PPAH是常见的新生儿危重症疾病之一,其发病率约2‰[3],多见于存在围生期窒息、呼吸窘迫综合征、胎粪吸入、败血症等新生儿,也可能发生于存在先天性肺血管发育异常的新生儿。临床上除了对原发疾病的治疗外,主要治疗方案包括机械通气呼吸及使用正性肌力药物维持体循环压力。近年来,使用血管扩张剂直接降低肺循环压力也越来越常见,但该方案存在体循环低血压的风险,其安全性和有效性尚未完全明确。由于一氧化氮是一种具有较强扩张血管作用的内皮血管扩张因子,其对肺血管具有高度选择性的扩张作用,在快速降低肺动脉压力的同时不影响体循环压力,具有增加肺血流、减少肺内血管分流、提高肺泡通气与血流比值的效果,可减少体外膜肺的使用,故iNO治疗PPAH安全、有效[4]。
研究表明,新生儿窒息是发生PPAH的高危因素之一[5]。本研究结果显示,新生儿窒息是PPAH足月或近足月儿iNO治疗后死亡的独立危险因素(P<0.05),存在新生儿窒息者的死亡风险是无新生儿窒息者的11.353倍。新生儿出生后血管内皮细胞分泌血管舒张因子内源性一氧化氮,从而有效地扩张肺血管,降低肺动脉压力;但因出生过程中及出生后一些病理因素导致一氧化氮被氧化成亚硝酸盐而引起肺血管收缩,使得肺循环阻力增高。决定一氧化氮生物利用度的主要因素是体内超氧阴离子的血液浓度,产时缺氧、肺部病变、窒息后大量吸入高浓度氧等因素共同导致机体内氧化应激加重,超氧阴离子浓度增加,引起一氧化氮失活;补充外源性一氧化氮时也可能出现一氧化氮被氧化而产生大量亚硝酸盐的风险,进而加重病情[6]。因此,存在新生儿窒息高危因素的足月或近足月PPAH患儿行iNO治疗后预后更差。Morel等[7]的研究结果也提示新生儿窒息复苏影响足月或近足月的呼吸衰竭患儿iNO的治疗效果。但也有研究表明,对于胎龄小于34周的早产儿,严重产时窒息对iNO治疗后的疗效和死亡均无明显影响,其原因主要与早产儿高肺循环和肺发育不成熟及肺血管床少相关:早产儿肺血管系统对于氧依赖的肺血管扩张应答不佳,因此无论窒息发生情况如何,大部分早产儿的iNO治疗效果均不佳[8]。
肺泡表面活性物质是由Ⅱ型肺泡上皮细胞合成和分泌的一种磷脂蛋白复合物,能够降低肺泡表面张力、增加肺的顺应性,维持相对稳定的肺泡内压,其主要用于肺泡表面活性物质分泌不足或缺失的新生儿呼吸系统疾病的治疗。有研究表明,iNO治疗有益于降低肺泡表面张力,且能够明显提高肺泡表面活性物质蛋白A和蛋白B的mRNA表达水平,故肺泡表面活性物质气管内滴注联合iNO治疗能够促进肺泡复张,改善患儿氧合功能[9-10]。有研究结果显示,iNO治疗联合应用肺泡表面活性物质能够显著地降低体外膜肺氧合的使用率和患儿死亡率,且早期两者联合使用能够降低氧合指数为15~20的患儿呼吸衰竭恶化的风险[11]。本研究结果显示,生后3 d内行iNO治疗但未使用肺表面活性物质的患儿预后更差,其死亡风险是已使用肺表面活性物质患儿的10.915倍,提示使用肺表面活性物质是PPAH患儿行iNO治疗预后的保护性因素。因此,使用表面活性物质气管内滴注疗法能够改善 PPAH患儿行iNO治疗的预后。
本研究结果显示,死亡组iNO治疗时间、机械通气、氧疗及住院时间均短于存活组(P<0.05),其主要原因为死亡组患儿因行iNO治疗效果不佳而放弃进一步治疗,或者因短期内病情进行性加重而死亡,故未将这些数据列入回归分析中。
综上所述,新生儿窒息和未使用肺表面活性物质是生后3 d内进行iNO治疗的足月或近足月PPAH患儿死亡的危险因素。因此,尽可能避免新生儿窒息并及时使用肺表面活性物质可改善PPAH患儿行iNO治疗后的预后。由于本研究样本数有限,故关于围生期病史、机械通气模式的选择、呼吸机参数的设置等方面对iNO治疗PPAH患儿的预后的影响还需要大样本的研究证实。
