乳化交联法和蒸发溶剂法制备柠檬精油微球的比较
2021-10-12常香玉李慧卿曹叶霞张馨蕊
常香玉 李慧卿 曹叶霞 张馨蕊
(1. 山西大学分子科学研究所,山西 太原 030000;2. 忻州师范学院化学系,山西 忻州 034000)
柠檬又称洋柠檬、宁果、益母果等,为双子叶纲芸香料柑橘属植物[1-2],在全球被广泛种植[3]。柠檬精油分布于柠檬皮中,是柠檬香味的主要来源[4-5],具有抗菌、消炎和感官保护等多种功能[6]。但由于柠檬精油易挥发、易降解,限制了其应用范围。精油微球化可以克服柠檬精油相关稳定性的限制,延长其保质期[7-8]。
微球的制备方法很多,有溶剂挥发法、乳化交联法、凝聚法、微孔淀粉吸附、相分离法等多种方法[9-10]。试验采用两种最普遍的技术,溶剂挥发法和乳化交联法制备微球。海藻酸钠是一类阴离子的水溶性多糖,具有易降解、低毒、生物相容性等特点,在温和条件下可与二价阳离子(如钙离子)发生凝胶化[11],非常适合于作为微球壁材包裹各种内容物。明胶是一种来源于变性胶原蛋白的蛋白质,乳化性好,增稠性好,具有良好的生物相容性和可降解性,也是制备药物载体或微球壁材的主要原料。但单一壁材的微球,结构相对疏松、内容物容易突释,难以实现良好的缓释。明胶与海藻酸钠混合,两者可以通过形成均匀的溶液,再通过共价交联剂形成不溶性凝胶。这种复合壁材更有利于内容物包埋和缓释,因而试验以海藻酸钠/明胶作壁材。海藻酸钠/明胶制备微球,文献中多采用锐孔悬滴法,其制作的多为胶囊,径粒在80 μm以上[12-13],且容易脱水。采用乳化交联法,可以制备径粒更小,且更易于分散的稳定微球颗粒。聚乳酸—羟基乙酸共聚物(PLGA)为另一种生物相容性的合成聚合物,在生药领域已被广泛作为载体使用,而其作为壁材制备微球,一直以来,主要采用溶剂蒸发法[14]。但以PLGA壁材制备微球,径粒也多在50 μm以上[10,14],而且以其壁材对疏水性精油的包结微球目前尚未见报道,更未发现针对两种微球技术对相同精油的包结行为进行的比较研究,对精油微球的应用作参考性指引。故试验拟通过上述方法制备两种柠檬微球,通过扫描电镜(SEM)对其形貌进行表征,并基于包封率、产率、负载率、抗氧化性、热稳定性等参数对两种微球进行评估,以期为利用精油增香、防腐、抗氧化、抗菌等功能开发新产品提供依据。
1 材料与方法
1.1 材料与仪器
1.1.1 材料与试剂
柠檬皮:市售;
海藻酸钠:分析纯,国药集团化学试剂有限公司;
明胶:生物试剂级,国药集团化学试剂有限公司;
聚乳酸—羟基乙酸共聚物(PLGA):两种分子数比为50∶50,MW38 000~54 000,国药集团化学试剂有限公司;
聚乙烯醇(PVA):Mw约27 000,国药集团化学试剂有限公司;
吐温80:生物技术级,国药集团化学试剂有限公司;
司盘80:化学纯,国药集团化学试剂有限公司。
1.1.2 主要仪器设备
紫外可见分光光度计:UV-2450型,上海精密科学仪器有限公司;
数控超声波清洗机:KQ-400KDZ型,深圳市昌源科技有限公司;
真空冷冻干燥机:LGJ-10型,深圳市科力易翔仪器设备有限公司;
高压均质机:APV-1000型,上海顺仪实验设备有限公司;
扫描电镜:TESCAN型,泰思肯(中国)有限公司;
热分析仪:STA 449 F5 Jupiter型,德国耐驰公司;
高效液相色谱仪:LC610型,北京普瑞分析仪器有限公司。
1.2 方法
1.2.1 柠檬精油的提取
(1) 水蒸气蒸馏法:取新鲜柠檬手工剥皮,去除皮内白色纤维物,粉碎,过80目塞,备用。精密称取40.0 g柠檬果皮碎粒置于250 mL的圆底烧瓶中,加50 mL蒸馏水,超声30 min,采用精油蒸馏装置提取2 h,收集馏出液上层,重复两次,计算提取率[13]。所得精油于冰箱贮存。
(2) 柠檬精油提取率的计算:
(1)
式中:
Y——提取率,%;
m1——柠檬精油质量,g;
m2——柠檬皮质量,g。
1.2.2 柠檬精油微球制备
(1) 海藻酸钠/明胶微球:利用乳化法制备微球,然后与氯化钙交联[14-16]。柠檬精油(对照空白微球不加精油)溶于1.5 mL吐温80中,明胶加热融溶于10 mL水中,混匀,加入5%海藻酸钠水溶液(10 mL)中,然后将混合液倾入含有司盘80的液体石蜡(V司盘∶V石蜡=1∶10)中,在1 500~2 000 r/min转速下搅拌60 min。氯化钙溶解于甲醇和异丙醇(V甲醇∶V异丙醇=2∶3)的混合溶剂中配成浓度为0.2 mol/L溶液,取10 mL加入乳化液中,继续搅拌1 h以确保有效交联。真空过滤收集微球,异丙醇洗涤3次,脱水处理。将脱水后的湿微球铺平在表面皿中,将表面皿放入50 ℃电热鼓风干燥箱中,干燥1.5 h后取出。
(2) PLGA微球:采用溶剂蒸发技术制备微球。柠檬精油(对照空白微球不加精油),PLGA溶于二氯甲烷,高速搅拌混合均匀。混合溶液慢慢转入1 g/100 mL的PVA溶液中,均化。再将乳液加入0.3 g/100 mL PVA水溶液中,高速搅拌均匀。继续以适当速度搅拌12 h,蒸发有机溶剂。得到的微球过滤,用水洗涤3次,真空干燥(40 ℃,1 h)。
1.2.3 柠檬微球载油率、包封率和产率 准确称量柠檬精油微球溶解在适量的二氯甲烷中,加入一定量体积的含0.1 g/100 mL的吐温80的双蒸馏水,磁力搅拌器搅拌过夜,以去除有机相。溶液过滤,用分光光度分析测定253 nm处吸光度(柠檬烯特征吸收)。用含0.1 g/100 mL吐温80的双蒸馏水配制不同浓度的柠檬精油,测定253 nm处吸光度作标准曲线,根据标准曲线确定包封精油含量[17]。根据式(2)~式(4)计算载油率、包封率和产率[18]。
(2)
(3)
(4)
式中:
EE——包封率,%;
mO——包封入微球的精油的质量,g;
mTO——投放精油的质量,g;
LE——负载率,%;
mM——微球的质量,g;
Y——产率,%;
mTW——投放壁材的质量,g。
1.2.4 柠檬微球缓释性能测定 将定量的精油微球悬浮在已知体积的含0.1 g/100 mL Tween 80的双蒸馏水中,用磁力搅拌器以200 r/min恒转速旋转,温度设定在25 ℃。每隔一定时间间隔,提取5 mL等量样品,离心(4 000 r/min,3 min),取上清液测定253 nm处柠檬烯特征吸收,并补充同体积新鲜溶液于母液中。根据标准曲线,从吸光度值确定释放精油量。根据精油负载率,计算定量微球中精油总量,释放精油量与微球负载量的比值为释放百分率。重复以上操作,平行对照3组试验,取平均值。
1.2.5 柠檬精油抗氧化能力测定
(1) 清除DPPH自由基能力:配制质量浓度为0.1 mmol/mL 的DPPH乙醇溶液,备用。另取2 mL无水乙醇溶液和DPPH溶液,混合均匀,在517 nm处测定其吸光度值(A1);分别取质量浓度为1,2,4,6,8 mg/mL柠檬精油乙醇溶液2 mL于5支比色管中,各加入DPPH乙醇溶液2 mL,混合均匀后放置于暗处反应20 min,测定517 nm处吸光度值(A2);分别取质量浓度为1,2,4,6,8 mg/mL柠檬精油乙醇溶液2 mL于5支比色管中,各加入2 mL乙醇溶液,测定其517 nm处吸光度值(A3)。根据式(5)计算柠檬精油对DPPH自由基的清除率。
(5)
式中:
K——DPPH自由基清除率,%;
A1——DPPH自由基517 nm处吸光度;
A2——加样后DPPH自由基吸光度;
A3——样品517 nm处吸光度。
(2) 海藻酸钠/明胶微球和PLGA微球清除DPPH自由基能力:烧杯中加入定量柠檬精油微球,用10 mL无水乙醇浸泡,于100 ℃超声1 h,每隔一定时间取上清液0.1 mL并加入0.1 mmol/L的DPPH乙醇溶液3.9 mL,混合均匀后于暗处反应20 min,于517 nm处测其吸光度值(A1)。另取一试管用0.1 mL无水乙醇代替试样,所测吸光度为A2;取0.1 mL微球乙醇溶液并加入3.9 mL无水乙醇溶液,测定其吸光度值(A3)。每间隔测定上述的吸光度值。根据式(5)分别计算出两种微球对DPPH自由基的清除率。
2 结果与讨论
2.1 柠檬精油的提取
提取柠檬精油经济实惠的方法主要是冷榨和水蒸气蒸馏法。传统的冷榨虽然便捷,但冷榨会使香芹醇、萜等含量下降[13],而且容易溶入其他非芳香组分。而水蒸气蒸馏得到的馏分为挥发性芳香组分,少有其他非香味成分,因而被采用。精油的挥发性成分由碳氢化合物和倍半萜以及含氧衍生物:醛、醇、酯和氧化物组成。它也包括醇、醛和脂族酯。柠檬果皮精油主要成分为柠檬烯,占72.5%~76.4%,其次为β-蒎烯,占11.6%~18.7%。其他几种单萜类化合物含量也较高,分别为松油烯(2.88%~8.26%)、α-蒎烯(1.4%~1.5%)和月桂烯(0.95%~1.12%)[19]。水蒸气蒸馏方法获得柠檬精油与超临界萃取、压榨法等相比,单萜、倍半萜、含氧化合物等主要成分的含量差别不大[20]。试验所得精油为无色透明的油状物,密度为0.857~0.862,有香浓的柠檬味道,产率为6.79%,柠檬烯为其主要成分。
2.2 柠檬精油微球的电镜分析
从图1可以看出,无论是空白还是载油,海藻酸钠/明胶微球都是径粒均匀的球体或类球体,直径约为2~4 μm,载油微球无明显增大。PLGA微球径粒基本在2~10 μm,其载油微球比空白微球也无明显增大,但表面明显比海藻酸钠/明胶光滑(图2)。PLGA与海藻酸钠虽分别为合成材料与天然材料,但都是易与生物体相容的高分子材料,其微球产品适宜于食品、药品等相关行业应用。径粒微小的微球由于分散性更好,更易于投放及保存,更适宜于上述行业。海藻酸盐液体的黏度很高,采用锐孔滴定等形成液滴的方法会产生大尺寸的微粒,试验所用的两种方法制备的微球,径粒相对较小,满足其作为精油负载体的需求。
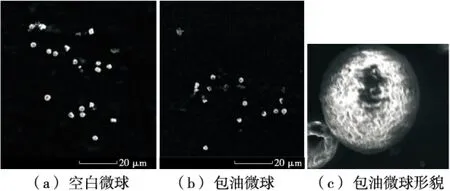
图1 海藻酸钠/明胶微球Figure 1 SEM photograph of sodium alginate/gelatinmicrospheres

图2 PLGA微球扫描电镜图Figure 2 SEM photograph of PLGA microspheres
2.3 两种微球的载油率效果比较
海藻酸钠/明胶精油微球的包封率为(57.83±1.35)%,微球产品产率(62.16±1.80)%。PLGA微球包封率和产率都有所下降,分别为(13.07±1.62)%和(40.37±1.57)%(表1)。说明试验条件下,海藻酸钠/明胶微球较PLGA微球对柠檬精油的承载效果好。在PLGA微球形成过程中,伴随着溶剂蒸发,可能存在精油的挥发,从而引起包封率的变化。除了方法的差异之外,海藻酸钠/明胶复合壁材组合,存在氨基、羟基、羰基等多种官能团,对包结行为较为有利,但微球表面相对而言不是特别光滑,使其更容易附着精油,可能也是其包封率较高的原因。

表1 两种微球的载油率效果比较
2.4 两种微球的缓释性能分析
如图3所示,海藻酸钠/明胶微球和PLGA微球中精油释放过程,几乎都可以概括为3个阶段:快速释放阶段(前5 h)、持续稳定释放阶段(5~16 h)和衰减阶段(16 h后)。第一阶段虽然释放较快,但两种微球均未出现爆发式的突释,可能是受制备过程中初始水相溶剂的影响[21]。两种微球在16 h时累计释放率分别为39.9%和22.5%。而在16 h后两种微球的释放曲线趋势较为平缓,24 h内均未超过40%,出现了缓慢释放阶段,实现了持续的释放。
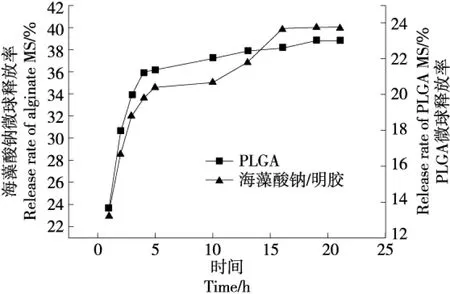
图3 两种微球的缓释曲线Figure 3 Cumulative release curves from two kindsof microspheres
2.5 柠檬精油微球的抗氧化能力
据报道[19],约34种柑桔类精油及其组分对DPPH自由基都具有清除活性,并且所有成分的清除活性均在17.7%~64.0%。试验所提取的柠檬精油对DPPH自由基有明显的清除作用,清除率随着柠檬精油浓度的增加而增大,最高达到72.36%,具有很强的抗氧化能力。精油之所以能清除自由基,在于其组分中具有共轭双键的次生物质或酚类、多羟基类物质,比如香芹醇、柠檬烯、大茴香醇等,它们通过转移电子或氢给自由基从而实现清除目的。精油微球化使用,无法定量与精油抗氧化性比较,但其自由基清除能力与其缓释行为应存在相关性。图4是两种微球对DPPH自由基的清除率随着浸泡时间的变化曲线,随着时间的延长,两者对DPPH自由基的清除率逐渐增高。0~6 h两种微球的DPPH自由基清除率呈迅速增加趋势,但在6 h之后两种微球对DPPH自由基的清除率呈缓慢增加趋势。由于包封的精油含量不同,虽然等量的海藻酸钠/明胶微球在同样的时间内释放百分率相同,但释放的净质量不同。海藻酸钠/明胶微球释放的精油多于PLGA微球的,因而清除效果优于PLGA微球。虽然两者清除效果有差别,但两者对DPPH自由基的清除率与其精油缓释行为一致。与未包封的柠檬精油相比,微球中柠檬精油,由于高分子量的壁材在水化后形成了一层厚厚的凝胶层,起到了屏障作用,使精油逐渐缓缓溶出逐步发挥作用。这种释放速率较慢,需要延续时间逐渐累积清除效果,但可以控制释放行为。
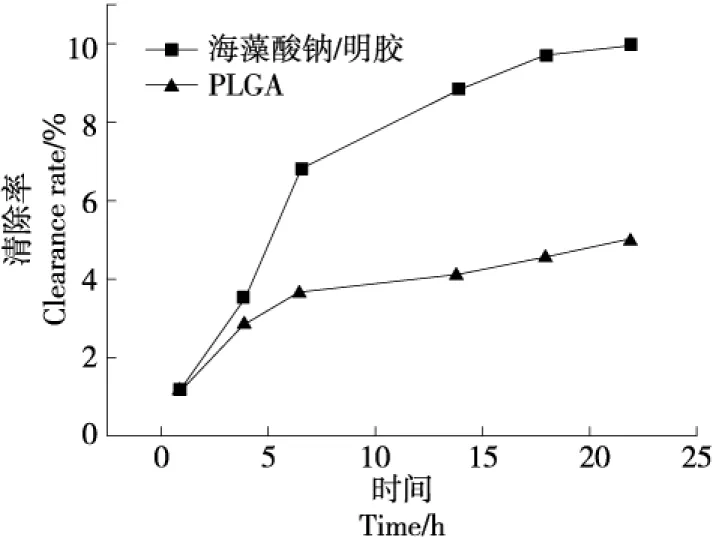
图4 包被海藻酸钠/明胶与PLGA的精油微球的DPPH清除率
2.6 精油微球的热稳定性分析
由图5可知,海藻酸钠/明胶微球分解为4个阶段,而PLGA微球分解近似分为3个阶段。海藻酸钠/明胶微球升温到180 ℃时失重可分为两个阶段,初始在达到50 ℃前,失重和缓,失重较少,为表面携带少量精油或少部分水分子挥发[22];从50~180 ℃失重曲线变陡,失重量明显增大,到拐点超过20%,主要对应于精油及结合水损失[23]。阶段三对应180~210 ℃的升温过程中,失重约为30%~80%,应为主要壁材分解阶段。最后阶段,海藻酸钠/明胶微球在210~500 ℃时恒重,表明还有些许材料残余,这应该与无机钙通过配位与材料交联有关。
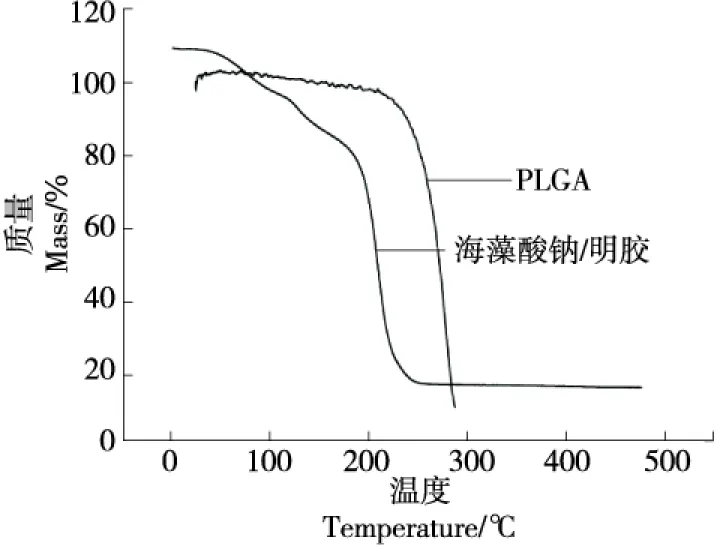
图5 两种微球的热稳定性曲线Figure 5 Thermal stability curves of two kindsof microspheres
而PLGA微球在第一阶段升温至200 ℃时,PLGA微球的整体热失重趋势比较平稳,失重不足10%,应为芯材挥发过程。在阶段二,对应200~270 ℃的升温过程中,包含了20%~90%的失重,这意味着壁材的分解[24]。最后,由250 ℃升温至500 ℃的过程中,PLGA微球的壁材和芯材已经完全分解挥发殆尽。
微球不同的失重曲线主要来自壁材材质结构的差异,PLGA聚合分子本身比海藻酸钠有较高的分解温度,从而也表现在微球特点上。钙离子交联海藻酸钠/明胶,并未给微球主体分解带来额外明显的稳定作用。虽然两种微球在180 ℃以下,几乎可以稳定存在,但PLGA微球表现出了更好的对热稳定性。
3 结论
水蒸气蒸馏方法提取得到柠檬精油,产率为6.79%;然后以海藻酸钠/明胶和PLGA壁材,分别采用乳化交联法和溶剂蒸发方法制备微球。两者均得到了径粒在10 μm以内的微球,海藻酸钠/明胶微球包封率和产量均高于PLGA微球的;比较缓释行为,海藻酸钠/明胶微球,24 h内累积释放率微高于PLGA微球,但PLGA微球的热稳定性强于前者,可以在200 ℃下稳定存在。如应用于冷饮类食品,海藻酸钠/明胶微球具有优势,但PLGA微球可能更适用于需要高温烘培的食品。相比文献[13-14,22,24]记录的同壁材微球,试验制备的两类微球径粒更小,使之能很好地分散在食品基质中,而不影响食品本身的特性。
