基于层次分析法和正交设计法优选盆消灌肠液的提取工艺
2021-08-26蔡妮娜曹富宁范源俊李小金夏循明
蔡妮娜,曹富宁,谢 宁,范源俊,李小金,夏循明
(南宁市中医医院,广西 南宁 530001)
盆消灌肠液的立方根据慢性盆腔炎热、毒、湿、瘀、寒的病机特点,以清热利湿、活血化瘀、养血通络为治疗原则,由丹参、赤芍、三棱、莪术、当归、大血藤、蒲公英、紫花地丁、败酱草、桂枝、马鞭草等多种药材配伍组成。前期临床观察发现,盆消灌肠液具有清热解毒、活血化瘀、止痛之功效,对缓解慢性盆腔炎腹痛、腰骶胀痛、带下量多、经期腹痛、炎性包块及子宫压痛等症状有显著的疗效[1-2]。通过查阅文献[2-7]可知,盆消灌肠液中,各药材有效组分主要为酚酸类、苯丙素类、苷类及黄酮类等,均以一定比例乙醇作为提取溶剂,为使有效成分充分浸出,同时满足本院制剂生产实际条件,本研究采用渗辘提取法,以方中有效成分绿原酸、咖啡酸、芍药苷、阿魏酸、丹酚酸B的含量和干膏得率作为评价指标,采用层次分析法(AHP)确定各指标权重系数,以乙醇浓度、乙醇用量、浸渍时间和渗漉速度为考察因素,结合正交设计实验法优选出最佳渗辘提取工艺,为该制剂的大生产提供理论依据。
1 仪器与材料
1.1 仪器
1260 InfinityⅡ型HPLC仪,包括四元泵、自动进样器、柱温箱、DAD检测器、色谱工作站 (美国Agilent公司);十万分之一XS205电子分析天平(梅特勒-托利多仪器上海有限公司);WH-800超声波清洗机(济宁万和超声电子设备有限公司,功率:800 W,频率:40 kHz);Best-S30超纯水机(芷昂仪器上海有限公司)。
1.2 材料
丹参、赤芍、三棱、莪术、当归、大血藤、蒲公英、紫花地丁、败酱草、桂枝、马鞭草饮片均购于安徽德昌药业饮片有限公司,经南宁市中医医院制剂室曹富宁副主任中药师鉴定,符合有关规定;绿原酸(中国食品药品检定研究院,批号:110753-200413,纯度:98.70%)、咖啡酸(成都曼思特生物科技有限公司,批号:MUST-20032003,纯度:99.48%)、芍药苷(成都曼思特生物科技有限公司,批号:MUST-19110118,纯度:98.69%)、阿魏酸(成都曼思特生物科技有限公司,批号:MUST-20032928,纯度:98.32%)、丹酚酸B(成都曼思特生物科技有限公司,批号:MUST-19062808,纯度:99.79%);乙腈为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 正交试验设计
在预试验基础上,确定乙醇浓度(A)、乙醇用量(B)、浸渍时间(C)和渗漉速度(D)为影响因素,每个因素各取3个水平进行 L9(34)正交试验,正交试验因素水平见表1。

表1 盆消灌肠液正交试验因素水平
2.2 供试品的制备
按处方2倍量称取丹参、赤芍、三棱、莪术、当归、大血藤、蒲公英、紫花地丁、败酱草、桂枝、马鞭草等药材各9份,每份765 g,打成粗粉,按表1因素水平安排渗漉提取实验,各组药液分别用纱布过滤后,最后定容至500 mL,即得。
2.3 干膏率测定
精密吸取供试品25 mL,置于已干燥至恒重的蒸发皿中,水浴蒸干后,移至烘箱中,105 ℃干燥3 h,取出,置干燥器中冷却30 min,迅速取出,精密称定质量,根据公式计算干膏率:干膏率(%)=(所得浸膏净重/药材量)×100%。正交试验干膏率结果,见表4。
2.4 绿原酸、咖啡酸、芍药苷、阿魏酸、丹酚酸B的含量测定
2.4.1 色谱条件 色谱柱:ZORBAX Eclipse XDB-C18(4.6 mm×250 mm,5 μm);以乙腈(A)-0.1%磷酸(B)为流动相进行梯度洗脱(0~10 min,10%A,10~40 min,10%→17%A,40~45 min,17%→24%A,45~60 min,24%A);5种成分的检测波长分别为:0~20 min绿原酸及咖啡酸320 nm,20~30 min芍药苷230 nm,30~40 min阿魏酸320 nm,40~60 min丹酚酸B 280 nm;流速:1.0 mL/min;柱温:35 ℃,进样量:10 μL[8]。
2.4.2 溶液制备 对照品溶液配制:各对照品储备液制备:精密称取绿原酸、咖啡酸、芍药苷、阿魏酸、丹酚酸B对照品适量,加甲醇制成每1 mL含绿原酸0.632 0 mg、咖啡酸0.215 0 mg、芍药苷2.406 mg、阿魏酸0.040 0 mg、丹酚酸B 2.088 mg的溶液。混合对照品溶液:分别精密吸取各对照品储备液适量,加甲醇制成每1 mL含绿原酸0.075 8 mg、咖啡酸0.025 8 mg、芍药苷0.481 2 mg、阿魏酸0.008 0 mg、丹酚酸B 0.250 6 mg的混合对照品溶液。
供试品溶液配制:精密吸取供试品5 mL,置于20 mL容量瓶,加相应溶剂稀释至刻度,摇匀,经0.45 μm微孔滤膜过滤,即得供试品溶液。
阴性对照品溶液配制:取缺少莪术、桂枝、三棱、马鞭草药材的处方量,按“2.2”项下方法,制备阴性对照样品,按“2.4.2”项下供试品溶液的制备方法制备,即得阴性对照品溶液。
2.4.3 系统适应性试验 取“2.4.2”项下对照品溶液、供试品溶液、阴性对照品溶液适量,按“2.4.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,供试品溶液色谱图中,在与对照品色谱相应位置上有相同的色谱峰,且阴性对照品对测定无干扰,说明该方法可行。
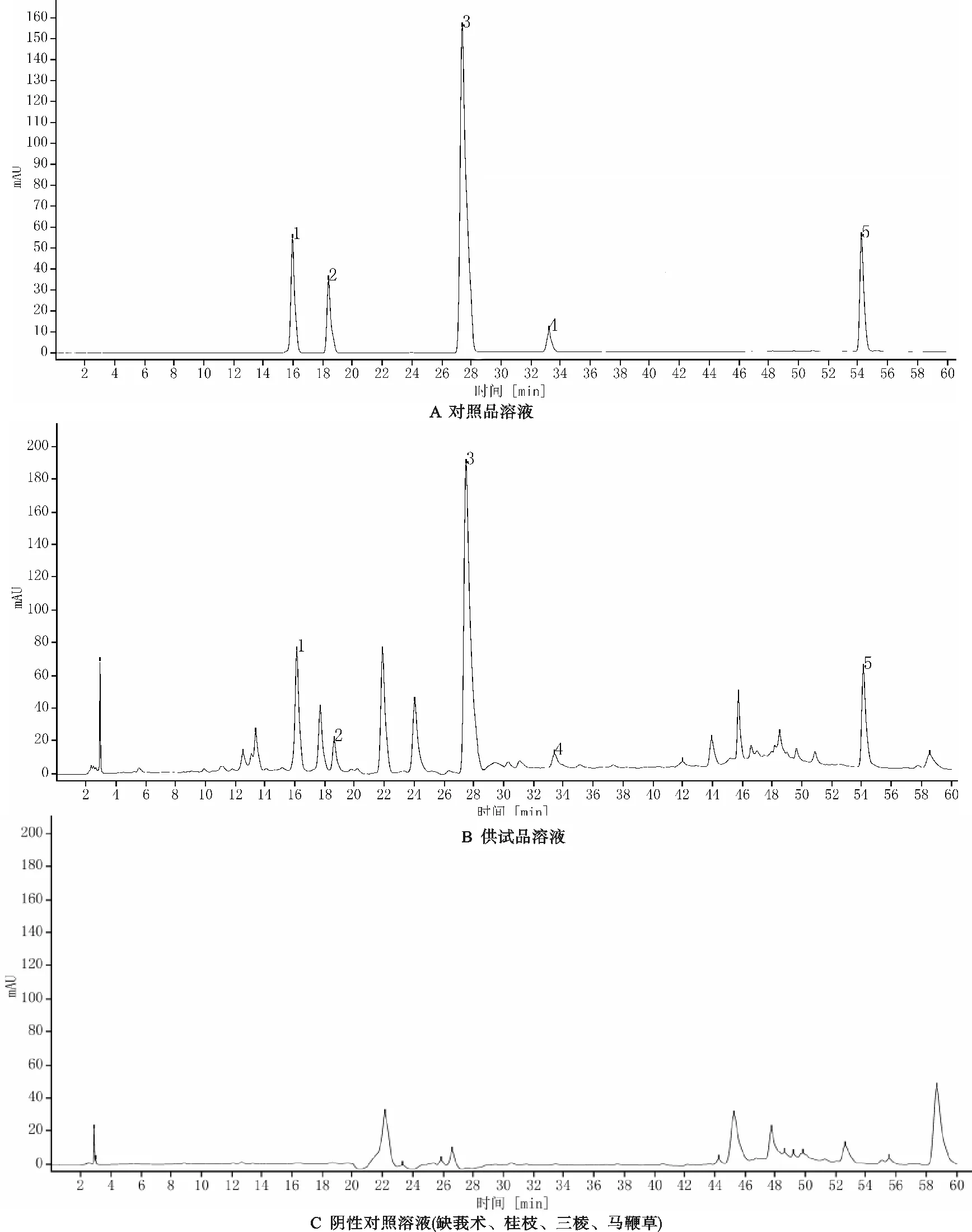
注:1.绿原酸;2.咖啡酸;3.芍药苷;4.阿魏酸;5.丹酚酸B。
2.4.4 线性关系考察 分别精密吸取混合对照溶液2、6、8、14、20 μL,注入高效液相色谱仪,测定峰面积。以峰面积为纵坐标、进样量为横坐标,进行线性回归计算,即得绿原酸、咖啡酸、芍药苷、阿魏酸、丹酚酸B的回归方程、相关系数及线性范围。结果表明,5种指标成分在各自含量范围内线性关系良好,见表2。
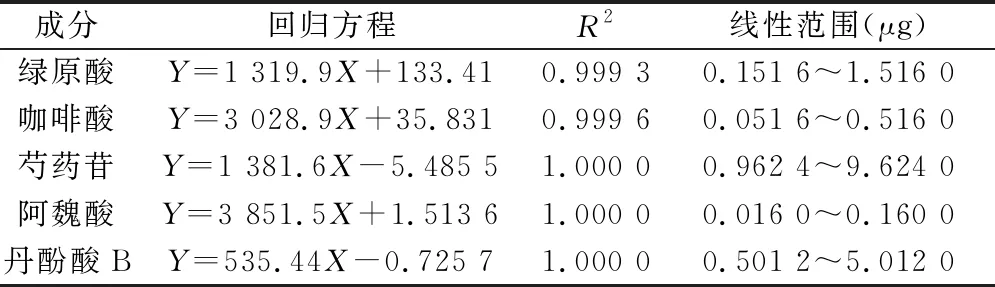
表2 线性关系考察结果
2.4.5 定量限与检测限考察 精密吸取“2.4.2”项下对照品溶液适量,倍比稀释,按“2.4.1”项下色谱条件进样测定,记录峰面积。按信噪比为10∶1、3∶1 分别计算定量限、检测限。结果,绿原酸、咖啡酸、芍药苷、阿魏酸、丹酚酸B定量限分别为25.28、8.600、802.0、11.43、417.6 ng,检测限
分别为7.584、2.580、240.6、3.428、125.3 ng。
2.4.6 精密度考察 精密吸取混合对照品溶液10 μL,按“2.4.1”项下色谱条件连续进样测定6次,以峰面积指标计算RSD(n=6)。结果:绿原酸、咖啡酸、芍药苷、阿魏酸、丹酚酸B峰面积的RSD分别为1.36%、1.30%、0.76%、1.24%、0.56%,表明仪器精密度良好。
2.4.7 重复性考察 取同一供试品适量,按“2.4.2”平行制备6份供试品溶液,按“2.4.1”项下色谱条件,同时测定绿原酸、咖啡酸、芍药苷、阿魏酸、丹酚酸B的峰面积,计算其峰面积RSD分别为0.82%、0.48%、0.56%、0.36%、1.61%(n=6),表明方法重复性良好。
2.4.8 稳定性考察 取同一供试品溶液,分别于制备后0、2、4、8、16、24 h,按“2.4.1”项下色谱条件进样,测定绿原酸、咖啡酸、芍药苷、阿魏酸、丹酚酸B的峰面积,计算其峰面积RSD分别为1.89%、0.76%、0.43%、0.79%、1.58%(n=6),表明供试品溶液在24 h内的稳定性良好。
2.4.9 加样回收实验 分别精密吸取已知各成分含量(绿原酸0.398 9 mg/mL、咖啡酸0.055 0 mg/mL、芍药苷1.882 4 mg/mL、阿魏酸0.027 7 mg/mL、丹酚酸B 0.948 0 mg/mL)的供试品溶液0.5 mL,共6份,分别置于5 mL量瓶中,精密加入适量对照品储备液溶液,按“2.4.2”项下方法制备供试品溶液。按“2.4.1”项下色谱条件进样,测定峰面积,计算绿原酸、咖啡酸、芍药苷、阿魏酸、丹酚酸B平均加样回收率分别为97.93%、97.75%、96.86%、97.11%、98.67%,RSD值分别为1.81%、2.63 %、1.84%、2.99%、2.87%,表明方法回收率良好。
2.5 层次分析法(AHP)确定各考察指标的权重系数
2.5.1 构建成对比较的判断优先矩阵 根据盆消灌肠液的处方方解及各成分药理作用强弱,采用1~9标度法对6项指标进行两两比较评判重要性,确定绿原酸、咖啡酸、芍药苷、阿魏酸、丹酚酸B的含量、干膏得率6项指标的优先顺序:绿原酸=咖啡酸=丹酚酸B>芍药苷=阿魏酸>干膏率,构建成对比较的判断优先矩阵,见表3。
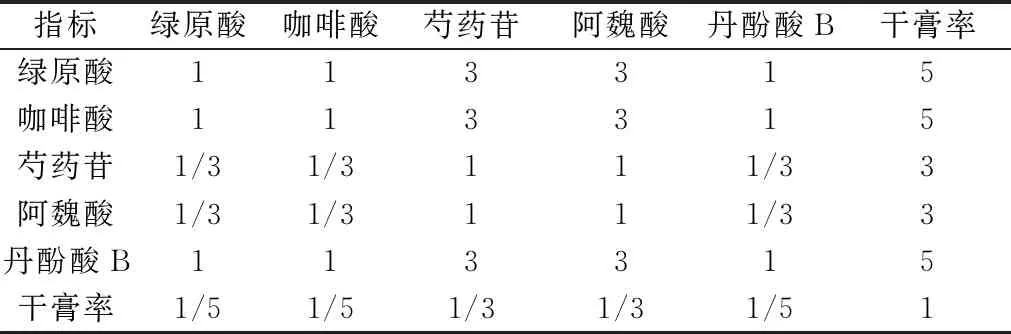
表3 各指标3个层次的优先矩阵
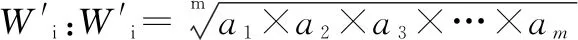
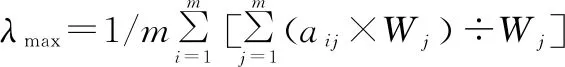
2.6 基于层次分析法的 L9(34)正交试验分析
按“2.4.1”项下色谱条件测定各指标性成分的含量,按“2.3”项下方法计算供试品溶液的干膏率。采用归一化法计算每个指标分值,综合评分计算公式如下:综合评分=(绿原酸含量/最大绿原酸含量)×100×W1+(咖啡酸含量/最大咖啡酸含量)×100×W2+(芍药苷含量/最大芍药苷含量)×100×W3+(阿魏酸含量/最大阿魏酸含量)×100×W4+(丹酚酸B含量/最大酚酸B含量)×100×W5+(大干膏率/最大干膏率)×100×W6。以综合评分考察乙醇浓度、乙醇用量、浸渍时间和渗漉速度对渗漉提取工艺的影响,通过直观分析和方差分析优选出最佳渗漉提取工艺条件。结果见表4、表5。

表4 正交试验安排与结果
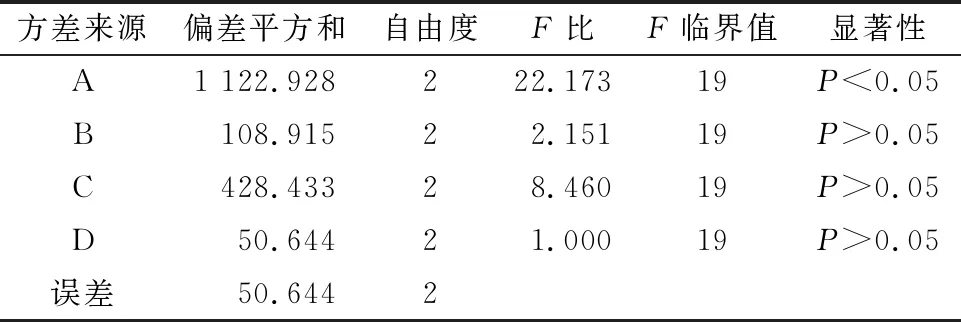
表5 方差分析
实验结果表明,各因素对盆消灌肠液提取工艺作用主次为A>C>B>D,即乙醇体积分数>浸渍时间>乙醇用量>渗辘速度,乙醇体积分数对提取效果的影响最大,而渗辘速度影响最小。方差分析表明,A因素对提取效果具有显著性影响(P<0.05)。根据直观分析结果,取各因素较高水平组合,最终确定最佳工艺参数为A2B2C3D1,即加8倍量70%乙醇,浸渍48 h后,以3 mL/min流速进行渗辘提取,收集渗漉液。
2.7 渗漉提取工艺验证
按最佳提取工艺制备3批样品,测定样品中绿原酸、咖啡酸、芍药苷、丹酚酸B、阿魏酸含量和干膏得率,结果表明该渗漉提取工艺稳定可行,见表6。
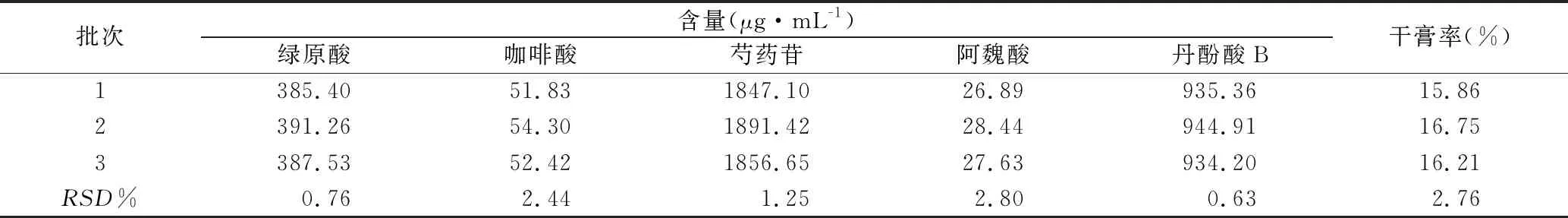
表6 提取工艺验证结果
3 讨论
中药复方具有多组分、多靶点的作用特点,设置多指标检测标准已成为优化中药复方制剂提取工艺的重要手段[10]。本研究采用主、客观结合的权重系数法-层次分析法,以确定多项指标的权重值。本制剂具有清热解毒、活血化瘀、止痛之功效,在各项指标两两比较判断矩阵中,大血藤、蒲公英、紫花地丁、败酱草、丹参主要发挥了本方“清热解毒,祛瘀止痛”之功效,且在方中用量较大,因此以大血藤、蒲公英、紫花地丁、败酱草共有成分[11-13]绿原酸、咖啡酸的含量和丹参的丹酚酸B的含量作为最重要的指标,计分最高;赤芍的芍药苷及当归的阿魏酸重要程度次之。提取液中的多糖、淀粉以及鞣质、树胶、树脂等成分并非本实验提取的最终目标,故干膏率重要程度要次于其他考察指标。因此,确定各指标优先顺序为:绿原酸=咖啡酸=丹酚酸B>芍药苷=阿魏酸>干膏率。结果显示,指标权重系数符合一致性评价要求,表明该评价方法具有可行性。
本研究确定盆消灌肠液最佳渗漉提取工艺为:处方量药材粉碎成粗粉,加8倍量70%乙醇作溶剂,浸渍48 h后,以3 mL/min的速度渗漉,收集渗漉液。该提取工艺条件经验证,合理可行,能为盆消灌肠液制剂大生产提供参考依据。
