“化合价”教学设计
2021-08-09周伟明
周伟明

课题:人教版初中化学教材九年级上册“化学式与化合价”。
化合价是初中化学教学的难点,但该内容是初中化学知识链中的重要环节,是学好化学非常有用的工具,贯穿化学学习的始终,对学生后面的学习有十分重要的影响,如能加深学生对物质组成的深层理解,降低酸碱盐化合物知识的学习难度等。笔者十分重视化合价概念理解过程的教学,在实践中收到了良好的教学成效。
【教学目标】
1.通过回顾典型化合物的形成,知道元素化合价与原子得失电子数目的关系,增强对物质组成结构探究的兴趣,感受物质组成的复杂性和可认识性。
2.通过观察分析,能说出化合价的一些简单规律,能说出常见元素和根的化合价,增强记忆和利用化合价的兴趣。
3.通过练习初步学会标出物质中常见元素的化合价,初步学会根据化学式计算化合价的方法,初步学会利用化合价写出常见化合物的化学式。
【教学重难点】
1.熟记常见元素的化合价和原子团的化合价,知道化合物中元素化合价的一些规律。
2.会标出物质中常见元素的化合价,会利用化合价书写简单的化学式。
【教学过程】
一、创设问题情景,化学式中的數字是怎么来的?
在此前的化学课中我们了解到一些物质的分子结构模型和它们的化学式,如:
【屏显】
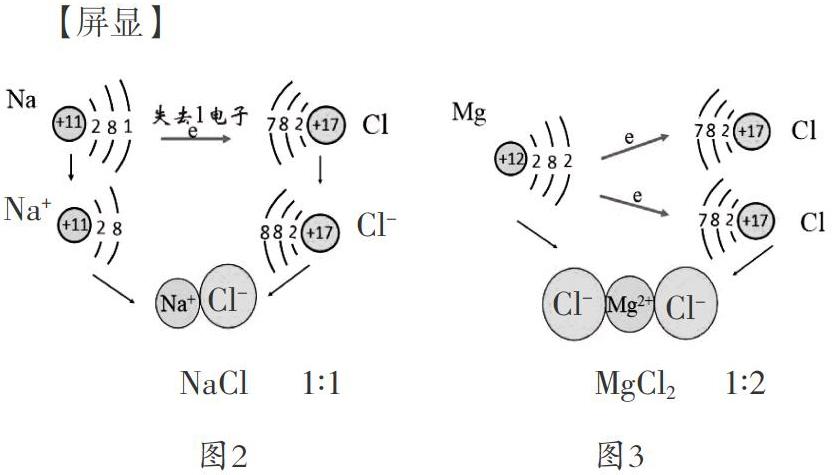
图1所示物质的化学式中元素符号的右下角有一些数字,它们表示该物质中不同元素结合时的原子个数比,其他化合物如NaCl、Fe2O3、P2O5、MnO2等也如此。我们可以看出不同的化合物,其中的原子个数比或离子个数比不一定相同,如NaCl中的个数比是1∶1;H2O是2∶1;Fe2O3是2∶3;P2O5是2∶5等,这是为什么呢?为什么每一种化合物的原子个数比或离子个数比不是任意的,而是具有确定的数值,是一个固定值?我们如何知道这个固定的比值呢?科学从来没有无缘无故,我们从原子的最外层电子数入手来探究这些问题。
二、探究发现端倪,化合价是枯燥的数据吗?
1.发现:原子个数比与原子得失电子的数目有关。
我们学习过用核外电子的变化理解钠和氯气反应生成氯化钠的过程,如图2所示。
【屏显】
钠与氯结合时,钠离子与氯离子个数比为1∶1,能形成稳定的化合物,所以氯化钠的化学式为NaCl。如果Mg与Cl形成化合物时,离子个数比是不是1∶1呢?镁原子要失去2个电子,需要2个氯原子接收这两个电子。形成化合物时,镁离子与氯离子个数比为1∶2,氯化镁的化学式为MgCl2,如图3。
2.说明:从以上分析可以看出,不同元素相互结合的原子个数比或离子个数比,与原子形成稳定结构需要得失电子的数目有关。化学家在研究了大量化合物组成的基础上,总结出用元素的“化合价”来认识其中的规律。
如在氯化钠的形成过程中,为了达到相对稳定的结构,一个钠原子失去了最外层的一个电子,且带上正电荷,所以氯化钠中钠元素的化合价为+1价,一个氯原子得到了钠失去的那个电子,带上负电荷,所以氯化钠中氯元素的化合价为-1价。同理,氯化镁中的镁元素为+2价,氯元素为-1价,分别表示为:
【屏显】
由此看出化合价不是死记硬背的枯燥数据,而是我们对微观原子行为和结构的一种认识。一般情况下,在由离子构成的化合物中,元素化合价的数值就是这种元素的一个原子得失电子的数目。原子失电子带上正电荷,其元素化合价为正;原子得电子带上负电荷,其元素化合价为负。
【屏显】
由图4可见化合价表明原子的结合能力,是原子相互结合时的一种“价位”。一个钠原子只能与一个氯原子化合,化合价为+1,一个镁原子却可以与两个氯原子化合,化合价则为+2。多像日常生活中的商品等价交换,就比如1千克大米能兑换2千克大豆或4千克玉米,若玉米的价格为1,则大豆的价格为2,大米的价格为4。
【设计意图】化合价的概念过于抽象,定义不易表述清楚。学生刚开始学习化学,掌握的物质和有关物质组成的知识不多,缺乏一定的认知基础,理解化合价概念十分困难。如果教学中教师采取避开或弱化化合价概念理解过程的教学,直接让学生记元素的化合价,并进行应用训练,使学生掌握物质化学式的书写,则学生对这些来历不明的数据会心存疑惑,不利于学习兴趣的培养和素养的养成。
考虑到学生的接受水平,教学时我将化合价概念的理解进行适当的简化处理,降低门槛而不让学生感到困难,从原子的最外层电子数入手,使学生初步感知化合价不是来路不明的简单数据,物质组成蕴含着规律,化合价是在研究分析大量物质组成的基础上,对构成物质的微粒相互结合时规律的总结,是打开物质组成之门的“密码”。随着后续学习的深入,如高中阶段共用电子对偏移、氧化还原反应等,学生会完成对化合价知识的整体把握。
3.大胆尝试:根据上面的学习,你能确定Al、O等元素的化合价吗?你能写出Mg和O相互结合形成的氧化镁,Al和Cl相互结合形成的氯化铝的化学式吗?请同学们大胆尝试,并将它们写出来。
Mg为+2价,O为-2价,1个镁离子可以结合1个氧离子生成氧化镁,所以氧化镁的化学式为MgO。同理,Al为+3价,Cl为-1价,当铝与氯气反应时,1个铝离子结合3个氯离子生成氯化铝,所以氯化铝的化学式为AlCl3。
物质有很多种,利用元素的化合价,我们就能简单地解决化学式的书写问题,而不必像学习英语单词一样死记硬背了。因此,了解记忆元素的化合价及其规律十分重要。
【设计意图】我以“Na、Mg、Al、Cl、O”五种常见元素的化合价为例,降低学生的学习难度,减轻学习压力,调动学生自主思考,鼓励学生积极探索与尝试,让学生体会到这些数据是自己参与分析研究的结果,让他们体验成功的喜悦,建立自信,消除疑惑,提高学习兴趣,使化合价知识变得生动具体。这样,学生应用和记忆化合价就更加灵活有效了。
三、观察总结规律,熟记元素的化合价真的很重要。
1.元素的化合价有哪些规律?观察课本表4-2,一些常见元素和根的化合价,讨论与交流,你能发现什么规律?
(1)计算NaCl、MgCl2、H2O中各元素化合價代数和,能得到什么结论?
分析:如氯化镁中1个镁原子失去2个电子,1个氯原子得到1个电子,两个氯原子得到镁原子失去的2个电子。打个比方我给你两个苹果,我失去两个苹果,你得到几个苹果呢?也是两个,即不同原子相互化合时失去电子总数与得到电子总数是相等的。这种情况反映在化合价上就体现为正负化合价代数和为零。我们可以利用它去计算化合物中某元素的化合价。
例题:已知O为-2价,求Fe2O3中铁元素的化合价。
(2)分析NaCl、MgCl2、MgO中各元素种类和化合价的正负,并观察金属元素与非金属元素化合价,总结特点并讨论缘由。
(3)观察Fe、Cu、Mn、Cl、S、N等元素的化合价有什么特点?
说明:某些元素有不同的化合价是由于该元素的原子在不同条件下,得失电子的数目不同引起的。
例题:已知K为+1价,O为-2价,根据化合物中,正负化合价代数和为零的规律,分别求出KMnO4、K2MnO4和MnO2中锰元素的化合价。了解KMnO4和K2MnO4的不同读法。
(4)阅读课文确定单质氧气(O2)、红磷(P)、铁(Fe)中元素的化合价。
化合价是不同原子相互化合时体现的性质,如果是相同原子的化合,由于没有明显的电子得失,因此单质中元素化合价为零。
(5)氢氧化钙的化学式中为什么有括号?了解原子团的知识,认识原子团的化合价。
2.比一比,看谁能寻找到记忆化合价的好方法?讨论与交流,利用集体的智慧,寻找适合自己的记忆方法?教师适时分析点评,如可以从原子的结构示意图与元素化合价的关系的角度来记忆;可以自编口诀来记忆;也可以用分类归纳法来记忆:
【屏显】
“+1”价:K、Na、Ag、H、NH4+;
“+2”价:Ca、Mg、Ba、Zn、Cu、Fe;
“+3”价:Fe、Al;
“-1”价:F、Cl、OH-、NO3-、HCO3-;
“-2”价:S、O、SO42-、CO32-。
我利用《樱花草》的曲子,现场弹奏吉他,演唱《化合价之歌》,一价钾钠氯氢银,二价氧钙钡镁锌……课堂气氛达到高潮,极大地激发了学生记忆化合价的兴趣。
3.化合价和离子符号的表示方法不同。
比较:说出下列符号表示的意义。
分别表示:每个镁离子带2个单位的正电荷;+2价的镁元素;在氧化镁中镁元素的化合价为+2价。比较它们的不同。
总结:
离子符号:所带电荷数标在元素符号的右上角,“+、-”号在后,数值在前,“1”要省略,如Mg2+、Na+、Cl-。
化合价:标在元素符号的正上方,“+、-”号在前,数值在后,“1”不能省略,化合价和离子所带电荷的正负与数值相同。
【设计意图】通过交流化合价记忆方法,培养学生的创新精神和合作精神;以歌曲作为载体,激发学生学习记忆化合价的热情;通过观察比较,使学生掌握化合价表示方法的特点。
四、掌握方法,化合价与化学式不得不说的故事。
1.根据化学式,练习标出或确定化合物中元素的化合价。
练习(1):标出下列化合物各中元素的化合价。
氯化钡BaCl2 金属锌Zn 二氧化硅SiO2
练习(2):标出下列物质中元素和根的化合价。
硝酸钠NaNO3 碳酸钙CaCO3 氢氧化钠NaOH
硫酸铜CuSO4 氯化铵NH4Cl
2.根据元素的化合价写出物质的化学式。
例题:已知某种磷的氧化物中磷为+5价,氧为-2价,写出这种磷的氧化物的化学式。
练习(3):根据元素或根的化合价写出下列物质的化学式:
氧化钙 ,氯化锌 ,氢氧化铜 ,碳酸钙 。
说明:最简便的方法是标出化合价,然后用十字交叉法将数字写到元素符号的右下方。若有最大公约数则化成最简比即可。
【反思】化合价知识虽然是教学的难点,但只要教师潜心钻研,精心设计,就能突破难点,设计出有助于学生理解的教学过程,并使学生素养得到提升。
责任编辑 邱 艳
