基于数据挖掘、网络药理学及临床观察探究贾跃进治疗女性失眠症用药规律及机制
2021-08-05王瑞敏彭雪峰贾跃进
刘 毅,王瑞敏,彭雪峰,李 菲,赵 飞,刘 宁,贾跃进
1.山西中医药大学第二临床学院,山西 太原 030024
2.山西中医药大学附属医院 科教科,山西 太原 030024
3.山西中医药大学附属医院 医务科,山西 太原 030024
4.山西中医药大学附属医院 治未病中心,山西 太原 030024
失眠症指以入睡困难、睡眠维持困难或早醒,并伴有疲劳、注意力不足和情绪不稳定等日间功能障碍为主症的疾病[1],女性患病率约是男性的1.5倍[2],通常被认为是高血压、糖尿病、抑郁症、焦虑症等躯体或精神疾病的危险因素[3-4],故对女性群体有较大的危害。目前现代医学虽然对失眠症的相关研究取得了长足进展,但仍无公认的疾病模型,尽管有多种可选择的治疗药物,但并无理想药物[5-6]。而中医学早在《内经》就已经以“天人相应”为基础构建了“营卫”“阴阳”睡眠节律模型,并提出了失眠总病机,且中医药擅长治病求本,临床应用广泛,具有安全、有效性,因此通过挖掘名老中医治疗女性失眠症的经验方则有利于中医思想的传承及相关药物的研发,从而缓解患者痛苦、指导临床应用。
贾跃进是第六批全国老中医药专家学术经验继承工作指导老师,有40 余年的行医经验,在遍阅中医经典、熟稔各种方药的基础上,结合临床形成了独到的诊疗思路。以中医《内经》理论为基础,从“气”的角度分析疾病,再以方对证、药对症的思路辨治,获效甚众。贾跃进临床尤擅治疗失眠症、抑郁症、焦虑症在内的多种精神障碍以及调治亚健康状态。鉴于当前大数据环境下中医药临床数据具有的“全数据”“知识密集型数据”的特点[7],采用第四科研范式,即以数据驱动并将理论、计算机仿真和实验归一的“数据密集型科学”的研究模式[7],将有利于更好地把握研究探索的方向,发现并解决新的问题,本研究结合贾跃进的临床理论,采用数据挖掘、网络药理学、分子对接和临床验证的方法,从中医数据的整体性、混杂性和相关联系性出发,全面探索贾跃进治疗女性失眠症的机制。
1 数据挖掘方法与结果
1.1 资料与方法
1.1.1 数据收集 收集山西中医药大学附属医院贾跃进门诊自2015年1月1日至2020年1月1日诊断为失眠症的女性患者的资料及完善的病案。
1.1.2 纳入和排除标准
(1)纳入标准:根据《中国精神障碍分类与诊断标准》(CCMD-3)[8]明确诊断为失眠症;年龄在20~65 岁的女性患者;单纯口服中药颗粒剂治疗;结合比较治疗前后匹兹堡及SPIEGEL 量表评分及随访判断为有效;从治疗前后进行的基本检查(血、尿常规、肝肾功能、心电图等)判断具有安全性。
(2)排除标准:诊断和效果不明确、资料缺失或安全性存疑的病案;合并影响判断的其他严重躯体及精神病者;干预方式非单纯中药或使用中药其他剂型或使用中药方式非口服者。
1.1.3 数据标准化、录入与挖掘 通过纳入和排除标准进行筛选,以双人双录入法将筛选出的病案录入至古今医案云平台V2.2.3 提供的模板中,确保准确后使用其数据标准化模块结合《中国药典》2015年版[9]与《中药学》第7 版[10]规范中药名称。获得标准化数据库后,使用数据挖掘模块分别对其进行药物频次、性味归经统计[9-10],并通过关联分析、聚类分析和复杂网络分析获得核心组方。
1.2 数据挖掘结果
1.2.1 药物频次及属性统计 共收集病案455 例,按纳入、排除标准筛选,获得验案221 例。221 例验案包含方剂258 首,涉及中药139 味,其中药物应用百分比大于20%的有19 味,见表1。将258 首方剂中139 味药物进行性味归经分析,结果以雷达图(图1)表示,其中中药药性分布为平、温、微寒、寒;药味为甘、辛、苦;药物归经为肝、脾、心、肺、肾、胃经。

表1 258 首处方药物使用频次及频率 (频率>20%)Table 1 Frequency of drugs usage in 258 prescriptions (frequency > 20%)

图1 258 首处方中四气 (左)、五味 (中)、归经 (右) 频次分布雷达图Fig.1 Radar chart of the frequency distributions of four characters (left), five tastes (middle), and channel tropism (right) in 258 prescriptions
1.2.2 药物关联分析、聚类分析、复杂网络分析及核心组方确定 将258 首处方利用云平台数据分析,设置置信度>0.90,支持度>0.35,得到20 组药物关联分析结果,见表2;将药物应用频率>20%的19味中药进行聚类分析,同时设置距离类型为欧氏距离,聚类方法为最长距离法,可将其分为C1 类:川楝子、枳实、莱菔子;C2 类:麦芽、远志、党参、半夏、陈皮;C3 类:香附、白术、茯苓、合欢皮;C4 类:龙骨、栀子、白茅根、柴胡、牡丹皮、白芍、当归4 个聚类处方,见图2;最后设置节点度不小于150,进行中药-中药复杂网络分析,得到1 个由11味中药组成的核心组方,见图3。综合以上并结合药物频次得出核心组方为茯苓、白术、合欢皮、柴胡、香附、白芍、龙骨、当归、牡丹皮、栀子、白茅根。
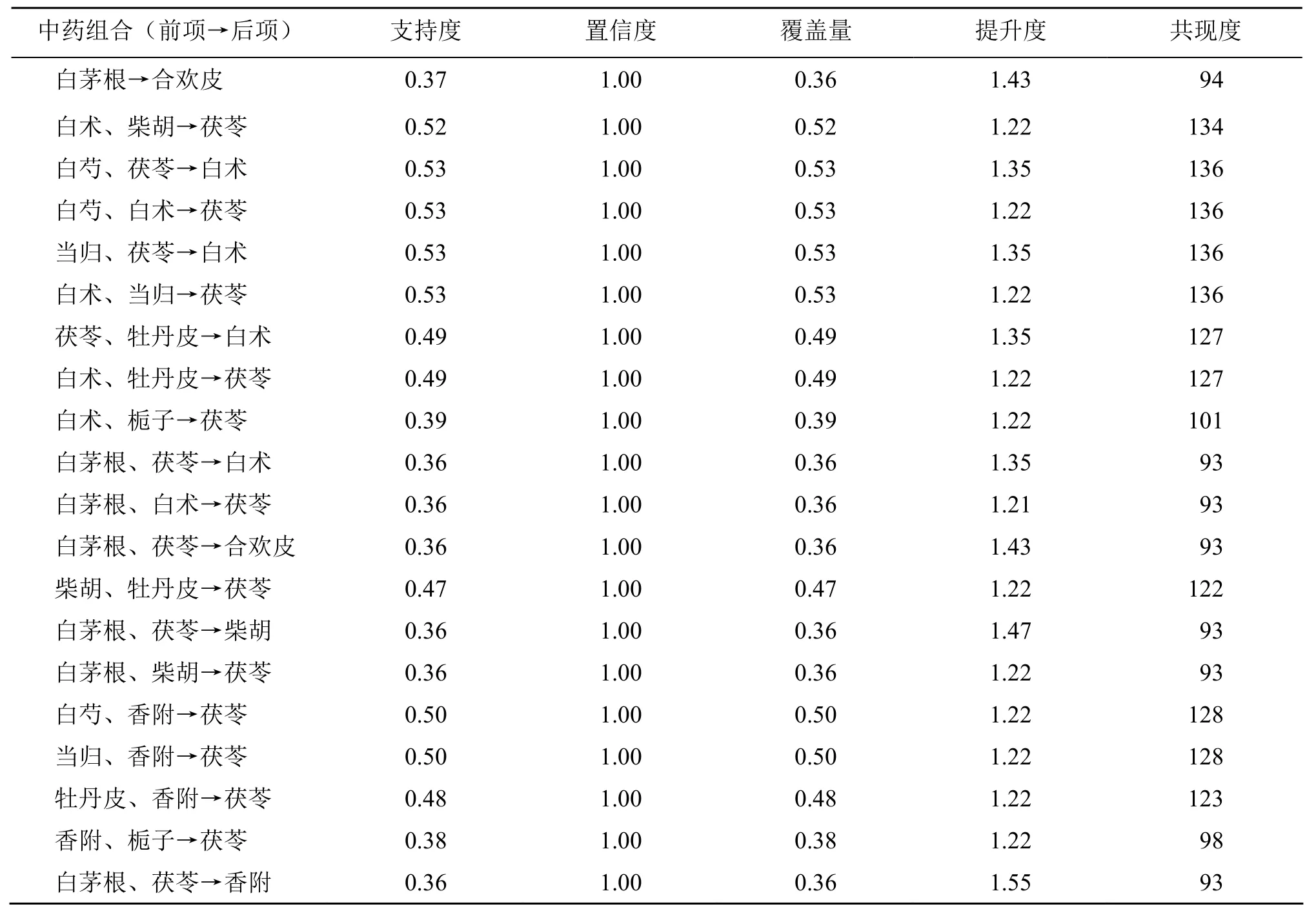
表2 258 首处方中药物关联分析 (置信度>0.90,支持度>0.35)Table 2 Association rule analysis of drugs in 258 prescriptions (confidence > 0.90, support > 0.35)

图2 258 首处方中药物聚类分析Fig.2 Cluster analysis of drugs in 258 prescriptions
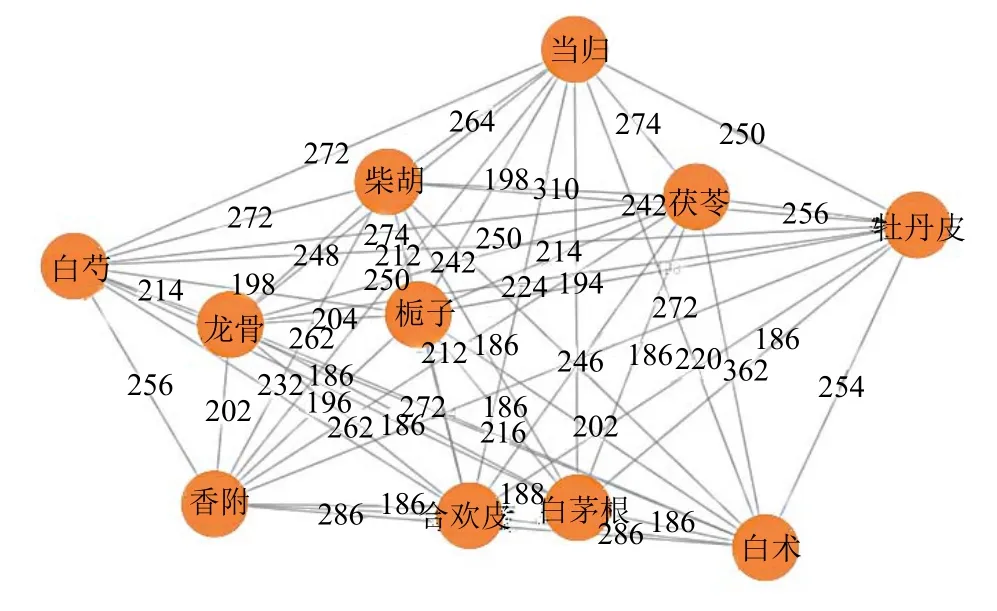
图3 258 首处方中药物复杂网络分析Fig.3 Complex network analysis of drugs in 258 prescriptions
2 网络药理学方法与结果
2.1 资料与方法
2.1.1 核心组方中药物有效成分及对应靶点筛选 利用TCMSP 数据库(http://tcmspw.com/tcmsp.php)检索核心组方中各药物成分,并限定口服生物利用度(oral bioavailability,OB)≥30%、血脑屏障(blood brain barrier,BBB)≥−0.3、类药性(drug likeness,DL)≥0.18,并匹配各成分靶点,对于无靶点记录的有效成分则利用 SwissTargetPrediction 平台(http://www.swisstargetprediction.ch/)预测靶点,将 靶点在Uniprot 数据库(https://www.uniprot.org/)中匹配基因名。
2.1.2 疾病靶点获取 在GEO(https://www.ncbi.nlm.nih.gov/)、Genecards(https://www.genecards.org/)、OMIM(https://omim.org/#)、TTD(http://db.idrblab.net/ttd/)数据库中检索“insomnia disorder”,得出失眠症相关靶点,并将3 个数据库所得失眠症相关靶点合并、去重,再利用Uniprot 数据库筛选。
2.1.3 药物-疾病交集靶点获得 将各有效成分相关靶点与疾病相关靶点利用微生信(http://www.bioinformatics.com.cn/)平台取交集,获得核心组方中药物的有效成分直接与疾病相关的靶点。
2.1.4 疾病-药物-成分-靶点及蛋白相互作用(protein- protein interaction,PPI)网络构建 以疾病、核心组方、各药物、有效成分和相关靶点为节点,其相互关系为边,在CytoscapeV3.8.0 中构建网络,并利用 MCODE 插件对 String 数据库( https:// string-db.org/)所得PPI 网络进行聚类分析。
2.1.5 基因本体(gene ontology,GO)富集分析和京都基因及基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)通路富集分析 将交集靶点导入Cytoscape 的BiNGO、ClueGO 插件分别进行GO 和KEGG 通路富集分析,然后将其可视化。
2.1.6 关键有效成分与关键靶点分子对接分析 根据节点度筛选“2.1.4”构建的2 个网络中的关键有效成分及关键靶点分别在 Zinc(https://zinc.docking.org/)、PDB(http://www.rcsb.org/)数据库中获取3D 结构,对于没有结构记录的靶点则利用SWISS-MODEL 平台(https://swissmodel.expasy.org/)模拟构建其3D 结构,然后使用Vina 分子对接,并选择对接最好的组合使用Pymol 进行可视化。
2.2 网络药理学结果
2.2.1 核心组方有效成分和对应靶点 通过检索TCMSP 数据库,结合SwissTargetPrediction 预测靶点,筛选出核心组方各药物有效成分及相关靶点。经过去重、排除后,总计获得有效成分65 种,重复成分5 种,相关靶点490 个。具体成分信息如表3所示。

表3 核心处方有效成分相关信息Table 3 Information of active ingredients of core prescription

续表3
2.2.2 疾病靶点 将GEO 数据库得到的失眠症相关数据集(编号GSE122541)使用R 语言进行差异性分析,共得到100 个差异基因靶点,如图4 所示;将GeneCards数据库中得到的2563个失眠相关基因按照相关度大于中位数进行筛选,可获得1074 个疾病靶点;此外OMIM 和TTD 分别得到295、28 个靶点。将以上所得靶点处理后,共计获得失眠靶点1205 个。

图4 GEO 数据集失眠症差异基因分析结果Fig.4 Results of analysis of differentially expressed genes in insomnia disorder from GEO datasets
2.2.3 药物-疾病靶点交集 利用微生信平台将药物靶点与疾病靶点取交集,共获得142 个药物与疾病直接相关的交集靶点,如图5 所示。

图5 核心组方药物-疾病交集靶点Fig.5 Core prescription drugs-disease intersection targets
2.2.4 疾病-药物-成分-靶点网络和PPI 网络构建 将数据导入Cytoscape 软件,构建疾病-核心组方-有效成分-交集靶点网络,见图6。从该网络筛选出节点度较大(degree≥20)的13 个关键有效成分,编号分别为A、C、HHP1、HHP8、FL4、FL6、XF1、BZ1、HHP12、HHP10、HHP9、XF5、HHP6。在String 中导入142 个交集靶点构建PPI 网络,然后将数据导入Cytoscape,使用MCODE 插件对PPI网络进行聚类,得出3 个聚类网络,如图7 所示。选取每个聚类网络中节点度最大的前1/8 的靶点作为关键靶点,分别为聚类1:蛋白激酶Bα(protein kinase Bα,AKT1)、白细胞介素-6(interleukin-6,IL-6)、原癌基因c-Fos(proto-oncogene c-Fos,FOS)、tumor necrosis factor(肿瘤坏死因子,TNF)、血管内皮生长因子A(vascular endothelial growth factor A,VEGFA);聚类 2:5-羟色胺受体 1A(5- hydroxytryptamine receptor 1A,HTR1A);聚类3:多巴胺受体D2(dopamine receptor D2,DRD2)。
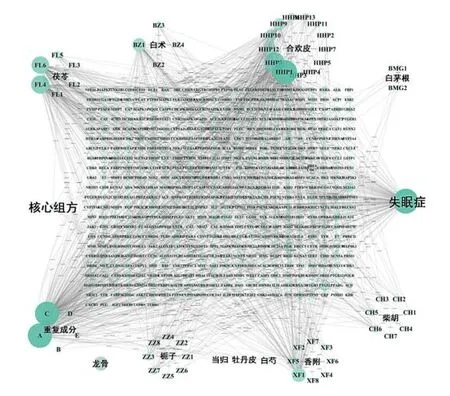
图6 疾病-核心组方-有效成分-交集靶点网络Fig.6 Disease-drug-active ingredient-target network
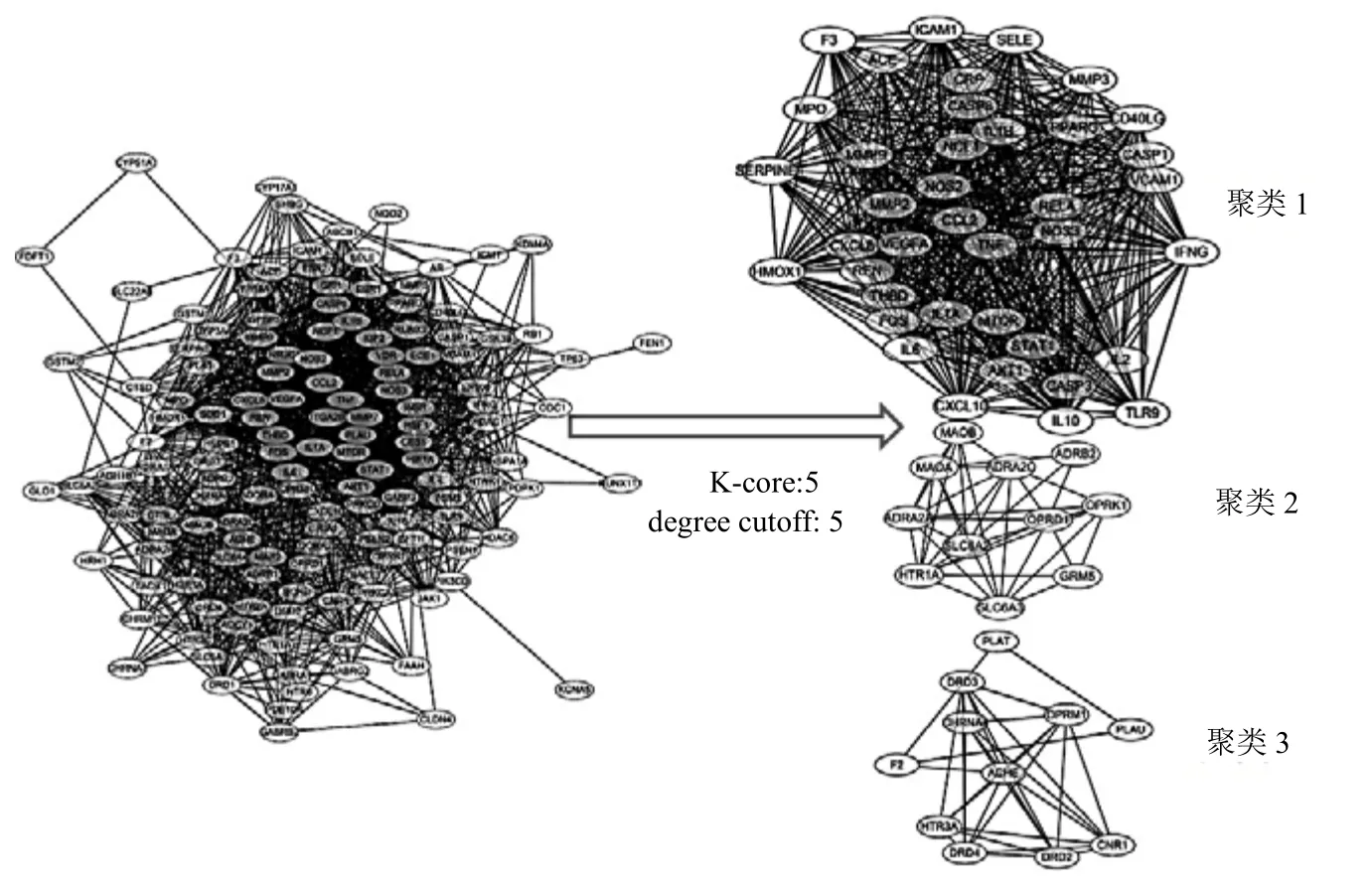
图7 交集靶点PPI 网络聚类图Fig.7 Cluster PPI network of intersection targets
2.2.5 GO 和KEGG 富集分析结果 将交集靶点导入BinGO,并设置置信水平为0.01,进行GO 富集分析,如图8 所示,可得GO 生物过程主要包括:生物调节、细胞过程、代谢过程、信号过程、对刺激的应答等;GO 分子功能则包括:结合、催化活性、分子转导活性等;而GO 细胞成分以突触、胞外区、细胞外域等为主。再将交集靶点导入ClueGO,设定P≤0.01,最小聚类为4,K-score 为0.5 进行KEGG 通路富集分析,如图9 所示,根据P值选取其中主要通路为神经活性配体-受体相互作用、血清素能突触、多巴胺能突触、雌激素信号通路、TNF信号通路等。
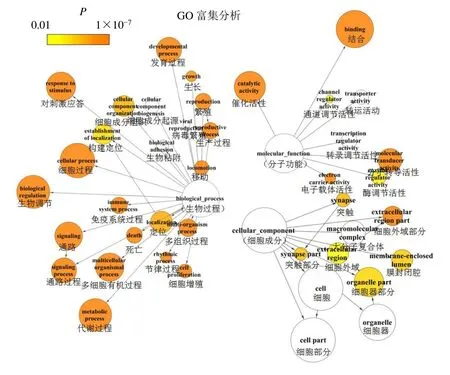
图8 交集靶点GO 富集分析主要结果关联图Fig.8 Main results of GO enrichment analysis of intersection targets

图9 交集靶点KEGG 关键通路图Fig.9 Key pathways for KEGG enrichment analysis of intersection targets
2.2.6 分子对接结果 关键靶点和关键成分分子对接结果大多结合能≤−20.90 kJ/mol,提示关键成分 与关键靶点大多可能形成稳定结构,具体见表4,而取其中对接最好的组合如图10 所示,可见其对接方式主要为疏水口袋及氢键。

表4 关键成分与关键靶点分子对接结果Table 4 Results of molecular docking between key ingredients and key targets

图10 关键成分与关键靶点对接构象Fig.10 3D image of molecular docking between key ingredients and key targets
3 临床研究
3.1 材料
3.1.1 临床资料 收集2020年6月至2021年3月山西中医药大学附属医院治未病中心门诊符合纳入标准的失眠症女性患者,所有患者均签署知情同意书,并通过山西中医药大学伦理审查(编号为2021LL052)。
(1)纳入标准:符合失眠症诊断标准,包括《中国精神障碍分类与诊断标准》(CCMD-3)[8]中的症状标准、严重标准、病程标准等;女性患者,年龄在20~65 岁;患者知情,并同意接受本临床治疗者。
(2)排除标准:未按规定,无法判断或数据不全等,影响疗效和安全性判断者;妊娠、哺乳期妇女,使用雌激素药物或对本药物过敏者;严重躯体疾病、实质性脏器损害、神经系统疾病及其他精神 疾病者;酗酒或药物依赖者。
3.1.2 药品与试剂 核心组方(茯苓15 g、白术12 g、合欢皮12 g、柴胡12 g、香附10 g、白芍15 g、龙骨30 g、当归12 g、牡丹皮12 g、栀子10 g、白茅根15 g)配方颗粒剂(批号分别为20101171、20100681、20101301、20122271、20090341、20111331、21030641、21041211、20110481、20090701、20071201),江阴天江药业有限公司;舒眠胶囊(0.4 g×36 粒,批号20200502)购于贵州大隆药业有限责任公司;人血清 褪 黑 素( melatonin, MT )、 γ- 氨 基 丁 酸(γ-aminobutyric acid,GABA)、多巴胺(dopamine,DA)、5-羟色胺(5-hydroxytryptamine,5-HT)酶联免疫吸附(ELISA)检测试剂盒(货号分别为CEA908Ge、CEA900Ge、CEA851Ge、CEA808Ge),武汉云克隆科技股份有限公司。
3.1.3 主要仪器 DRAGONLAB MX-S 可调式混匀仪,大龙兴创实验仪器(北京)股份公司;LDZ5-2型离心机,北京离心机厂;THZ-92B 气浴恒温振荡器,上海博迅有限公司设备厂;VERSA max-BNRO5709酶标仪,美谷分子仪器(上海)有限公司。
3.2 研究方法
3.2.1 分组及治疗方法 共纳入患者42 例,随机分为对照组和治疗组各21 例。治疗组服用核心组方,1 剂/d,分2 次于早餐前半小时、睡前1 h 空腹200 mL 水冲服。对照组口服舒眠胶囊,3 粒/次,晚饭后、临睡前各服用1 次。观察期间,2 组病例均不得加服其他抗焦虑药及安眠药物,疗程为4 周。
3.2.2 疗效及安全性评价 统计治疗前后对照组和治疗组匹兹堡睡眠量表指数(PSQI)[11]及SPIEGEL 量表[12]评分变化,比较分析临床效果。前者根据睡眠质量、入睡时间、睡眠时间、睡眠效率、睡眠障碍、催眠药物、日间功能障碍7 项指标评分,后者则包括入睡时间、睡眠总时间、夜醒次数、睡眠质量、梦扰多少、醒后感觉6 项指标;前者总分21 分,其中6~10 分为睡眠基本正常,后者总分42 分,以小于12 分为睡眠基本正常,两者均为得分越高,睡眠质量越差。统计治疗前后两组患者心电图、肝肾功能、血尿常规情况以判断药物基本安全性。
3.2.3 血清MT、GABA、DA、5-HT 水平 治疗前后分别空腹抽取患者静脉血,离心(5400 r/min、10 min)获得血清,将血清分装后,−20 ℃避光保存,检测时解冻后用ELISA 试剂盒检测其血清中的MT、GABA、DA、5-HT 水平,并统计两组治疗前后的变化情况。
3.2.4 统计学分析 使用SPSS 22.0 软件分析数据,计量资料用±s描述,若符合正态性、方差齐性采用成组t检验,自身前后比较用配对t检验;不符合方差齐性时用t´检验;未满足要求者自身前后比较用配对秩和检验;不符合正态分布选择秩和检验;计数资料则使用χ2检验,确定P<0.05 为有统计学差异。
3.3 临床研究结果
3.3.1 患者一般资料比较 纳入失眠症女性患者42 例,其中对照组年龄28~65(51.33±9.83)岁,失眠病程1~9(4.24±2.57)个月;治疗组年龄32~64(51.90±9.91)岁,失眠病程2~9(4.48±2.34)个月,两组患者之间无统计学意义(P>0.05)。
3.3.2 两组疗效及安全性比较 两组患者在治疗前PSQI 评分差异无统计学意义(P>0.05),治疗后PSQI评分均降低,与治疗前相比差异有统计学意义(P<0.05),其中治疗组下降更明显;SPIEGEL 量表评分得到相同结果,见表5;两组患者治疗前后肝肾功能、心电图、血尿常规变化均无统计学意义(P>0.05),见表6。未见与服用2 种药物相关的不良反应。
表5 两组治疗前后量表总体评分比较 ( ± s, n = 21 )Table 5 Comparison on total scores before and after treatment between two groups ( ± s, n = 21 )

表5 两组治疗前后量表总体评分比较 ( ± s, n = 21 )Table 5 Comparison on total scores before and after treatment between two groups ( ± s, n = 21 )
与同组治疗前比较:*P<0.05;与对照组治疗后比较:#P<0.05;与对照组比较:△P<0.05,表7 同*P < 0.05 vs same group before treatment; #P < 0.05 vs control group after treatmennt; △P < 0.05 vs control group, same as fig.7
PSQI SPIEGEL 组别 治疗前 治疗后 治疗前后差值 治疗前 治疗后 治疗前后差值 对照 15.05±4.25 10.90±4.27* 4.14±2.76 19.14±7.26 12.38±4.57* 6.76±4.39 治疗 15.90±3.14 9.62±4.36* 6.29±5.64△ 19.95±7.07 9.71±4.85*# 10.24±5.94△

表6 两组患者治疗前后安全性相关指标比较Table 6 Comparison on safety factor before and after treatment between two groups
3.3.3 两组治疗前后血清MT、GABA、DA、5-HT水平比较 两组患者治疗前4 项指标差异均无统计学意义,治疗组患者治疗后MT 水平升高,5-HT 及DA 水平降低并差异有统计学意义(P<0.05),GABA 水平升高但无统计学意义;治疗组与对照组相比,治疗前后MT、5-HT、DA 水平的差值有统计学意义,见表7。
表7 两组患者治疗前后血清MT、GABA、DA、5-HT 水平比较 ( ± s, n = 21)Table 7 Comparison on the serum MT, GABA, DA and 5-HT levels before and after treatment between two groups ( ± s, n = 21)

表7 两组患者治疗前后血清MT、GABA、DA、5-HT 水平比较 ( ± s, n = 21)Table 7 Comparison on the serum MT, GABA, DA and 5-HT levels before and after treatment between two groups ( ± s, n = 21)
MT/(pg·mL−1) GABA/(pg·mL−1) DA/(ng·mL−1) 5-HT/(pg·mL−1) 组别 治疗前 治疗后 治疗前后差值 治疗前 治疗后 治疗前后差值 治疗前 治疗后 治疗前后差值 治疗前 治疗后 治疗前后差值对照 197.08±61.05 201.50±86.63 −4.42±83.52 16.76±7.09 18.28±12.61 −1.52±8.86 200.14±75.19 170.48±116.79 29.66±155.53 108.71±67.79 118.91±93.52 −10.20±49.06 治疗 197.46±52.26 266.37±65.81*# −68.92±85.04△ 17.63±7.57 23.09±7.92* −5.46±5.77 206.65±106.89 113.15±50.38*# 93.50±88.38△ 122.06±51.14 79.11±50.89*# 42.95±30.48△
4 讨论
4.1 贾跃进治疗女性失眠思路
《灵枢·大惑论》[13]有:“卫气不得入于阴,长留于阳,留于阳则阳气满,……不得入于阴则阴气虚,故目不瞑矣”之说。因此失眠的本质就是营卫、阴阳之气运行节律的紊乱,失眠的总病机为“营卫失和、阴阳不交”[14]。同时营卫、阴阳之气是一身之气的组成部分,受一身之气的调控,故贾跃进认为治疗失眠症应“调气”为先,“调气”的重点则是调气机,具体到脏腑,应责之与气机相关性较大的肝、脾(胃)二枢机。女子以肝为先天,以血为本,脾胃亦为气血生化之源,丹溪有言“气血冲和,万病不生,一有怫郁,诸病生焉”[15],故女子较之男子更易出现“郁”,从而引发气机不畅以及在此基础上造成的气血两方面皆生成或代谢障碍,最终导致失眠。且其失眠往往病程较长,易出现“气郁则生湿,湿郁则成热,热郁则成痰,痰郁则血不行,血郁则食不化”[15]的传变。故临床治疗女性失眠,贾跃进常注重疏肝行气、调护脾胃及通降腑气,多以逍遥散类方佐以香附、陈皮、川楝子、元胡、丹皮、栀子、知母、玫瑰花、合欢皮、党参、麻子仁、炒莱菔子、半夏、杏仁等药物,疗效颇佳。
4.2 数据挖掘探究用药规律
从数据挖掘结果可得,治疗药物中使用频率最高者为茯苓、白术、合欢皮、柴胡、香附、白芍、龙骨、当归、牡丹皮、栀子、白茅根。现代药理学研究认为这些药物具有镇静催眠、抗抑郁、抗焦虑或神经保护的作用,其中一些药物兼具缓解女性更年期症状、保护肝脏、治疗消化疾病的功效[16-26]。根据药性分布规律分析,应用最多者为平、温、微寒、寒,可见从整体来看,贾师对于女性失眠症的治疗并无明显寒热偏向,因气血运行障碍寒热均可见,即“气有余便是火,气不足便是寒”“血证有四:曰虚,曰瘀,曰热,曰寒”;而药味主要分布在甘、辛、苦,与药性结果相一致,其中甘味药有补益气血、顾护脾胃、调和诸药之功,辛、苦味药辛开苦降,燮理枢机,令气血自和;药物的归经则主要归肝、脾、心、肺、肾、胃6 经,其中中焦斡旋、龙虎回环、水火相济都与周身气机运行密切相关,此处足见贾跃进治疗女性失眠的调气为先、整体论治之思路。药物关联分析中筛选出的20 对核心关联组合均是茯苓、白术、合欢皮、柴胡、香附、白芍、当归、牡丹皮、栀子、白茅根10 味药物的组合,其中丹皮、栀子、当归、白芍、柴胡、茯苓、白术7 味是丹栀逍遥散的主要药物,可以治疗肝郁血虚脾弱或郁而化热之候,为中医妇科常用方;香附为“气中之血药”,在行气解郁的同时兼顾血分;合欢皮解郁安神、白茅根凉血清热兼降肺气,诸药充分体现了应对女子失眠应兼治气血两纲,顾护后天、佐以清热的治疗原则。聚类分析所得的4 个聚类处方中C1为贾跃进治疗女性失眠常用之佐使药,意在通腑降气;C2、C3 分别是二陈汤、四君子汤及其类方的主要成分,体现了女性失眠治疗中以中焦枢纽为中心的调气方法,即“一气周流”;C4 则主要是关联分析中所得的成分,故不赘述。复杂网络分析中所获的核心药物组成与关联分析中的10味药物重合度极高,仅龙骨一味出入,综合龙骨的用药频率,故取之为核心组方,该组方经过贾跃进分析,认为可反映其临床用药,并曾在临床上经过一定的使用,安全有效。
4.3 网络药理分析作用机制
根据网络药理学网络构建,得出核心组方治疗女性失眠症的13 个主要有效成分,其涉及除龙骨、牡丹皮外的所有药物,可见其多药物、多成分的作用机制,尤其是编号为A 和C 的成分,体现了方中药物的共性,两成分是存在于多种中药材中的植物甾醇,前者在动物实验中被验证可上调谷胱甘肽、GABA 水平,下调DA、丙二醛、TNF-α、乙酰胆碱酯酶水平从而调节精神症状、改善脑功能[27],后者则可通过抑制TNF-α 的炎症反应来发挥神经保护作用[28],亦有实验证实其可增加小鼠中枢神经系统中的去甲肾上腺素、5-HT 等神经递质的水平而表现抗抑郁活性[29];编号FL4、FL6 的成分属于茯苓中的三萜类化合物,研究显示其具有一定镇静作用[30];XF1 属香附中的挥发油类,动物实验得出该类物质能通过调节胆碱能系统及5-HT 水平而表现抗焦虑的作用[31];XF5 是已知的镇静、镇痛、助眠药物;BZ1 为主要成分的混合物被研究证实具有治疗抑郁症的潜力[32];HHP8 为合欢皮中的木脂素类成分,有研究报道称该物质可有安神活性[33];HHP1为多种植物中存在的黄酮类,动物实验认为其可增加非快速眼动睡眠[34]。根据PPI 网络所得的靶点聚类中,聚类1 主要包括IL-2、IL-6、TNF、VEGFA等参与免疫的细胞因子以及一些参与合成、代谢的激酶,而免疫与睡眠是双向关联的[35];聚类2、3则主要包括5-HT、DA 等神经递质,而睡眠-唤醒过程被认为是由神经递质介导的。
目前失眠症的病理机制并不明确,但较公认的有神经递质调节障碍(GABA、5-HT、DA、去甲肾上腺素等)、信号传导障碍(下丘脑-垂体-肾上腺轴、HPA 轴)、代谢障碍(能量、脂质、氨基酸及肠道微环境等)、内分泌失调(生长激素、食欲素、性激素等)、免疫功能异常(炎症)、遗传(基因)及心理因素刺激等引起睡眠-唤醒节律紊乱[36-38],而就女性失眠症而言,女性一生的睡眠状况受到雌、孕激素的调节[39],而其中雌激素是神经系统的有效调节剂,可通过直接与雌激素受体结合或调节GABA 能、DA 能、5-HT 能突触传递而调节中枢神经系统,而这几方面都是参与调节睡眠-觉醒的主要机制[40-44]。由GO 富集分析得到的主要生物结果对以上女性失眠的机制几乎都有涉及,可见核心组方参与多种机制,可从多个途径对女性失眠症发挥治疗作用。KEGG 通路分析结果显示,神经活性配体- 受体相互作用、血清素能突触、多巴胺能突触为最主要的通路,另外还有雌激素信号通路及TNF 信号通路亦涉及女性失眠症的有关机制。由分子对接结果可发现核心组方的关键分子与关键靶点大多可形成稳定结构,其中对接分数较高的靶点为AKT1、HTR1A、DRD2。综上,核心组方可得主要在于其多成分通过神经递质方面的途径,涉及神经递质方面的靶点发挥其治疗作用,而神经递质主要涉及5-HT、DA,故选两者及当下治疗失眠药物的主要作用靶点GABA 和治疗围绝经期失眠药物的主要作用靶点MT[45]作为研究指标。
4.4 临床对照研究验证假设
本研究采用的对照组舒眠胶囊为临床应用广泛且较多研究认为安全、有效的药物,可以治疗以肝郁气滞为主的多种证型的失眠症,而贾跃进经多年临床实践认为女性失眠多以肝郁气滞及其相关证型为主,因此选择该药为疗效的阳性对照药物,而相关动物实验则证实其可通过调节GABA、5-HT等神经递质而实现镇静催眠作用[46],故其亦可作为作用机制的阳性对照药物。虽其与核心组方存在药物的交集(柴胡、白芍、合欢皮),但其无论是剂型、用量和其他成分都存在差异性,另外通过数据挖掘与分子对接的分析可以看出,核心组方发挥作用的主要药物可能集中在白术、茯苓等药物,故两者差异性较之相似性更甚,存在比较的意义。通过临床研究得出,两组患者临床量表分析皆显示其症状缓解,说明了两者的有效性,两者相比则核心组方的2 项量表评分下降更为明显,故更加有效,而这种疗效的差异性可能在于核心组方来源于贾跃进临床治疗女性失眠的有效验方,故相比于舒眠胶囊,在应对女性失眠症中存在一定的特异性,且与核心组方组成相似的方剂丹栀逍遥散,多用于临床治疗女性包括失眠症的多种疾病[47-50];而服药前后体检指标则说明两者皆具安全性;相比对照组,服用核心组方后的患者血清MT 水平明显升高,5-HT 及DA 水平明显下降,且治疗前后3 者水平差值相较对照组亦具有统计学意义,但血清GABA 水平两组皆无统计学意义的变化,但其治疗前后GABA 水平差值两组相比则有统计学意义。鉴于目前公认5-HT 和DA 的作用是促进清醒和抑制慢波睡眠或快速眼动睡眠[51],MT、GABA 的作用则相反[52-53],因此可一定程度认为核心组方可通过升高MT 水平,降低5-HT、DA 水平而起到治疗女性失眠的作用,而对GABA 的调节则证据不显著,此结果对网络药理学的结论也实现了验证,证明其有一定的指导作用。但是目前关于失眠神经递质的研究亦有指向5-HT含量增高有益于睡眠,与本研究结论有一定出入,而相关研究也确认在某些情况下(多为兼有抑郁),5-HT 会促进睡眠[54],故其具体机制仍需要进一步研究,笔者认为该差异可能与本研究探讨的女性病例大多属于失眠的肝郁化热型而处于机体代谢较旺盛而非抑郁状态有关,另外网络药理学所得的涉及雌激素及免疫的结论仍有待进一步研究。
5 结论
综上所述,贾跃进老中医治疗女性失眠症的用药思路是以调理枢机为主,兼顾气血两纲,重在调和肝脾;而据其用药规律则可得治疗女性失眠症的核心组方为茯苓、白术、合欢皮、柴胡、香附、白芍、龙骨、当归、牡丹皮、栀子、白茅根;根据网络药理学和临床研究得出该核心组方主要通过升高MT,降低5-HT、DA 2 类神经递质而发挥对女性失眠症的治疗作用。该结论可为女性失眠症的进一步研究及临床用药提供指导。
利益冲突所有作者均声明不存在利益冲突
