三维斑点追踪技术评估缺血性二尖瓣反流患者左心功能
2021-07-19杨道玲王戏丹吴玉莲陈静婉
杨道玲 王戏丹 吴玉莲 陈静婉
缺血性二尖瓣反流(ischemic mitral regurgitation,IMR)是由于慢性冠状动脉出现病变导致机体左室整体或局部病理重塑的并发症[1-2],长期IMR会对人体心功能产生较大影响,使左房承受过大压力及负荷,导致患者左房体积和射血分数增加,左室受到不良影响,机体心排血量不足,引起多种临床症状[3]。研究[4]表明,IMR患者预后较差,病变进展过程中可出现心力衰竭、中风及死亡等不良结局,因此监测IMR患者左房应变功能对评估其预后有着重要意义。三维斑点追踪(three-dimensional speckle tracking imaging,3D-STI)技术是评估心肌功能的重要手段之一,既往有学者[5]应用3D-STI评估2型糖尿病、肾病患者左房功能,本研究旨在探讨3D-STI评估IMR患者左心功能变化的应用价值。
资料与方法
一、研究对象
选取2018年10月至2020年5月我院收治的冠状动脉粥样硬化性心脏病(以下简称冠心病)患者104例,根据其有无继发于二尖瓣反流分为单纯冠心病患者40例(单纯冠心病组)和IMR患者64例(IMR组),IMR组进一步根据美国超声心动图学会制定标准[6]分为轻度反流23例、中度反流22例、重度反流19例。纳入标准:①均为心绞痛或心肌梗死患者;②冠状动脉造影显示狭窄程度>75%;③心电图为窦性心律;④均行3D-STI检查;⑤临床及影像学检查资料完整。排除标准:①合并高血压病、先天性心脏瓣膜病、先天性心脏病、心肌病、心力衰竭或内分泌疾病的患者;②图像质量不佳者;③妊娠期及哺乳期妇女。单纯冠心病组中男22例,女18例,年龄45~74岁,平均(56.31±8.22)岁,体质量指数(body mass index,BMI)18.3~31.0 kg/m2,平均(25.22±5.38)kg/m2;IMR组中男34例,女30例,年龄46~73岁,平均(56.89±8.12)岁,BMI 18.0~32.0 kg/m2,平均(24.73±5.56)kg/m2。另选同期于我院体检的健康成人42例为对照组,男22例,女20例,年龄42~70岁,平均(57.64±8.26)岁,BMI 18.5~32.0 kg/m2,平均(24.92±5.61)kg/m2,均接受超声心动图和3D-STI检查。各组性别比、年龄、BMI、血压、心率、血脂及血糖等一般资料比较差异均无统计学意义。本研究经我院医学伦理委员会批准,所有受检者均知情同意。
二、仪器与方法
1.仪器:使用Philips EPIQ 7C彩色多普勒超声诊断仪,S5-1探头,频率1~5 MHz;X5-1探头,频率1~5 MHz;配备Tom-Tec工作站。
2.方法:受检者取左侧位,先行常规超声心动图扫查,测量左室收缩、舒张末期内径(LVIDS、LVIDD)及收缩末期左房前后径(LAD),脉冲多普勒测量左室舒张早期与晚期二尖瓣环运动速度峰值的比值(Em/Am)、血流速度比(E/A);使用Simpson法测量左室射血分数(LVEF)。然后切换至3D全容积扫描模式,待心尖四腔心切面显示清晰后连接心电图,设置为“Full Volume”显像,嘱受检者呼气后屏住呼吸,获取3个以上心动周期图像并存储,对三维图像进行脱机定量分析。记录患者左房整体纵向应变(GLS)、圆周应变(GCS)及径向应变(GRS),计算各应变达峰时间标准差(TLS-SD、TCS-SD、TRS-SD),同时获得受检者心动周期各时相中左房最大、最小、收缩前容积(LAVmax、LAVmin、LAVp),计算左房总射血分数(LAEF)、被动排空分数(LApEF)及主动射血分数(LAaEF)。
三、统计学处理
应用SPSS 22.0统计软件,计量资料以±s表示,两组比较行t检验,多组比较采用单因素方差分析;计数资料以频数表示,行χ2检验。3D-STI指标与LAEF的相关性采用Pearson相关分析法;绘制受试者工作特征(ROC)曲线分析TLS-SD、TCS-SD、TRS-SD评估左房功能改变的效能。P<0.05为差异有统计学意义。
结果
一、常规超声心动图检查结果
各组LVIDD、LVIDS、LAD、Em/Am、LVEF比较,差异均有统计学意义(均P<0.05);其中LVIDS、LVEF各组间两两比较,差异均有统计学意义(均P<0.05)。见表1。
表1 各组常规超声心动图指标比较(±s)

表1 各组常规超声心动图指标比较(±s)
与对照组比较,*P<0.05;与IMR组比较,#P<0.05。LVIDD:左室舒张末期内径;LVIDS:左室收缩末期内径;LAD:左房前后径;Em/Am:左室舒张早期与晚期二尖瓣环运动速度峰值的比值;E/A:血流速度比;LVEF:左室射血分数
LVEF(%)58.35±4.31*#51.64±6.07*65.73±3.51102.116<0.001组别单纯冠心病组IMR组对照组F值P值LVIDD(cm)5.20±0.65*5.26±0.63*4.62±0.5415.354<0.001 LVIDS(cm)3.35±0.51*#3.87±0.48*3.04±0.1252.473<0.001 LAD(cm)3.93±0.45*3.96±0.42*3.53±0.1418.985<0.001 Em/Am 0.63±0.52*0.58±0.49*0.82±0.243.8760.023 E/A 0.85±0.50*0.82±0.53*0.91±0.110.5280.591
二、3D-STI检查结果
各组3D-STI指标LAVmin、LAVp、LAEF、LAaEF、GLS、GCS、GRS、TLS-SD、TCS-SD、TRS-SD比较,差异均有统计学意义(均P<0.05);其中LAVmin、LAEF、LAaEF、GLS、GCS、GRS、TLS-SD、TRS-SD各组间两两比较,差异均有统计学意义(均P<0.05)。见表2和图1~3。
图1 IMR组3D-STI图像
表2 各组3D-STI指标比较(±s)
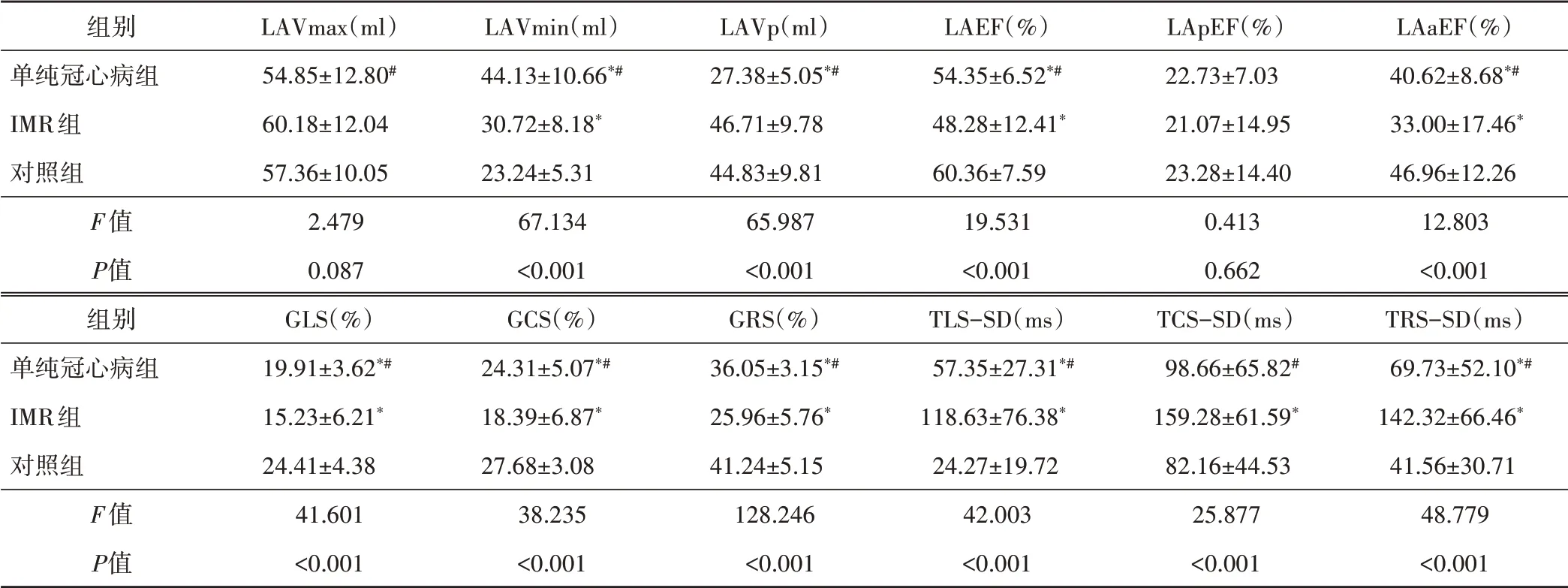
表2 各组3D-STI指标比较(±s)
与对照组比较,*P<0.05;与IMR组比较,#P<0.05。LAVmax、LAVmin、LAVp:分别为左房最大、最小、收缩前容积;LAEF:左房总射血分数;LApEF:被动排空分数;LAaEF:主动射血分数;GLS、GCS、GRS:分别为左房整体纵向应变、圆周应变、径向应变;TLS-SD、TCS-SD、TRS-SC:分别为纵向应变、圆周应变、径向应变达峰时间标准差
LAaEF(%)40.62±8.68*#33.00±17.46*46.96±12.2612.803<0.001 TRS-SD(ms)69.73±52.10*#142.32±66.46*41.56±30.7148.779<0.001组别单纯冠心病组IMR组对照组F值P值组别单纯冠心病组IMR组对照组F值P值LAVmax(ml)54.85±12.80#60.18±12.0457.36±10.052.4790.087 GLS(%)19.91±3.62*#15.23±6.21*24.41±4.3841.601<0.001 LAVmin(ml)44.13±10.66*#30.72±8.18*23.24±5.3167.134<0.001 GCS(%)24.31±5.07*#18.39±6.87*27.68±3.0838.235<0.001 LAVp(ml)27.38±5.05*#46.71±9.7844.83±9.8165.987<0.001 GRS(%)36.05±3.15*#25.96±5.76*41.24±5.15128.246<0.001 LAEF(%)54.35±6.52*#48.28±12.41*60.36±7.5919.531<0.001 TLS-SD(ms)57.35±27.31*#118.63±76.38*24.27±19.7242.003<0.001 LApEF(%)22.73±7.0321.07±14.9523.28±14.400.4130.662 TCS-SD(ms)98.66±65.82#159.28±61.59*82.16±44.5325.877<0.001
三、相关性分析
IMR患者GLS、GCS、GRS与LAEF均呈正相关(r=0.210、0.383、0.381,均P<0.05)。
四、ROC曲线分析
ROC曲线分析结果显示,TLS-SD、TCS-SD、TRSSD截断值分别为53.9 ms、139.3 ms、89.2 ms时,其评估左房功能改变的曲线下面积分别为0.862、0.841、0.924,敏感性分别为70.3%、65.6%、78.1%,特异性分别为100%、90.5%、100%。见图4。
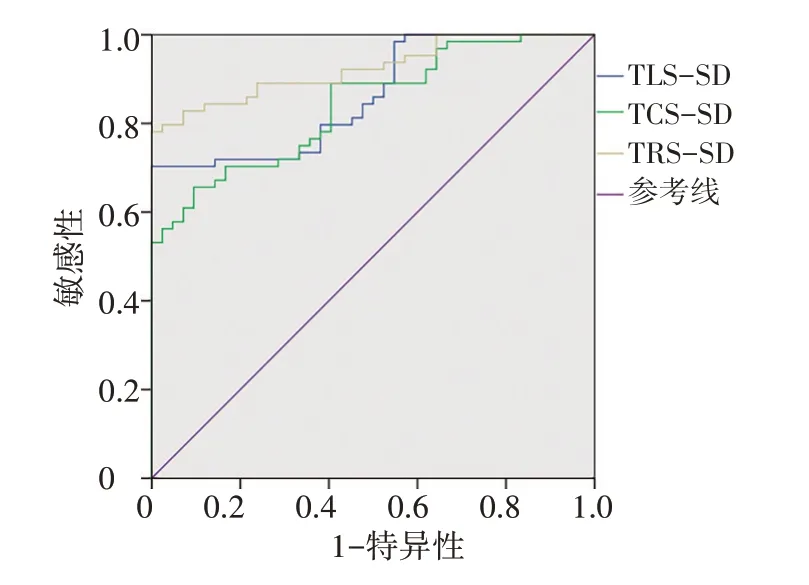
图4 TLS-SD、TCS-SD、TRS-SD评估左房功能改变的ROC曲线图

图2 单纯冠心病组3D-STI图像
图3 对照组3D-STI图像
讨论
IMR患者除二尖瓣功能改变外,还常伴左室、乳头肌、瓣环等多种组织异常[7]。研究[8]显示,超声心动图在心功能定量评估中有一定作用,但该方法测量心脏形态变化或重构患者左房大小可能有一定误差,临床应用有一定局限。3D-STI可对人体空间层面上心肌斑点的运动进行追踪,评估受检者心肌三维动态容积指标,能多方位评价心室的收缩及应变功能,该技术不受不同时点上心肌运动轴改变的影响,无角度依赖性,可以实时获取心肌空间应变指标,在左房功能的评估及早期异常监测中更加准确[9-10]。人体左房主要作用是储存、管道及辅助泵等,储存是指左房排空的血容量,以LAEF表示;管道作用即肺静脉血液流入左房内,然后于左室舒张开始则输入左室内,以LApEF表示;辅助泵则是指左室收缩完成后左房心肌开始收缩,将血液泵入左室内,以LAaEF表示。当机体出现生理或病理改变,则可通过左房来调节左室工作,使机体保持其自身所需的心搏量。
本研究常规超声心动图检查结果显示,IMR组患者LVIDD、LVIDS、LAD均较单纯冠心病组和对照组增大,Em/Am、LVEF均降低(均P<0.05),可能与IMR患者冠状动脉出现病变使机体心肌供血异常、心室壁运动出现相应改变有关,导致其左室收缩功能受到影响。各组E/A比较差异无统计学意义,分析原因可能为IMR患者左室收缩期血液反流至左房内,使机体左房充盈,左室开始舒张时其房室压差值升高,导致血流变快,E峰偏高,表明IMR患者房室血流变化会对其左室舒张产生影响,评估左室功能可能不够准确[11]。本研究3D-STI检查显示,IMR组LAVmin、LAEF、LAaEF、GLS、GCS、GRS、TLS-SD、TRS-SD与单纯冠心病组和对照组比较,差异均有统计学意义(均P<0.05);IMR组患者LAVmin较对照组增高,LAEF、LAaEF均较对照组降低,差异均有统计学意义(均P<0.05);而两组LAVmax和LApEF比较差异均无统计学意义,提示IMR患者左房储存及辅助泵能力均下降,分析原因为IMR患者左房主动收缩时,其血流动力学出现异常且心肌运动会减弱,LAVmin升高、LAEF降低,虽然患者左室舒张能力降低,但其舒张时反流及肺静脉流经左房血液均会经开放的二尖瓣到达左室,故LApEF(管道功能)无明显改变,但长期冠状动脉病变会导致心肌功能损害,再加上房室血流动力的变化会对房壁运动有一定影响,使患者辅助泵能力降低[12]。
人体左房心肌走行为纵向分层,而机体心脏工作过程中各层心肌的运动方向也各不一致,深层主要包括纵向运动和圆周运动,浅层则为较薄的心肌组织,主要是径向走行[13]。本研究3D-STI检查显示,IMR组患者GLS、GCS、GRS与对照组和单纯冠心病组比较,差异均有统计学意义(均P<0.05),说明冠状动脉病变会导致患者心房壁运动异常,而IMR持续时间较长,心脏血流动力学出现异常,因此IMR患者在纵向、圆周及径向运动上均受到限制,心肌收缩及左房整体应变能力受到影响。另外,本研究相关性分析结果显示,IMR患者GLS、GCS、GRS与LAEF均呈正相关(r=0.210、0.383、0.381,均P<0.05),表明IMR患者心肌应变多呈下降趋势,进而导致左房容积出现相应改变,储蓄和收缩能力下降。本研究IMR组TLS-SD、TCS-SD、TRS-SD均高于对照组(均P<0.05),提示IMR患者多存在左房心肌运动不同步现象,分析原因为人体左房心肌同步收缩主要取决于电生理传导和细胞收缩耦联过程,IMR患者多有左房负荷较大或心肌功能异常,在该耦联过程中受到阻碍,使心肌出现代偿做功,心房发生重构,心肌运动同步性受到影响,收缩出现不协调,最终影响左室功能[14]。本研究ROC曲线分析显示,TLS-SD、TCS-SD、TRS-SD评估左房功能改变的曲线下面积分别为0.862、0.841、0.924,表明上述指标对左房心肌功能的改变均有较高的评估价值,与姜婧璇等[13]研究结论一致。
本研究的局限性:①样本量较小;②3D-STI成像受较多因素影响,对心内膜显示要求高,若心脏体积过大、内膜显像不佳或患者声透性差则很难获得清晰的心内膜影像,对其评估有一定影响;③未对IMR患者进行随访,无法分析其预后,患者心底大血管、左心耳对左房可能产生的影响也无法避免,需今后进一步完善和分析。
综上所述,3D-STI能准确评估IMR患者左房容积及心肌应变的变化,在左房功能评估中具有较高的应用价值,对临床干预有重要作用。
