紫苏叶化学成分及其体外抗炎活性
2021-06-26王宇宁樊晖梁克利
王宇宁樊 晖梁克利
(1.沈阳市第七人民医院,辽宁 沈阳 110000;2.辽宁中医药大学附属医院,辽宁 沈阳 110847;3.哈尔滨商业大学,黑龙江 哈尔滨 150076)
紫苏Perilla frutescens(L.)Britt.为唇形科紫苏属植物,具有较高的食用及药用价值,在我国应用历史悠久,紫苏叶可做香料使用,紫苏种子油可供食用,也可用于工业防腐用途[1],我国资源丰富,华北、华中、华南、西南及台湾省均有野生种和栽培种,印度、缅甸、日本、朝鲜、韩国、印度尼西亚、俄罗斯等国家均有分布[2],具有宣肺化痰、解表散寒、行气和胃等功效,传统临床常用于胃炎、支气管炎、以及肾炎等炎症性疾病的治疗[3]。目前关于紫苏叶的抗炎作用尤其是治疗溃疡性结肠炎的作用越来越得到重视,现代药理学研究表明其提取物抗炎作用与抑制炎症介质释放、调控活性氧簇一氧化氮水平等机制有关[4],它含有丰富的挥发油、酚酸、黄酮等成分,被认为是其主要的抗炎活性物质[5-7]。因此,本课题组在相关文献基础上进一步对紫苏叶的化学成分进行分离纯化,并以RAW264.7 细胞为评价模型,采用Western-blot 法检测化合物对iNOS 及COX-2 等相关蛋白表达的影响,初步对其抗炎活性进行评价。
1 材料
Bruker-400 核磁共振仪(德国Bruker 公司,内标TMS);Agilent 1100 高效液相色谱仪(美国Agilent 公司,UV 检测器);电泳仪(北京君意东方电泳设备有限公司);全自动化学发光成像分析仪(上海天能科技有限公司);柱色谱用硅胶(青岛海洋化工厂);大孔吸附树脂D101 填料(沧州宝恩树脂科技有限公司);ODS 填料(美国Welch公司)。DMSO(美国Sigma 公司);Peroxidaseconjugated Affinipure Goat Anti-Rabbit 及Anti-β-actin(美国Proteintech 公司);P-Tau Rabbit mAb(美国Cell Signaling Technology 公司);Tau Rabbit mAb(英国Abcam 公司);Marker(上海信裕生物科技有限公司);细胞裂解液、PMSF、ECL 发光液等(上海碧云天生物技术有限公司);TEMED 及PVDF 膜(沈阳鼎国生物技术有限公司);RAW264.7 细胞株(美国ATCC 公司)。紫苏叶购自辽河大药房,由沈阳市第七人民医院王宇宁中药师鉴定为紫苏Perilla frutescens(L.)Britt.干燥叶。甲醇等溶剂均购自于天津大茂化学试剂有限公司。
2 提取与分离
紫苏叶干燥全草15 kg 粉碎后,采用8 倍量75%乙醇回流提取2 次,每次2 h,提取液合并后减压浓缩至无醇味,得到提取物浸膏2.3 kg,蒸馏水溶解后用D101 大孔吸附树脂进行分离,以乙醇-水(0~100%)梯度洗脱,60%洗脱部分经正相硅胶柱,二氯甲烷-甲醇(100∶0~1∶1)梯度洗脱,取20∶1 洗脱部分进行分离,经ODS 反相柱,分别采用10%、30%、50%、70%、100% 甲醇-水洗脱,进一步采用半制备型HPLC,以甲醇-水洗脱纯化,其中10% 部分经过纯化分离,得化合物1;30%部分经过纯化分离,得到化合物2~4、5、6~7。
3 结构鉴定
化合物1:白色无定形粉末。1H-NMR(400 MHz,DMSO-d6)中显示δH1.15(3H,d,J=6.3 Hz,H-10),1.10(3H,s,H-13),1.01(3H,s,H-12),0.73(3H,s,H-11)提示为4 个甲基上的氢信号,δH5.69(1H,dd,J=15.9,0.9 Hz,H-7),5.68(1H,dd,J=15.9,5.9 Hz,H-8)为一组反式双键上的氢信号。 δH1.50(1H,d,J=12.0 Hz,H-2),1.27(1H,dd,J=12.0,3.0 Hz,H-2)和δH1.59(2H,m,H-4)为两组亚甲基上的氢信号;13C-NMR(100 MHz,DMSO-d6)中显示δC27.3,27.1,26.0,24.8 提示为4 个甲基碳信号,δC135.1,129.2 为一组双键上的碳信号。以上数据与文献 [8] 基本一致,故鉴定为(3R,5S,6S,7E,9S)-megastiman-7-ene-3,5,6,9-tetrol。
化合物2:无色油状物。1H-NMR(400 MHz,DMSO-d6) δ:6.92(1H,d,J=8.2 Hz,H-6′),6.78(1H,d,J=1.9 Hz,H-3′),6.66(1H,dd,J=8.2,1.9 Hz,H-5′),4.44(2H,m,H-9′),4.06(1H,m,H-2),3.72(3H,s,2′-OCH3),3.54(2H,m,H-1),3.54(2H,m,H-3),2.62(2H,m,H-7′),1.68(2H,m,H-8′);13C-NMR(100 MHz,DMSO-d6) δ:60.4(C-1),81.5(C-2),60.4(C-3),145.7(C-1′),150.0(C-2′),116.6(C-3′),135.7(C-4′),120.3(C-5′),113.1(C-6′),31.5(C-7′),34.7(C-8′),60.5(C-9′),55.7(2′-OCH3)。以上数据与文献 [9] 基本一致,故鉴定为 2-[4-(3-hydroxypropyl)-2-methoxyphenoxy] propance-1,3-diol。
化合物3:黄色油状物。1H-NMR(400 MHz,DMSO-d6) δ:6.97(1H,d,J=8.2 Hz,H-6′),6.79(1H,d,J=1.8 Hz,H-3′),6.67(1H,dd,J=8.2,1.8 Hz,H-5′),4.29(1H,m,H-2),4.29(2H,m,H-9′),4.19(1H,d,J=7.8 Hz,H-1″),4.05(1H,m,H-6″),3.92(1H,m,H-5″),3.88(2H,m,H-3),3.73(3H,s,2′-OCH3),3.63(1H,m,H-4″),3.59(1H,m,H-3”),3.58(1H,m,H-6″),3.57(2H,d,J=11.1 Hz,H-1),3.28(1H,m,H-2″),2.53(2H,m,H-7′),1.69(2H,m,H-8′);13C-NMR(100 MHz,DMSO-d6)δ:68.0(C-1),78.9(C-2),60.1(C-3),145.1(C-1′),149.6(C-2′),116.1(C-3′),135.6(C-4′),120.0(C-5′),112.8(C-6′),31.3(C-7′),34.5(C-8′),60.2(C-9′),55.5(2′-OCH3),103.5(C-1″),73.4(C-2″),76.7(C-3″),70.0(C-4″),76.9(C-5″),61.0(C-6″)。以上数据与文献 [10] 基本一致,故鉴定为 1-O-(β-Dglucosyl)-2-[2-methoxy-4-(-hydroxypropyl)-phenoxy] -propan-3-ol。
化合物4:黄色油状物(甲醇)。1H-NMR(400 MHz,DMSO-d6) δ:6.38(1H,brs,H-2′),6.63(1H,brs,H-2),6.38(1H,brs,H-6′),6.15(1H,brs,H-5),4.62(1H,d,J=8.0 Hz,H-7′),3.78(2H,m,H-9),3.74(3H,s,3-OCH3),3.72(3H,s,3′-OCH3),3.72(3H,s,5′-OCH3),2.72(2H,m,H-7),3.20(2H,m,H-9′),2.18(1H,m,H-8′),1.68(1H,t,J=8.4 Hz,H-8);13C-NMR(100 MHz,DMSO-d6) δ:132.7(C-1),112.0(C-2),145.7(C-3),144.3(C-4),116.3(C-5),127.3(C-6),32.4(C-7),38.3(C-8),63.8(C-9),136.3(C-1′),106.9(C-2′),148.0(C-3′),134.0(C-4′),148.0(C-5′),106.9(C-6′),49.0(C-7′),46.4(C-8′),60.0(C-9′),55.7(3-OCH3),56.2(3′-OCH3),56.2(5′-OCH3)。以上数据与文献 [11] 基本一致,故鉴定为 5-methoxyisolariciresinol。
化合物5:黄色油状物(甲醇)。1H-NMR(400 MHz,DMSO-d6) δ:7.00(1H,d,J=8.0 Hz,H-5),6.84(1H,brs,H-2),6.84(1H,brs,H-2′),6.72(1H,d,J=8.0 Hz,H-5′),6.70(1H,brd,J=8.0 Hz,H-6),6.70(1H,d,J=8.0 Hz,H-6′),4.85(1H,d,J=7.3 Hz,H-7),4.67(1H,d,J=6.8 Hz,H-1″),3.87(1H,m,H-9′),3.76(6H,s,3,3′-OCH3),3.68(2H,m,H-9),3.62(1H,m,H-6″),3.57(1H,m,H-9′),3.47(1H,m,H-6″),3.26(1H,m,H-3″),3.25(1H,m,H-5″),3.20(1H,m,H-4″),3.17(1H,m,H-7′),3.12(1H,m,H-2″),2.88(1H,m,H-8′),2.61(1H,m,H-7′),2.47(1H,m,H-8);13C-NMR(100 MHz,DMSO-d6) δ:134.9(C-1),110.2(C-2),149.0(C-3),145.7(C-4),115.6(C-5),118.4(C-6),82.0(C-7),52.5(C-8),58.8(C-9),134.9(C-1′),113.3(C-2′),147.4(C-3′),145.0(C-4′),115.2(C-5′),120.6(C-6′),32.4(C-7′),42.0(C-8′),72.0(C-9′),55.8(3,3′-OCH3),100.6(C-1″),73.4(C-2″),77.2(C-3″),69.9(C-4″),77.0(C-5″),60.9(C-6″)。以上数据与文献[12] 基本一致,故鉴定为lariciresinol 4′-O-β-D-glucopyranoside。
化合物6:白色结晶(甲醇)。1H-NMR(CDCl3)谱中的δH7.99 和δH6.91 显示各有2 个氢存在,分别被邻位、间位相互偶合裂分为dd 峰,表明苯环为对位取代;由13C-NMR 和1H-NMR 可知该化合物含有苯环,1 个甲基,4 个亚甲基,3 个次甲基,3 个季碳。以上数据与文献[13] 基本一致,故鉴定为butyl p-hydroxybenzoate。
化合物7:黄绿色无定形粉末。1H-NMR(400 MHz,DMSO-d6) δ:8.10(1H,s,H-7),7.65(1H,s,H-8′),7.46(1H,d,J=8.4 Hz,H-6),7.25(1H,d,J=8.4 Hz,H-5),7.24(1H,s,H-6′),6.60(1H,s,H-3′);13C-NMR(100 MHz,DMSO-d6) δ:123.2(C-1),123.2(C-2),136.2(C-3),141.1(C-4),119.8(C-5),121.3(C-6),127.3(C-7),127.2(C-8),167.7(C-9),110.2(C-1′),145.0(C-2′),104.0(C-3′),148.2(C-4′),142.7(C-5′),108.3(C-6′),126.6(C-7′),110.9(C-8′)。以上数据与文献[14] 基本一致,故鉴定为mongolicumin A。
4 抗炎活性筛选
将RAW264.7 细胞培养与DMEM 培养基中(含有10% FBS),细胞按每孔8×104/0.5 mL 浓度接种至24 孔板内,孵育24 h。待测化合物(DMSO 溶解,终浓度为80 μmol/L)及阳性药10 μg/mL地塞米松(DEX)预处理1 h 后,脂多糖(LPS,质量浓度为100 ng/mL)刺激18 h。再提取细胞总蛋白,用于iNOS 和COX-2 蛋白的电泳及检测。
结果显示,经LPS 刺激后iNOS 和COX-2 蛋白表达明显增强,提示造模成功。DEX 在10 μg/mL质量浓度下可显著抑制iNOS、COX-2 蛋白表达,而化合物2可显著抑制iNOS 蛋白表达,提示它有一定的抗炎活性。见图1。
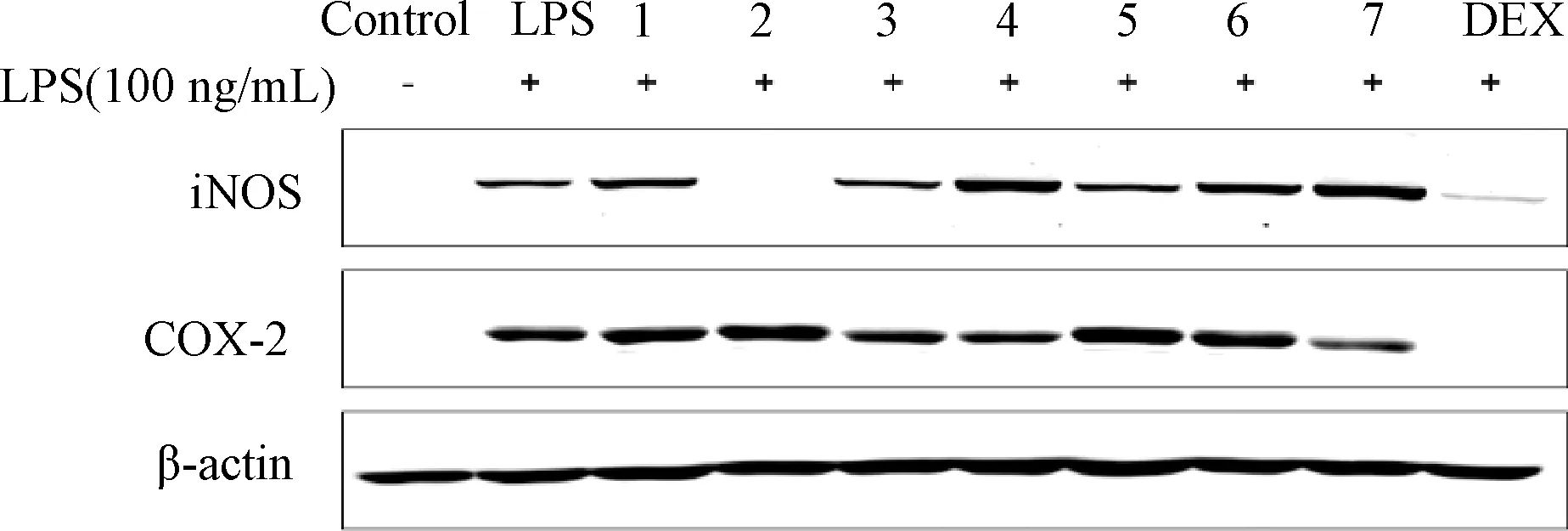
图1 各化合物对RAW264.7 细胞中iNOS、COX-2蛋白表达的影响Fig.1 Effects of various compounds on protein expressions of iNOS and COX-2 in RAW264.7 cells model
5 结论
诱导型iNOS 是利用一氧化氮的氧化应激,协助巨噬细胞在免疫系统中对抗病原体的一类酶。其在细胞受到刺激而被激活后才发挥功效,并且所生成的一氧化氮数量较多。COX 又称前列腺素过氧化物合成酶,是前列腺素(PG)合成过程中一个重要的限速酶,可将花生四烯酸代谢成各种前列腺素产物,从而在机体的生理和病理过程中发挥作用。以上两者均为重要的炎症介质,其表达程度可以作为炎症的判断标准。
本研究对紫苏叶乙醇提取物中化学成分进行系统分离纯化,得到7 个化合物,并对分离得到的各单体化合物体外抗炎活性进行初步评价。其中化合物2在80 μmol/L 时可以显著的抑制iNOS 的蛋白表达,显示出一定的抗炎活性。以期该研究为紫苏叶开发应用提供部分前期工作基础。
