列线图模型预测冠心病患者经皮冠状动脉介入治疗术后因严重支架内再狭窄导致再次血运重建的研究
2021-06-17张琳赟刘杰吴皖灵罗园媛朱红潘德锋
张琳赟 刘杰 吴皖灵 罗园媛 朱红 潘德锋
冠状动脉粥样硬化性心脏病(简称“冠心病”)是心血管系统最常见的疾病之一,其高死亡率及高致残率严重影响人们的生活。据估算,心血管病现患人数2.9亿,其中冠心病患者达1100万[1]。冠心病的流行病学和危害是巨大的公共卫生问题,其诊断及治疗值得关注。目前经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)是治疗冠心病的一种有效手段。但是由于PCI术后支架内再狭窄(in-stent restenosis,ISR)等因素造成患者再次血运重建,仍是PCI术后不可忽视的问题之一,也是临床医师关注的热点之一。
目前研究大多集中于预测PCI术后ISR的发生,但是ISR的程度有所不同,并不是所有ISR都需要进行再次血运重建。目前关于PCI术后因再狭窄导致再次进行血运重建的相关研究很少,较单独预测是否发生ISR更具临床意义。且目前研究多数集中于独立危险因素的分析及回归方程预测,而构建列线图模型较传统的预测方法具有更加直观、形象、简便的优势。因此,本研究从患者的一般情况、实验室检查、手术资料等方面回顾性分析了因严重ISR导致冠心病患者PCI术后再次血运重建的危险因素,并构建列线图临床预测模型,旨在筛选出高危患者,以期进一步指导临床决策。
1 对象与方法
1. 1 研究对象
回顾性分析2013年6月至2019年6月于徐州医科大学附属医院(简称我院)行PCI术并复查冠状动脉造影(coronary angiography,CAG)的1083例患者的病例资料。ISR定义为原支架及其边缘两端5 mm以内存在血管直径>50%的狭窄[2]。根据患者是否因ISR再次血运重建分组:因严重ISR行血运重建(ISRRevasc)组(209例)、无或轻中度ISR无需行血运重建(N-Revasc)组(874例)。纳入标准:于我院心内科行CAG术,根据结果诊断为严重冠心病(定义为至少一支主要冠状动脉血管中存在≥70%的管腔狭窄),首次成功行PCI术(药物洗脱支架);再次血运重建治疗均为临床症状及客观指标(心电图、心肌酶学等)驱使的PCI;若有多次血运重建史,则选取前2次连续性病例资料。排除标准:(1)既往于外院有PCI史;(2)无法在PCI术后于我院复查CAG;(3)复查CAG示病变较重,拒绝PCI,建议行冠状动脉旁路移植术;(4)计划内分次行PCI;(5)严重肝肾功能不全、先天性心脏病、风湿性心脏病、病毒性心肌炎、无法控制的严重感染、血液系统疾病或恶性肿瘤,预期寿命<12个月。
1. 2 临床资料收集
1. 2. 1 一般资料 收集入组患者首次入院时的一般临床资料及既往病史情况,主要包括:年龄、性别、糖尿病病史、高血压病史、吸烟史、饮酒史、冠心病家族史、急性心肌梗死病史、卒中/短暂性脑缺血发作(transient ischemic attack,TIA)病史、术后是否正规行双联抗血小板治疗(阿司匹林+氯吡格雷/替格瑞洛)12个月等。
1. 2. 2 实验室检查 所有患者于首次入院后24 h内采集静脉血行实验室检查。生化指标包括:入院时糖化血红蛋白(glycated hemoglobin,HbA1c)、空腹血糖(fasting blood-glucose,FBG)、血清肌酐(serum creatinine,Scr)、血尿酸(uric acid,UA)、白细胞计数(white blood cell count,WBC)、中性粒细胞计数(neutrophil count,NE)、淋巴细胞计数(lymphocyte count,LY)、血红蛋白(hemoglobin,HGB),并计算中性粒细胞/淋巴细胞比值(neutrophil-to-lymphocyte ratio,NLR)。监测血脂控制情况,包括:第二次入院复查时低密度脂蛋白胆固醇(low density lipoproteincholesterol,LDL-C)是否>1.8 mmol/L、脂蛋白a[lipoprotein(a),Lp(a)]是否>300 mg/L。
1. 2. 3 PCI术资料 CAG时一般采用标准体位:左冠状动脉至少投照4个体位,右冠状动脉至少投照2个体位,且每支血管至少选取两个相互垂直的标准体位进行投照,依据患者冠状动脉解剖特点不同可适当增加投照体位。根据病变的特征及临床情况选择合适的PCI策略。复查CAG时采用相同的投照体位。CAG及PCI术均由经验丰富的心内科介入医师实施。通过影像归档和通信系统及定量冠状动脉造影,由两名经验丰富的临床医师对图像进行分析,并收集以下手术资料:2次手术间隔随访时间,病变支数,靶血管,是否急诊PCI,靶病变有无慢性完全闭塞(chronic total occlusion,CTO)病变、钙化病变、分叉病变、开口病变、扭曲成角病变,置入支架总长度,平均置入支架直径,置入支架数量,是否在血管内超声(intravenous ultrasound,IVUS)或旋磨辅助下治疗等。
1. 3 统计学分析
采用SPSS 22.0、Medcalc 15.0软件对收集的所有数据进行统计分析。计数资料采用频数及率表示,采用χ2检验或Fisher精确概率法检验。正态分布的计量资料采用(x-±s)表示,采用t检验;偏态分布的计量资料用中位数及四分位数间距[M(Q1,Q3)]表示,采用Mann-WhitneyU检验。多因素分析采用logistic回归法进行分析,并计算比值比及95%可信区间。检验水准设为α=0.05,以P<0.05为差异有统计学意义。通过R Studio软件对模型进行Bootstrap内部验证,并输出列线图模型。
2 结果
2. 1 两组患者一般资料比较
相比于N-Revasc组,ISR-Revasc组患者糖尿病史占有更高的比例(41.6%比22.2%,P<0.001),差异有统计学意义。两组患者男性、年龄、高血压病史、吸烟史、饮酒史、冠心病家族史、既往心肌梗死病史、既往卒中/TIA病史、术后双联抗血小板治疗12个月(阿司匹林+替格瑞洛/氯吡格雷)等比较,差异均无统计学意义(均P>0.05,表1)。
2. 2 两组患者实验室检查结果比较
ISR-Revasc组的HbA1c高于N-Revasc组[6.3%(5.9%,7.2%)比6.2%(5.9%,6.8%),P=0.045],且ISR-Revasc组患者LDL-C>1.8 mmol/L、Lp(a)>300 mg/L所占的比例明显高于N-Revasc组(68.9%比49.8%、56.9%比25.4%,均P<0.001),差异均有统计学意义。两组FGB、Scr、UA、WBC、NE、LY、NLR、HGB比较,差异均无统计学意义(均P>0.05,表2)。
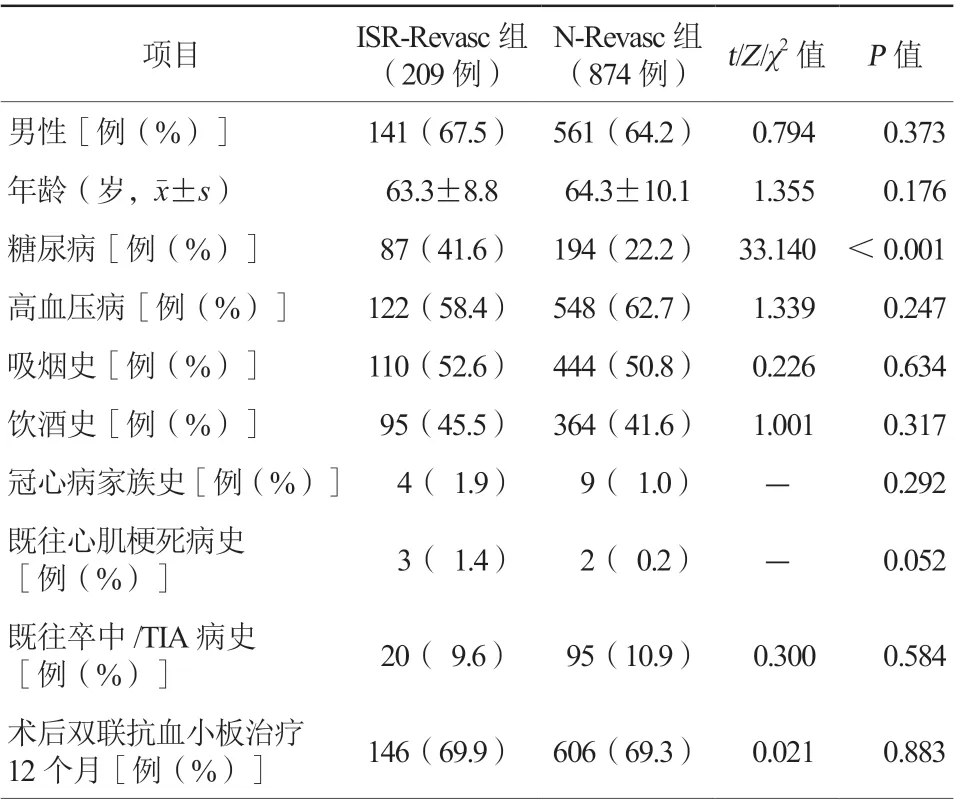
表1 两组患者一般资料比较
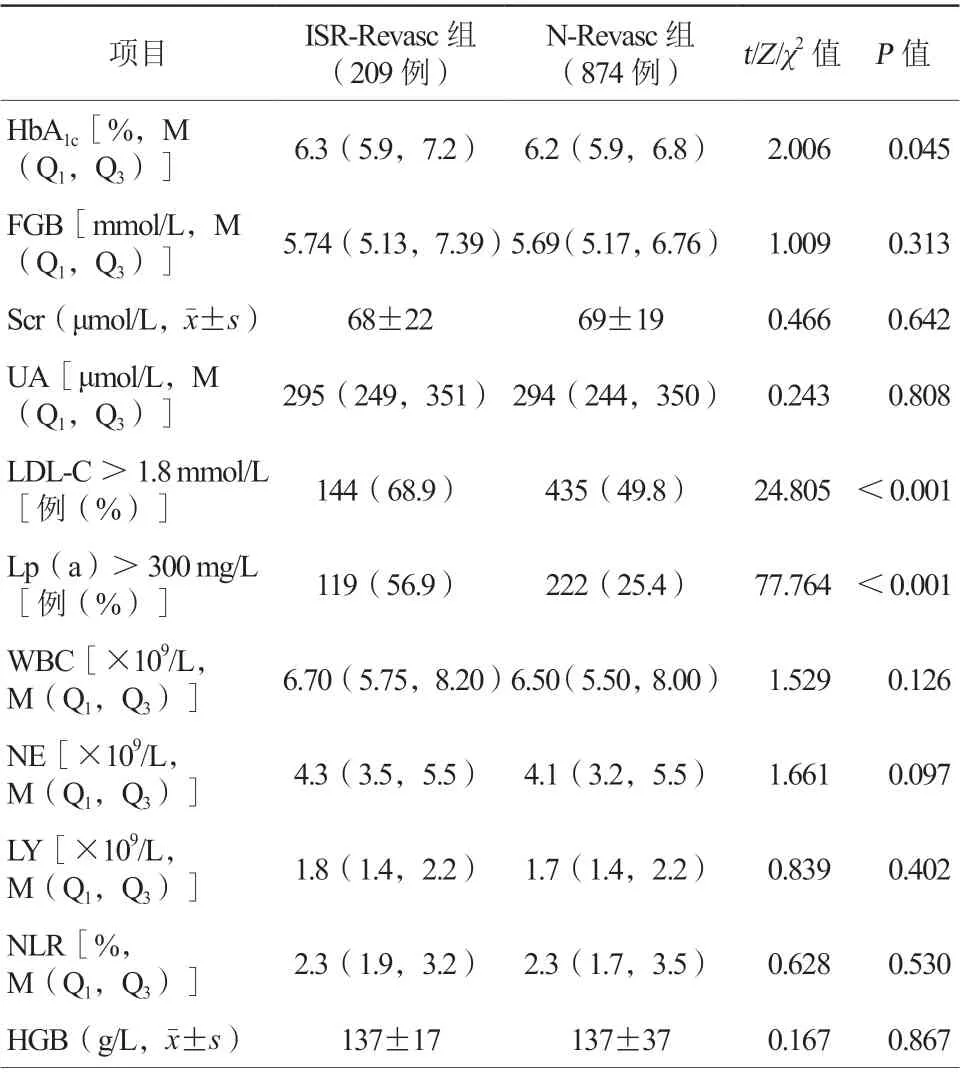
表2 两组患者实验室检查结果比较
2. 3 两组患者手术情况比较
与N-Revasc组相比,ISR-Revasc组在多支病变(multivessel disease,MVD)(88.5%比77.7%)、同时处理多支血管(43.5%比36.2%)、CTO病变(15.8%比7.8%)上有更高的比例,且置入支架总长度[58(33,95)mm比41(24,65)mm]更长、数量[2(1,3)枚比2(1,2)枚]更多、直径[2.80(2.66,3.00)mm比2.90(2.74,3.16)mm]更小,差异均有统计学意义(均P<0.05)。两组随访时间、钙化病变比例、分叉病变比例、开口病变比例、扭曲成角病变比例、靶血管分布、急诊PCI比例、IVUS辅助比例、旋磨仪器辅助比例比较,差异均无统计学意义(均P>0.05,表3)。
2. 4 严重ISR导致冠心病患者PCI术后再次血运重建的独立危险因素
根据上述单因素分析结果,将差异有统计学意义的指标及有明确临床意义的指标全部纳入logistic多因素回归,纳入指标为糖尿病史、HbA1c水平、LDL-C>1.8 mmol/L、Lp(a)>300 mg/L、MVD、同时处理多支血管、CTO病变、置入支架总长度、平均支架直径、支架置入数量。logistic多因素回归结果显示:Lp(a)>300 mg/L(P<0.001,OR3.579,95%CI2.561~5.003),LDL-C>1.8 mmol/L(P=0.001,OR1.834,95%CI1.294~2.599)、糖尿病病史(P<0.001,OR2.426,95%CI1.637~3.595)、MVD(P=0.014,OR1.844,95%CI1.133~3.002)、支架置入长度(P<0.001,OR1.025,95%CI1.014~1.037)是冠心病患者PCI术后因严重ISR导致再次血运重建的独立危险因素(图1)。
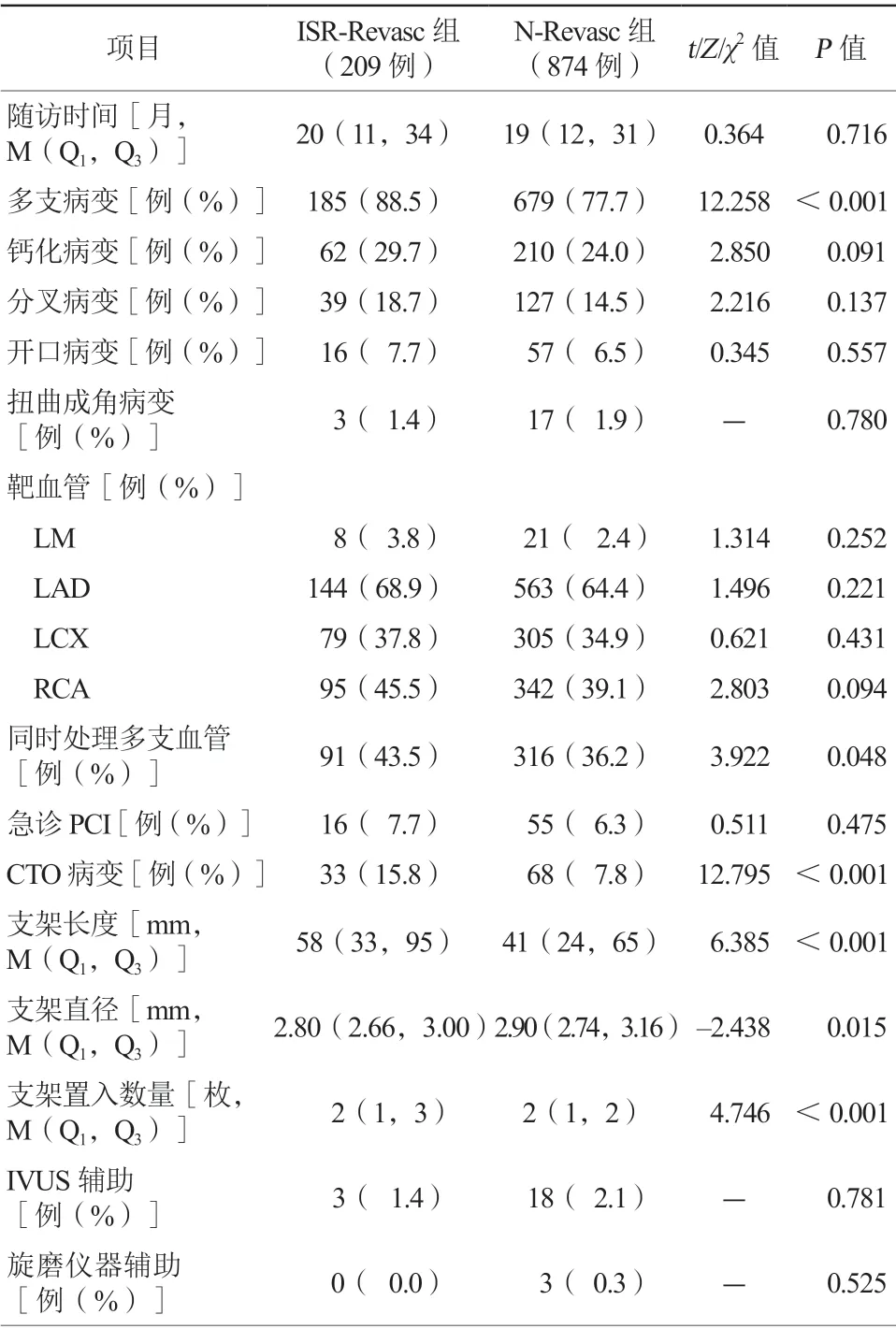
表3 两组患者手术情况比较
2. 5 logistic模型的建立
根据logistic多因素回归分析的结果[Lp(a)>300 mg/L、LDL-C>1.8 mmol/L、糖尿病病史、MVD、支架置入长度]及各个指标的回归系数,建立回归方程。P为预测发生再次血运重建的概率,取值为0~1,P值越大,则患者PCI术后需要再次血运重建的可能性越大,回归方程如下:Logit(P)=-2.804+0.866×(糖尿病病史,有=1,无=0)+1.275×[Lp(a)>300 mg/L,是=1,否=0]+0.606×(LDL-C>1.8 mmol/L,是=1,否=0)+0.612×(MVD,有=1,无=0)+0.025×置入支架长度(mm)。
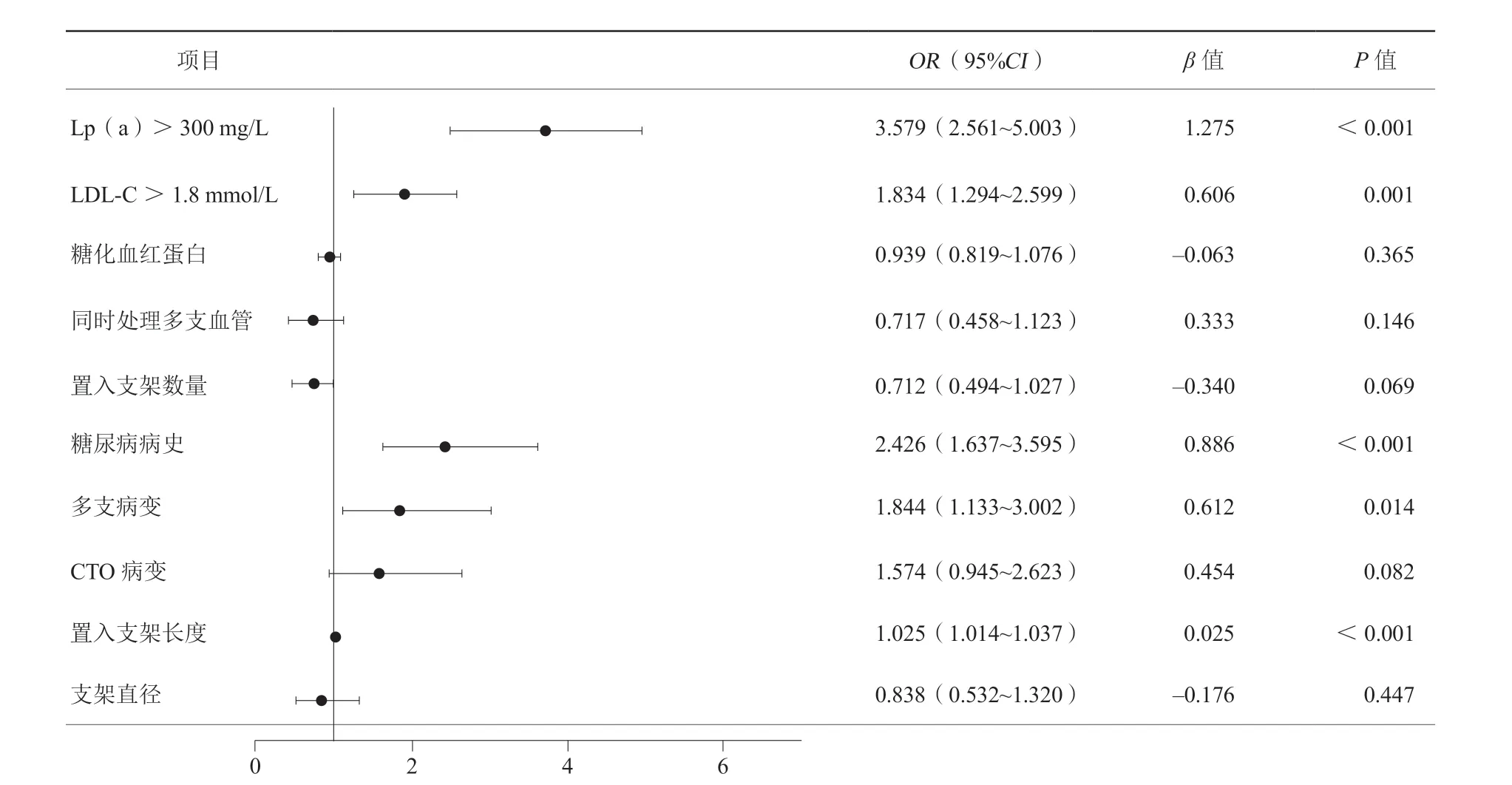
图 1 严重ISR行再次血运重建logistic多因素回归森林图
2. 6 预测模型的验证及评估
通常用受试者工作特征(receiver operating characteristic,ROC)曲线评估预测模型的区分度/鉴别能力。将患者是否再次血运重建作为状态变量,将logistic回归得出的5个独立危险因素作为检验变量,绘制ROC曲线(图2),曲线下面积为0.766,标准误为0.0184,95%CI为0.740~0.791,区分度较好。通过Hosmer-Lemeshow拟合优度检验来评价预测模型的适配度。结果显示,Hosmer-Lemeshowχ2=8.948,P=0.347>0.05,提示模型适配度较好。模型预测值与实际观测值之间差异无统计学意义,预测模型有较好的校准能力。
采用Bootstarp方法从纳入研究的受试者中内部验证风险模型,再抽样次数B=1000,并绘制校准曲线。结果显示:校准图形中标准曲线与预测校准曲线贴合良好,表示模型符合度良好(图3)。
2. 7 列线图的绘制
根据logistic回归结果绘制列线图(图4)。列线图是使用一些互不相交的线段来推算事件的发生概率,它把原本由字母数字组成的公式以图形的形式可视化展示,这是列线图的优势。
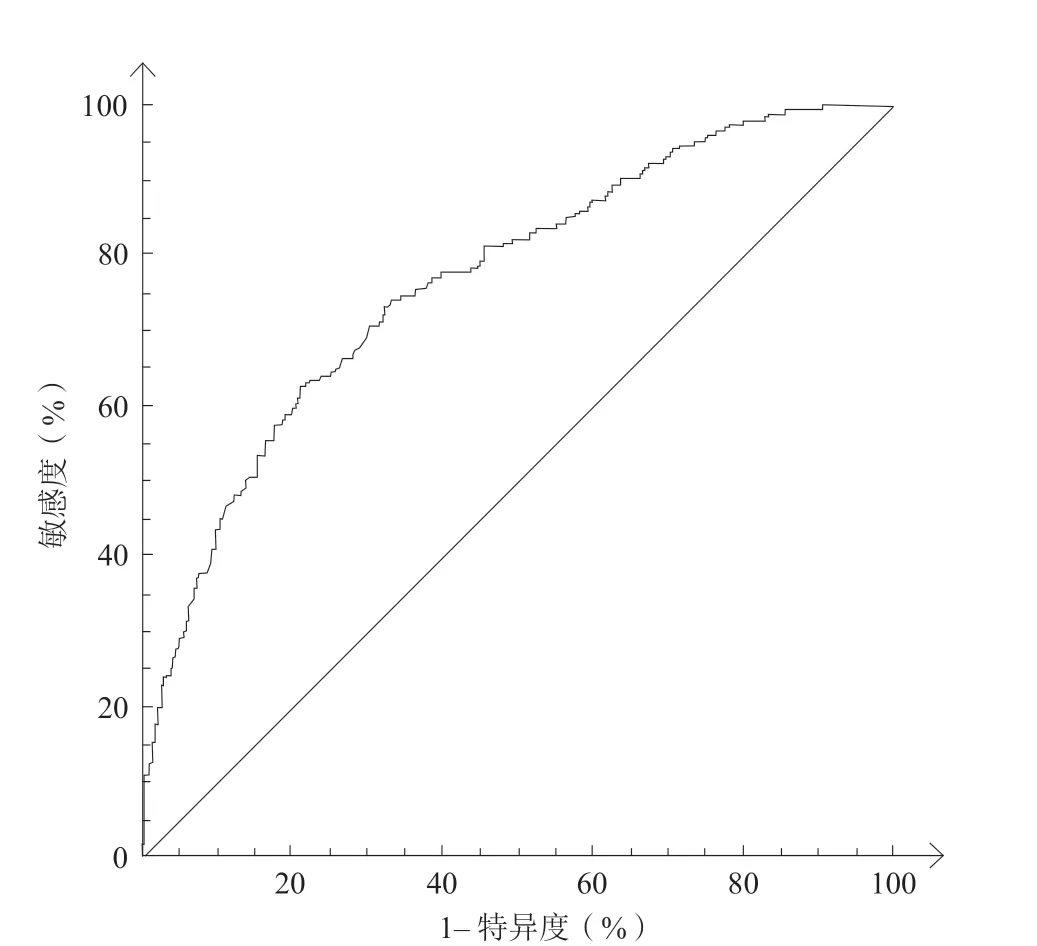
图 2 预测模型ROC曲线
3 讨论
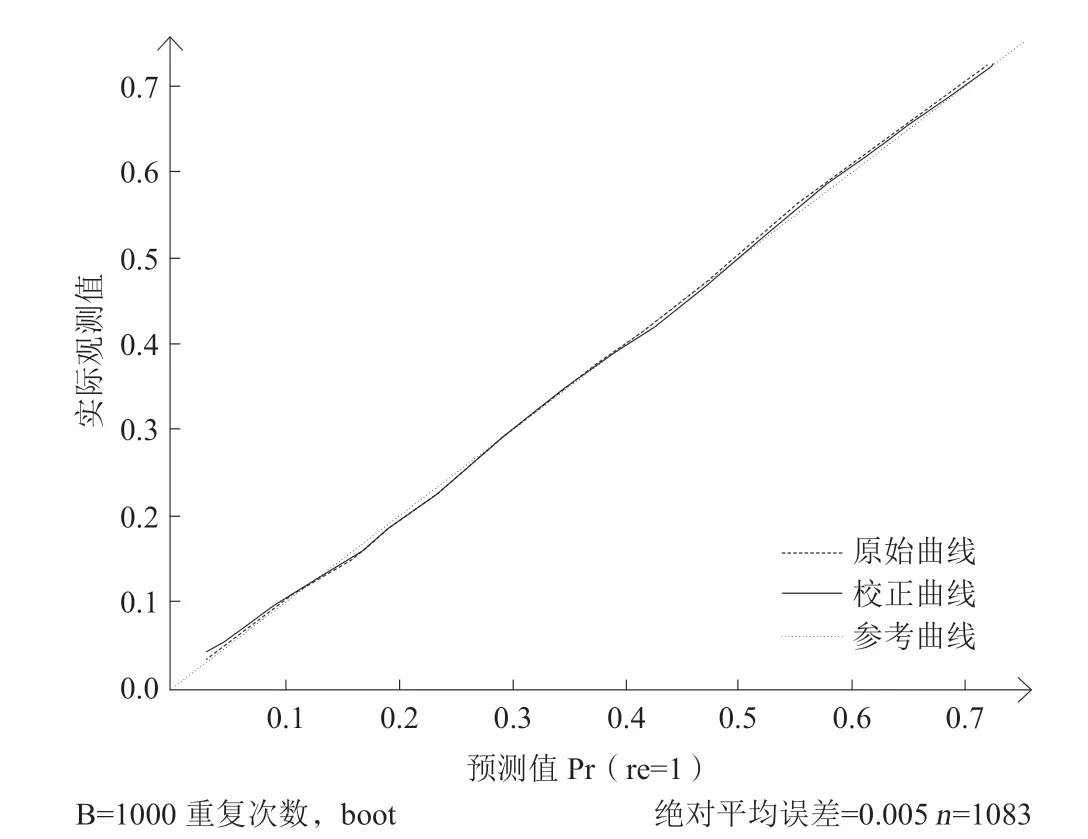
图 3 预测模型校准曲线(重复抽样Bootstarp法,B=1000)
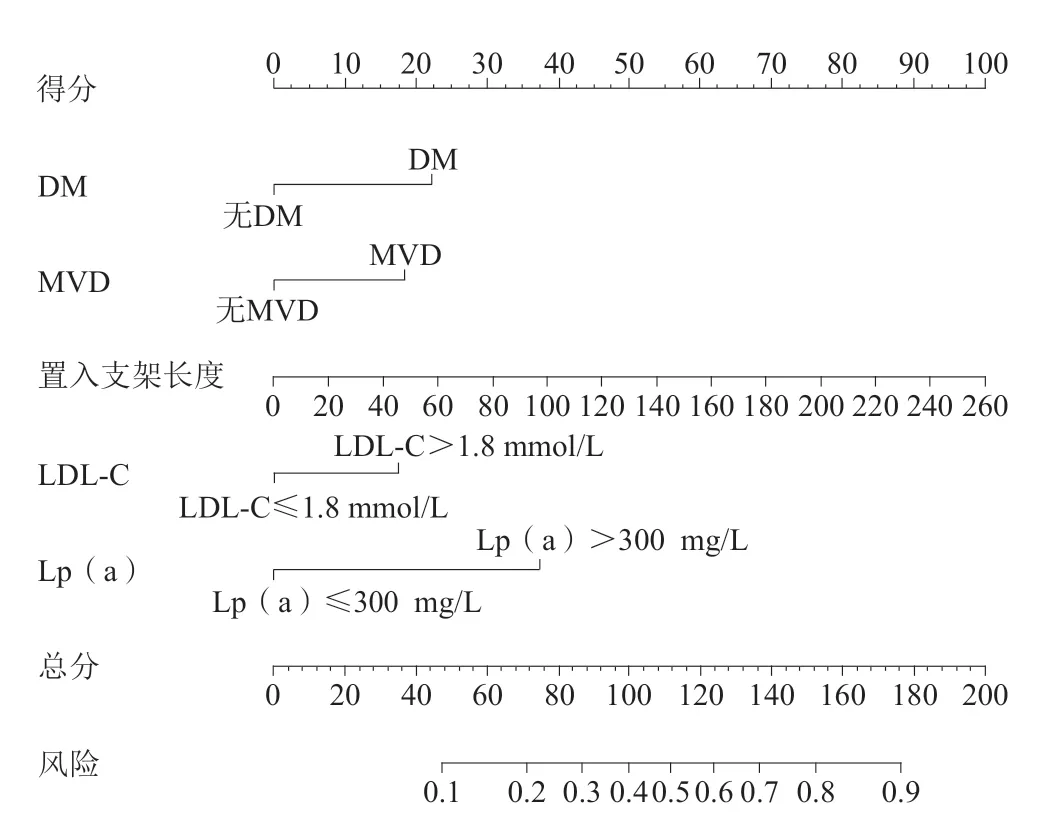
图 4 冠心病患者PCI术后因严重ISR导致再次血运重建的临床预测模型列线图
冠心病的患病率及死亡率逐年攀升,其高致死率、致残率严重影响了患者的生活质量。PCI术的发展和普及改善了冠心病患者的预后,目前广泛应用于临床。但在目前临床实践中,由于PCI术后存在ISR等问题,再次血运重建仍然常见。虽然第二代药物洗脱支架的使用进一步降低了支架的再狭窄率,但有研究报道,冠心病患者PCI术后再狭窄发生率仍高达10%[3]。再次血运重建目前仍然是PCI面临的主要临床挑战[2]。因此,预测严重ISR导致的再次血运重建、筛选出高危患者具有重要的临床意义和指导意义。本研究冠心病患者PCI术后ISR的发生率为19.3%,高于平均水平,可能与徐州地区高盐高脂饮食有关。
本研究通过回顾性分析发现, Lp(a)>300 mg/L及LDL-C>1.8 mmol/L、糖尿病病史、MVD、支架置入长度是冠心病患者PCI术后因严重ISR导致再次血运重建的独立危险因素,这与国内外多位学者研究结果[4-6]相似,同时也验证了本研究结果的可靠性。LDL-C的重要性不言而喻,大量研究证实,血脂异常,尤其是LDL-C升高是导致冠状动脉粥样硬化性心血管病(arteriosclerotic cardiovascular disease,ASCVD)发生、发展的关键因素,建议将LDL-C作为血脂控制的首要目标。根据我国《血脂异常基层诊疗指南(2019年)》[7],对于极高危的ASCVD患者,建议将LDL-C控制在1.8 mmol/L以下,并施行积极的生活干预。而Lp(a)与LDL-C在脂质成分上十分相似,Lp(a)的载脂蛋白部分由一分子载脂蛋白B100和一分子载脂蛋白A共同组成。Lp(a)经氧化修饰后,在清道夫受体及吞噬作用下,可被单核巨噬细胞大量摄取和降解,形成大量泡沫细胞,从而引发一系列的动脉粥样硬化过程。而且Lp(a)在结构上与纤溶酶原相似,可与纤溶酶原激活剂竞争,使纤溶功能降低,引起凝血功能亢进,这会使动脉粥样硬化斑块表面形成血栓的概率增大,从而加速动脉粥样硬化病变的发展[8]。《中国成人血脂异常防治指南(2016年修订版)》[9]也指出,通常以300 mg/L作为切点,极高的Lp(a)可能代表一种新的遗传性脂质紊乱,与极高的ASCVD终身风险相关。Arnold等[10]研究发现,多支病变是PCI术后再次血运重建的强独立预测因子。在我国汉族人群中,多支病变依然是冠状动脉粥样硬化病情进展的独立预测因子[11]。目前虽然MVD已被广泛研究,但是它导致疾病预后恶化的直接机制仍不清楚。MVD患者的心血管危险因素更多,合并症发生率更高,左心室功能更差,心肌梗死前缺血率更高,所有这些都可能导致预后不佳。置入支架总长度越长,意味着更容易出现贴壁不良,更容易损伤血管内膜,并且内膜损伤的面积更大,释放的炎性因子更多[12];且出现血管内膜撕裂或者夹层的风险越大,导致血小板黏附、凝聚,平滑肌细胞向内膜迁移、增殖,更容易引起ISR[13]。糖尿病患者由于血糖的高渗透作用,损伤血管内皮导致炎性反应,从而引起凝血因子的生成破坏失衡,导致ISR形成。我国指南还推荐将高危患者的HbA1c控制在7%以下[14]。但Cassese等[4]还认为,小血管病变也是ISR的强独立危险因子。分析二者差异的原因,Cassese等[4]试验中以最小支架直径进行分析,而本研究中采用的是支架直径中位数间接评估病变血管直径,这可能是造成差异的主要原因。
目前还有研究认为,女性、吸烟等因素也是再次血运重建的独立危险因素[15]。该研究认为,吸烟会导致血管舒张功能受损,促进炎症因子的释放,还参与脂质修饰,从而导致冠状动脉粥样硬化进展。而绝经后的女性失去了雌激素的“保护作用”,因此增加了罹患冠心病的风险。但本研究并未得出相似的结果。分析其原因,可能与以下几点有关:本研究入组患者中男性占比65%,明显高于女性,可能存在偏倚,而吸烟者约98%为男性,可能使得性别这一危险因素并不突出。
传统的预测方法大多集中于危险因素的分析及公式预测,但是这些方法并不直观,而且公式冗长,计算繁琐,并不适于推广。近年来,列线图备受研究者们青睐,它可以通过合并每个危险因素的加权贡献来预测单个患者的结果,已被广泛用于预测疾病的发生及生存率,尤其在肿瘤学领域。列线图在多因素回归的基础上,将复杂的回归方程转变为了简单且可视化的线段,使预测模型的结果更形象直观,具有可读性,且方便使用,具有更高的实用价值[16]。目前,关于PCI术后严重ISR导致再次血运重建很少有适用的临床模型。本研究通过对PCI术后严重ISR导致再次血运重建的多因素回归分析,筛选出5个独立危险因素:Lp(a)>300 mg/L、LDL-C>1.8 mmol/L、糖尿病病史、MVD、支架置入长度,并建立简易的列线图模型,最后对模型进行验证:曲线下面积为0.766,标准误为0.0184,95%CI为0.740~0.791,区分度较好。通过Hosmer-Lemeshow拟合优度检验来评价预测模型的适配度,结果提示模型适配度较好。采用Bootstarp内部验证法并绘制校准曲线,提示模型符合度良好。
本研究的局限性:对患者手术情况收集时,并没有对患者分叉病变、CTO病变的类型及术式进行详细分析;收集患者既往病史时,主要依靠电子病历系统,并未对患者进行诊断性实验,结果可能存在偏差;单中心、回顾性研究,可能存在偏倚。本研究结果尚需其他中心的数据或者前瞻性随机对照试验来进行验证。
综上所述,本模型可以筛选出PCI术后严重ISR导致再次血运重建的高危患者,具有一定的临床使用价值。
