2-苯基环己硫醇在γ-Al2O3和SiO2负载的MoS2催化剂上的脱硫反应
2021-05-20周学荣王安杰刘盛男
王 琳, 周学荣, 李 翔, 王安杰, 刘盛男
(1.大连理工大学 精细化工国家重点实验室, 辽宁 大连 116024;2.天津科技大学 化工与材料学院,天津 300457;3.辽宁省高校石油化工技术与装备重点实验室,辽宁 大连 116024)
过渡金属硫化物是目前工业上主要的加氢脱硫(HDS)催化剂[1-3],主活性组分为MoS2和WS2[4-5]。二苯并噻吩类含硫化合物是燃料油中最难通过加氢脱硫脱除的含硫化合物[6-10]。为了开发高性能HDS催化剂,达到深度脱硫的目的,需要掌握二苯并噻吩类芳香杂环含硫化合物的HDS反应机理和反应过程。但是这些含硫化合物反应网络复杂[11-12],只从二苯并噻吩类含硫化合物出发难以认清反应机理和催化剂构效关系。笔者所在课题组在前序工作中合成了2-苯基环己硫醇(2-PCHT),研究了其在临氢和非临氢条件下于γ-Al2O3和SiO2作载体的WS2催化剂上的脱硫反应[13],发现2-PCHT是一种良好的模型含硫化合物。这为系统研究含硫化合物中C-S键断裂方式,深入认识催化剂反应特性提供了新的可能。MoS2是工业HDS催化剂的主要活性组分[14-15],比WS2更为常用。因此笔者以2-PCHT作为模型含硫化合物,分别研究了其在临氢和非临氢条件下在负载型MoS2/Al2O3和MoS2/SiO2催化剂上的脱硫反应,探讨了环烷基C-S键在MoS2催化剂上的断裂方式及载体对MoS2催化剂性能的影响,并对比了MoS2和WS22种主要加氢脱硫催化剂的特性。
1 实验部分
1.1 原料和试剂
1-苯基环己烯(1-PCHE),阿拉丁化学试剂公司产品;硫代乙酸(CH3COSH)、无水乙醇(C2H5OH)、氢氧化钾(KOH)、乙酸(CH3COOH)、石油醚、硅胶(200~300目)、十氢萘、石英砂(20~40目)、哌啶、乙酸乙酯(CH3COOCH2CH3)、碳酸氢钠(NaHCO3)、氯化钠(NaCl)、无水硫酸镁(MgSO4)、四水合钼酸铵((NH4)6Mo7O24·4H2O)、苯并噻吩(BT),均为分析纯,国药集团化学试剂有限公司产品;载体为γ-Al2O3(中国石化大连石油化工研究院产品)和白炭黑(沈阳化工股份有限公司产品);H2(体积分数99.99%)、Ar(体积分数99.99%)、10%(体积分数) H2S/H2,中国科学院大连化学物理研究所提供。
1.2 催化剂前体的制备
采用等体积浸渍方法[16]制备催化剂前体。称取3.0 g的γ-Al2O3和白炭黑。根据载体孔体积(γ-Al2O3为0.6 mL/g,白炭黑为2.3 mL/g),称取0.3 g四水合钼酸铵((NH4)6Mo7O24·4H2O)和相应体积去离子水配成浸渍液,逐滴缓慢滴加至载体中并搅拌均匀。室温静置4 h,120 ℃烘干12 h,500 ℃焙烧4 h后得到氧化物前体,其中MoO3负载质量分数为8.0%。
1.3 脱硫反应
参照文献[13]合成2-PCHT。其脱硫反应在内径为8 mm的不锈钢固定床反应器中进行。氧化态前体经压片、粉碎、筛分至20~40目,用量为0.1 g。反应前,在1.0 MPa下用H2S体积分数为10%的H2S/H2气体对催化剂进行预硫化。硫化完成后降温至240 ℃,在总压5.0 MPa、气/液体积比800、反应气体为H2或Ar的条件下进行反应。前期研究工作[17-18]表明,当气/液体积比大于600、催化剂的颗粒粒径小于16目(1.18 mm)时,可排除外扩散和内扩散对反应的影响。合成反应条件满足上述要求,故均已排除传质对反应的影响。反应原料是2-PCHT质量分数为1.25%的十氢萘溶液。当考察含氮化合物对脱硫反应的影响时,在上述原料中加入质量分数为0.07%的哌啶。按照催化剂装填质量计算停留时间τ(g·min/mol),τ为催化剂质量/单位时间内流过催化剂床层总摩尔流量,其中气/液体积比保持不变。采用美国安捷伦公司生产的Agilent-6890 N气相色谱仪和HP-INNOWax聚乙二醇极性色谱柱对液相脱硫反应产物进行离线分析,测得反应体系中各组分的质量浓度。反应物和可能检测到的产物结构及缩写列于表1。

表1 反应物和产物的结构及缩写Table 1 Structures and acronyms of reactant and products
利用归一化法,以反应物及产物的实际摩尔浓度为基准,用摩尔分数表述各组分含量的变化。反应体系中各组分的摩尔分数(xi)和产物选择性(si)按照式(1)和式(2)计算。
(1)
(2)
式中:C2-PCHT为反应器出口反应物的摩尔浓度,mol/mL;Ci表示反应器出口组分i的摩尔浓度,mol/mL,其中i代表1-PCHE、3-PCHE、4-PCHE、CHB、BP、TH-DBT、HH-DBT、CPEMB、CPMB、2-PCHT,Ci的摩尔浓度按式(3)计算。
Ci=ρi/Mi
(3)
式中:ρi为反应器出口组分i的质量浓度,g/mL;Mi表示反应器出口各组分的摩尔质量,g/mol。
2-PCHT的转化率按照式(4)计算。
X2-PCHT=100%-x2-PCHT
(4)
式中:X2-PCHT为反应物2-PCHT的转化率,%;x2-PCHT表示反应器出口反应物的摩尔分数,%。
1.4 催化剂的表征
采用日本理学Rigaku D/MAX-2400型X-射线衍射(XRD)仪测定催化剂的晶相,CuKα辐射源,Ni滤波,管电压40 kV,电流100 mA。采用Micromeritics Instrument Corporation公司生产的TristarⅡ3020分析仪测定催化剂的N2吸附-脱附等温曲线,并通过Brunauer-Emmett-Teller(BET)法计算催化剂的比表面积,用BJH法计算脱附分支数据,得到载体负载氧化物前后的孔径分布。测定前,样品首先在120 ℃下真空脱气处理4 h。采用美国康塔公司生产的Chembet-3000型分析仪测得催化剂的H2-TPR谱图。采用美国FEI公司生产的JEM-100CX Ⅱ型透射电子显微镜(TEM)表征催化剂颗粒形貌及晶格参数,加速电压为180 kV。
2 结果与讨论
2.1 催化剂的物性表征
2.1.1 XRD表征
图1为催化剂前体MoO3/Al2O3与MoO3/SiO2的XRD谱图。图1中没有观察到钼氧化物的衍射峰。在MoO3/Al2O3的谱图中,2θ为37.6°、45.8°和66.8° 处的衍射峰分别对应γ-Al2O3的(311)、(400)和(440)晶面(PDF#29-0063)[19-20]。在MoO3/SiO2的谱图中,23° 左右的宽峰为无定形SiO2的特征峰[21-22]。以上结果说明MoO3高度分散在载体γ-Al2O3和SiO2中。这与WO3不同,在WO3/SiO2的XRD谱图中观察到了WO3的特征衍射峰[13]。可能的原因是WO3与SiO2相互作用较弱,在SiO2载体中发生了团聚。
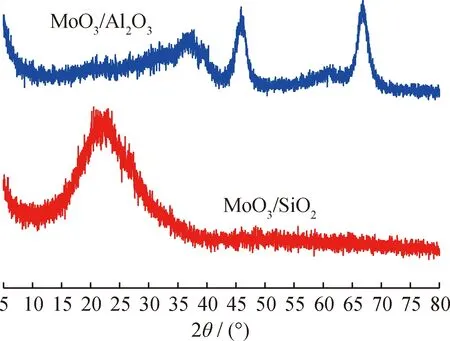
图1 MoO3/Al2O3和MoO3/SiO2的XRD谱图Fig.1 XRD patterns of MoO3/Al2O3 and MoO3/SiO2
2.1.2 H2-TPR表征
为了研究MoO3与载体的相互作用,对催化剂前体开展了TPR测试,结果示于图2。由图2看到:MoO3/Al2O3与MoO3/SiO2出现2个主要的氢耗峰,低温氢耗峰峰值在460 ℃左右,归属于八面体配位的Mo6+向Mo4+的转变[23-24];700 ℃以上高温氢耗峰可归属于四面体配位的Mo物种的还原[25-26]。MoO3/Al2O3和MoO3/SiO2二者低温氢耗峰温度接近,MoO3/Al2O3的高温氢耗峰比 MoO3/SiO2的高了100 ℃左右。说明MoO3与γ-Al2O3相互作用更强,更难被还原。
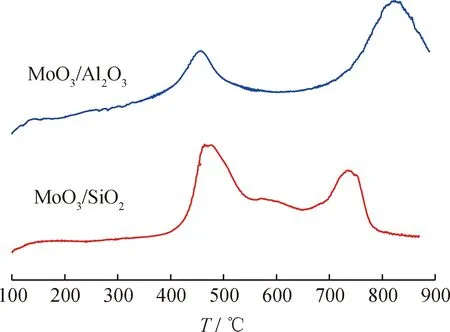
图2 MoO3/Al2O3和MoO3/SiO2的H2-TPR谱图Fig.2 H2-TPR profiles of MoO3/Al2O3 and MoO3/SiO2
2.1.3 N2物理吸附表征
表2列出了载体和催化剂前体的比表面积和孔结构参数。由表2可见,SiO2的比表面积、孔体积和平均孔径均大于γ-Al2O3。负载活性组分后,γ-Al2O3比表面积、孔体积和平均孔径均下降,这可能是由于活性组分进入γ-Al2O3载体的孔道所致。负载MoO3后SiO2比表面积下降幅度大于γ-Al2O3,MoO3/SiO2的比表面积小于MoO3/Al2O3;MoO3/SiO2的孔体积和平均孔径均增加,且均大于MoO3/Al2O3。图3示出了载体及其负载氧化物前后的孔径分布图。由图3可见,γ-Al2O3负载前后孔分布曲线基本相似,孔径主要分布在8~11 nm。SiO2负载前孔径主要分布在17~23 nm,负载后平均孔径增大,主要分布在19~27 nm。
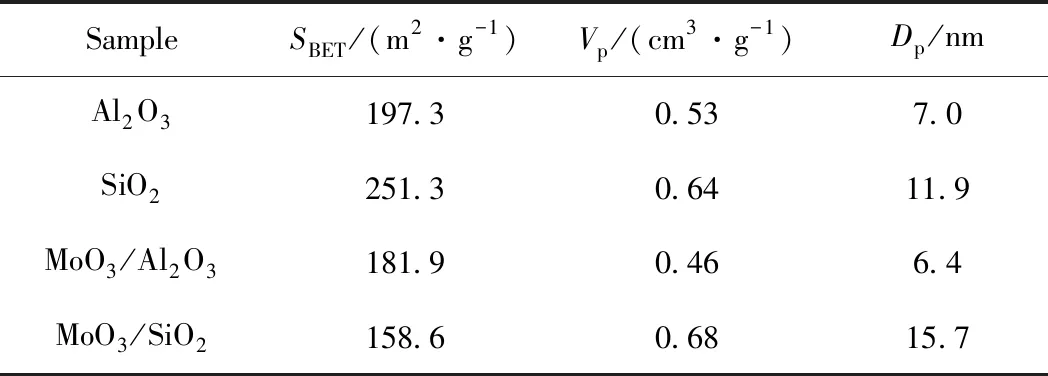
表2 Al2O3和SiO2载体及其负载MoO3前后的比表面积和孔结构参数Table 2 Surface areas and pore parameters of Al2O3,MoO3/Al2O3, SiO2 and MoO3/SiO2
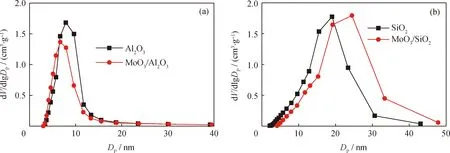
图3 Al2O3和SiO2载体及其负载MoO3前后的孔径分布图Fig.3 Pore size distribution of Al2O3, MoO3/Al2O3, SiO2 and MoO3/SiO2(a) Al2O3 and MoO3/Al2O3; (b) SiO2 and MoO3/SiO2
2.1.4 TEM表征
MoS2/Al2O3和MoS2/SiO2催化剂的TEM照片示于图4。图4中晶面间距为0.22 nm归属于MoS2(103)晶面的条纹,表明硫化后2种催化剂的氧化态前体转化为硫化态的活性相。MoS2均匀地分散在载体表面,没有发现较大MoS2晶粒的聚集。根据文献[27]报道方法,统计分析了MoS2的2个结构参数:平均片晶长度(L)和平均堆叠层数(N)。MoS2/Al2O3中MoS2的平均片晶长度L为2.7 nm,平均堆叠层数N为1.44,MoS2/SiO2中其值分别为3.1 nm和1.48。对于硫化物而言,载体与硫化物前体的相互作用较弱,有利于高堆叠层数的出现[28],片晶的长度越小,暴露的原子率越高[29]。MoS2/SiO2的堆叠层数和片晶长度均比MoS2/Al2O3的高,进一步证实MoO3与SiO2之间相互作用比MoO3与γ-Al2O3之间的弱,MoO3在γ-Al2O3上的分散度更好,暴露的原子率高,活性位点可能更多。

图4 MoS2/Al2O3和MoS2/SiO2的TEM照片Fig.4 TEM images of MoS2/Al2O3 and MoS2/SiO2(a) MoS2/Al2O3; (b) MoS2/SiO2
2.2 临氢条件下2-PCHT的脱硫反应
图5为临氢条件下原料中有无哌啶时2-PCHT在MoS2/Al2O3上脱硫反应的反应物和产物摩尔分数及产物选择性随停留时间的变化。图5结果显示,2-PCHT 在MoS2/Al2O3上表现出较高的活性。由图5(a)和(b)可见:无哌啶添加时,在τ=0.8 g·min/mol 时,2-PCHT转化率达89.5%;主要脱硫产物摩尔分数由高到低顺序依次是CHB、3-PCHE、4-PCHE、1-PCHE。CHB的选择性从低停留时间(τ=0.2 g·min/mol)的62.0%增加到高停留时间(τ=0.8 g·min/mol)的71.0%,并具有非零的初始选择性,说明CHB是反应的直接产物也是最终产物。3-PCHE和1-PCHE都表现出反应中间体的特征,其摩尔分数分别在停留时间为0.56 g·min/mol 和0.19 g·min/mol时达到最大值,并且选择性均随停留时间增加而降低;二者都表现出非零的初始选择性,表明它们都是2-PCHT反应的直接产物。4-PCHE的摩尔分数和选择性都随停留时间的增加而增加。此外,还检测到痕量的CPMB、BP和CPEMB。
由图5(c)和(d)可见,哌啶抑制了2-PCHT在MoS2/Al2O3上的加氢脱硫反应。在τ=0.8 g·min/mol时,2-PCHT的转化率为79.9%。产物中只检测到了CHB、3-PCHE、1-PCHE以及痕量的BP和4-PCHE 5种脱硫产物,产物分布与不添加哌啶的情况相同。CHB摩尔分数仍然最高并且几乎不受添加哌啶的影响,其他产物的摩尔分数在添加哌啶后明显降低。因此,与不添加哌啶的情况相比,添加哌啶后CHB选择性显著增加,哌啶完全抑制了CPMB和CPEMB的生成。
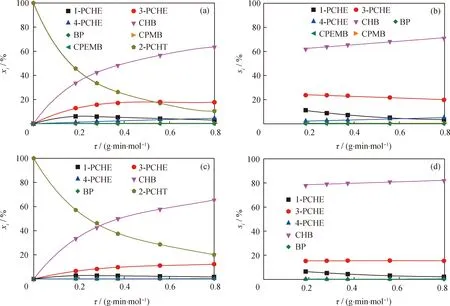
图5 临氢条件下原料中有无哌啶时2-PCHT在MoS2/Al2O3上脱硫反应的反应物和产物摩尔分数及产物选择性随停留时间的变化Fig.5 Mole fractions of the reactant and products as well as the product selectivities in the desulfurization of 2-PCHT over MoS2/Al2O3 in the absence or presence of piperidine as a function of space time(a), (b) w(Piperidine)=0; (c), (d) w(Piperidine)=0.07%T=240 ℃; p(H2)=5.0 MPa; m(Cat)=0.1 g; V(H2)/V(2-PCHT)=800
图6为临氢条件下原料中有无哌啶时2-PCHT在MoS2/SiO2上脱硫反应的反应物和产物摩尔分数及产物选择性随停留时间的变化。与图5中的相同条件下比较,图6中2-PCHT在MoS2/SiO2上的转化率略低于MoS2/Al2O3。由图6(a)和(c)可见:添加哌啶后,τ=0.8 g·min/mol时,2-PCHT 在MoS2/SiO2上的最大转化率由未添加哌啶时的82.9%降为73.0%,降低9.9百分点;而在MoS2/Al2O3上,与未添加哌啶时相比,添加哌啶后2-PCHT的最大转化率降低9.6百分点(图5)。说明哌啶对2-PCHT在MoS2/SiO2上加氢脱硫反应的抑制作用与在MoS2/Al2O3上的相当。同时,2-PCHT 在MoS2/SiO2上(图6)的产物分布与MoS2/Al2O3上(图5)相似。相同条件下,在MoS2/SiO2上CHB的摩尔分数比在MoS2/Al2O3上的低,但1-PCHE和3-PCHE的摩尔分数略高。因此与MoS2/Al2O3上相比(图5(b)和图5(d)),MoS2/SiO2上CHB的选择性降低而1-PCHE和3-PCHE的选择性增加(图6(b)和图6(d))。由图6还看到:哌啶的加入促进了CHB的生成,但抑制了其他产物的生成;在τ=0.8 g·min/mol时,CHB的摩尔分数比未添加哌啶时增加了4.1百分点。
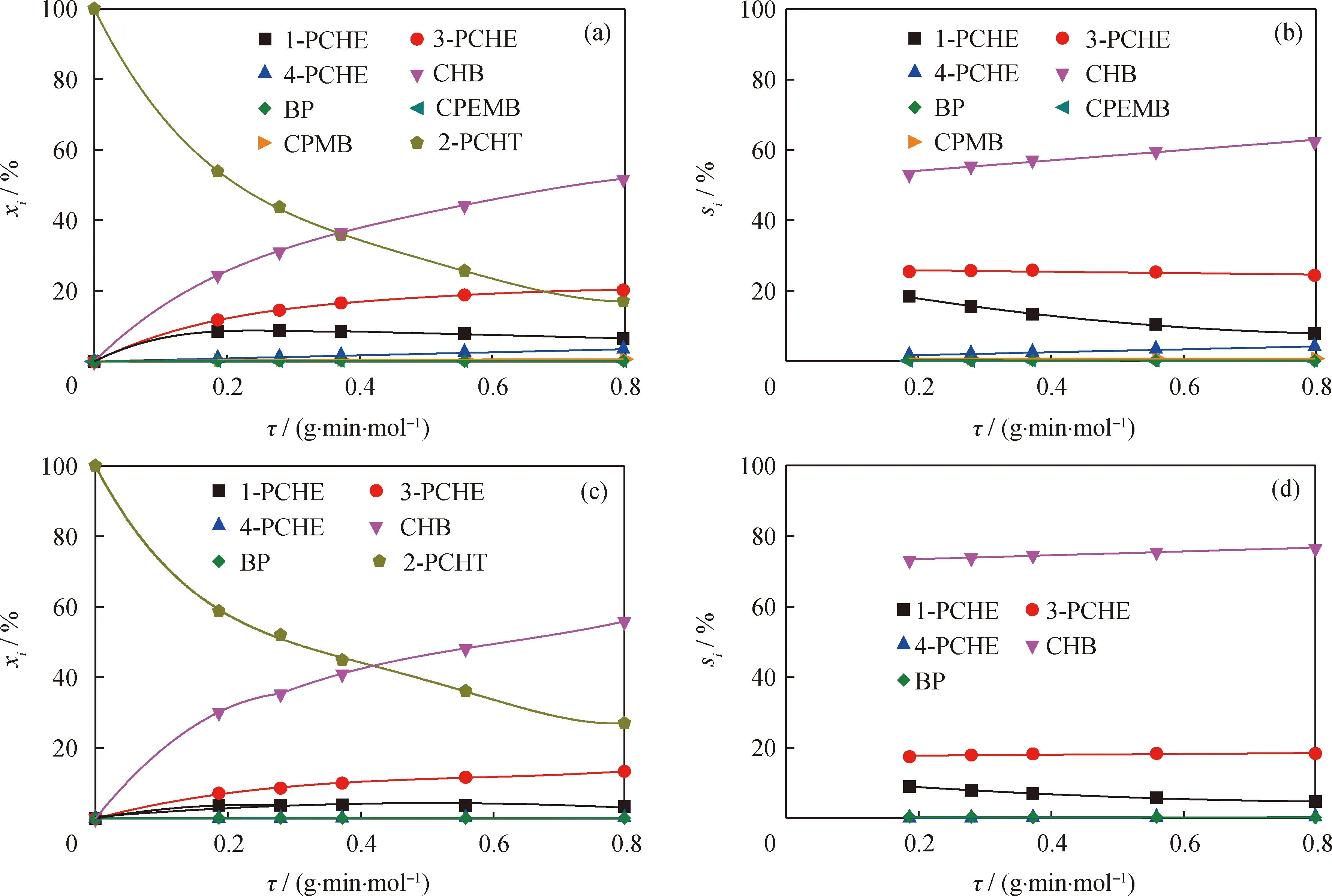
图6 临氢条件下原料中有无哌啶时2-PCHT在MoS2/SiO2上脱硫反应的反应物和产物摩尔分数及产物选择性随停留时间的变化Fig.6 Mole fractions of the reactant and products as well as the product selectivities in the desulfurization of 2-PCHT over MoS2/SiO2 in the absence or presence of piperidine as a function of space time(a), (b) w(Piperidine)=0; (c), (d) w(Piperidine)=0.07% T=240 ℃; p(H2)=5.0 MPa; m(Cat)=0.1 g; V(H2)/V(2-PCHT)=800
2.3 非临氢条件下2-PCHT的脱硫反应
图7为非临氢以及原料中有无哌啶条件下2-PCHT 在MoS2/Al2O3上脱硫反应的反应物和产物摩尔分数及产物选择性随停留时间的变化。由图7 看到,在MoS2/Al2O3催化剂上,2-PCHT在非临氢条件下转化率显著低于相同条件下临氢时的转化率。由图7(a)和(b)看到,在Ar气氛下,τ=0.8 g·min/mol、未添加哌啶时,2-PCHT在MoS2/Al2O3上的转化率仅为24.3%,主要产物摩尔分数从高到低的顺序依次为1-PCHE、3-PCHE、BP、CHB、TH-DBT。它们的初始选择性均不为零,表现出直接产物的特征,且选择性均不随停留时间变化而变化,说明它们的进一步反应可能很慢;苯基环己烯和BP是主要产物;1-PCHE和3-PCHE总选择性大于60%;BP选择性随停留时间增加由21.5%降至15.7%。添加哌啶显著抑制了2-PCHT的活性以及苯基环己烯和BP的生成,但基本没有影响CHB的摩尔分数。在较低的停留时间下,CHB的摩尔分数仅低于1-PCHE,其摩尔分数和选择性都随停留时间的增加而增加,并且在τ=0.8 g·min/mol 时,摩尔分数和选择性都大于1-PCHE;1-PCHE的摩尔分数大于3-PCHE,1-PCHE 和3-PCHE的总选择性降至50%左右;BP选择性则比未添加哌啶时降低了约3百分点。另外,添加哌啶还完全抑制了4-PCHE和CPEMB的生成。
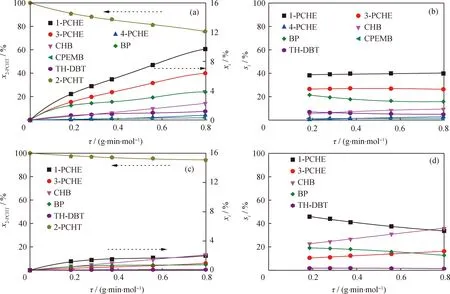
图7 非临氢以及原料中有无哌啶条件下2-PCHT在MoS2/Al2O3上脱硫反应的反应物和产物摩尔分数及产物选择性随停留时间的变化Fig.7 Mole fractions of the reactant and products as well as the product selectivities in the desulfurization of 2-PCHT overMoS2/Al2O3 in the absence or presence of piperidine as a function of space time(a), (b) w(Piperidine)=0; (c), (d) w(Piperidine)=0.07% T=240 ℃; p(Ar)=5.0 MPa; m(Cat)=0.1 g; V(Ar)/V(2-PCHT)=800
图8为非临氢以及原料中有无哌啶条件下2-PCHT 在MoS2/SiO2上脱硫反应的反应物和产物摩尔分数及产物选择性随停留时间的变化。由图8可知,非临氢条件下,2-PCHT在MoS2/SiO2上的转化率不仅低于MoS2/Al2O3,且在2种催化剂上的产物分布也有明显区别。1-PCHE仍是摩尔分数最高的脱硫产物。但与MoS2/Al2O3上不同的是,未添加哌啶时,在MoS2/SiO2上BP的摩尔分数和选择性都高于3-PCHE(图8(a)和图8(b))。由图8(c)和(d)看到,添加哌啶后,除CHB的摩尔分数基本不变,其他产物的摩尔分数均有不同程度的降低,因此CHB的选择性比未加哌啶时明显增加,1-PCHE的选择性略有增加,而3-PCHE、BP、TH-DBT的选择性明显降低。
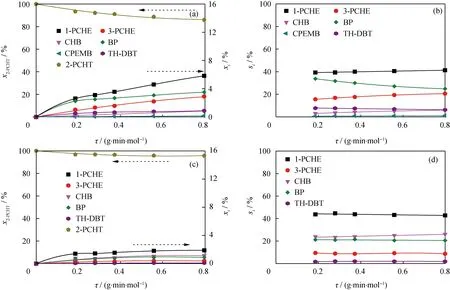
图8 非临氢以及原料中有无哌啶条件下2-PCHT在MoS2/SiO2上脱硫反应的反应物和产物摩尔分数及产物选择性随停留时间的变化Fig.8 Mole fractions of the reactant and products as well as the product selectivities in the desulfurization of 2-PCHT over MoS2/SiO2 in the absence or presence of piperidine as a function of space time(a), (b) w(Piperidine)=0; (c), (d) w(Piperidine)=0.07% T=240 ℃; p(Ar)=5.0 MPa; m(Cat)=0.1 g;V(Ar)/V(2-PCHT)=800
2.4 2-PCHT的反应途径
在前序工作中发现[13]:在WS2催化剂上,2-PCHT 在临氢条件下产物可分为3类,即CHB、苯基环己烯和BP,分别是氢解、β消除和脱氢脱硫的产物;而在非临氢条件下,CHB、苯基环己烯和BP及少量的TH-DBT则可能是C-S键均裂或氢解、β消除和脱氢脱硫的产物。类似地,在MoS2催化剂上,CHB、苯基环己烯和BP以及少量的 TH-DBT 在脱硫过程中无论在临氢还是非临氢条件下,均有非零的初始选择性,都表现出直接产物的特征。非临氢条件下,未添加哌啶时,BP在MoS2/Al2O3和MoS2/SiO2上的摩尔分数显著高于CHB,说明BP不是苯基环己烯的歧化反应产物,否则CHB与BP的摩尔分数比值应该在2左右[30]。因此,2-PCHT在MoS2催化剂上的反应网络与WS2催化剂上的类似[13]。
但是在MoS2催化剂上,临氢和非临氢条件下β消除反应路径的产物分布有明显区别。2-PCHT可以通过与C2相连的β氢发生消除反应生成1-PCHE(β1路径),也可以通过与C6相连的β氢发生消除反应生成3-PCHE(β2路径)[31](见图9)。1-PCHE中双键与芳环存在共轭效应,因此比3-PCHE更稳定;但是C2还连结着较大的芳基,空间位阻较大。由此可见,有多个因素能够影响β消除反应路径。临氢条件下,在MoS2/Al2O3和MoS2/SiO2催化剂上3-PCHE 的摩尔分数大于1-PCHE;而在非临氢条件下,1-PCHE则为β消除反应的主要产物。虽然笔者研究结果还不能揭示造成β消除反应路径差别的原因,但是可以推测在临氢和非临氢条件下,MoS2的β消除活性中心或反应过程可能不同。
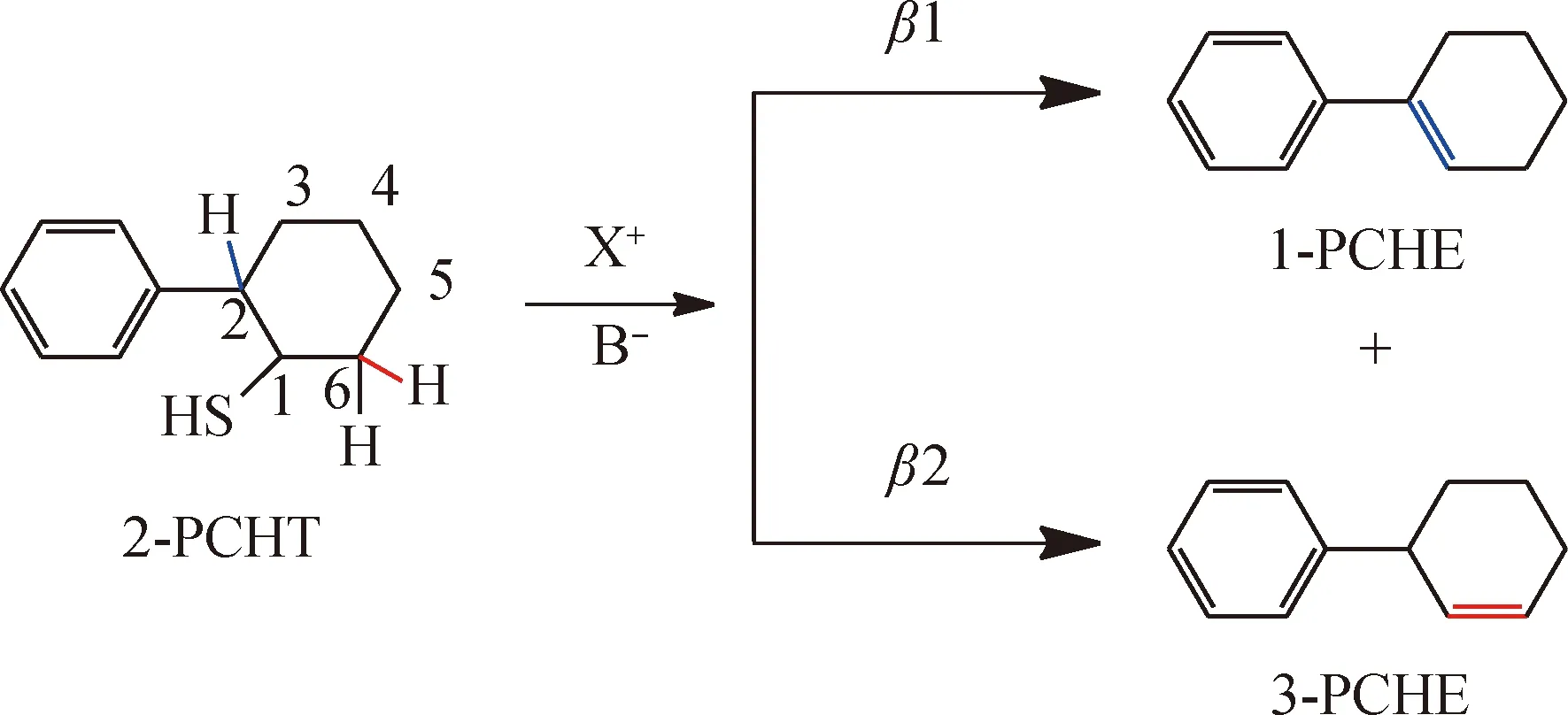
β 1—β-elimination pathway to form 1-PCHE;β 2—β-elimination pathway to form 3-PCHE;X+—Acid sites or vacancies; B-—Basic sites图9 2-PCHT在MoS2催化剂上的β消除示意图Fig.9 Diagram of the β-elimination reactions of 2-PCHT on MoS2 catalyst
2.5 载体和哌啶对2-PCHT脱硫反应的影响
在临氢、无哌啶条件下,2-PCHT在MoS2/Al2O3和MoS2/SiO2上主要产物为苯基环己烯与CHB(图5(a)和图6(a))。CHB选择性在53%~71%之间(图5(b)和图6(b)),苯基环己烯的总选择性分别为28%~37%和36%~46%(图5(b)和图6(b)),说明临氢条件下在MoS2催化剂上2-PCHT主要通过β消除、氢解路径脱硫,并且氢解的反应速率快于β消除,脱氢路径占的比重很小。临氢条件下MoS2/Al2O3的催化活性略高于MoS2/SiO2。从产物分布看,MoS2/Al2O3上CHB摩尔分数高于MoS2/SiO2,但苯基环己烯摩尔分数差别不大,说明MoS2/Al2O3的氢解反应活性高于MoS2/SiO2,但二者β消除活性相当。非临氢、无哌啶条件下,2-PCHT在MoS2/Al2O3和MoS2/SiO2上主要通过β消除和脱氢2条路径脱硫。苯基环己烯的总选择性分别为65%~69%和55%~62%,BP选择性小于34%(图7(b)和图8(b)),说明β消除是主要的反应路径。产物中BP及TH-DBT的摩尔分数在2种催化剂上基本一致(图7(a)和图8(a)),表明载体对MoS2催化剂脱氢活性基本没有影响。可见,非临氢、无哌啶条件下,MoS2/Al2O3的反应活性高于MoS2/SiO2,主要在于其较高的β消除活性。针对汽油中噻吩类小分子含硫模型化合物的研究数据表明,MoS2片层长度越小,HDS活性越高[32]。从2.1节表征结果来看,MoS2/Al2O3相对于MoS2/SiO2,比表面积大、分散度好、片晶长度短、暴露的表面活性位点多,因而更有利于2-PCHT的吸附和活化,这可能也是MoS2/Al2O3的反应活性优于MoS2/SiO2的原因。
在临氢、添加哌啶条件下,哌啶主要抑制了β消除反应路径,但是对氢解反应路径基本没有影响。在MoS2/Al2O3和MoS2/SiO2上引入哌啶后,苯基环己烯的总选择性降至20%左右(图5(d)和图6(d))。在非临氢条件下,哌啶对2-PCHT在MoS2/Al2O3催化剂上β消除反应路径表现出更强的抑制作用。加入哌啶后,苯基环己烯的总选择性在MoS2/Al2O3上下降幅度比MoS2/SiO2更明显(图7(d)和图8(d))。此外,哌啶还强烈抑制了脱氢脱硫反应路径,并且对2-PCHT在MoS2/SiO2催化剂上脱氢反应路径表现出更强的抑制作用。加入哌啶后,BP在MoS2/SiO2上的选择性下降比 MoS2/Al2O3上明显(图7(d)和图8(d))。哌啶对2种催化剂上C-S键的均裂几乎没有影响。在加入哌啶的情况下,CHB取代3-PCHE或BP,在产物中摩尔分数仅次于1-PCHE。强碱性哌啶比 2-PCHT 可能更容易吸附于MoS2/Al2O3和 MoS2/SiO2表面的酸性活性中心和硫空位,而在氢解活性中心的吸附相对较弱[33],因此哌啶对β消除、脱氢路径的抑制作用强于其对氢解路径的抑制作用。
2.6 WS2与MoS2催化剂对2-PCHT脱硫性能比较
在临氢条件下,苯基环己烯在MoS2/Al2O3和MoS2/SiO2上都表现出明显的中间产物的特征。1-PCHE 和3-PCHE的摩尔分数随停留时间变化出现极值,并且选择性随停留时间增加而降低(图5和图6)。因此笔者考察了1-PCHE的加氢反应。在含硫化合物(苯并噻吩质量分数0.3%)存在条件下,1-PCHE 在MoS2/Al2O3和MoS2/SiO2上都发生了加氢反应,转化率几乎为100%,主要产物为CHB。而在相同条件下,1-PCHE在WS2/Al2O3和WS2/SiO2上加氢转化率分别为87%和42%[13]。可以看出,MoS2催化剂的加氢活性高于WS2催化剂。另外,图10为临氢或非临氢条件下2-PCHT在MoS2和WS2上转化率与停留时间的关系。由图10可见,无论在临氢还是非临氢条件下,MoS2催化剂对2-PCHT的脱硫活性都高于WS2催化剂。2-PCHT 在MoS2/Al2O3和MoS2/SiO2上转化率显著高于WS2/Al2O3和WS2/SiO2,并且以γ-Al2O3为载体负载的MoS2和WS2催化剂的脱硫活性均优于以SiO2为载体的催化剂。从产物分布看,临氢条件下,MoS2催化剂的氢解和β消除反应活性均大于WS2。但是在MoS2催化剂上氢解快于β消除,而在WS2催化剂上β消除比氢解快。与SiO2载体相比,采用γ-Al2O3作载体更有利于 2-PCHT 的氢解反应,但WS2/Al2O3和 WS2/SiO2催化剂上β消除和氢解2种不同反应的速率常数却相近。非临氢条件下,主要反应路径β消除和脱氢脱硫路径选择性在MoS2和WS2上差别不大。这些反应结果说明,MoS2和WS2暴露的边缘活性位点的类型、数量是不同的,MoS2相比WS2具有更多活性位点,尤其是脱硫、加氢和氢解活性位点。
在临氢条件下,MoS2的耐氮性好于WS2,载体γ-Al2O3和SiO2对临氢条件下活性组分的耐氮性影响不大。在τ=0.8 g·min/mol时,引入相同量的哌啶后,2-PCHT在MoS2/Al2O3和MoS2/SiO2上的转化率降为原来的89%和88%;而在WS2/Al2O3和WS2/SiO2上转化率降为原来的65%和66%。非临氢条件下,在τ=0.8 g·min/mol时,引入相同量的哌啶后,2-PCHT在MoS2/Al2O3和MoS2/SiO2催化剂上的转化率降为原来的23%和30%;而在WS2/Al2O3和WS2/SiO2上转化率降为原来的38%和45%,可见引入哌啶对MoS2催化剂的抑制作用更强。笔者所在课题组前期研究表明,含氮化合物与含硫化合物存在明显的竞争吸附作用,当哌啶质量分数0.07%的转化率达到96%时,4,6-DMDBT 才开始进行HDS反应[34]。非临氢条件下,由于缺少氢,哌啶的脱除率进一步降低,进而表现出比临氢条件下更强的抑制作用。临氢和非临氢条件下,MoS2和WS2催化剂上2-PCHT各脱硫反应路径的占比不同,哌啶对各反应路径的抑制程度不同,可能是导致临氢和非临氢下2种催化剂耐氮性反转的主要原因。临氢条件下,WS2上β消除反应占比大于氢解,而MoS2上氢解的占比大于β消除,哌啶对β消除路径的抑制作用强于氢解,因此临氢条件下MoS2的耐氮性能优于WS2催化剂。非临氢条件下,MoS2和WS2催化剂均以β消除路径为主,且MoS2催化剂上β消除路径的占比较大,哌啶主要抑制β消除路径和脱氢路径,因此非临氢条件下MoS2的耐氮性能低于WS2催化剂。
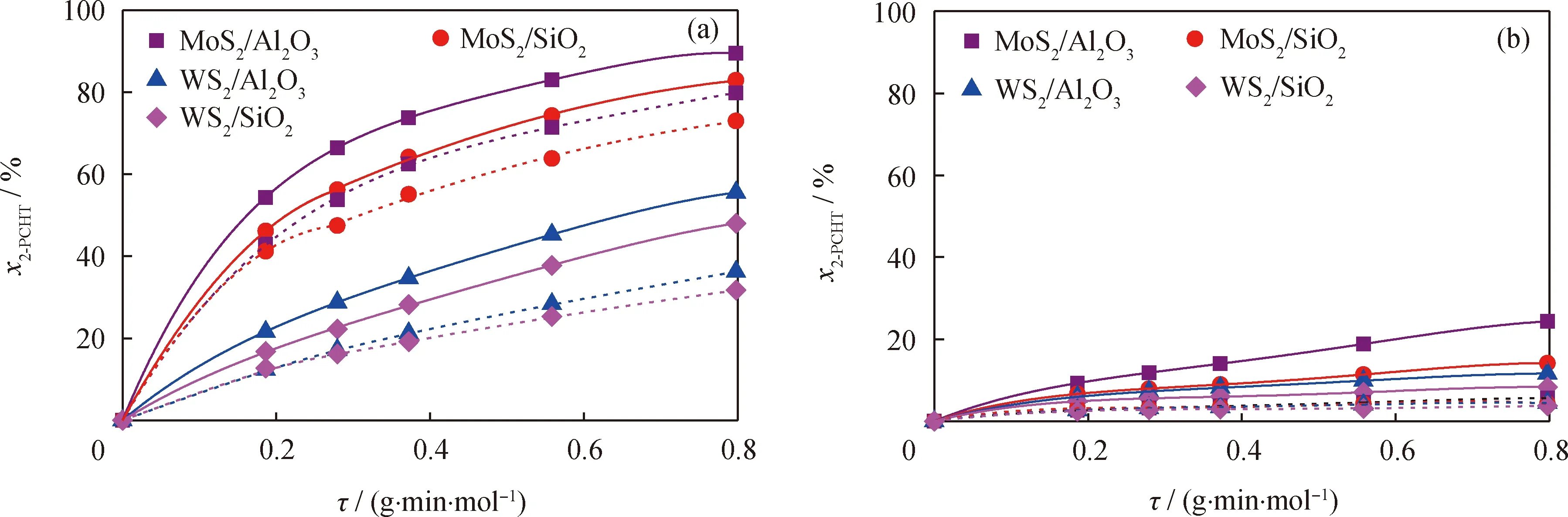
图10 临氢或非临氢条件下2-PCHT在MoS2和WS2上转化率与停留时间的关系Fig.10 Conversions of 2-PCHT as a function of space time over MoS2 and WS2 under 5.0 MPa H2 or Ar condition Solid lines represents the absence of piperidine and dashed lines represents the presence of 0.07% piperidine.(a) p(H2)=5.0 MPa; (b) p(Ar)=5.0 MPa T=240 ℃; m(Cat)=0.1 g; V(H2)/V(2-PCHT) or V(Ar)/V(2-PCHT)=800
2.7 2-PCHT脱硫动力学
在前序研究中发现,临氢条件下2-PCHT在WS2催化剂上的反应可以用假一级反应[35-36]描述,但是在非临氢条件下则不能用简单的幂函数描述。在平推流反应器中一级速率方程可表示为:
-ln(1-X2-PCHT)=k·τ
(5)
式中:k为反应速率常速数,mol/(g·min)。笔者也用假一级反应动力学[37]拟合了2-PCHT 在MoS2/Al2O3和MoS2/SiO2上的反应动力学,结果见图11。由图11可以看出,所得直线与实验数据点偏差较大,表明2-PCHT在MoS2催化剂上反应复杂,不能用假一级反应描述。这也说明2-PCHT在MoS2和WS2上反应过程不同,这是笔者所在课题组将来的一个重要研究课题。
3 结 论
(1)2-PCHT在MoS2和WS2催化剂上的反应网络相似。在240 ℃、5 MPa和临氢条件下,2-PCHT 在Al2O3和SiO2负载的MoS2催化剂上通过氢解、β消除、脱氢3条平行路径进行脱硫。氢解和β消除是主要反应路径,并且氢解快于β消除。在非临氢条件下,2-PCHT主要通过β消除、C-S均裂或氢解以及脱氢3条平行路径脱硫,β消除是主要反应路径。临氢和非临氢条件下,2-PCHT在MoS2催化剂上β消除路径不同,说明临氢和非临氢条件下,MoS2催化剂β消除活性中心或反应过程可能不同。
(2)临氢条件下,MoS2/Al2O3的反应活性优于MoS2/SiO2。在MoS2/Al2O3上,2-PCHT的氢解和β消除的活性都高于MoS2/SiO2。相对于SiO2载体,Al2O3更有利于提高MoS2催化剂上的氢解活性。非临氢条件下,在MoS2/Al2O3上的反应活性优于MoS2/SiO2,主要在于其较高的β消除活性。
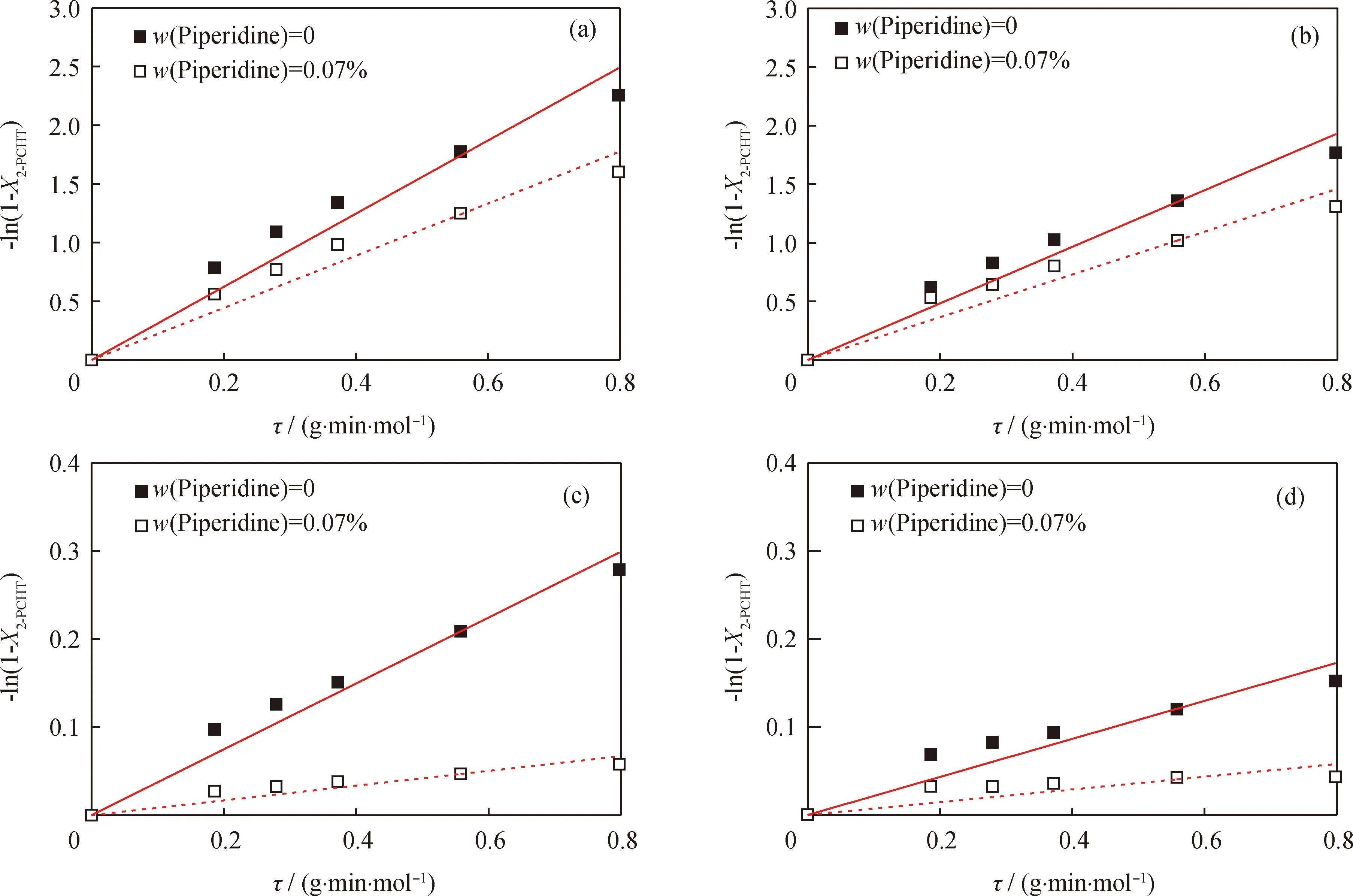
图11 在临氢或非临氢条件下2-PCHT在MoS2/Al2O3和MoS2/SiO2上脱硫反应-ln(1-X2-PCHT)-τ的相关曲线Fig.11 -ln(1-X2-PCHT)-τ for the desulfurization of 2-PCHT over MoS2/Al2O3 and MoS2/SiO2 under H2 or Ar(a) MoS2/Al2O3, p(H2)=5.0 MPa; (b) MoS2/SiO2, p(H2)=5.0 MPa; (c) MoS2/Al2O3, p(Ar)=5.0 MPa;(d) MoS2/SiO2, p(Ar)=5.0 MPa
(3)临氢条件下,哌啶对β消除路径的抑制作用略大于脱氢,对氢解几乎没有影响。MoS2/Al2O3与MoS2/SiO2耐氮性相近,哌啶对MoS2/Al2O3和MoS2/SiO2上的β消除反应和氢解反应抑制作用相近。非临氢条件下,哌啶主要抑制了β消除和脱氢反应路径,对C-S均裂几乎没有影响。
(4)MoS2的加氢活性以及对2-PCHT的脱硫活性均优于WS2催化剂。临氢条件下MoS2的耐氮性能优于WS2催化剂,非临氢条件下WS2的耐氮性能优于MoS2催化剂。无论在临氢或非临氢条件下,在本研究实验条件下,2-PCHT在MoS2上的动力学不能用简单的假一级模型描述。
