超分子网状材料在药物递送中的应用*
2021-05-06周斌铖金燕琦黄思思葛雨欣陈希敖雷
周斌铖,金燕琦,黄思思,葛雨欣,陈希,敖雷
(嘉兴学院,浙江 嘉兴 314001)
自1987年Jean-Marie Lehn[1]提出的超分子化学概念获诺贝尔化学奖以来,将超分子化学应用在工业、国防、农业及医药学等邻域的研究成果层出不穷[2]。近年来,通过超分子间动态可调节的非共价键相互作用(氢键、静电作用、主客体相互作用、π-π相互作用以及范德华力[3])而设计相关药物载体递送系统的研究引起了广大科学家的强烈兴趣。该研究可以做到在分子水平控制载体材料的构筑,并可以结合靶向递药的药学理论以及各种生理指标的特点设计出可控的靶向药物载体递送体系超分子网状水凝胶凭借着其特殊的物理化学性质以及多组分凝胶的三维空间结构,在药物递送邻域有着显著的优势[4]。在一些通过特定基团构建的载药体系中(如:脂质体、壳聚糖纳米微球等)可同时具备亲水性和疏水性,为药物的包载及释放提供了结构基础。然而超分子相互作用力便可促进具有多孔网络结构或多相材料的生成(例如三维超分子材料),其亲疏水的特征结构也可引申出利用材料的特异的理化性质来包封药物或控制药物及一些具有治疗作用的蛋白质的释放。用于医学邻域的超分子网状生物材料通常是由两种基本的机制之一而形成的:1)通过物理缠结和捆绑而形成一维的分子“堆叠”物——通常可由有序的氢键或小的π-π相互作用形成。2)通过末端或悬垂的超分子大环主体与药物客体的亲和力介导,实现聚合物或低聚体构件的延伸或交联[5]。这两种机理被认为是在传统聚合物体系的背景下衍生的[6~8]。
这些材料通常具有热力学性质,因此,当已知自组装分子的临界聚集浓度或亲和基序的平衡结合常数和速率常数等性质时,通常可以定量地描述这些材料。总而言之,其优点是可以依据它的热力学特性进行定量描述,然而无论是亚稳态中间体还是几何受限的超分子组装体都存在着依赖合成路径的非平衡状态。因此,可以根据这些特性可以构建不同的纳米结构材料,但又要考虑在合成时确保其重现性。
1 网状水凝胶超分子载药体系
网络状生物材料为通过扩散和渗透的机制控制药物从多孔结构内的释放提供了可能性[9]。一般来说,网状材料可以根据包裹药物分子量的释放动力学,通过来调节网状结构中空隙的大小以及网络结构中溶剂的流动性来达到控释目的。因此,可利用这一类材料来促进小分子药剂、生物蛋白、核酸或生物聚合药物的包封率和缓控释。
迄今为止,水凝胶作为超分子生物材料被频繁运用。超分子网络生物材料中蛋白质的释放可以通过材料本身的各种性质来调节。超分子水凝胶网络的网格大小可以通过改变构建材料的浓度和分子量以及超分子交联的程度来调节[10]。聚合物交联反应动力学在利用超分子材料制备主-客体、药物三元复合物中也有助于调节药物的释放。例如:Appel, R. A. Forster等人[11]利用富含电子的客体和缺乏电子的客体与葫芦脲(CB8)通过主客体识别作用形成水凝胶来包裹货物,水凝胶内的网状结构则为溶蚀作用或Fickian扩散来释放包含物提供了结构基础。此外,形成水凝胶网络的交联态超分子聚合物之间的亲和力也可以被调节,从而可以为释放药物后的材料代谢问题提供了解决思路[12]。
2 具亲疏水特性及静电相互作用的网状超分子载药体系
药物的包封及释放不仅可由超分子构建的特殊网状结构来调节,驱动许多超分子材料组装的潜在亲疏水相互作用也为药物在水/油相体系中的可控释放创造了机会。在这种特性中,药物的释放可能会因其在材料的油状或亲水结构域内的优先分配状况而改变。许多具有生物活性的小分子相对疏水。因此,具有疏水结构域的超分子材料在喜树碱等水不溶性药物的包封和释放中已被证明是有效的,可通过在超分子肽纤维中的包封来增强化疗活性[13]。同样,一些抗氧化药物,如姜黄素,可以通过包封在另一类肽凝胶的疏水结构域中来提高其抗氧化作用[14]。在另一种方法中,肽凝胶的疏水区可被用来包裹和稳定一个小分子重氮二醇基硝氧供体,以延长NO信号气体在血管损伤部位的释放[15]。Zhang等人[16]根据β折叠而成的肽链网络中存在疏水域的特性,提出利用β折叠肽与疏水性药物通过可降解连接键链接成载药纳米粒作为一种可自组装的前药。2020年,Jingjing Gao[17]课题组在以PEG5000和可降解PDS分别作为亲水和疏水基的基础上包封二硫苏糖醇(DTT)这一小分子有机还原剂形成功能化的水凝胶,当其被细胞摄入后可被细胞的氧化还原环境所触发,使得PDS交联疏水单元中的二硫键断裂,将疏水内核转变为完全的亲水链段相比一般两亲性递药体系,在促进药物在机体内的释放率上具有很大的优势(图1)。
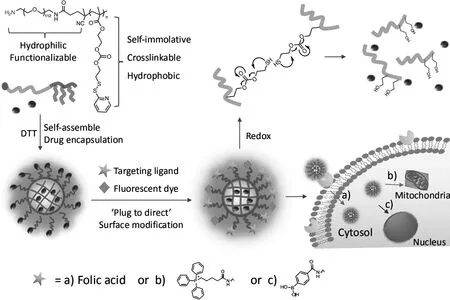
图1 功能化纳米凝胶的示意图 (用于靶向递送到胞浆和亚细胞器)
除了亲疏水作用以外,药物还可通过静电力与超分子体系相互作用,以调节其释放[18]。 例如,Wang[19]等人报道了药物苏拉明和超分子肽组件之间的静电相互作用,由于药物诱导的材料交联不仅稳定了纤维结构,还促进了纤维间的桥接,使材料的力学性能也发生了变化。
3 生物肽网状自组装载药体系
药物递送领域的另一种治疗策略集中在含有生物分子(如生物肽分子、核酸、蛋白质)的超分子材料上,其中细胞分泌调节生物功能的可溶性活性因子可作为另一个活跃的研究领域基础——用于药物递送的超分子生物材料应用[20~22]。该材料可为细胞和组织的功能健康提供支持,同时可通过旁分泌呈现细胞分泌的可溶性信号分子来发挥作用。这些信号可被作为“药物”,而细胞可被当作是一座“工厂”不断生产和释放这类“药物”。
载药体系的特性不仅由材料的物理结构特征决定,改变其化学特征也可使之呈现对一些蛋白质药物的特定亲和力,从而控制其从超分子网络中的释放速率。在利用这种方法的基础上,最常被探索使用的超分子生物材料为超分子组装肽,因为它们潜在的在自组装机制使其在物质表面的函数分布呈现出高密度性[23]。例如:噬菌体展示的与蛋白质识别结合的寡肽序列信息被认为是一种可以用来利用的生物信号[24]。这些短序列随后可以在超分子肽组件表面以高密度的形式呈现[25]。通过这种办法,已经开发出利用超分子肽组件来结合和释放用于软骨和骨头再生的生物信号分子。利用来自噬菌体中显示的结合序列可以以促进与TGF-β(β转化生长因子)的结合,从而用于软骨再生[26~27]。在另一种方法中,超分子材料可被设计用来结合和呈现类硫酸乙酰肝素糖胺聚糖分子;利用一些蛋白质可与肝素结合的这一天然亲和力,GAGs分子可以结合并传递强有力的生长因子和信号分子[28]。这为与肝素相结合具有高亲和力的蛋白质在生物体内的递送实现了一个模块化的途径,可用于刺激新血管的生长、心肌的再生或促进骨骼的生长[29~30]。与此相关的是,一种模仿肝素结构特征的超分子材料已被报道为是利用蛋白质与肝素结合的天然亲和力的单一组分模块蛋白传递材料[31~32]。
4 结语
综上概述了多种超分子网状自组装材料,及其所具有的有利于构建药物载体递送体系的特殊性质。多年来超分子材料的研发为药物控释提供了研究基础,这些超分子材料可进一步设计为具有特定功能的生物标志物或疾病指标指示剂(如:光敏超分子材料、热敏超分子材料、特殊酶反应超分子材料等)。超分子网状水凝胶、生物肽网状超分子材料已经展现了其在网状载药体系中的特殊优势及实践应用,我们可以依托构建基团的特殊性质以及生物体所表现的亲和特性等研究基础,利用超分子材料在药物递送领域中研发更有效且具可控性的递药体系。
