应用Markov-Monte Carlo 模型评价抗血小板药物CYP2C19基因检测的药物经济学分析
2021-04-30汤敏婷谢伟蓉林嘉昌
汤敏婷,谢伟蓉,林嘉昌
(1.广东省人民医院南海医院药剂科,广东 佛山528200; 2.广东省中西医结合医院静脉配置中心,广东佛山528200)
抗血小板药物治疗为急性冠状动脉综合征(acute coronary syndrome,ACS)患者接受经皮冠状动脉介入术或支架植入术术后常用治疗策略,目的在于预防血栓相关并发症发生[1]。相对于单药抗血小板治疗,双联抗血小板治疗(阿司匹林+P2Y12 受体抑制剂)更能有效减少血栓和主要不良心脏事件(major adverse cardiac events,MACE)风险[2]。CYP2C19基因为人体内重要的药物代谢酶,其多态性是导致同一药物在不同个体和种族间表现出不同代谢能力的重要原因。多项研究证实,氯吡格雷抵抗与CYP2C19基因多态性密切相关[3]。替格瑞洛为新型P2Y12受体抑制剂。研究发现,与氯吡格雷相比,替格瑞洛药物代谢过程不受CYP2C19基因多态性影响,且可显著降低MACE发生率,但可增加患者出血并发症风险[4]。目前国内外针对中国ACS 患者抗血小板药物CYP2C19基因检测指导抗血小板药物应用的可行性研究较少且多采用Markov 模型。而该模型强调运行周期,更适用于慢性病患者研究。同时由于该模型参数不确定性,不易进行敏感性分析。因此,本研究应用Markov-Monte Carlo 模型进行评价,旨在为临床提供更合理和安全的参考依据。
1 资料与方法
1.1 临床资料
回顾性分析2017 年9 月-2019 年8 月广东省人民医院南海医院心血管内科收治的213例ACS患者资料,根据治疗策略分为氯吡格雷组(n=52)、替格瑞洛组(n=83)和基因检测组(n=78)。纳入标准:①18~75 岁;②明确诊断为ACS[5];③拟接受经皮冠状动脉介入术和必要时支架植入术;④接受抗血小板药物治疗;⑤基因检测组入院后接受CYP2C19基因检测。排除标准:①既往抗血小板治疗史;②除氯吡格雷、替格瑞洛和阿司匹林外使用其他影响血小板功能药物或存在本研究使用药物禁忌症;③严重肝、肾、心、肺等功能不全。三组患者一般情况比较,差异无统计学意义(P>0.05),见表1。研究符合医院伦理委员会规定。
1.2 CYP2C19基因检测
抽取患者外周静脉血1 mL,收集于含EDTA 抗凝管内;按照血液DNA 基因组提取试剂盒说明书操作提取并纯化DNA;配置PCR 扩增液,加入5 μL 的DNA 溶液;混匀后,置于PCR 仪进行扩增;取扩增产物,按照CYP2C19基因检测试剂盒(DNA 微阵列芯片)说明书操作,在e-Hyb 全自动杂交仪中进行杂交显色;ArrayDoctor2.0 软件判断CYP2C19基因型,CYP2C19*2/*2、*2/*3、*3/*3 为 慢 代 谢 基 因 型,CYP2C19*1/*1、*1/*2、*1/*3为快代谢。

表1 各组患者一般情况Table 1 Analysis of general data
1.3 治疗方案
氯吡格雷组:硫酸氢氯吡格雷片,首次负荷剂量300~600 mg,后75 mg/次,1 次/d,阿司匹林肠溶片,75~100 mg/次,1次/d,持续治疗12个月替格瑞洛组:替格瑞洛片,首次负荷剂量180 mg,后90 mg/次,2 次/d,阿司匹林肠溶片,75~100 mg/次,1 次/d,持续治疗12个月。基因检测组:慢代谢基因型使用替格瑞洛+阿司匹林治疗,剂量和用法同替格瑞洛组;快代谢基因型使用氯吡格雷+阿司匹林治疗,剂量和用法同氯吡格雷组。
1.4 Markov模型建立
根据临床观察ACS 疾病发展情况和国内相关研究[6-7]建立Markov模型;针对患者第1年治疗情况,本研究将ACS 治疗后可能结果分为无事件状态、全因死亡状态、非致死性心梗状态、非致死性卒中状态等4 种状态,设定模型循环周期为1 年,模型运行终点为30年。
1.5 模型参数确定
1.5.1 转移状态概率
通过转换公式[8]将事件发生率转化为各状态间转移概率,转移概率(Pt)=1-e-rt,其中r为文献中获取的时间t内事件发生率,见表2。
1.5.2 转移状态健康效用值
模型中ACS 患者转移状态健康效用值参考国内相关文献[11-12]确定,全因死亡效用值设为0,表3。
1.5.3 成本参数
模型成本参数包括ACS 患者首次治疗总费用和治疗1 年内非致死性心梗、非致死性卒中治疗总费用以及持续治疗总费用。费用包括药品成本和治疗1年内非致死性心梗、非致死性卒中治疗成本,其中药品成本采用本省药品招标官方网站公布的现行有效的药品中位价格,治疗成本参照国内相关文献[6,11]。
1.6 评价指标
利用质量调整寿命年(quality-adjusted life years,QALYs)评价健康效用值,增量成本-效果比(incremental cost-effectiveness ratio,ICER)评价治疗策略经济学效益,将ICER 与中国社会意愿支付(willingness to pay,WTP)阈值比较,以ICER<WTP是获得最高QALYs 的治疗策略为成本效用最高的策略。参照2015 年中国药物经济学评价指南[13],根据2017 年中国人均国内生产总值(gross domestic product,GDP)评价治疗策略是否具有经济学优势的阈值标准,以ICER≤1 倍人均GDP 为具有显著经济学优势,1 倍人均GDP<ICER<3 倍人均GDP 为具有经济学优势,ICER≥3 倍人均GDP 为不具有经济学优势,本研究根据2017年国民经济和社会发展统计公报报道数据[14],将人均GDP(CNY 59 660 元)作为模型阈值,健康效用值和成本采用3%贴现率,并进行半循环矫正。

表2 转移状态概率估计结果Table 2 Estimation results of transition state probability

表3 转移状态健康效用值参数Table 3 Parameters of health utility value in transition state
1.7 敏感性分析
采用一元、二元、概率敏感性分析各参数对模型基础分析结果的影响。一元和二元敏感性分析中,成本和健康效用值上下限取值为基础值±20%,转移状态概率上下限取值为基础值±10%,贴现率取值范围为0%~8%。概率敏感性分析中,设定成本参数服从正态分布,健康效用值及转移状态概率服从β分布,采用Monte Carlo模拟法随机抽样1 000次确定模型参数不确定性,绘制成本-效果可接受曲线和增量成本-效果散点图。
1.8 统计学方法
采用SPSS20.0 软件对数据进行统计分析。符合正态分布计量资料用(x±s)表示,3 组比较采用单因素方差分析,两两比较Snk-q检验。计数资料用频数(%)表示,采用卡方非校正法。P<0.05为差异具有统计学意义。
2 结果
2.1 成本-效果分析结果
与氯吡格雷比较,替格瑞洛和基因检测治疗1年QALYs 增加,但成本相应增加且ICER>WTP。见表4。

表4 长期成本-效果分析结果Table 4 Long term cost-effectiveness analysis
2.2 一元敏感性分析结果
氯吡格雷组和替格瑞洛组,对ICER 影响较大的不确定因素为氯吡格雷和替格瑞洛无事件状态成本和替格瑞洛第1 年全因死亡率;氯吡格雷组和基因检测组,对ICER 影响较大的不确定因素为氯吡格雷和替格瑞洛无事件状态成本以及健康效用值;替格瑞洛组和基因检测组,对ICER 影响较大的不确定因素为氯吡格雷和替格瑞洛第1年全因死亡率、替格瑞洛健康效用值和第1 年非致死性心梗发生率。
2.3 二元敏感性分析结果
基于一元敏感性分析结果,对ICER 影响最显著的不确定因素(替格瑞洛无事件状态成本、氯吡格雷无事件状态成本)进行二元敏感性分析,结果显示当WTP 为59 660 元/QALY 时,净收益占比从高到低依次为替格瑞洛、氯吡格雷、基因检测。
2.4 概率敏感性分析结果
采用Monte Carlo 模拟法对模型进行概率敏感性分析,结果显示替格瑞洛具有成本-效果性概率随WTP 增加呈上升趋势;当36 971≤WTP≤59 660 元/QALY 时,具有成本-效果性概率从高到低依次为替格瑞洛、氯吡格雷、基因检测组;当59 660<WTP<69 782 元/QALY 时,具有成本-效果性概率从高到低依次为替格瑞洛、氯吡格雷、基因检测组;当WTP≥69 782 元/QALY 时,具有成本-效果性概率从高到低依次为替格瑞洛、基因检测组、氯吡格雷,见图1。采用Monte Carlo 模拟法随机抽样1 000 次确定模型参数不确定性,结果显示氯吡格雷和替格瑞洛,当WTP 阈值为59 660 元/QALY 时,替格瑞洛具有成本-效果优势性概率为80.13%;氯吡格雷和基因检测组,当WTP 阈值为59 660 元/QALY 时,基因检测组具有成本-效果优势性概率为47.64%;替格瑞洛和基因检测组,当WTP 阈值为59 660 元/QALY 时,替格瑞洛具有成本-效果优势性概率为64.97%,见图2。
3 讨论
国内外指南均将抗血小板治疗作为治疗ACS患者的Ⅰ类推荐,其中双联抗血小板治疗为临床常用方案。氯吡格雷和替格瑞洛均属P2Y12 受体抑制剂。其中氯吡格雷主要经肝脏代谢,且在ACS 中疗效确切。但有研究发现,氯吡格雷抗血小板聚集效果存在个体差异性,部分患者治疗后并不能达到预期药效学作用[15]。CYP2C19基因为体内重要的药物代谢酶。研究发现,任何能够抑制CYP3A4 或以CYP3A4 为底物的药物均可影响氯吡格雷生物转型形成活性代谢物,即CYP2C19基因多态性与氯吡格雷抵抗有关[16]。替格瑞洛为新型P2Y12 受体抑制剂,其代谢不受CYP2C19基因多态性影响。有研究发现,与氯吡格雷相比,替格瑞洛血小板抑制率高,MACE 发生率低,但出血和呼吸困难风险高[17]。目前,并未有相关指南明确指出,CYP2C19基因检测在ACS 患者抗血小板治疗中的必要性。本研究从药物经济学角度分析各治疗策略的可行性。
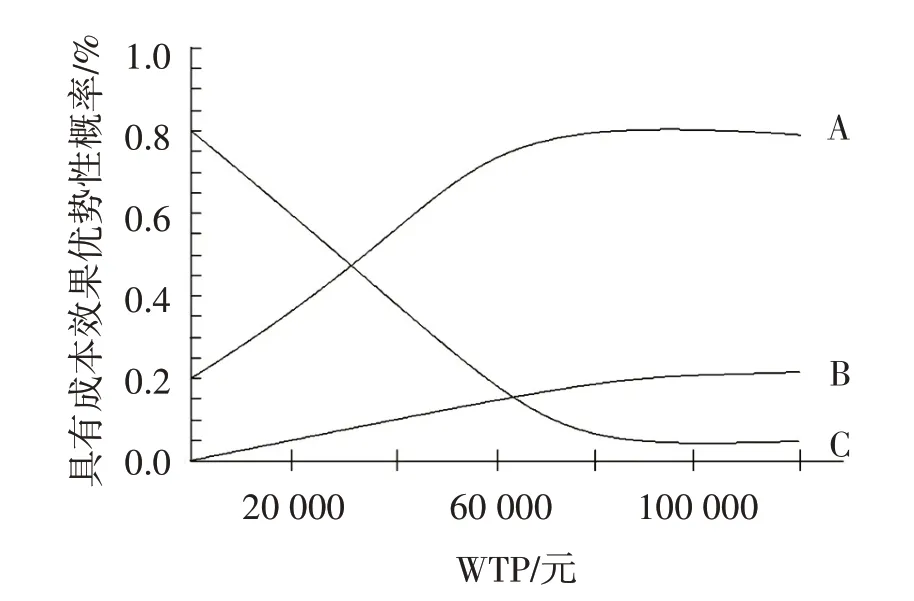
图1 成本-效果可接受曲线Figure 1 Cost-effectiveness acceptable curve

图2 增量成本-效果散点图Figure 2 Incremental cost-effectiveness scatter plot
安小芳等[18]采用2015 年中国3 倍人均GDP 值作为WTP 阈值,治疗1 年发现,氯吡格雷、替格瑞洛和基因检测成本分别为32 760 元、34 620 元、34 181元,与氯吡格雷相比,替格瑞洛和基因检测成本较高,但效用确有所提升,ICER>3倍人均GDP,而在治疗5年发现,与氯吡格雷相比,替格瑞洛和基因检测成本仍较高,但此时两种策略ICER<3 倍人均GDP。本研究采用2017 年中国1 倍人均GDP 作为WTP 阈值,治疗1 年发现,氯吡格雷、替格瑞洛和基因检测成本稍高于安小芳等[18]报道的成本值,可能与中国人均GDP 值逐年上升有关,替格瑞洛和基因检测ICER均大于1倍人均GDP,但小于3倍人均GDP,提示当WTP 阈值为1 倍人均GDP 时,相对于氯吡格雷,替格瑞洛和基因检测可能具有一定的经济学优势。一元敏感性结果显示,对ICER 影响最显著的不确定因素为替格瑞洛无事件状态成本、氯吡格雷无事件状态成本。基于此,研究进行了二元敏感性分析,结果显示,当WTP 为59 660 元/QALY 时,替格瑞洛净收益占比最高,其次为氯吡格雷和基因检测,提示替格瑞洛可能具有更高的成本-效果优势。目前使用的Markov 模型存在参数不确定性问题。而Monte Carlo 模拟可通过随机抽样解决难以直接抽样分布的模拟问题。本研究在Markov 模型基础上进行Monte Carlo 模拟发现,当WTP 阈值为59 660元/QALY 时,替格瑞洛最具成本-效果优势性,其次为基因检测,符合Borse等[19]报道,与氯吡格雷比较,替格瑞洛对ACS 患者尤其是发生出血不良事件者具有更小的经济负担。
综上所述,相对氯吡格雷而言,替格瑞洛和CYP2C19基因检测指导的个性化治疗方案对中国ACS 患者均具有一定药物经济学优势,根据我国人均国内生产总值水平,替格瑞洛显示出更显著的药物经济学优势。
