AA型淀粉样变性的研究进展
2021-03-16综述黄湘华审校
赵 亮 综述 黄湘华 审校
AA型淀粉样变性是一种由急性期反应蛋白血清淀粉样蛋白A(SAA)组成的淀粉样纤维在细胞外沉积所致的系统性疾病。炎症和自身免疫性疾病、慢性感染、肿瘤等多种疾病与SAA形成有关,这些疾病均伴随长期、间歇性或持续性SAA升高。淀粉样纤维可沉积在全身多个器官和组织,如脾、肝、肾、胃肠道、心肌和皮肤等。其病因在世界范围内具有显著的区域差异,在贫穷国家,慢性感染是主要病因,而在工业化发达国家,自身免疫性疾病所占的比例更高。本文归纳总结了AA型淀粉样变性病因、发病机制及诊治的研究进展。
AA型淀粉样变性的发生机制
AA型淀粉样变性的发病机制是众多因素相互作用的结果(图1)。
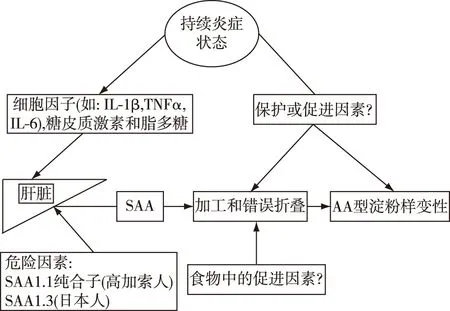
图1 AA型淀粉样变性的发病机制IL-1β:白细胞介素1β;TNF-α:肿瘤坏死因子α;IL-6:白细胞介素6;SAA:血清淀粉样蛋白A;SAA1.1:血清淀粉样蛋白A等位基因1.1;SAA1.3:血清淀粉样蛋白A等位基因1.3
前体蛋白及其浓度AA型淀粉样变性的前体蛋白是SAA,主要由肝细胞合成,巨噬细胞、内皮细胞和平滑肌细胞等也能合成SAA。其合成受炎性细胞因子正性调节,如肿瘤坏死因子α(TNF-α)、白细胞介素1β(IL-1β)和IL-6,糖皮质激素和脂多糖(LPS)对SAA也有调节作用[1]。肝脏持续合成高浓度SAA是发病的先决条件,健康人SAA的中位血浆浓度为3 mg/L,急性期反应时SAA浓度可高达2 000 mg/L,其浓度也是疾病活动的敏感指标[2]。
基因易感性AA型淀粉样变性不是遗传性疾病,尚未发现SAA的致病基因突变。但仅少数慢性炎症患者发生AA型淀粉样变性,基因多态性可能是影响其发病的重要因素。人类SAA编码基因包括SAA1、SAA2和SAA4三个位点,SAA1和SAA2的产物在急性炎症状态下显著升高,称为急性期SAA,超过90%的AA型淀粉样变性的前体蛋白来源于SAA1,极少数来源于SAA2。SAA1有5种等位基因(SAA1.1-1.5),日本研究发现SAA1.1、1.3和1.5是该国人群常见的亚型,SAA1.3是类风湿性关节炎(rheumatoid arthritis,RA)相关AA型淀粉样变性的危险因素,而SAA1.1是保护因素[3]。但欧洲研究却发现SAA1.1纯合子是AA型淀粉样变性的危险因素。提示基因易感性还存在种族差异。SAA4是一种非急性期SAA,SAA4基因突变可通过非淀粉样纤维形成途径导致AA型淀粉样变性[4]。
蛋白质水解和错误折叠很多蛋白质都存在易形成淀粉样纤维的氨基酸序列,但这些序列被折叠在蛋白质内部。水解和错误折叠暴露了这些氨基酸序列,使其容易聚集形成淀粉样纤维[5]。SAA的一级结构有104个氨基酸,但在AA型淀粉样变性中,SAA的C末端总是缺失,因此推测C末端水解可能与其致病性密切相关[6]。基质金属蛋白酶(matrix metalloproteinases,MMP)是一类高度保守的蛋白水解酶,MMP1、MMP2和MMP3在人类AA型淀粉样变性的沉积物中均有发现,可能通过蛋白水解作用参与AA型淀粉样变性的发生和进展[7]。
淀粉样沉积物的其他组分除了淀粉样纤维,淀粉样沉积物中还存在其他成分,包括硫酸乙酰肝素蛋白聚糖(heparan sulfate proteoglycan,HSPG)和SAP,HSPG参与β片层状结构形成,而SAP则能防止淀粉样纤维被降解[8]。另外SAA在血浆中几乎全部与高密度脂蛋白(HDL)结合, SAA如何与HDL解离并形成淀粉样纤维的具体机制尚未明确,HSPG可能在解离过程中起重要作用[9]。
衰老与淀粉样变性AA型淀粉样变性多见于老年人。衰老细胞内的蛋白质稳态失衡是导致错误折叠蛋白质产生和释放的重要因素,晚期糖基化终末产物(advanced glycation end products,AGE)和氧化应激(oxidative stress,OS)也可能通过改变蛋白质分子性质使其更容易形成淀粉样纤维[10]。
AA型淀粉样变性相关疾病
明确病因对于AA型淀粉样变性的诊断和治疗均具有重要意义,常见病因包括炎症和自身免疫性疾病、感染性疾病、遗传性疾病和肿瘤等,少数病例无明确病因,称为特发性AA型淀粉样变性。Brunger等[11]系统回顾了795篇AA型淀粉样变性文献,根据基础疾病与AA型淀粉样变性的相关强度分为:强、弱、不清楚和不可能四个等级。根据作者定义的标准,有48种疾病为强相关,19种弱相关,23种不清楚,60种为不可能相关(表1、2)。下面将分不同类型重点介绍常见病因。

表1 与AA型淀粉样变性相关性强的疾病

续表1 巨球蛋白血症 霍奇金病 非霍奇金淋巴瘤肿瘤 恶性肿瘤 肺癌 间皮瘤 肾细胞癌 良性肿瘤 castlemans病 肝细胞腺瘤特发性疾病 大疱性表皮松解 化脓性汗腺炎

表2 与AA型淀粉样变性弱相关性的疾病
炎症和自身免疫性疾病在西方国家,炎症和自身免疫性疾病是AA型淀粉样变性最常见的病因。美国的研究发现, RA和青少年特发性关节炎(juvenile idiopathic arthritis,JIA)占病因的12%~21%,炎症性肠病(inflammatory bowel disease,IBD)占16%~17%,银屑病性关节炎(psoriatic arthritis,PA)占10%~12%[12]。英国的研究发现:RA占23%~51%,JIA占11%~17%,强直性脊柱炎(ankylosing spondylitis, AS)占0%~12%,PA占4%,克罗恩病占2%~5%[13]。近年来,随着新型药物如TNF-α和IL-6单克隆抗体的出现,炎症和自身免疫性疾病得到了更好的控制,使其相关的AA型淀粉样变性在西方国家也变得更少见[14]。
感染性疾病在人类历史上,AA型淀粉样变性曾经是最常见的淀粉样变性,其主要原因是肺结核的流行。乌普萨拉大学对1911年~1913年尸检标本的研究发现,701例中有156例患肺结核,其中48例合并淀粉样变性[15]。慢性骨髓炎和梅毒也曾是AA型淀粉样变性的常见病因[16],内脏放线菌病和牙齿慢性感染也可导致AA型淀粉样变性[17-18]。截瘫患者常合并褥疮和尿路感染,持续产生SAA,导致AA型淀粉样变性。支气管扩张也是AA型淀粉样变性的病因之一。如今,随着高效抗菌药物的广泛使用,随着高效抗菌药物的广泛使用,慢性感染继发的AA型淀粉样变性已变得罕见。
遗传性疾病在某些特定地区,遗传性疾病是AA型淀粉样变性的重要原因[19]。在土耳其,家族性地中海热(familial Mediterranean fever,FMF)是60%以上病例的病因,MEFV M694V(FMF最常见突变基因)与AA型淀粉样变性的发病密切相关。还有一些罕见遗传性疾病与AA型淀粉样变性相关,例如高IgD综合征和甲羟戊酸尿症都是甲戊酸激酶(mevalonate kinase,MVK)基因突变所致,通过检测MVK基因的突变可帮助确诊。脓皮病痤疮脓疱病心律失常综合征与CD2BP1基因突变有关。Blue综合征(BS)是一种儿童期发病的家族性结节病,与CARD-15基因突变有关。肿瘤坏死因子受体相关周期性发热综合征与TNFRSF1A基因突变相关,其临床症状与FMF相似。
肿瘤大多数肿瘤仅与AA型淀粉样变性弱相关。肿瘤炎症微环境可能在其发生和进展中起重要作用[20]。研究认为,20%的肿瘤与慢性感染有关(例如霍奇金病和大B细胞淋巴瘤与EB病毒感染;结肠癌和膀胱癌与血吸虫或类杆菌属细菌感染),30%与吸烟和吸入污染物相关(如肺癌和间皮瘤),35%与饮食因素相关,20%与肥胖相关[21]。
特发性AA型淀粉样变性特发性AA型淀粉样变性定义为:明确存在淀粉样变性且为AA型淀粉样变性,同时排除其他类型的淀粉样变性以及与AA型淀粉样变性相关的疾病[11]。该类别的存在说明人们对该病发病机制认识不足,因此,在研究中不断积累相关病例并寻找其共同特征尤为重要。有研究表明,肥胖、SAA1.1/1.1纯合子和CRP升高是特发性AA型淀粉样变性的危险因素。一项纳入37例特发性患者的研究发现,约一半(18例)患者的体质量指数(BMI)>30,因此作者认为肥胖是特发性AA型淀粉样变性重要的易感因素[22]。
AA型淀粉样变性的临床表现
AA型淀粉样变性的临床表现由基础疾病和器官受累情况共同决定。淀粉样纤维沉积在肾、肝、脾、肾上腺、胃肠道、心肌和皮肤等多个器官和组织导致相应的临床表现。肾脏受累最常见的临床表现是蛋白尿,95%患者表现为不同程度的蛋白尿,50%表现为肾病综合征,肾小球滤过率下降也很常见,约11%患者确诊时已出现肾衰竭[13]。肝、脾受累早期常无明显临床表现,晚期可出现肝脾肿大甚至肝脾破裂[23]。胃肠道受累可导致吸收不良,假性肠梗阻,腹泻,腹痛和消化道出血等临床表现[24]。心脏受累较少见,但也有导致心力衰竭的报道[13]。其他引起临床表现的器官受累还包括肾上腺、甲状腺、肺等。
诊 断
活检是确诊系统性淀粉样变性唯一的方法。活检部位可选择临床受累的内脏器官,伴肾脏损害表现的通常可行肾活检。其他常见活检部位还包括直肠活检、皮肤脂肪活检、唇腺活检等。受累组织刚果红染色呈阳性,在偏振光显微镜下呈苹果绿双折射。确诊后需要明确分型,高锰酸钾刚果红染色法曾被用于鉴别AL和AA型淀粉样变性,高锰酸钾刚果红染色不抵抗是AA型淀粉样变性的典型特点,但该方法存在假阳性的问题[25],目前免疫组化是鉴别不同类型淀粉样变性的首选方法,活检组织A蛋白染色阳性可诊断AA型淀粉样变性。但免疫组化也并非完全可靠[26]。目前,利用激光显微切割联合蛋白质质谱分析技术是进行系统性淀粉样变性分型最可靠的方法[27]。
治 疗
由于AA型淀粉样变性病因多样,临床缺乏通用的治疗方案。虽然新型靶向药物如抗SAP抗体已在临床试验中取得了较好的结果[28],动物实验显示阻断SAA的mRNA转录以及采用氯膦酸盐清除巨噬细胞对淀粉样变性具有潜在治疗价值[29],但是,这些方案均尚未应用于临床。目前,治疗方案仍以治疗原发病和对症支持治疗为主。
治疗原发病控制原发病,减轻急性期反应,降低循环SAA水平,是稳定和减轻AA型淀粉样变性最有效的方案。有效的抗结核治疗后,淀粉样变性相关的肾病综合征能够得到缓解。大剂量秋水仙碱能有效控制FMF的系统炎症状态,用于诱导相关AA型淀粉样变性缓解。抗IL-1抗体阿那白滞素(anakinra)和卡纳单抗(canakinumab)是对秋水仙碱抵抗、不耐受、治疗后复发以及合并血管炎的FMF患者的一线治疗方案[30]。在一些炎症性关节病和炎症性肠病患者,免疫抑制剂如环磷酰胺和他克莫司以及生物制剂如英夫利西单抗、依那西普和托珠单抗等,对控制蛋白尿进展和改善长期预后有良好效果[31]。外科手术例如局灶性castleman’s病切除,可迅速减轻血清急性期反应蛋白水平[32]。
器官支持和对症治疗器官支持和对症治疗是AA型淀粉样变性的基础治疗。例如,对于肾脏受累患者,应注意肾脏低灌注、肾毒性药物、高血压和感染等相关情况。表现为肾病综合征的患者应限制钠、水摄入,适当应用利尿剂、AECI和ARB类药物。氟氢可的松或米多君对体位性低血压有一定疗效。严重腹泻和蛋白质营养不良的患者可尝试采用调节肠道菌群、糖皮质激素冲击、糖皮质激素联合奥曲肽等治疗[33]。器官功能衰竭患者在基础疾病得到有效控制后可行器官移植。
总结:AA型淀粉样变性是由不同病因引起的循环SAA升高所致,常见病因包括炎症和自身免疫性疾病、慢性感染、遗传性疾病和肿瘤等,少数无法明确病因者称为特发性AA型淀粉样变性。明确病因与发病机制对诊断和治疗均具有重要意义。随着研究的进展,该病的病因谱逐渐扩大,发病机制的研究也逐渐深入到分子水平。蛋白质质谱分析技术大大提高了诊断和分型的准确性。目前,治疗仍以原发病治疗、器官支持和对症治疗为主。针对SAP和SAA的靶向治疗药物有望成为治疗AA型淀粉样变性的新手段。
