肛瘘保留括约肌手术的发展与实践*
2021-01-19李璐王蓉陈玉根孙桂东邵万金
李璐,王蓉,陈玉根,孙桂东,邵万金
1 江西中医药大学附属医院肛肠科 江西南昌 330006
2 南京中医药大学第一临床医学院 江苏南京 210029
3 南京中医药大学附属医院肛肠科 江苏南京 210029
肛瘘是肛肠科常见病、多发病,对于低位单纯性肛瘘的治疗,多种手术方式均可取得良好的效果,但复杂性肛瘘的治疗目前仍面临巨大挑战。复杂性肛瘘的手术治疗,若过于保守,易导致肛瘘持续存在或复发,但可保护肛门功能;若过于激进,肛瘘治愈率可能提高,但损伤肛门功能的风险亦高。括约肌对维持肛门自制起重要作用,术中切开过多括约肌可能导致术后肛门失禁。如何在追求治愈率和保护肛门功能之间取得平衡,是肛肠科医师一直在探讨和努力的方向。随着人们生活水平的提高,患者不再接受以损伤肛门功能或影响生活质量为代价来治愈肛瘘,使得各种保留括约肌手术成为新热点。本文通过查阅文献,结合作者团队的临床实践经验,将目前几种肛瘘保留括约肌术式的发展历史和应用现状进行述评,以期为临床应用提供指导。
1 经肛括约肌间切开术(transanal opening of intersphincteric space,TROPIS)
早在二十世纪五六十年代,Eisenhammer[1]认为括约肌间肛腺感染是形成肛瘘的主要原因,并建议采用内括约肌切开术治疗肌间脓肿。Parks等[2]和Hanley[3]指出高位肌间脓肿可向上蔓延,进入肛提肌上间隙形成急性脓肿,应行完全内括约肌切开术使脓肿从肠腔内引流,错误的手术入路可能导致“医源性复杂的括约肌上/外肛瘘”。2017年,Garg[4]将这种经肛入路直肠腔内引流的方式重新归纳总结,提出一种新的手术方式,即经肛括约肌间切开术(TROPIS)。该术式沿肛瘘内口直接切开肛管近端皮肤、内括约肌和直肠远端进入括约肌间隙对脓腔进行引流(图1)。对于高位肌间马蹄形脓肿或肛瘘,从肠腔内后正中切开,并在弯钳引导下向两侧弧形扩大创面;如果合并有直肠继发内口,切口可延伸至肛提肌上方直肠内口,此时由于切开位置过高,术中应严密止血,可在切开直肠黏膜顶端作袋形缝合,防止出血的同时也避免创面过早粘连影响引流,有条件的医院可采用超声刀切开预防出血。TROPIS手术仅切开部分内括约肌,无需切开外括约肌,即使肌间脓肿过大波及外括约肌,此入路对外括约肌的损伤也是最小的,因此对肛门功能影响很小。Garg[4]采用该手术治疗61例高位复杂性肛瘘患者,中位随访时间9个月,治愈率高达90.4%,术后患者肛门失禁评分无明显变化;Teoule等[5]采用TROPIS手术治疗直肠后肛提肌上方脓肿共109例,总体治愈率达94.5%。括约肌间型肛瘘占所有肛瘘类型的75%以上,因此掌握TROPIS术可以有效治疗大部分肛瘘。由于创面位于肠腔内,患者疼痛轻,无明显不适,肛门外几乎看不到伤口,因此不需要特殊护理,可在术后2~3周做直肠指诊检查创面,防止粘连形成假性愈合。
最近的研究证实,复杂的腺源性肛瘘发生于肛管括约肌间后深间隙(deep posterior intersphincter-ic space,DPIS)远多于肛管后深间隙(deep postanal space,DPAS)。正常情况下DPIS在MRI中并不显露,当有感染形成时将此间隙撑开,形成密闭的小脓肿,当压力过大时则向组织薄弱的地方突破蔓延,形成各种类型的复杂性肛瘘[6]。我们在临床中也发现,大部分后方高位复杂性肛瘘手术失败或复发的原因是没有处理此间隙,TROPIS手术则会对此间隙进行处理。因此,对于高位经括约肌肛瘘或坐骨直肠窝马蹄形脓肿合并有DPIS感染,可采用TROPIS联合其他手术方式(改良Hanley、改良Parks松挂线术等)治疗,以达到更好的效果。

图1 TROPIS 手术治疗后侧高位肌间脓肿
2 改良Parks松挂线术(loose seton technique,LST)
公元前460~377年,希波克拉底首次描述应用马鬃挂线治疗肛瘘。1976年,Parks和Stitz[7]提出应用松挂线术治疗高位经括约肌和括约肌上肛瘘,术中切开部分内括约肌和下1/3的外括约肌,剩余瘘管穿过的外括约肌(若为括约肌上型则包括耻骨直肠肌)予橡皮筋松挂线引流,数月后可直接拆除橡皮筋或分次紧线。Parks发现仅松挂线的患者肛门功能下降的有17%,而后期紧线的为39%,因此他认为应保留更多的括约肌。直到1990年,Kennedy和Zegarra[8]对Parks的技术进行改良,术中切开括约肌外侧的瘘管,切开部分内括约肌以开放括约肌间隙,清除内口和肌间原发感染灶,瘘管穿过的所有外括约肌予松挂线,一旦创面有良好的愈合迹象,生长到靠近外括约肌时则直接拆除橡皮筋(图2)。Kennedy和Zegarra采用改良Parks松挂线术治疗32例患者,拆除橡皮筋的时间为2~16周(平均7周),平均随访36个月,治愈率为78%,部分患者有轻微的漏气或溢液,仅1例(3%)偶有稀便失禁,无患者出现固便失禁。目前文献报道松挂线术的治愈率在53%~89.7%,失禁率在0.9%~36%[7-14](见表1),显著低于切割挂线的失禁率(20%~67%),且患者疼痛感明显减轻,因此虽然切割挂线的成功率达90%以上,但会导致肛门括约肌损伤,需要谨慎选择[15]。改良Parks松挂线术不切断任何外括约肌,保留了外括约肌的完整性,最大程度保护肛门功能,可作为治疗复杂性肛瘘的确定性手术。文献报道拆除橡皮筋的时间为6周至6个月不等,我们的经验是一般放置2股橡皮筋,2~4周内予以分次拆除,拆线的标准为按压切口无分泌物、冲洗切口流出液干净及创底长实转动橡皮筋有阻力。如果为肛管后深间隙(DPAS)马蹄形脓肿/肛瘘,可结合改良Hanley术在两侧坐骨直肠窝脓肿或支管作切口对口引流。
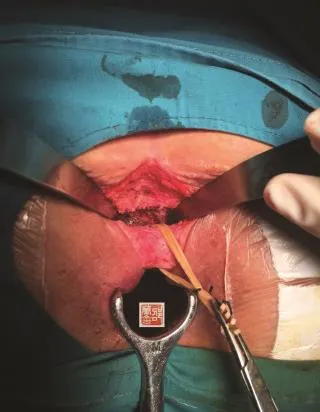
图2 改良Parks松挂线术
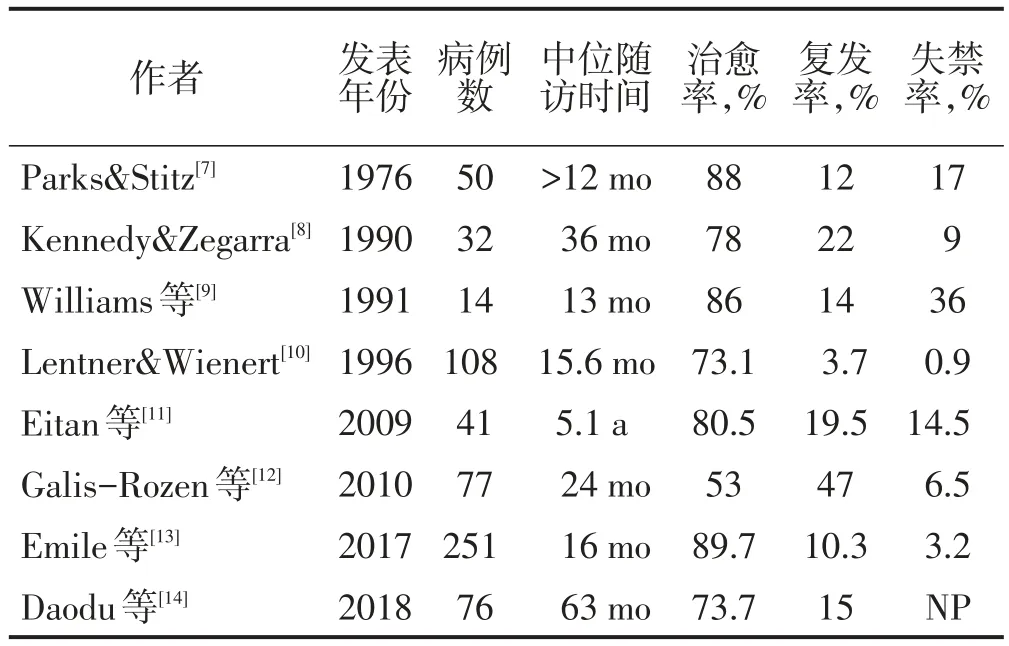
表1 改良Parks 松挂线文献回顾
松挂线术不仅可作为复杂性肛瘘的确定性治疗,也可作为其他确定性手术(如Flap、LIFT等)前的引流术,促进瘘管纤维化;克罗恩病肛瘘患者采用永久性松挂线引流,可有效地防止发生局部感染,且并发症少[12]。术后瘘管复发或失败的患者也可重复使用此技术,因为虽然初次挂线失败,但由于橡皮筋逐渐侵蚀瘘管和括约肌,使得内口逐渐向肛管远端移动到高压区外,原发瘘管在术后常变得更短、更清晰[14]。虽然大部分患者不需要切开括约肌而达到治愈,但存在一定的失败率,因此再次行Parks松挂线术时应与患者协商沟通,遵循患者意愿,或者把选择权交给患者[16]。
3 推移瓣修补术(advancement flap,AF)
1902年,Noble[17]首次描述了采用该技术治疗直肠阴道瘘,1912年,Elting[18]采用直肠黏膜推移瓣治疗复杂性肛瘘,这是第一种保留括约肌治疗肛瘘的方法。目前可通过转移直肠内的组织做直肠推移瓣(endorectal advancement flap,ERAF),或采用肛周皮肤作经肛推移皮瓣(dermal advancement flap,DAF)来实现。直肠推移瓣是向头侧端游离顶窄底宽的“U”形黏膜肌瓣(由黏膜、黏膜下层和部分直肠环肌组成),厚约1 cm,长3~4 cm,底边长度是顶边长度的2倍(图3),可在黏膜下层注射稀释肾上腺素溶液(20 mL生理盐水滴入6~8滴肾上腺素)有助于分离和止血;清除内口、剔除上皮化瘘管并用可吸收线闭合;切除推移瓣的远端,缝合固定在内口下方。经肛推移皮瓣[19]同样将正常组织转移至内口,然而游离的是含皮肤和皮下脂肪的“U”形宽基皮瓣(图4),将皮瓣移入肛管并缝合在内口上,外口通常开放引流。推移瓣通过移动正常组织分两层关闭和覆盖原发内口,切断肠腔与瘘管的连接,而括约肌复合体保持不变,瘘管因无肠腔内容物和细菌进入而逐渐愈合。目前的文献数据显示推移瓣的治愈率为66%~87%[20-21]。Soltani等[22]发表了一篇系统综述,纳入35项研究共2 065例患者,分析结果显示腺源性肛瘘和克罗恩病肛瘘的治愈率分别为80.8%和64%,失禁率分别为13.2%和9.4%。对于复发的病例,重复行推移瓣术仍有可能获得治愈。因此推荐推移瓣术既可用于直肠阴道瘘的治疗,也可用于治疗复杂性肛瘘。
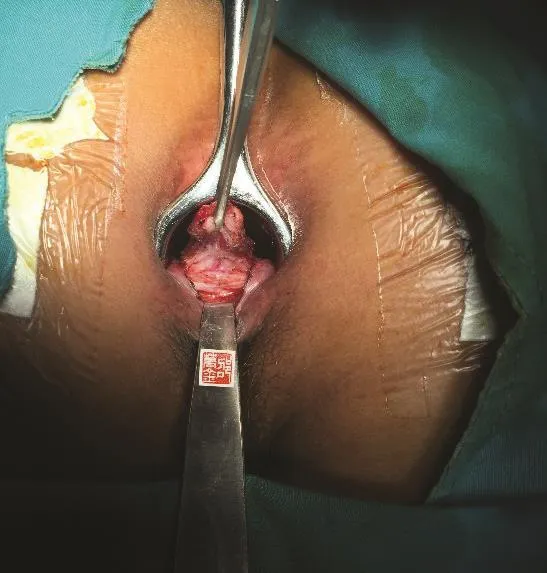
图3 直肠黏膜推移瓣
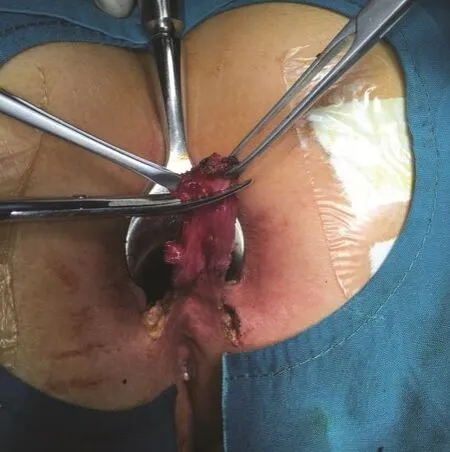
图4 经肛推移皮瓣
推移瓣修补术失败的危险因素有:(1)脓肿未引流和/或支管持续存在;(2)既往手术史引起会阴部瘢痕,导致组织解剖层次不清,血供较差;(3)皮瓣游离太薄(只含黏膜层)导致皮瓣缺血坏死,游离不充分或基底部太窄导致皮瓣存在张力,甚至回缩;(4)合并克罗恩病,有活动性直肠炎或肛管狭窄;(5)直肠阴道瘘瘘口直径>2.5 cm;(6)恶性肿瘤或与放疗有关的瘘管。使用探针正确识别瘘管,明确内口,充分游离适当的正常组织,保证良好的血供和无张力缝合是手术成功的关键。外口需充分搔刮彻底引流,防止术后过早闭合导致脓肿形成;可通过外口注射生理盐水来检查内口是否完全闭合,再间断缝合黏膜肌瓣,注意消灭死腔,尽量减少手术部位的积液。术后控制排粪3 d,卧床休息,避免活动和术后重力的影响。
4 经括约肌间瘘管结扎术(ligation of the intersphincteric fistula tract,LIFT)
2007年,泰国Arun Rojanasakul教授[23]首次描述了一种新的完全保留括约肌的术式——经括约肌间瘘管结扎术(LIFT),该手术组织损伤小、愈合时间短、治愈率高达94.4%,且几乎不损伤任何括约肌,对肛门功能影响甚微,术后如果肛瘘复发并不影响再次手术,既往有肛瘘手术史的患者也可实施该术式,使得该术式目前在国内外非常流行。手术步骤:在瘘管上的括约肌间沟作弧形切口,沿括约肌间分开内、外括约肌,游离瘘管周围组织,用弯直角钳挑起括约肌间瘘管,然后缝扎近侧端(近内括约肌)和远侧端(近外括约肌)瘘管,在两结扎点之间离断瘘管,括约肌间和皮肤切口无张力缝合,外口至外括约肌外侧缘的瘘管予切开或隧道式挖除(手术经典步骤示例见图5)。Arun Rojanasakul教授经过10年的随访研究,对251例患者中位随访71个月,总治愈率为87.65%[24]。文献荟萃分析结果显示,虽然纳入的研究在数量和质量上有差异,LIFT手术治疗肛瘘的成功率在71%~81%,愈合时间通常为4~8周,在接受肛门功能评定的患者中,仅6%的患者有轻度的肛门失禁[25-27]。改良LIFT手术(LIFT+挂线、LIFT+推移瓣、LIFT+肛瘘栓、LIFT+补片)成功率并没有明显提高[28]。我们对60例高位经括约肌肛瘘患者经过3~120个月的随访,总体治愈率为71.4%,无术中及术后并发症,仅1例患者出现术后肛门轻微溢液,最终的结果与已有报道相似。因此,LIFT术是治疗经括约肌肛瘘安全有效、并发症少的保留括约肌手术,2016年美国ASCRS指南推荐单纯性和复杂性肛瘘采用LIFT手术治疗[15]。
LIFT手术失败的原因可能有[29]:(1)术中将括约肌间瘘管分破或残留支管;(2)括约肌间瘘管尚未局限或存在肌间马蹄形脓肿;(3)肌间瘘管过于复杂(高位肌间存在盲瘘、直肠存在继发内口、括约肌上肛瘘),由于肌间的分离较深,视野有限,手术操作相对较难。因此,良好把握手术适应证,选择肌间成熟的瘘管进行操作,术中应在探针引导下精准细致地游离括约肌间纤维化瘘管,结扎完后尽可能多地切除肌间瘘管,并再次予可吸收线缝扎内口侧和外口侧,将两侧瘘管包埋,可有效防止结扎线脱落;为增加手术的成功率,括约肌间瘘管结扎后可经外口注射双氧水以证实瘘管已阻断,切断括约肌间瘘管后可再次经外口注射双氧水以明确肌间外口已完全关闭。Tan等[30]归纳了LIFT手术失败或复发的3种常见类型:第一种为局部括约肌间切口裂开,只需换药或搔刮引流等保守治疗伤口可自行愈合;第二种为部分失败,瘘管走行从内口到括约肌间创面,即将经括约肌肛瘘转变成括约肌间肛瘘,行肛瘘切开术即可;第三种为完全失败,仍为经括约肌肛瘘,可选择再次行LIFT手术或其他保留括约肌手术。了解失败的类型有助于指导后续治疗,以最大程度地提高治愈率[31]。
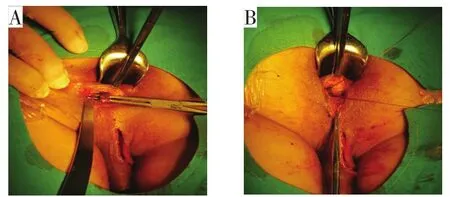
图5 LIFT 手术经典步骤示例
5 其他保留括约肌手术
5.1 纤维蛋白胶和肛瘘栓
1991年,Hjortrup等首次提出了使用纤维蛋白胶(fibrin sealant,FS)治疗肛瘘的理念[32]。纤维蛋白胶是一种促进成纤维细胞生长和瘢痕形成的生物支架,将材料注射到搔刮干净的瘘管内使其填满整个管腔从而促进瘘管愈合。由于其为液体材料,很容易从瘘管内排出导致手术的失败,因此Johnson等[33]在2006年提出采用肛瘘栓(anal fistula plug,AFP)进行治疗。肛瘘栓插入瘘管固定在内口上,植入数月后瘢痕组织取代肛瘘栓而使瘘管愈合。由于这两种手术不需要切开任何括约肌,因此术后发生肛门失禁的风险很小。但二者的成功率差异较大,注射纤维蛋白胶的治愈率在14%~84%,肛瘘栓在20%~86%,且注射纤维蛋白胶复发率更高(54%~69%)[34-37]。最近有报道称,注射纤维蛋白胶的短期成功率为70%~74%,长期治愈率低至16%~54%[38],随着随访时间的延长,肛瘘栓的成功率由80%下降至32%[36]。因此,2016年美国ASCRS指南认为由于远期疗效的不确定性,肛瘘栓和纤维蛋白胶对肛瘘的治疗相对无效,但因其具有潜在的成功率、低风险且是基于括约肌保护的技术,因此,只要外科医师对患者的预期治愈率给予适当的解释,这两种方法在临床上仍可以作为治疗肛瘘的选择。
5.2 视频辅助肛瘘治疗技术(video-assisted anal fistula therapy,VAAFT)
Meinero和Mori[39]于2011年首次报道了这项新型微创技术,运用肛瘘镜在显示器上显露整个瘘管、内口,并可以在外接的显示器上观看到手术全过程。VAAFT技术可用于肛瘘的诊断和治疗。诊断阶段,肛瘘镜从外口进入瘘管,发现内口以及支管或脓腔。治疗阶段采用电灼破坏瘘管,内镜刷冲洗清除坏死组织,再用缝线、推移瓣或吻合器关闭内口,据报道其术后复发率接近26.5%,87%的患者在至少6个月的随访中获得痊愈,无复发、无并发症。Emile等[40]系统性回顾7篇文献共纳入788例患者,使用VAAFT的内口检出率为93.3%,复发率因内口闭合方式的不同存在差异,使用吻合器为15.3%,直接缝合为17.7%,推移瓣为25%,平均复发率为17.7%,并发症发生率为4.8%,所有的研究均显示未影响肛门功能。虽然VAAFT是治疗复杂性肛瘘的一种新型保护括约肌的微创手术,但设备昂贵,在基层医院较难开展,目前我国还缺乏大规模的临床实践报道,其效果还需要进一步的前瞻性研究来证实。
5.3 干细胞移植术
干细胞移植术是指将提取的间充质干细胞注射至搔刮干净后的瘘管内,然后缝合内口和外口关闭瘘管。目前用于复杂性肛瘘的间充质干细胞主要来源于脂肪组织(adipose-derived stem cells,ASCs),具有抗炎、再生分化、免疫调节及组织修复潜能等生物学特性。为数不多的一些文献报道其治愈率在56.3%~83%,目前较多研究用于克罗恩病肛瘘的治疗[41-42]。ASCs因其作为一种新的治疗方法受到广泛关注,但缺乏标准化的临床治疗方案,对ASCs作用机制研究尚不足,远期临床疗效有待观察,目前处于探索阶段,未在临床普及。
6 小结与展望
临床上错综复杂的肛瘘常累及多个间隙,用一种手术往往无法解决所有问题,需多种手术方式相结合。目前仍没有一种手术方式能完美地治愈肛瘘并保护肛门功能,临床工作中医师需要掌握各种手术的适应证和技术要点,选择患者获益最大化、自己擅长的手术方式进行。随着外科医师治疗理念的不断更新和改变,目前保留括约肌手术已成为一种趋势,可作为治疗复杂性肛瘘的一线选择。新的技术给患者带来了希望,但还需要更多的研究和长期随访数据来支持其可行性。
