Compritol®888 ATO 对双氯芬酸钠的缓释作用
2020-12-29平其能孙敏捷
常 梅,平其能,孙敏捷
(中国药科大学 药学院 药剂学教研室,江苏 南京 211198)
Compritol®888 ATO(山嵛酸甘油酯)是由山嵛酸(二十二烷酸)和甘油经酯化得到的多功能脂质辅料,喷雾干燥形成平均粒径为50 μm的球形颗粒,主要成分为山嵛酸单甘酯(12%~18%质量分数)、山嵛酸二甘酯(45%~54%质量分数)和山嵛酸三甘酯(28%~32%质量分数),其分子碳链长,疏水性好(亲水亲油平衡值HLB值约为2),广泛应用于食品、药品以及化妆品领域,其中在药剂学领域中的应用主要是作为片剂及胶囊剂的润滑剂[1-2]、缓释材料[3-5]、脂质载体传递系统[6-8]以及掩味[9]。
热熔挤出技术(HME)是近年来在制药行业逐渐兴起的制剂新技术,该技术实施过程中无溶剂参与,无须干燥,工序少[11],连续化的生产方式易于放大,并可实现在线监测[12]。热熔挤出技术在制剂工业中应用广泛,包括提高水难溶性药物的口服生物利用度、缓控释、掩味以及局部制剂的制备[13],已成为国外制备固体分散体的主导技术。
笔者以双氯芬酸钠(DS)为模型药物探究Compritol®888 ATO的缓释效果。首先,以溶解度参数(solubility parameters)为指标预测药物与载体的相容性。溶解度参数被定义为物质内聚能密度的平方根,广泛用于预测共晶[14]、固体分散体的形成[15]以及制剂中药物与辅料的相容性[16]。溶解度参数差异值小于7时,两物料很可能能混容,当差异值大于10时很可能不能混容,差异值在7~10的物质需要进一步考虑极性相互作用和氢键作用[17]。物质的溶解度参数值可通过试验法、计算法和计算机模拟来获取,目前广泛应用的是基团贡献计算法[18]。迄今已发展了多种基团贡献计算方法,这些方法在计算时均做了一系列假设,计算结果差异不大。双氯芬酸钠和Compritol®888 ATO的溶解度参数值分别是27.79[19]和18.89[17],两者的差异值为8.9,需进一步考虑相互作用。因此,笔者采用DSC实验的方法评价两者的相容性,由熔点相图判断所形成体系的类型。其次,分别利用傅里叶红外变换光谱(FT-IR)和粉末X线衍射(PXRD)探究两者之间的相互作用以及熔融冷却后是否有晶型变化。最后,探究Compritol®888 ATO对双氯芬酸钠释放的影响,并以市售双氯芬酸钠缓释片为参比,通过处方筛选与工艺优化得到体外释放一致的自制片。
1 材料与方法
1.1 试剂与仪器
双氯芬酸钠原料药(纯度99%),武汉远成共创科技有限公司;双氯芬酸钠缓释片(Voltaren-SR),瑞士诺华制药有限公司;Compritol®888 ATO,嘉法狮(上海)贸易有限公司;蔗糖,北京凤礼精求医药股份有限公司;聚乙烯吡咯烷酮(PVP)K90,德国巴斯夫有限公司;黄原胶,阿拉丁工业有限公司;SiO2(医药级,EY-CD1)、硬脂酸镁(医药级),安徽山河药用辅料有限公司;NaOH(分析纯),西陇化工股份有限公司;KH2PO4、NaH2PO4(分析纯),上海凌峰化学试剂有限公司;磷酸(分析纯),国药集团化学试剂有限公司;甲醇(色谱纯),美国TEDIA公司;其余试剂均为市售分析纯。
BSA 124S型分析天平,北京赛多利斯仪器系统有限公司;Netzsch DSC 204 F1 Phoenix 差示扫描热分析仪,Netzsch 公司;Nicolet Impact 410 型红外光谱仪,Thermo Fisher Scientific 公司;D8 Advance X 线衍射仪,Bruker 公司;TDP单冲压片机,上海天祥健台制药机械有限公司;YPD-300D型片剂硬度仪,上海黄海药检仪器有限公司;ZE-16型双螺杆热熔挤出机,ATS工业系统有限公司;ZRS-8G型智能溶出仪,天津市天大天发科技有限公司;LC-20AT型高效液相色谱仪,日本岛津公司;T6型新世纪紫外可见分光光度计,北京普析通用有限公司;PHS-3C型雷磁pH计,上海仪电科学仪器股份有限公司。
1.2 Compritol®888 ATO与双氯芬酸钠二元体系的研究
1.2.1 Compritol®888 ATO与双氯芬酸钠熔融物制备
按质量比称取不同比例(1∶ 5、1∶ 3、1∶ 2、1∶ 1、2∶ 1、3∶ 1、7∶ 1、10∶ 1和12∶ 1)的Compritol®888 ATO与双氯芬酸钠,过0.180 mm筛,数次混合均匀,置于80 ℃油浴中用研钵研磨混合10 min,趁热过0.850 mm筛并自然冷却到室温。
1.2.2 差示扫描量热分析(DSC)考察二者的相容性
取Compritol®888 ATO、双氯芬酸钠以及各比例熔融物3~5 mg置于铝坩埚中,用差示扫描量热仪进行检测,升温速率为 10 ℃/min,温度测定范围为室温~400 ℃。数据用 Origin Pro 2017处理。
1.2.3 粉末X线衍射(PXRD)检测固体分散体中药物的晶型
取Compritol®888 ATO、双氯芬酸钠以及各比例熔融物适量,采用Cu靶,波长为0.154 06 nm,管压40 kV,管流40 mA,步长0.02°,扫描速度2°/min,扫描范围2θ3°~40°。
1.2.4 傅里叶红外变换光谱分析(FT-IR)考察药物与载体的相互作用
取Compritol®888 ATO、双氯芬酸钠以及各比例熔融物适量,采用KBr压片法对样品进行处理,用傅里叶变换红外光谱进行检测,扫描范围为4 000~400 cm-1(cm-1为波数),扫描分辨率为4 cm-1。数据用OMNIC 8.0处理。
1.3 制备工艺中双氯芬酸钠的热稳定性考察
由于制备工艺涉及热的过程,因此需要考察药物的受热稳定性。参照《美国药典》(USP38-NF33)中双氯芬酸钠缓释片的含量检测方法,建立高效液相色谱条件:色谱柱为Welch Xtimate C8(4.6 mm×250 mm,5 μm),流动相为甲醇-NaH2PO4缓冲液(0.01 mol/L,磷酸调节至pH 2.5,两者体积比7∶ 3),检测波长为254 nm,流速为1.0 mL/min,柱温为30 ℃,进样体积为10 μL。
对照品溶液配制。精密称定双氯芬酸钠对照品100 mg于100 mL容量瓶中,用体积分数70%甲醇溶液稀释定容,配制成1 mg/mL的双氯芬酸钠溶液,作为储备液。精密移取5.0 mL储备液于10 mL容量瓶中,用70%甲醇溶液稀释定容,配制成0.5 mg/mL的双氯芬酸钠对照品溶液。
样品溶液配制。取适量Compritol®888 ATO与双氯芬酸钠(质量比1∶ 1)的熔融物(油浴80 ℃,熔融10 min),于研钵中研细,精密称取相当于双氯芬酸钠100 mg的粉末,置于200 mL容量瓶中。先加150 mL 70%甲醇溶液,水浴加热10 min,超声30 min,冷却至室温,用70%甲醇溶液稀释定容。将容量瓶冰浴并不时振摇使蜡质析出。取适量,趁冷过0.22 μm微孔滤膜,取续滤液,放置至室温,对其进行含量测定。
1.4 双氯芬酸钠缓释片体外释放度方法的建立
依照《美国药典》中双氯芬酸钠缓释片(diclofenac sodium extened-release tablet)项下溶出方法Test 1法,由于0.05 mol/L pH 6.8磷酸盐缓冲液的区分力比0.05 mol/L pH 7.5磷酸盐缓冲液好,因此选择900 mL的0.05 mol/L pH 6.8磷酸盐缓冲液为溶出介质筛选处方,温度(37±0.5)℃,选用桨法(加沉降篮),转速50 r/min,分别于1、2、3、5、8、10、12、16和24 h取样10 mL,同时补加等体积溶出介质。样品经过0.45 μm的微孔滤膜过滤,用溶出介质稀释至合适浓度,以溶出介质做空白,于276 nm处测定吸光度。同时,另取原料药对照品适量,精密配制成浓度约为15 μg/mL的样品作为对照,同法测定吸光度。按外标法计算累积释放度。
1.5 固体分散体制备工艺筛选
分别采用熔融法(油浴80 ℃,10 min)和热熔挤出法(工艺参数:转速16 r/min,温度62、64、64、64、64和62 ℃)制备Compritol®888 ATO与双氯芬酸钠的固体分散体,过0.850 mm筛制粒,冷却后压片,每片含双氯芬酸钠约100 mg。根据工艺便捷性及体外释放确定固体分散体制备工艺;将所得固体分散体粉碎过0.180 mm筛,与其他辅料过筛混合均匀,再加入硬脂酸镁总混合,采用9 mm的圆形浅凹冲压片,控制片剂硬度为7~9 kg,每片含双氯芬酸钠约100 mg,片质量约290 mg。
1.6 双氯芬酸钠缓释片处方筛选
以市售双氯芬酸钠缓释片Voltaren-SR为参比,探究处方中骨架材料Compritol®888 ATO用量和黏合剂用量对药物释放的影响,并采用正交设计筛选处方,最终得到体外释放与参比一致的自制缓释片。
2 结果与讨论
2.1 Compritol®888 ATO与双氯芬酸钠二元体系的研究结果
2.1.1 DSC分析考察二者相容性结果
Compritol®888 ATO(C888)、双氯芬酸钠以及各比例熔融物的DSC图谱见图1。由图1可知,Compritol® 888 ATO与双氯芬酸钠分别在69.0和288.3 ℃有单一的吸热峰,是各自的熔点峰。熔融物的DSC图谱中Compritol®888 ATO的熔点峰位置基本不变而双氯芬酸钠的熔点显著降低,并且随着双氯芬酸钠占比的下降而降低,表明两者可混容且可能存在某种相互作用。

图1 Compritol®888 ATO、双氯芬酸钠以及各比例熔融物的DSC图Fig.1 Differential scanning calorimetry thermograms of Compritol®888 ATO, DS and their melt mixtures
根据各比例熔融物的初熔点与终熔点建立Compritol®888 ATO与DS二元体系的熔点相图,结果见图2。由图2可知,Compritol®888 ATO与DS二元熔融物形成了偏晶体系。每个偏晶相图中上升的液相线对应于药物在载体熔融液中的溶解度曲线[20]。一般来说,随着温度升高,溶解在载体熔融液中的药物量增加,使得药物晶体在载体和纯药熔点之间的温度处完全消失[20]。DSC升温过程中双氯芬酸钠晶体在Compritol®888 ATO熔融液中发生溶解,破坏了双氯芬酸钠的晶体结构,导致晶格能降低,熔点下降。Compritol®888 ATO与DS的质量比为3∶ 1的图谱中DS的熔点峰非常小,这是因为DS含量少且部分溶解于Compritol®888 ATO熔融液中。
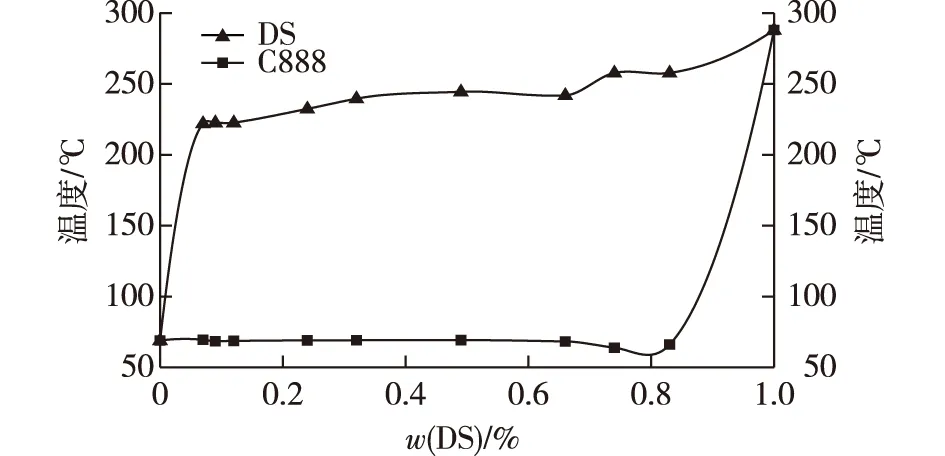
图2 通过DSC图谱得到Compritol®888 ATO与双氯芬酸钠二元体系的熔点相图Fig.2 Phase diagram of Compritol®888 ATO and DS binary systems by DSC
2.1.2 粉末X线衍射(PXRD)考察固体分散体中双氯芬酸钠的晶体状态
粉末X线衍射用于检测固体分散体中晶体的存在。Compritol®888 ATO、双氯芬酸钠以及各比例熔融物的PXRD图谱见图3。由图3可知,Compritol®888 ATO有2个特征峰,分别是位于21.27°的高强度峰和23.447°较小的峰,与文献[21]报道一致。DS的特征峰(2θ)位于6.664°、8.560°、11.265°、15.257°、19.928°、23.554°和27.132°。在Compritol®888 ATO与DS的质量比为1∶ 2 熔融物中,Compritol®888 ATO与DS的特征衍射峰仍然存在,且没有发生峰移位和新的峰出现,说明DS仍以晶体存在。Compritol®888 ATO与DS质量比为1∶ 1 熔融物中DS的特征峰消失,可能是因为DS部分溶解在Compritol®888 ATO中导致DS晶格缺陷,这与偏晶体系的特征相符。
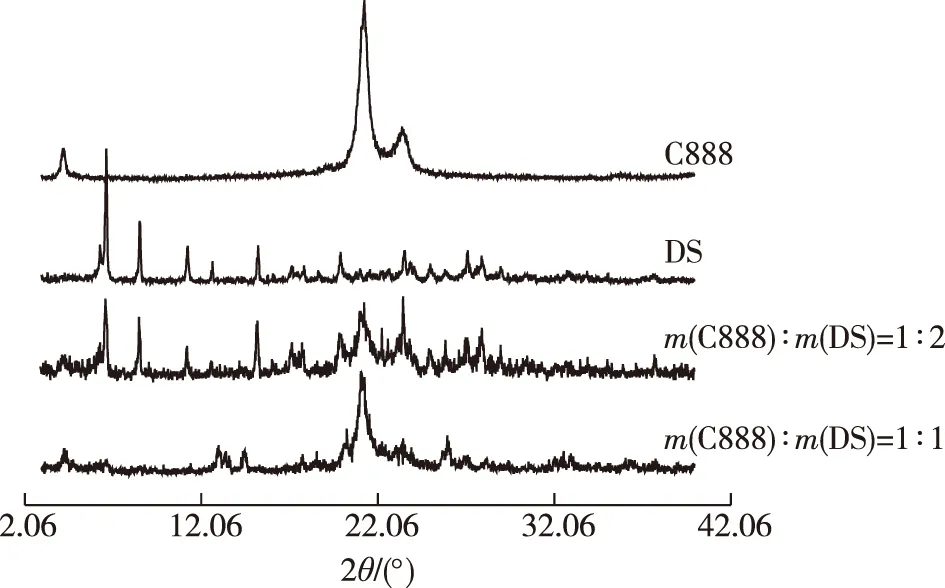
图3 由PXRD得到Compritol®888 ATO、双氯芬酸钠以及各比例熔融物的晶型图谱Fig.3 Powder X-ray diffraction patterms of Compritol® 888 ATO, DS and their melt mixtures
2.1.3 FT-IR分析固体分散体中药物与载体的相互作用
Compritol®888 ATO、双氯芬酸钠以及各比例熔融物的FT-IR图谱见图4。由图4可知,2 918、2 849 cm-1分别是Compritol®888 ATO中—CH2的反对称和对称伸缩振动,1 740 cm-1是酯羰基的伸缩振动。3 384 cm-1是双氯芬酸钠的—NH伸缩振动,位于3 256 cm-1处的吸收峰说明双氯芬酸钠分子间可能形成了氢键。Compritol®888 ATO与DS的质量比为2∶ 1物理混合物的图谱是Compritol®888 ATO与DS图谱的简单叠加,没有峰形和峰位变化,说明物理混合物没有发生相互作用。Compritol®888 ATO与DS的质量比为2∶ 1和1∶ 1熔融物在3 600~3 200 cm-1处出现了大的宽峰,掩盖了双氯芬酸钠的峰,可能是由于双氯芬酸钠的仲胺基与Compritol®888 ATO发生了更强的氢键缔和。Compritol®888ATO与DS的质量比为1∶ 2的图谱中仍然可以看到双氯芬酸钠的—NH伸缩振动和分子间氢键峰,这可能是因为双氯芬酸钠含量增加而导致在Compritol®888 ATO中溶解能力有限,双氯芬酸钠的峰响应更强烈。这与粉末X线衍射(PXRD)的结果一致。

图4 Compritol®888 ATO、双氯芬酸钠以及各比例熔融物的FT-IR吸收图谱Fig.4 Fourier transform infrared spectra of Compritol®888 ATO,DS and their melt mixtures
制剂中药物与辅料是否相容至关重要,研究固体分散体时应先一步考察药物与载体的相容性以及可能的相互作用,相容性的考察可以利用溶解度参数值也可利用DSC法。对药物与载体形成的二元体系进行DSC表征可得到一系列图谱,当两组分不可混容时,DSC图谱中两组分的熔点不受彼此的影响,这时两者的熔点相图是两条平行的直线。如果两组分的DSC图谱中熔点发生了变化,则可能形成了低共熔体系或偏晶体系。低共熔体系中两组分在某一比例时有最低共熔点,即形成了低共熔物,熔点相图中两条弯曲的曲线相交于最低共熔点。偏晶体系在冶金学中应用广泛,1980年由Kaur等[20]第一次在药学文献中进行报道。偏晶系统中一种组分作为离散的结晶颗粒存在于另一种组分中[23]。偏晶相图具有低共熔相图的形式,其中较低熔点组分的熔点曲线即固相线基本水平,固相线与弯曲的液相线没有交点。
2.2 制备工艺中双氯芬酸钠的热稳定性考察
采用高效液相色谱法考察工艺中双氯芬酸钠的热稳定性,对Compritol®888 ATO与双氯芬酸钠(质量比1∶ 1,80 ℃)的熔融物进行含量测定,结果见图5。由图5可知,双氯芬酸钠的平均含量为102.4%,符合90.0%~110.0%的标准,且无杂质峰出现,说明在工艺中双氯芬酸钠受热稳定,该偏晶体系中只有物理相互作用,无新物质生成。

图5 双氯芬酸钠对照品及样品溶液的HPLC图谱Fig.5 HPLC of DS and the molten material
2.3 固体分散体制备工艺筛选
利用FT-IR分析热熔(m(C888)∶m(DS)=1∶ 1)挤出产物,结果见图6。由图6可知,双氯芬酸钠的—NH伸缩振动峰和分子间氢键峰仍然存在,由于该条件下Compritol®888 ATO没有完全熔融,药物与载体间可能不存在相互作用。

图6 双氯芬酸钠和热熔挤出产物的FT-IR图谱Fig.6 FT-IR spectra of DS and hot melt extrudate
将两种工艺所得片剂在0.05 mol/L pH 6.8磷酸盐缓冲液中进行体外释放度考察,结果如图7所示。

图7 不同工艺及不同比例的双氯芬酸钠缓释片的体外释放曲线(pH 6.8,n=3)Fig.7 Dissolution profiles of compressed tablets in pH 6.8 buffer solutions with different amounts of Compritol®888 ATO and two kinds of processes(pH 6.8,n=3)
由图7可知,Compritol®888 ATO和DS形成了偏晶体系。此时,DS部分溶解于Compritol®888 ATO的熔融液中,导致DS晶体中分子间作用力减弱,理论上可在一定程度上加快药物的释放。但由图7的释放曲线可知,这种作用对药物释放的影响十分有限,只在前期略微加快了释放,没有显著性差别。此外,Compritol®888 ATO用量越多,药物释放越慢。这是因为Compritol®888 ATO碳链长,在片子中形成的致密的疏水性网络结构阻止了释放介质的渗透,从而延缓药物从骨架中的扩散。可见,Compritol®888 ATO形成的疏水性网络对药物的释放起决定性作用。与熔融法相比,热熔挤出工艺可使药物和骨架材料的混合效率更高,同时Compritol®888 ATO材料熔点低,非常适用于热熔挤出工艺。因此,考虑到工艺的便捷性以及偏晶体系对药物释放的影响,选择热熔挤出法作为固体分散体的制备工艺,并联合粉末直压制备缓释片。
2.4 双氯芬酸钠缓释片的释放度研究
对骨架材料的用量研究可知,当Compritol®888ATO与DS质量比约为1∶ 2时,药物中后期的释放与参比制剂一致,因此选择骨架材料用量为1∶ 2的比例探究黏合剂用量和致孔剂用量对药物释放的影响,并通过正交试验筛选出最优处方。采用热熔挤出联合粉末直压的工艺对表1中的3个处方制粒压片,所得片剂在0.05 mol/L pH 6.8磷酸盐缓冲液中进行释放度实验。图8是不同黏合剂用量的缓释片的释放曲线。黄原胶是一种由假黄单胞菌属发酵产生的单孢多糖,遇水快速水化形成的凝胶具有很强的黏性,有利于改善裂片情况,增强片子的稳健性。因此向处方中加入黄原胶并调整黏合剂PVP K90的用量,观察药物释放。由结果可知,在一定范围内药物释放速率随黏合剂PVP K90用量的增加而加快,这主要是因为PVP K90具有一定的表面活性。

图8 PVPK90用量对双氯芬酸钠缓释片释放效率的影响(pH 6.8,n=3)Fig.8 Effects of PVPK90 amounts on drug release ratio of DS compressed tablets in pH 6.8 buffer solutions (pH 6.8,n=3)
调整PVPK90与黄原胶用量,使药物释放与参比制剂Voltaren-SR相似。以相似因子为指标,采用IBM SPSS Statistics19设计二因素三水平正交试验,以填充剂蔗糖调节片子质量,考察黄原胶和PVPK90用量对药物体外释放的影响。各因素变量的信息表见表2。

表2 二因素三水平正交设计表Table 2 Design of subjects and factors
对正交试验结果进行方差分析,表3是多因素方差分析表。由表3可知,因素黄原胶的F=8.667,概率值(Sig.)P=0.035<0.05;因素PVPK90的F=0.498,概率值(Sig.)P=0.641>0.05,若按显著性水平α=0.05的检验水准,认为黄原胶对f2相似因子的影响显著,PVPK90影响不显著。按检验统计量F值的大小,黄原胶是主要因素,PVPK90是次要因素。边际均值估算结果见表4。由表4可知,黄原胶用量在4%时达到其最大均值82.000,PVPK90水平在25%时达到其最大均值71.000。因此,4%黄原胶、25%PVPK90是与原研相似的最优处方,释放曲线见图9,两因素的交互效应图见图10。由图9和图10可知,图中不同水平的3条折线均平行,表明这些因素之间不存在交互作用。

表3 多因素方差分析表Table 3 Analysis of variances of orthogonal experiments
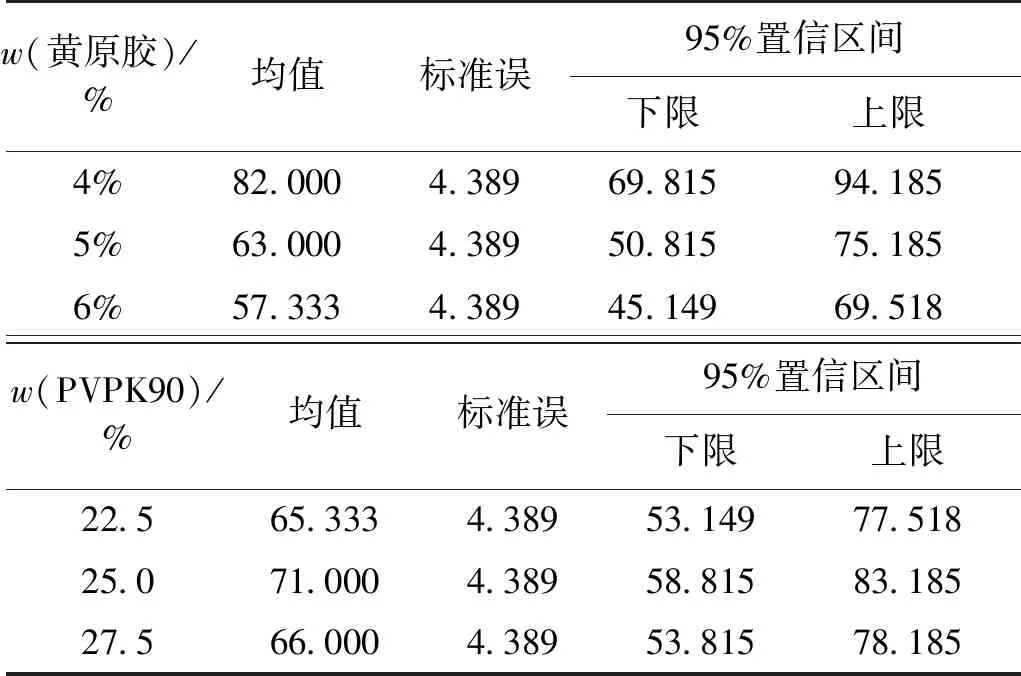
表4 估算边际均值结果Table 4 Results of estimated marginal means

图9 最优处方释放曲线(pH 6.8和pH 7.5)Fig.9 Release profiles of optimal formulation in pH 6.8 and 7.5 buffer solutions

图10 黄原胶与PVPK90的交互效应Fig.10 Profile plots of xanthangum and PVPK90
3 结论
利用一系列表征手段对载体与药物形成的二元体系考察得知,二者形成了偏晶体系。在DSC升温过程中,DS部分溶解在Compritol®888 ATO熔融液中,使药物的熔点降低。偏晶体系的形成使得药物分子间作用力减弱,在一定程度上应加快药物释放。但由研究结果可知,Compritol®888 ATO的疏水性对药物释放的影响更为显著。采用热熔挤出联合粉末直压的工艺制备双氯芬酸钠缓释片,考察了骨架材料、黏合剂和致孔剂用量对药物释放的影响,通过处方筛选与工艺优化得到与市售制剂体外释放一致的自制片。
