黄芪桂枝五物汤提取工艺的优化
2020-11-02佳王美慧谭镭詹雁徐超群
孙 兴 陈 旺 阮 佳王美慧谭 镭詹 雁徐超群∗
(1.成都中医药大学药学院, 四川 成都610075; 2.四川省中医药科学院, 四川 成都610041)
糖尿病周围神经病变是糖尿病常见并发症,具有高致残率和致死率[1],其症状表现和病机与中医“血痹” 范畴吻合[2],临床研究表明,黄芪桂枝五物汤对糖尿病周围神经病变有较好的治疗作用[3⁃4],由黄芪、桂枝、芍药、生姜、大枣配伍而成,具有补益气血、温通卫阳、散寒除痹之功效,被收录于国家中医药管理局发布的《古代经典名方目录(第一批)》[5]。
质量源于设计(QbD)的核心是确定制药过程中的关键质量属性和关键工艺参数,并通过建立工艺模型来确定关键工艺参数与关键质量属性的关系,以此构建设计空间,对药品进行质量控制[6⁃7]。本研究基于QbD 理念,应用风险分析、Box⁃Behnken 响应面法优化黄芪桂枝五物汤提取工艺,并建立相应设计空间,以期为该方进一步开发提供依据。
1 材料
Agilent 1260 高效液相色谱仪,配置Agilent 1260 DAD检测器、Agilent 1260 Infinity ⅡELSD 检测器(美国Agilent公司);UV⁃2401PC 紫外分光光度计(日本岛津公司);XS205 电子分析天平(瑞士梅特勒⁃托利多公司);SB⁃5200D 超声波清洗机(宁波新芝生物科技股份有限公司);ZDHW 调温电热套(北京中兴伟业仪器有限公司)。黄芪甲苷(110781⁃201717)、D⁃无水葡萄糖(110833⁃201508)对照品均购于中国食品药品检定院;芍药苷(17102709)对照品购于四川省维克奇生物科技有限公司。黄芪(批号1805070)、桂枝(批号1805124)、白芍(批号1806008)、大枣(批号1806141)均购于四川新荷花饮片股份有限公司,生姜购于成都荷花池中药材市场,经四川省中医药科学院舒光明研究员鉴定为正品,符合2015 版《中国药典》一部规定。
2 方法与结果
2.1 提取液制备 按照《古代经典名方目录(第一批)》中黄芪桂枝五物汤的处方组成及汉代剂量换算[8⁃9],称取黄芪41.4 g、桂枝41.4 g、白芍41.4 g、生姜41.4 g、大枣12 枚,按照一定参数进行提取,趁热滤过,减压浓缩并定容至100 mL 量瓶中,即得。
2.2 黄芪甲苷含有量测定
2.2.1 色谱条件 ZORBAX SB⁃C18色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈⁃水(33 ∶67);体积流量1.0 mL/min;柱温30 ℃;进样量20 μL,蒸发光散射检测器(ELSD);漂移管温度45 ℃;氮气体积流量1.0 mL/min。理论塔板数以黄芪甲苷计不低于5 000,分离度>1.5,阴性无干扰,色谱图见图1。
2.2.2 对照品溶液制备 精密称取黄芪甲苷对照品适量,加甲醇制成该成分质量浓度为0.98 mg/mL 的溶液,即得。
2.2.3 供试品溶液制备 精密量取“2.1” 项下提取液25 mL,加入40 mL 水饱和正丁醇萃取4 次,合并正丁醇液,氨试液充分洗涤2 次,每次50 mL,弃去氨液,蒸干,残渣用甲醇溶解并转移至5 mL 量瓶中,即得。
2.2.4 线性关系考察 取对照品溶液,甲醇依次稀释成0.098、0.196、0.392、0.588、0.784 mg/mL,各精密吸取20 μL,在“2.2.1” 项色谱条件下进样测定。以进样量对数值为横坐标(X),峰面积对数值为纵坐标(Y)进行回归,得方程为Y=1.709 9X+1.592 5(r=0.999 6),在0.098~0.784 mg/mL 范围内线性关系良好。
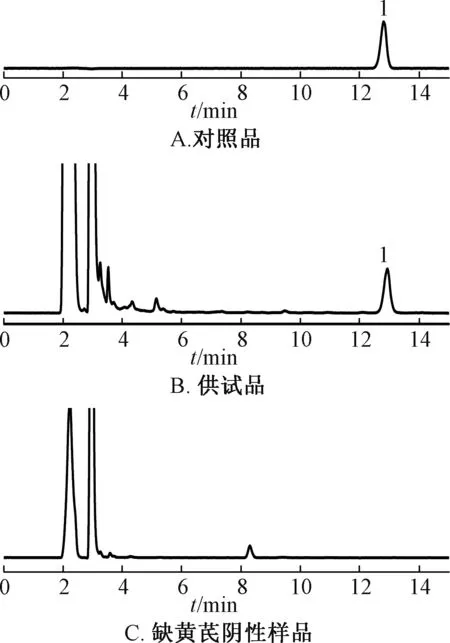
图1 黄芪甲苷HPLC 色谱图
2.2.5 精密度试验 取同一份供试品溶液,在“2.2.1”项色谱条件下进样测定6 次,测得黄芪甲苷峰面积RSD 为1.85%,表明仪器精密度良好。
2.2.6 稳定性试验 取同一份供试品溶液,于0、2、4、8、12、24 h 在“2.2.1” 项色谱条件下进样测定,测得黄芪甲苷峰面积RSD 为1.54%,表明溶液在24 h 内稳定性良好。
2.2.7 重复性试验 取同一份提取液,按“2.2.3” 项下方法平行制备6 份供试品溶液,在“2.2.1” 项色谱条件下进样测定,测得黄芪甲苷含有量RSD 为1.12%,表明该方法重复性良好。
2.2.8 加样回收率试验 精密量取黄芪甲苷含有量已知的提取液25 mL,共6 份,精密加入对照品溶液(含黄芪甲苷0.98 mg/mL)3 mL,按“2.2.3” 项下方法制备供试品溶液,在“2.2.1” 项色谱条件下进样测定,测得黄芪甲苷平均加样回收率为99.11%,RSD 为0.98%。
2.3 芍药苷、毛蕊异黄酮葡萄糖苷、肉桂酸含有量测定
2.3.1 色谱条件 ZORBAX SB⁃C18色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈(A)⁃0.1%甲酸(B),梯度洗脱(0~26 min,12%~13% A;26~30 min,13% A;30~48 min,13%~24% A;48~58 min,24% A;58~65 min,24%~44%A);体积流量1 mL/min;柱温30 ℃;DAD 检测器,检测波长230 nm(0~25 min,芍药苷)、260 nm(25~50 min,毛蕊异黄酮葡萄糖苷)、285 nm(50~65 min,肉桂酸);进样量10 μL;理论塔板数以各成分计不低于5 000,分离度>1.5,阴性无干扰,色谱图见图2。

图2 各成分HPLC 色谱图
2.3.2 对照品溶液制备 精密称取芍药苷、毛蕊异黄酮葡萄糖苷、肉桂酸对照品适量,置于量瓶中,甲醇制成三者质量浓度分别为7.570、1.156、1.282 mg/mL 的贮备液,分别精密吸取2、1、1 mL 至10 mL 量瓶中,甲醇定容至刻度,摇匀,即得。
2.3.3 供试品溶液制备 精密量取“2.1” 项下提取液2 mL 至10 mL 量瓶中,加 入50% 甲醇7 mL 超声处 理10 min,放冷,50%甲醇定容,摇匀,即得。
2.3.4 线性关系考察 精密量取对照品溶液0.2、0.5、1、2、4 mL 至5 mL 量瓶中,甲醇制成不同质量浓度,在“2.3.1” 项色谱条件下进样测定。以溶液质量浓度为横坐标(X),峰面积为纵坐标(Y)进行回归,得方程分别为芍药苷Y=13 074X-262.67(r=0.999 9),线性范围60.560~1 211.200 μg/mL;毛蕊异 黄酮葡 萄糖苷Y=27 179X-0.127 6(r=0.999 9),线性范 围4.624~92.480 μg/mL;肉桂酸Y=82 630X-42.623(r=0.999 9),线性范围5.124~102.480 μg/mL。
2.3.5 精密度试验 取对照品溶液适量,在“2.3.1” 项色谱条件下进样测定6 次,测得芍药苷、毛蕊异黄酮葡萄糖苷、肉桂酸峰面积RSD 分别为0.28%、0.17%、0.27%、表明仪器精密度良好。
2.3.6 稳定性试验 取同一份供试品溶液,于0、2、4、8、12、24 h 在“2.3.1” 项色谱条件下进样测定,测得芍药苷、毛蕊异黄酮葡萄糖苷、肉桂酸峰面积RSD 分别为0.18%、0.12%、0.67%,表明溶液在24 h 内稳定性良好。
2.3.7 重复性试验 取同一份提取液,按“2.3.3” 项下方法平行制备6 份供试品溶液,在“2.3.1” 项色谱条件下进样测定,测得芍药苷、毛蕊异黄酮葡萄糖苷、肉桂酸含有量RSD 分别为0.90%、0.46%、0.38%,表明该方法重复性良好。
2.3.8 加样回收率试验 精密量取各成分含有量已知的提取液1 mL,共6 份,精密加 入对照 品溶液(含芍药 苷7.570 mg/mL、毛蕊异黄酮葡萄糖苷0.115 6 mg/mL、肉桂酸0.256 4 mg/mL)各0.5 mL,按“2.3.3” 项下方法制备供试品溶液,在“2.3.1” 项色谱条件下进样测定,测得芍药苷、毛蕊异黄酮葡萄糖苷、肉桂酸平均加样回收率分别为100.15%、99.87%、99.91%,RSD 分别为1.02%、1.43%、1.51%。
2.4 总多糖含有量测定
2.4.1 对照品溶液制备 精密称取D⁃葡萄糖对照品适量,加水制成该成分质量浓度为1.420 2 mg/mL 的溶液,即得。
2.4.2 供试品溶液制备 精密量取“2.1” 项下提取液5 mL,加水定容至10 mL,摇匀,加入Sevag 试剂2 mL,振摇后离心收集上清液,重复操作至无沉淀,取上清液2 mL,加入5 倍量乙醇,冰箱中静置过夜后离心(4 000 r/min)10 min,沉淀加水溶解并转移至50 mL 量瓶中,摇匀,精密量取5 mL 于50 mL 量瓶中,加水至刻度,摇匀,即得。
2.4.3 线性关系考察 精密吸取0.5、1、1.5、2、2.5 mL对照品溶液,加水定容至50 mL 量瓶中,各取2 mL 至具塞试管中,加入5%苯酚溶液1 mL,混匀,迅速加入5 mL 浓硫酸,混匀,于80 ℃水浴中保温15 min,取出,置于冰水中冷却,以相应试剂为空白,在485 nm 波长处测定吸光度。以吸光度为纵坐标(A),溶液质量浓度为横坐标(X)进行回归,得方程为A=0.017 6X+0.017 1(r=0.999 1),在14.20~71.02 μg/mL 范围内线性关系良好。
2.4.4 精密度试验 取同一份供试品溶液,按“2.4.3”项下方法测定吸光度,测得其RSD 为0.10%,表明仪器精密度良好。
2.4.5 稳定性试验 取同一份供试品溶液,于10、20、30、60、90 min 按“2.4.3” 项下方法测定吸光度,测得其RSD 为0.50%,表明溶液在90 min 内稳定性良好。
2.4.6 重复性试验 精密量取供试品溶液6 份,按“2.4.3” 项下方法测定吸光度,测得其RSD 为1.82%,表明该方法重复性良好。
2.4.7 加样回收率试验 精密量取D⁃葡萄糖含有量已知的供试品溶液、对照品溶液各1 mL,按“2.4.3” 项下方法测定吸光度,测得总多糖平均加样回收率为98.94%,RSD为1.32%。
2.5 干膏率、提取率测定 精密吸取提取液10 mL,置于干燥至恒重的蒸发皿中,水浴蒸干,105 ℃下干燥至恒重,精密称定质量,计算干膏率,公式为干膏率=(干膏质量/处方药材质量)×100%。按“2.2” 至“2.4” 项下方法分别测定黄芪甲苷、毛蕊异黄酮葡萄糖苷、芍药苷、肉桂酸、总多糖含有量,计算提取率,公式为提取率=(各成分含有量/处方药材质量)×100%。
2.6 综合评分计算 首先按照表1 评分标准比较各指标相对重要性,构建成对比较的优先判断矩阵,见表2。计算初始权重,公式为,再计算权重W,公式为,测得黄芪甲苷、毛蕊异黄酮葡萄糖苷、总多糖、芍药苷、肉桂酸提取率及干膏率的权重系数分别 为0.290 0、0.290 0、0.172 6、0.101 6、0.101 6、0.044 1。参考文献[11],测得一致性比列因子CR(CI/RI,CI 为一致性指标,RI 为平均一致性指标)为0.028 9<0.10,表明判断矩阵具有一致性,权重系数合理有效。最后计算综合评分,公式为综合评分= [(黄芪甲苷提取率/最大提取率)×0.290 0+(毛蕊异黄酮葡萄糖苷提取率/最大提取率)×0.290 0 +(总多糖提取率/最大提取率)×0.172 6+(芍药苷提取率/最大提取率)×0.101 6+(肉桂酸提取率/最大提取率)×0.101 6+(干膏率/最大干膏率)×0.044 1]×100。

表1 各层次评分标准

表2 指标成对比较的优先判断矩阵
2.7 风险评估 根据生产经验结合鱼骨图分析确定影响提取工艺的潜在关键工艺参数,见图3,再采用失效模式与效应(FMEA)对其进行定量风险分析,从严重程度(S)、发生频度(P)、检查的难易程度(D)3 个方面进行评估[12],评分原则见表3,最后根据评分结果计算各因素风险优先度(RPN,S×P×D),大于10 的为高风险因素,可被识别为关键工艺参数[13],结果见表4。由此可知,提取次数、提取时间、溶剂用量为关键工艺参数。

图3 提取工艺鱼骨图

表3 S、P、D 评分原则
2.8 Box⁃Behnken 响应面法 按处方比例称取药材3 份,加入1 000 mL 水,室温下放置2 h,发现在70 min 时药材全部浸润,吸液率约为药材质量的1 倍,因此在第1 次提取时多加1 倍量水浸泡1 h。
采用Box⁃Behnken 响应面法,选择提取时间(A)、提取次数(B)、溶剂用量(C)作为影响因素,黄芪甲苷、毛蕊异黄酮葡萄糖苷、芍药苷、肉桂酸、总多糖提取率及干膏率作为评价指标,按“2.6” 项下公式计算综合评分,结果见表5。通过Design⁃Expert 8.0 软件进行二次多项式拟合,得到回归方程为综合评分=75.63 +3.03A+19.07B+4.96C-0.14AB+1.01AC+2.55BC-2.26A2-6.13B2-2.03C2,R2=0.964 4,Radj2=0.918 7,表明模型具有良好的拟合度。
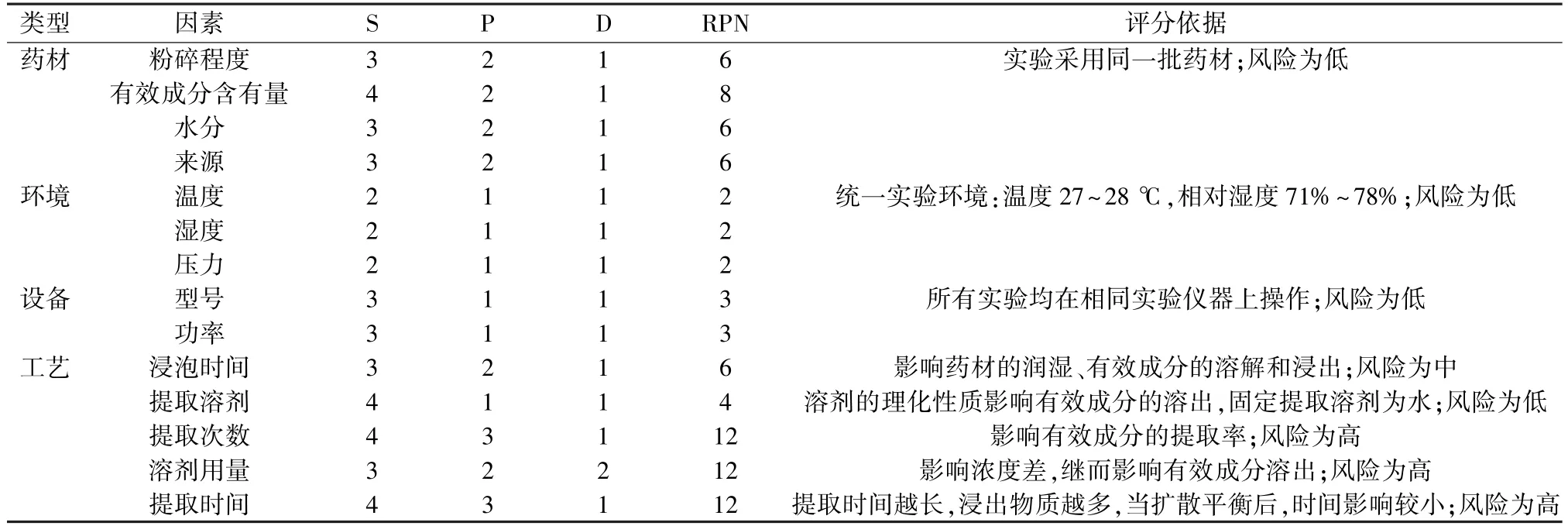
表4 FMEA 风险评估结果
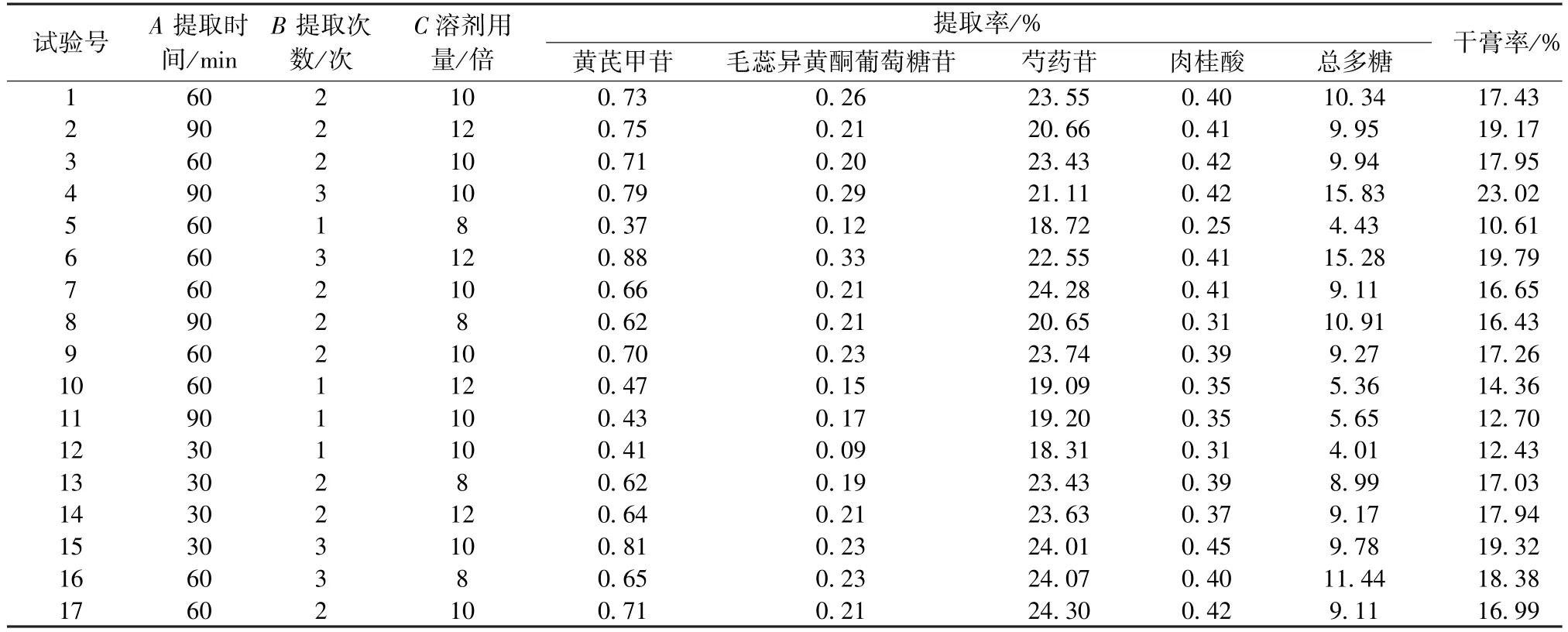
表5 试验设计及结果
方差分析见表6。由此可知,模型P<0.01,失拟项P>0.05,表明模型具有显著意义;信噪比S/N>4,表明模型预测精密度良好;各因素影响程度依次为B>C>A,其中因素C、B2有显著影响(P<0.05),B有极显著影响(P<0.01)。

表6 方差分析
响应面分析见图4。由此可知,因素B对综合评分的影响程度大于A、C,与表6 一致;在一定范围内提取次数越多,提取时间越长,溶剂用量越大,综合评分越高。
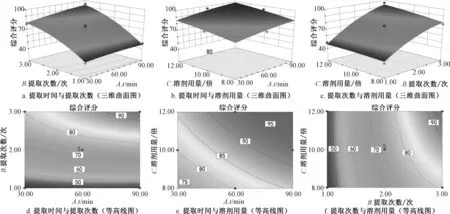
图4 各因素响应面图
通过Design⁃Expert 8.0 软件,根据产品质量要求设定综合评分目标范围大于85,建立提取工艺的设计空间,由于预测值与真实值之间存在一定差异,故加入α =0.05 的置信空间以提高准确度[14],结果以Overlay Plot 展示,见图5。由此可知,优化区域内的点均满足设计要求,而风险区域内的点有5%不满足。
选取5 个区域内的实验点进行验证试验,结果见表7。由此可知,预测值与实验值的偏差均小于5%,表明该模型预测能力良好;设计空间、置信区间内的点均能满足预期目标,而设计空间外的点均不满足,表明该设计合理可行。基于生产成本考虑,确定提取工艺的最优设计空间为提取时间60~78 min,提取次数3 次,溶剂用量10.5~11.5 倍。
3 讨论
3.1 评价指标筛选 在黄芪桂枝五物汤中,黄芪、白芍主要活性成分黄芪甲苷、毛蕊异黄酮葡萄糖苷、芍药苷均有增加胰岛素敏感性、降血糖、神经保护作用,可用于治疗糖尿病及其并发症[15⁃19];肉桂酸、桂皮醛为桂枝主要有效成分,具有降血糖、抗炎等作用,但水煎液中其含有量低于万分之一,故未列入考察指标,而肉桂酸含有量相对较高而稳定,故将其作为指标成分[20⁃21];多糖具有抗肿瘤、降血糖、改善胰岛素抵抗等作用[22],方中黄芪、桂枝、白芍和大枣均含该成分,故将其纳入研究。另外,干膏率在一定程度上可反映复方提取效果。因此,本实验选择黄芪甲苷、毛蕊异黄酮葡萄糖苷、芍药苷、肉桂酸、总多糖提取率及干膏率作为评价指标。

表7 验证试验结果(n=3)

图5 提取工艺设计空间
3.2 指标权重确定 中药复方是通过多成分来共同发挥作用,与单一指标相比,多指标综合评价更能反映其整体性,并且关键在于如何确定各指标权重。AHP 法是一种将定性与定量相结合,用于解决多目标问题的分析方法[23],故本实验通过该方法结合黄芪桂枝五物汤配伍规律来确定各指标权重系数,以保证综合评分的科学性和合理性。
3.3 提取工艺优化 QbD 理念是从设计层面确保产品质量,实际生产过程中可根据原料药材质量波动范围来调整工艺参数,从而提高产品一致性。基于该理念,本实验首先通过查阅文献结合前期研究来获得黄芪桂枝五物汤提取工艺的关键质量属性,以鱼骨图、FMEA 确定关键工艺参数,AHP 法确定各指标权重,计算综合评分,再采用Box⁃Behnken 响应面法建立提取工艺的数学模型,最后根据产品质量要求建立设计空间。
