环维黄杨星D 包合物微孔渗透泵控释片的制备及处方优化
2020-11-02王玉华杨海燕郝海军
王玉华 杨海燕 郝海军
(1.郑州卫生健康职业学院, 河南 郑州450199; 2.河南中医药大学第一附属医院, 河南 郑州450100;3.上海雷允上药业有限公司, 上海201401)
环维黄杨星D 是从黄杨科植物小叶黄杨Buxus sinica(Rehd.Et Wils)Cheng 中提取得到的一种生物碱,具有保护心肌、改善心脏功能、降低心肌耗氧量、增强心肌收缩力等药理作用[1],临床主要用于心脑血管疾病的治疗[2]。市场上其相关制剂主要是黄杨宁片,但患者每次需服用2~4 片,每天3 次,容易导致顺应性变差,故有必要开发其缓控释制剂。
前期药动学研究结果显示[3⁃4],环维黄杨星D半衰期为3.3~4.9 h,较为适中,而且该成分在胃肠道各段均有吸收[5],适合制成缓控释制剂,其口服吸收生物利用度为32%[3],而制成控释片、微丸后均有一定程度的提高[4,6]。姚琳等[4]制备了环维黄杨星D 缓释滴丸,但其释药方式为非匀速[7];虽然其双层渗透泵控释片[8]释药匀速,但制备工艺复杂[9];梁涛等[6]制备了其单层渗透泵控释片,但在12 h 内累积释放度仅为70%,可能与该成分溶解度较差有关。本研究采用包合技术提高环维黄杨星D 溶解度[10],并进一步将其制成微孔渗透泵控释片[11⁃12],该剂型无需打孔,工艺大大简化,再通过正交试验优化处方,以期为相关制剂革新提供借鉴。
1 材料
1.1 仪器 AB204⁃E 型电子分析天平(瑞士Mettler⁃Toledo 公司);Agilent 1260 型高效液相色谱仪(美国Agilent 公司);Edi⁃S10 型超纯水系统(上海和泰仪器有限公司);V5 型实验室粉体混匀机(广州康诺医药机械有限公司);RE⁃52AB 型旋转蒸发仪(上海亚荣生化仪器厂);HWS⁃12 型智能水浴锅(上海一恒科技有限公司);TDP 型单冲压片机(上海第一制药机械厂);DZF 型真空干燥箱(北京中科仪器有限公司);SHZ⁃D 型循环水式真空泵(巩义市予华仪器有限责任公司);ZRS⁃8型智能溶出试验仪(天津大学无线电厂);WKY⁃200 型小型包衣设备(沈阳明若轩制药设备有限公司)。
1.2 试剂与药物 环维黄杨星D 原料药(批号181022,纯度98%,南京青泽医药科技公司);环维黄杨星D 对照品(批号110888⁃201503,纯度99.8%,中国食品药品检定研究院)。黄杨宁片(批号190520,开封明仁药业有限公司)。羟丙基⁃β⁃环糊精(HP⁃β⁃CD,批号201805⁃3,淄博千汇生物科技有限公司);氯化钠(批号180614⁃8H,廊坊天科生物科技有限公司);聚氧乙烯(PEO,分子量1.05×105Da,上海甄准生物科技有限公司);醋酸纤维素(CA,含54.5%~56.0% 结合酸,国药集团化学试剂有限公司);乳糖(批号201710,郑州万顺食品科技有限公司);聚乙二醇400[PEG 400,批号72000050,巴斯夫(中国)有限公司];硬脂酸镁(批号150617,辽宁奥达制药有限公司);邻苯二甲酸二乙酯(批号170515,泰州市常佳化工有限公司)。
2 方法与结果
2.1 环维黄杨星D 含有量测定
2.1.1 色谱条件 Agilent C18色谱柱(250 mm×4.6 mm,5 μm);流动相0.01 mol/L 磷酸二氢钾与0.01 mol/L 庚烷磺酸钠等量混合溶液(稀磷酸调pH 至 3.5)⁃乙 腈(75 ∶ 25);体积流 量1.0 mL/min;柱温30 ℃;检测波长206 nm;进样量20 μL。
2.1.2 对照品溶液制备 称取环维黄杨星D 对照品10 mg,溶 于50 mL 乙腈中,作为贮备液(200 μg/mL),流动相依次稀释至10、5、2.5、1、0.5、0.05 μg/mL,即得。
2.1.3 供试品溶液制备
2.1.3.1 包合物 取包合物粉末约20 mg,加入流动相超声处理5 min 后定容至100 mL,0.45 μm微孔滤膜过滤,精密量取1 mL 滤液,置于10 mL量瓶中,流动相定容至刻度,即得。
2.1.3.2 微孔渗透泵控释片 取10 片微孔渗透泵控释片,研细,称取粉末约0.4 g,置于100 mL 量瓶中,加水定容至刻度,0.45 μm 微孔滤膜过滤,精密量取1 mL 滤液,置于10 mL 量瓶中,流动相定容至刻度,即得。
2.1.4 线性关系考察 取“2.1.2” 项下对照品溶液适量,在“2.1.1” 项色谱条件下进样测定。以溶液质量浓度为横坐标(X),峰面积为纵坐标(Y)进行回归,得方程为Y=21.250 7X-3.141 5(r=0.999 7),在0.05~10 μg/mL 范围内线性关系良好。
2.1.5 方法学考察 取“2.1.2” 项下0.05、5、10 μg/mL 对照品溶液适量,在“2.1.1” 项色谱条件下进样测定6 次,测得环维黄杨星D 峰面积RSD 分别为1.02%、0.31%、0.48%,表明仪器精密度良好。取“2.1.3” 项下2 种供试品溶液适量,于0、2、4、6、8、12 h 在“2.1.1” 项色谱条件下进样测定,测得环维黄杨星D 峰面积RSD分别为0.84%、1.07%,表明溶液在12 h 内稳定性良好。取包合物及其微孔渗透泵控释片适量,按“2.1.3” 项下方法各平行制备6 份供试品溶液,在“2.1.1” 项色谱条件下各进样测定6 次,测得环维黄杨星D 含有量RSD 分别为1.54%、1.21%,表明该方法重复性良好。取环维黄杨星D 包合物微孔渗透泵控释片适量,羟丙基⁃β⁃环糊精溶液制成3、4、5 μg/mL 溶液,每个质量浓度平行3 份,在“2.1.1” 项色谱条件下各进样测定3 次,测得环维黄杨星D 平均加样回收率分别为98.82%、100.19%、99.33%,RSD 分别为1.07%、0.64%、0.75%。取不含环维黄杨星D 包合物的空白微孔渗透泵控释片适量,按“2.1.3.2” 项下方法制备空白供试品溶液,以其稀释“2.1.2” 项下10 μg/mL对照品溶液至5、6、7 μg/mL,每个质量浓度平行3 份,在“2.1.1” 项色谱条件下各进样测定3 次,测得环维黄杨星D 平均加样回收率分别为98.49%、99.90%、99.31%,RSD 分别为1.82%、1.36%、1.55%,表明空白辅料对制剂制备无明显影响。
2.2 环维黄杨星D 包合物制备 参考文献[13⁃14]报道。称取环维黄杨星D 0.5 g,溶于80 mL无水乙醇中;称取羟丙基⁃β⁃环糊精2.1 g,溶于50 mL蒸馏水中,置于磁力搅拌器上,50 ℃下缓慢将环维黄杨星D 乙醇溶液滴加到羟丙基⁃β⁃环糊精溶液中,继续搅拌3 h 后抽滤,-75 ℃下冷冻24 h,再置于-35 ℃真空冷冻干燥机中干燥48 h,即得,其平均包封率为98.26%,环维黄杨星D 质量分数为0.187%,该成分溶解度由36.2 μg/mL 提高至386.8 μg/mL。
2.3 环维黄杨星D 包合物微孔渗透泵控释片制备
取32 mg/片环维黄杨星D 包合物及20 mg/片NaCl(促渗剂)、PEO、乳糖等辅料,采用等量递增法进行混匀,以70%乙醇为粘合剂制备片芯软材,过20 目筛,18 目筛整粒后干燥,加入1%硬脂酸镁作为润滑剂,压制片芯(硬度45~65 N)。取醋酸纤维素、PEG 400、邻苯二甲酸二乙酯适量,溶于丙酮⁃无水乙醇混合溶液(两者比例为9 ∶1,超声2 min 混匀)中形成包衣液,密封备用。设定包衣锅温度为35 ℃,转速为30 r/min,倾角调整为30°,体积流量为5 mL/min,将片芯置于包衣锅中进行包衣,再置于35 ℃鼓风干燥箱中固化3 h,即得,按上述处方量取样,共制备100 片。不加辅料,同法制备空白辅料渗透泵控释片。
2.4 累积释放度测定 采用转篮法。设定释放介质为900 mL 超纯水,溶出仪温度为(37±0.5)℃,转篮转速为100 r/min。溶出杯内外温度达到平衡后,于0、1、2、4、6、8、10、12 h 各自动取样3 mL(自动补加3 mL 释放介质),8 000 r/min 离心15 min 后取20 μL,在“2.1.1” 项色谱条件下进样测定,计算累积释放度。
2.5 单因素试验 一般来说,口服药物在胃肠道吸收部位的转运时间为10~12 h,故本实验设定控释时间为12 h。
2.5.1 PEO 用量 取32 mg/片环维黄杨星D 包合物、20 mg/片NaCl,并加入乳糖至400 mg/片以制备片芯。固定PEG 400 用量为30%(占醋酸纤维素用量的比例),增塑剂(邻苯二甲酸二乙酯)用量为20%(占醋酸纤维素用量的比例),配制包衣液后将片芯置于包衣锅中,设定包衣增重为5%,考察PEO 用量4、6、8 mg/片对恒速释放和累积释放度的影响,结果见图1。由此可知,当PEO 用量为4 mg/片时释药线性稍差,累积释放度仅为61.5%;为6、8 mg/片时释药线性良好,以8 mg/片累积释放度最高,达到88.4%。

图1 PEO 用量对累积释放度的影响Fig.1 Effect of PEO consumption on accu⁃mulative release rate
2.5.2 PEG 400 用量 取32 mg/片环维黄杨星D包合物、8 mg/片PEO、20 mg/片NaCl,并加入乳糖至400 mg/片以制备片芯。固定增塑剂用量为20%,配制包衣液后将片芯置于包衣锅中,设定包衣增重为5%,考察PEG 400 用量25%、30%、35%对恒速释放和累积释放度的影响,结果见图2。由此可知,随着PEG 400 用量增加,累积释放度逐渐升高,为30%时最高,但释药线性不理想;为20%或25%时释药线性理想,但累积释放度稍低。
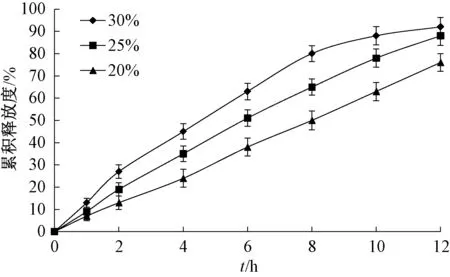
图2 PEG 400 用量对累积释放度的影响Fig.2 Effect of PEG 400 consumption on accumulative release rate
2.5.3 增塑剂(邻苯二甲酸二乙酯)用量 邻苯二甲酸二乙酯在包衣液中可提高包衣膜韧度,防止释药过程中微孔渗透泵控释片破裂,故本实验选择其作为增塑剂。取32 mg/片环维黄杨星D 包合物、8 mg/片PEO、20 mg/片 NaCl,并加入 乳糖至400 mg/片以制备片芯。固定PEG 400 用量为25%,配制包衣液后将片芯置于包衣锅中,设定包衣增重为5%,考察增塑剂用量15%、20%、25%对恒速释放和累积释放度的影响,结果见图3。由此可知,当增塑剂用量为15%时累积释放度最高,但释药线性不理想,并出现包衣膜破裂现象;为20%或25%时渗透泵控释片累积释放度稍低,但释药线性理想,而且其外形完整,无破裂现象。
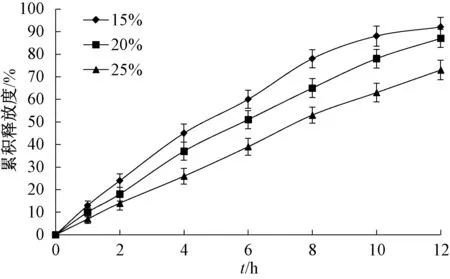
图3 增塑剂用量对累积释放度的影响Fig.3 Effect of plasticizer consumption on accumulative release rate
2.5.4 包衣增重 取32 mg/片环维黄杨星D 包合物、8 mg/片PEO、20 mg/片NaCl,加入乳糖至400 mg/片以制备片芯。固定PEG 400 用量为25%,增塑剂用量为20%,配制包衣液后将片芯置于包衣锅中,考察包衣增重3%、5%、7%对恒速释放和累积释放度的影响,结果见图4。由此可知,3 种包衣增重下释药线性均较好,为3%时累积释放度最高。

图4 包衣增重对累积释放度的影响Fig.4 Effect of coating weight gain on accumulative release rate
2.6 正交试验 在单因素试验基础上,确定因素水平分别为PEO 用量(A)7、8、9 mg/片,PEG 400 用量(B)28%、25%、22%,增塑剂用量(C)22%、20%、18%,包衣增重(D)2%、3%、4%,在兼顾释药线性的前提下测定渗透泵控释片在2 h(L1,考察有无时滞或突释)、6 h(L2,中间阶段释药情况)、12 h(L3,释药是否完全)内的累积释放度,计算综合评分L,公式为L=|L1-0.2 |×100×1+|L2-0.5 | ×100×1+|L3-0.9 | ×100×2。结果见表1,方差分析见表2。

表1 试验设计与结果Tab.1 Design and results of tests
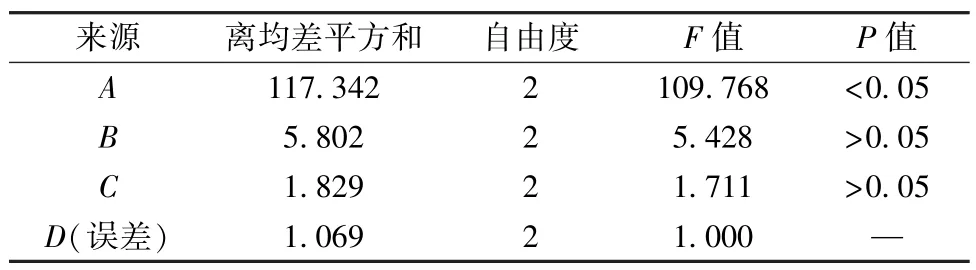
表2 方差分析Tab.2 Analysis of variance
由表1 可知,各因素影响程度依次为A>B>C>D;由表2 可知,因素A具有显著影响(P<0.05)。因此,确定最优处方为A2B2C3D2,即PEO 用量8 mg/片,加入乳糖至400 mg/片,PEG 400 用量25%,增塑剂(邻苯二甲酸二乙酯)用量18%,包衣增重3%,置于35 ℃鼓风干燥箱中固化3 h。
2.7 验证试验及模型拟合 按照优化处方平行制备3 批环维黄杨星D 包合物微孔渗透泵控释片,测定其释药线性和累积释放度,结果见图5,可知该处方重复性良好,12 h 内平均累积释放度为90.82%,符合2015 年版《中国药典》 9013 项下缓释、控释和迟释制剂指导原则规定(累积释放度达到90%以上),综合评分为17.8。
分别采用Higuchi 方程、一级方程、零级方程对环维黄杨星D 包合物微孔渗透泵控释片体外释药进行拟合,其中M∞为∞时累积释放度,t为时间,Mt为t时间点累积释放度,Mt/M∞为t时间点累积释放率,k为常数。结果,3 种方程分别为Mt/M∞=0.250 7t1/2-0.060 1(R2=0.924 2)、In(1-Mt/M∞)=-0.187 5t+0.191 2(R2=0.936 4)、Mt/M∞=0.076 6t+0.024 3(R2=0.992 4),可知该制剂体外释药最符合零级方程,即以恒速方式释放。
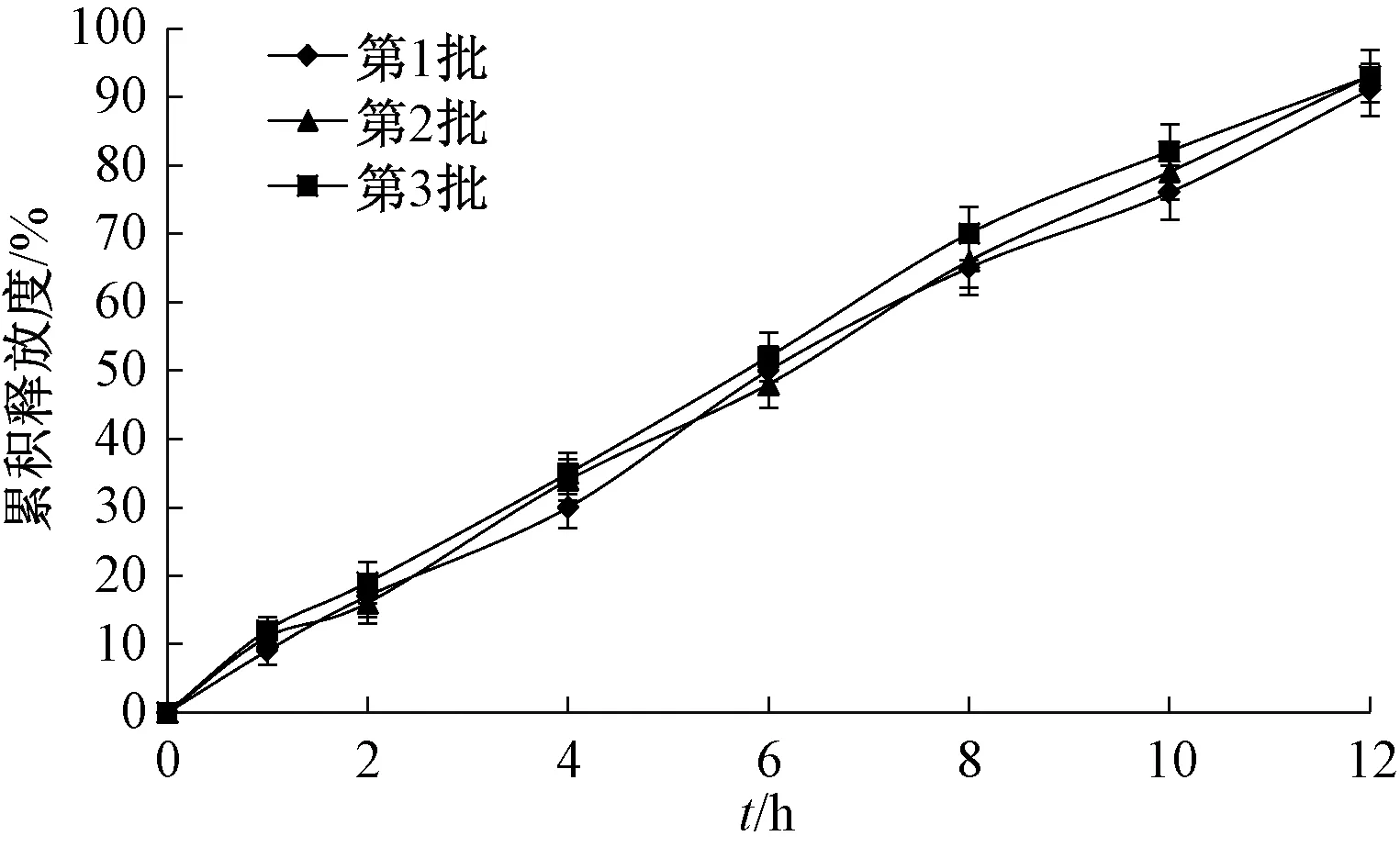
图5 3 批样品释药曲线Fig.5 Drug release curves for three batches of samples
2.8 体外释药比较 按照处方比例称取环维黄杨星D、羟丙基⁃β⁃环糊精适量,制备物理混合物,按优化处方制备微孔渗透泵控释片,并比较它与包合物微孔渗透泵控释片的释药线性和累积释放度,结果见图6。由此可知,2 种微孔渗透泵控释片的体外释药均基本以恒速方式进行,但环维黄杨星D 包合物微孔渗透泵控释片在不同时间点的累积释放度均明显高于物理混合物微孔渗透泵控释片。

图6 2 种微孔渗透泵控释片释药曲线Fig.6 Drug release curves for two microporous osmotic pump controlled release tablets
2.9 释放介质对释药的影响 考察环维黄杨星D包合物微孔渗透泵控释片在水、pH1.2 盐酸溶液、pH4.5 醋酸盐缓冲液、pH6.8 磷酸缓冲液中的体外释药,结果见图7。参考文献[15⁃16]计算2 种释药曲线之间的相似因子,发现均大于50,最低也有69.7,表明释放介质对该制剂体外释药无明显影响。另外,释放介质pH 可能会影响包衣膜中增塑剂(邻苯二甲酸二乙酯)性能[17],但环维黄杨星D 包合物微孔渗透泵控释片释药曲线的拟合度(R2)仍大于0.968 6。
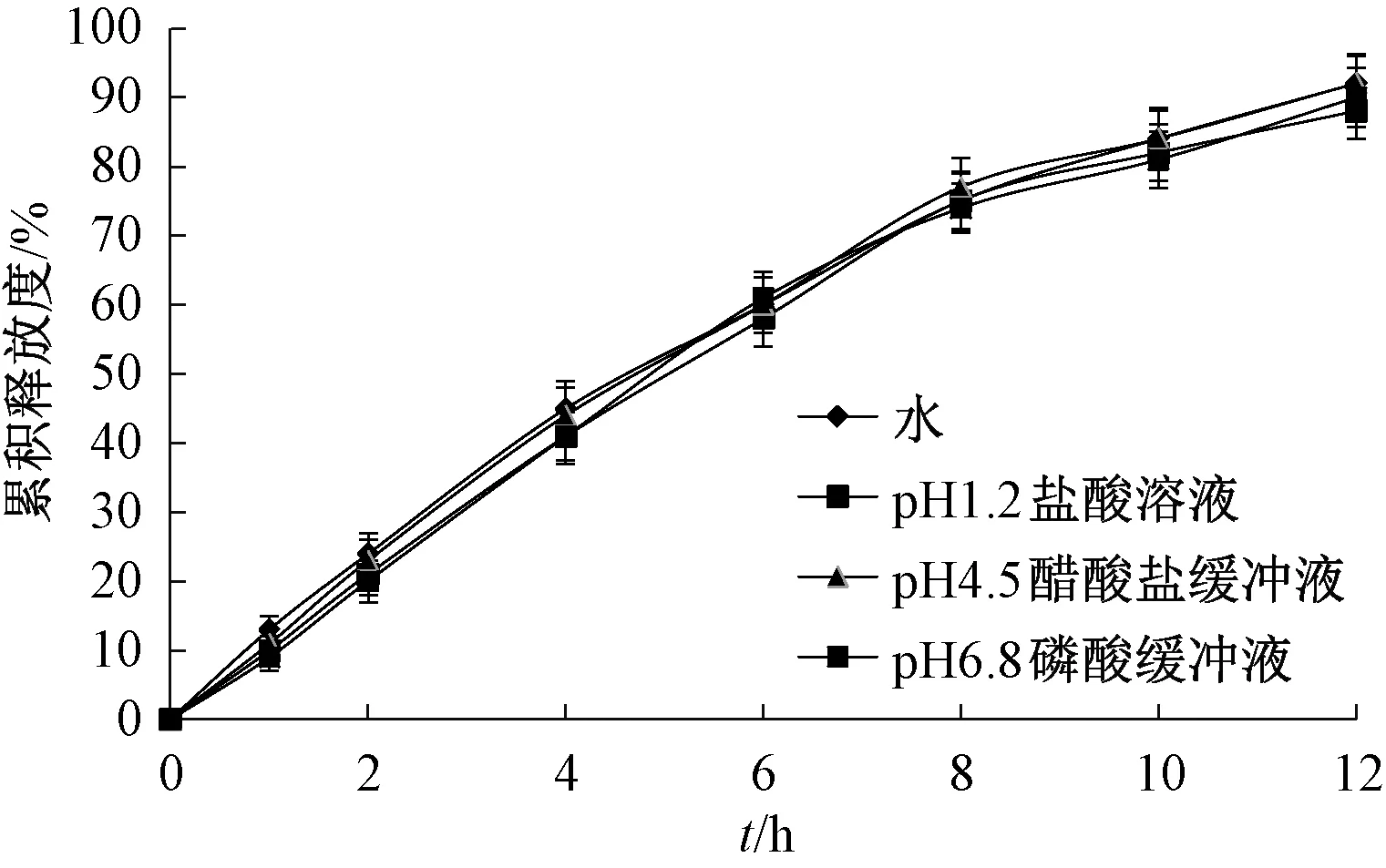
图7 释放介质对体外释药的影响Fig.7 Effect of release medium on in vitro drug release
3 讨论
微孔渗透泵控释片属于单层渗透泵,而药物溶解度、半透膜两侧渗透压等是影响其释药方式、释药速率、累积释放度的主要因素[10⁃11]。为了保证足够的渗透压,本实验首先将环维黄杨星D 制成包合物,可使其溶解度升至10.7 倍,同时处方中助悬剂PEO 及渗透活性物质NaCl 均可提高半透膜两侧渗透压,有助于药物顺利释放。
虽然NaCl 是处方中不可缺少的一种辅料,但由于它本身有吸湿性,前期预实验发现其用量过多时会对片剂包衣膜有一定影响,不利于长期保存,故将其控制在20 mg/片。同时,选择PEO 作为促渗聚合物,一方面可利用其吸水膨胀性质,增加渗透泵半透膜两侧渗透压;另一方面,可将药物与水形成混悬液以防止药物沉淀,从而有助于提高累积释放度[18⁃19]。
梁涛等[6]制备的环维黄杨星D 单层渗透泵控释片释放度不高,本实验采用包合技术提高其溶解度,印证增溶技术引入渗透泵控释片的必要性[20]。陈静等[21]比较了环维黄杨星D 及其包合物在大鼠体内的药动学,虽然生物利用度升至248.58%,但也加大了血药浓度的波动程度,本实验将环维黄杨星D 包合物制成缓释片后,由于渗透泵控释片控制了其缓慢释放,可有助于抑制血药浓度波动,降低不良反应,提高疗效。另外,黄杨宁片每天口服剂量为6 mg,故本实验将所制备环维黄杨星D包合物微孔渗透泵控释片的剂量也设定为6 mg,后续将对该制剂体内药动学、生物利用度等作进一步研究[22⁃23]。
